文档内容
云南师大附中 2027 届高一年级上学期教学测评期中卷
化学
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。第I卷第1页至第4页,第II
卷第4页至第6页。考试结束后,请将本试卷和答题卡一并交回。满分100分,考试用时90
分钟。
以下数据可供解题时参考。
可能用到的相对原子质量:
第I卷(选择题,共42分)
注意事项:
1.答题前,考生务必用黑色碳素笔将自己的姓名、准考证号、考场号、座位号在答题卡上
填写清楚。
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。在试题卷上作答无效。
一、选择题(本大题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项符合题目要求)
1.化学与生活密切相关。下列叙述不正确的是( )
A. 可用于焙制糕点
B.漂粉精可用于游泳池的消毒
C. 、 、 都是新型的自来水消毒剂
D.“洁厕灵”和“84消毒液”不能混用
2.下列关于物质分类的组合正确的是( )
酸性氧化
选项 碱性氧化物 酸 碱 盐
物
A 干冰 纯碱
B 熟石灰 小苏打
C 烧碱 胆矾
D 生石灰 食盐
3.下列推断正确的是( )
A. 的水溶液能导电, 是电解质
B. 、 组成元素相同,与 或 反应产物也相同
C.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色D. 难溶于水,向 溶液中逐滴加入稀硫酸,溶液的导电能力先减小后增大
4.有关物质燃烧时火焰颜色描述错误的是( )
A.硫在氧气中燃烧——绿色
B.乙醇在空气中燃烧——淡蓝色
C.钠在空气中燃烧——黄色
D.氢气在氯气中燃烧——苍白色
5.在指定溶液中能大量共存的是( )
A.无色溶液中: 、 、
B.饱和氯水中: 、 、
C.小苏打溶液中: 、 、
D.使酚酞试液变红的溶液中: 、 、
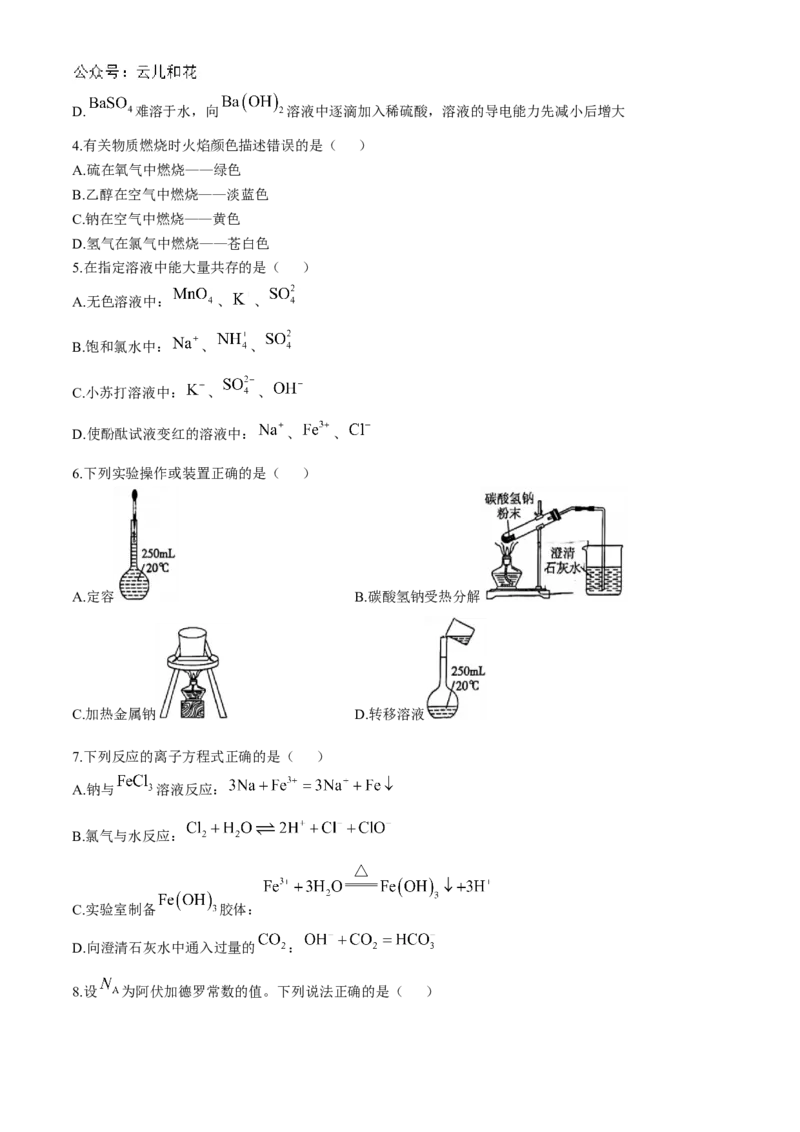
6.下列实验操作或装置正确的是( )
A.定容 B.碳酸氢钠受热分解
C.加热金属钠 D.转移溶液
7.下列反应的离子方程式正确的是( )
A.钠与 溶液反应:
B.氯气与水反应:
C.实验室制备 胶体:
D.向澄清石灰水中通入过量的 :
8.设 为阿伏加德罗常数的值。下列说法正确的是( )A. 固体中所含离子数为
B. 溶液中含有的 数为
C. 与 反应产生标准状况下 时转移的电子数为
D.用含 的饱和溶液制备 胶体,产生 个 胶粒
9.下列实验“操作和现象”与“结论”对应关系不正确的是( )
选项 操作和现象 结论
溶液和胶体的本质区别是能否产生丁达
A 用红色激光笔分别照射 溶液和 胶体,观
尔效应
察到后者中出现一条光亮的“通路”
室温下,分别取相同浓度的碳酸钠、碳酸氢钠溶液于试 相同温度和浓度时,碳酸钠溶液的碱性
B
管中,各滴入2 3滴酚酞试液,碳酸钠溶液红色较深 强于碳酸氢钠溶液
碳酸钠粉末遇水生成水合碳酸钠
C
向盛有约 碳酸∼钠粉末的试管中滴加5滴水,碳酸钠结
块变成晶体
D 用洁净的铂丝蘸取某溶液进行焰色试验,其火焰呈黄色 该溶液不一定是钠盐溶液
10.下列选项所示的物质间转化均能实现的是( )
A.
B.
C.饱和
D.饱和
11.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,甲的密度大
于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小
D.甲的相对分子质量比乙的相对分子质量小
12.已知还原性: 。 含等物质的量的 和 的混合溶液中通入 的
,有一半的 变为 。原溶液中 和 物质的量浓度均为( )
A. B. C. D.
13. 与一定浓度的 反应,生成 、 、 、 和水,当 利 的物质的量之比为 时,则反应中起酸性作用的 与被还原的 的物质的量之比为( )
A. B. C. D.
14.20℃时 溶于 水中,恰好形成 饱和溶液。下列关系式错误的是( )
A.该溶液的质量分数
B.该溶液的物质的量浓度
C.20℃时, 的溶解度
D.该溶液的密度
第II卷(非选择题,共58分)
注意事项:
第II卷用黑色碳素笔在答题卡上各题的答题区域内作答,在试题卷上作答无效。
二、填空题(本大题共4小题,共58分)
15.(14分)某兴趣小组在处理污水样品时,需用质量分数为98%、密度为 的浓硫酸配制
的稀硫酸。
(1) 易与水分子结合成水合氢离子,通常用 表示。 所含电子数约为________ 。
(2)质量分数为98%、密度为 的浓硫酸的物质的量浓度为________ ,本实验需要量
取该浓硫酸的体积为________ 。
(3)本实验用到的实验仪器有: 的________、烧杯、玻璃棒、胶头滴管、________。
(4)下列操作正确的是________(填序号)。
A.使用容量瓶之前一定要检查其是否漏液
B.进行容量瓶检查是否漏液时,倒置一次即可
C.容量瓶用蒸馏水洗净后,需要再用浓硫酸润洗
D.用量筒量取浓硫酸倒入容量瓶中,缓慢加水至离刻度线1 2 cm处,改用胶头滴管继续加蒸馏水至刻度
线
∼
(5)下列操作会导致所配的稀硫酸浓度偏高的是________(填序号)。A.用量筒量取浓硫酸时仰视读数
B.转移溶液之前,容量瓶中有少量蒸馏水
C.在烧杯中稀释浓硫酸时,没有冷却至室温就立即转移到容量瓶中
16.(15分)已知 和 两支试管中的透明溶液共含有 、 、 、 、 、 六种离
子,向试管 的溶液中滴入紫色石蕊试液呈蓝色。
(1)试管A的溶液中所含离子为________(填离子符号)。
(2)向试管B的溶液中加入苏打溶液,可观察到________(填实验现象)。
(3)向试管 的溶液中加入合适的试剂,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的
试剂是________(填化学式)。
(4)将试管A和B的溶液混合,发生反应的离子方程式为________、________(不考虑 与 的反
应)。
(5)若试管 和试管 中共有四种物质且按等物质的量溶解,再将两支试管中的溶液混合,过滤后所得
滤液中 、 和 的物质的量之比为1:________:________。
(6)检验试管A的溶液中含有 的实验操作为________。
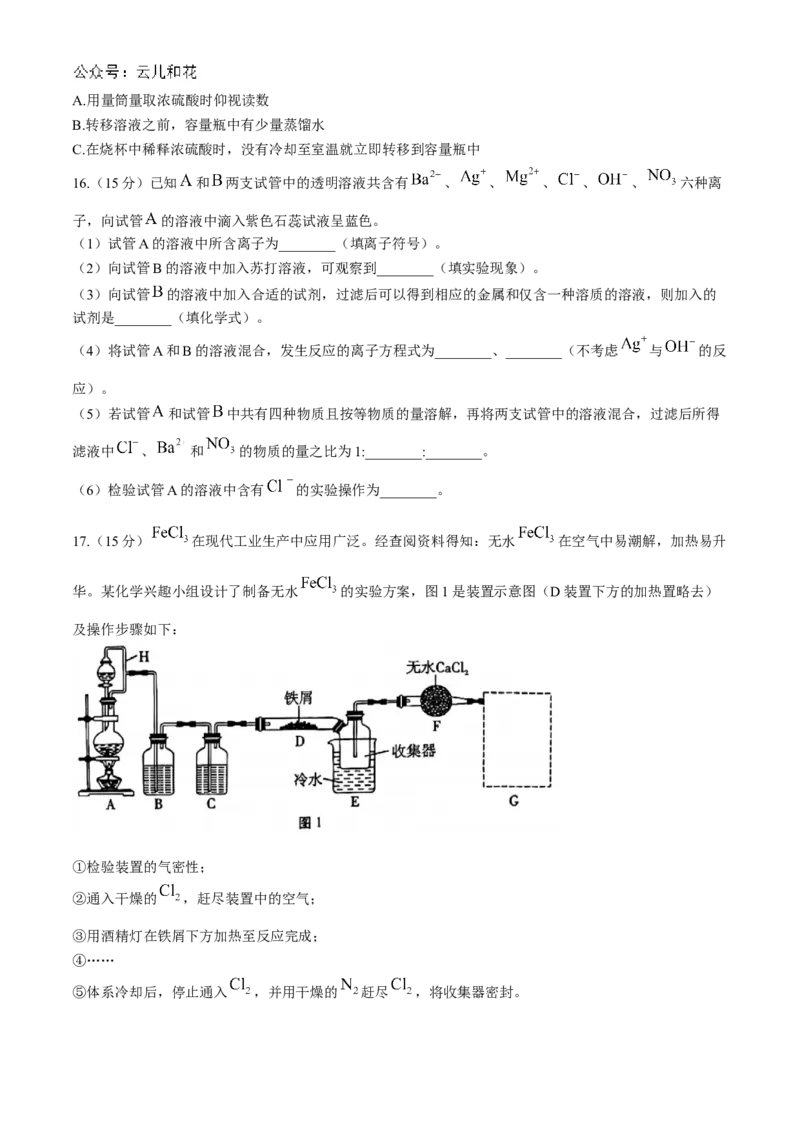
17.(15分) 在现代工业生产中应用广泛。经查阅资料得知:无水 在空气中易潮解,加热易升
华。某化学兴趣小组设计了制备无水 的实验方案,图1是装置示意图(D装置下方的加热置略去)
及操作步骤如下:
①检验装置的气密性;
②通入干燥的 ,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入 ,并用干燥的 赶尽 ,将收集器密封。(1)装置A中反应的离子方程式为________,装置B、C中盛放的试剂依次是________、浓 。
(2)H管的作用是________。
(3)第③步中生成的烟状 大部分进入收集器,少量沉积在反应管 右端。要使沉积的 进入
收集器,第④步操作是________。
(4)操作步骤①~⑤中,为防止 潮解所采取的措施有________(填步骤序号)。
(5)装置E中冷水浴的作用是________,装置F的作用是________。
(6)装置G用于处理尾气,最合适的装置为________(填序号)。
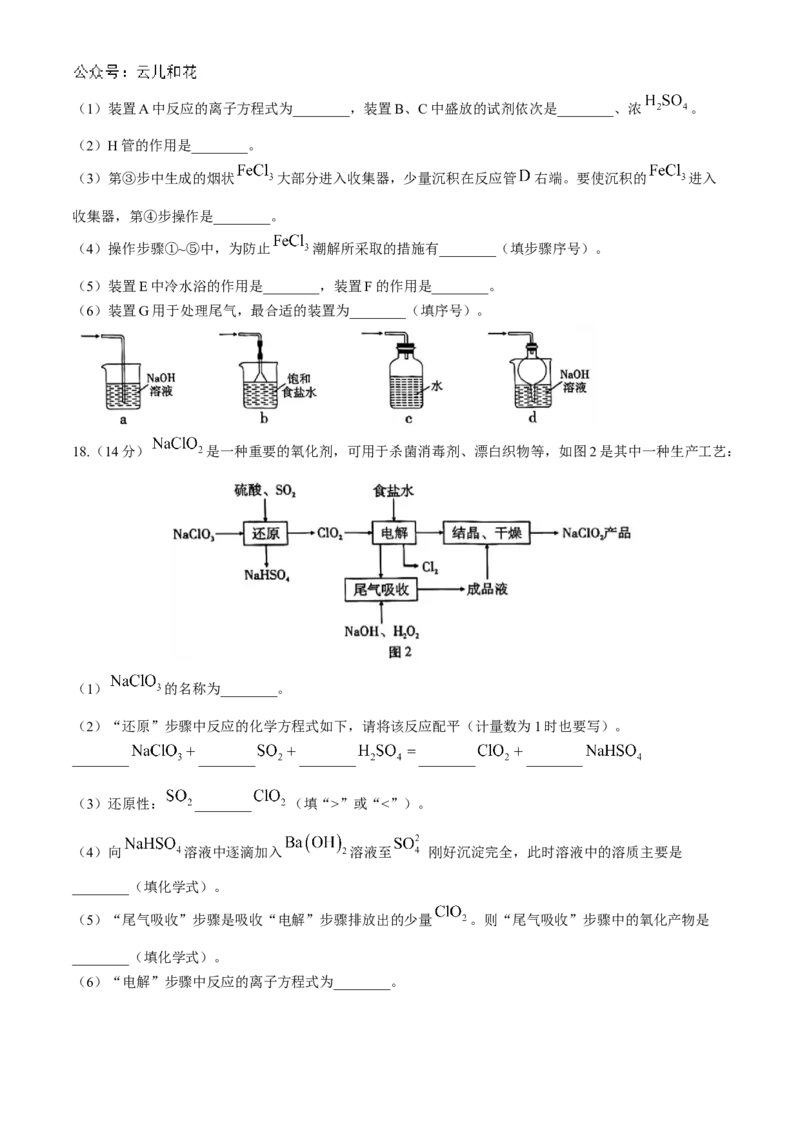
18.(14分) 是一种重要的氧化剂,可用于杀菌消毒剂、漂白织物等,如图2是其中一种生产工艺:
(1) 的名称为________。
(2)“还原”步骤中反应的化学方程式如下,请将该反应配平(计量数为1时也要写)。
________ ________ ________ ________ ________
(3)还原性: ________ (填“>”或“<”)。
(4)向 溶液中逐滴加入 溶液至 刚好沉淀完全,此时溶液中的溶质主要是
________(填化学式)。
(5)“尾气吸收”步骤是吸收“电解”步骤排放出的少量 。则“尾气吸收”步骤中的氧化产物是
________(填化学式)。
(6)“电解”步骤中反应的离子方程式为________。(7) 和 均能将电镀废水中的 氧化为无毒的物质,自身还原为 。处理含 相同量
的电镀废水,所需 的物质的量是 的________倍。参考答案
1、C 2、B 3、D 4.A 5.B 6.C 7、D 8.C 9.A 10.D 11.B 12.D 13.A 14.B
15.(1)6.02 (2)18.4 20.0 (3)量筒 200mL容量瓶 (4)A (5)AC
16.(1) 、 、 、(2)产生白色沉淀(3)Mg
(4)
(5)2 2
(6)取少量试管A的溶液于另外一支试管中,加入硝酸酸化的硝酸银溶液,若产生白色沉淀,则试管A
的溶液中含有
17.(1)MnO +4H++2Cl- Mn2++Cl↑+2H O 饱和食盐水
2 2 2
(2)平衡气压,使液体顺利流下 (3)在沉积的FeCl 固体下方加热 (4)②⑤
3
(5) 将FeCl 冷却沉积,便于收集产品 防止外界空气中的水蒸气进入E中导致 潮解
3
(6)a
18.(1)氯酸钠 (2)2 1 1 2 2 (3)>
(4)NaOH (5)O(6)2Cl— + 2ClO 电解 2ClO —+ Cl ↑
2 2 2 2
(7)2