文档内容
6.1.2 化学反应与电能 练习(解析版)
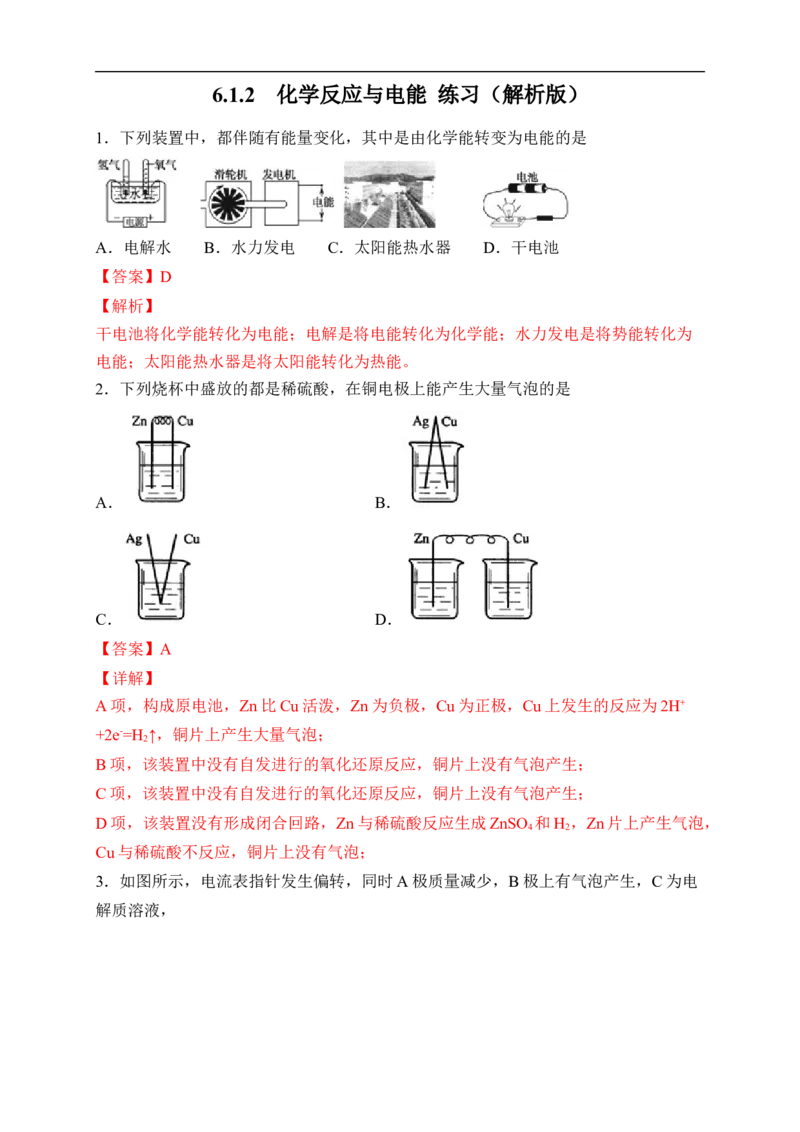
1.下列装置中,都伴随有能量变化,其中是由化学能转变为电能的是
A.电解水 B.水力发电 C.太阳能热水器 D.干电池
【答案】D
【解析】
干电池将化学能转化为电能;电解是将电能转化为化学能;水力发电是将势能转化为
电能;太阳能热水器是将太阳能转化为热能。
2.下列烧杯中盛放的都是稀硫酸,在铜电极上能产生大量气泡的是
A. B.
C. D.
【答案】A
【详解】
A项,构成原电池,Zn比Cu活泼,Zn为负极,Cu为正极,Cu上发生的反应为2H+
+2e-=H ↑,铜片上产生大量气泡;
2
B项,该装置中没有自发进行的氧化还原反应,铜片上没有气泡产生;
C项,该装置中没有自发进行的氧化还原反应,铜片上没有气泡产生;
D项,该装置没有形成闭合回路,Zn与稀硫酸反应生成ZnSO 和H ,Zn片上产生气泡,
4 2
Cu与稀硫酸不反应,铜片上没有气泡;
3.如图所示,电流表指针发生偏转,同时A极质量减少,B极上有气泡产生,C为电
解质溶液,下列说法错误的是
A.B极为原电池的正极
B.A、B、C可能分别为Zn、Cu、稀盐酸
C.C中阳离子向A极移动
D.A极发生氧化反应
【答案】C
【详解】
A.电流计指针偏转,证明形成了原电池,由于A极质量减少,B极上有气泡产生,则
A是原电池的负极,B是原电池的正极,正确;
B.A是负极,B是正极,负极金属活动性大于正极,而且在正极有气泡产生,则溶液
可能是酸,是H+得到电子,变为H 逸出,因此A、B、C可能分别为Zn、Cu、稀盐酸,
2
正确;
C.根据同种电荷相互排斥,异种电荷相互吸引的原则,溶液C中阳离子向正极B极
移动,错误;
D.电极A是负极,失去电子,发生氧化反应,正确。
故选C。
4.下列装置属于原电池装置的是
A. B.
C. D.
【答案】A
【解析】
分析:原电池的构成条件有:①有两个活泼性不同的电极,②将电极插入电解质溶液
中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,根据原电池的构成条件判断。
详解:A、符合原电池的构成条件,故A正确;B、乙醇属于非电解质,没有电解质溶
液,故B错误;C、没有构成闭合回路,故C错误;D、两个电极相同,没有两个活泼
性不同的电极,故D错误;故选D。
5.茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科
技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。在这种电池中
①铝合金是阳极 ②铝合金是负极 ③海水是电解液 ④铝合金电极发生还原反应
A.②③ B.②④
C.①② D.①④
【答案】A
【详解】
①原电池中电极分为正、负极,故①错误;
②一般较活泼的金属为原电池的负极,铝合金为负极,②正确;
③电极在海水中,故海水为电解质溶液,③正确;
④铝合金为负极,原电池的负极发生氧化反应,④错误;
答案选A。
6.下列关于原电池的叙述中错误的是( )
A.构成原电池的正极和负极必须是两种不同的金属
B.原电池是将化学能转变为电能的装置
C.在原电池中,电子流出的一极是负极,发生氧化反应
D.原电池放电时,电流的方向是从正极到负极
【答案】A
【详解】
A.构成原电池的正极和负极还可以是导电的非金属,如石墨,错误;
B.将化学能转变为电能的装置是原电池,正确;
C.在原电池中,电子流出的一极是负极,负极发生氧化反应,正确;
D.原电池放电时,电流的流向是从正极到负极,正确。
答案选A。
7.如图所示,铜片、锌片和石墨棒用导线连接后插入番茄里,电流计中有电流通过,
则下列说法正确的是 ( )A.石墨是阴极
B.两个铜片上都发生氧化反应
C.锌片是负极
D.两个番茄都形成原电池
【答案】C
【详解】
A、石墨和原电池正极相连做电解池的阳极,选项A错误;B、原电池中铜电极发生还
原反应,右装置是电解池,铜电极上发生还原反应,选项B错误;C、装置中依据活泼
性差别判断,锌为原电池负极,选项C正确;D、左装置是原电池,右装置是电解池,
选项D错误;答案选C。
8.①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,外电路
电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连
时,③的质量减少.据此判断这四种金属活泼性由大到小的顺序是( )
A.①③②④ B.①③④②
C.③④②① D.③①②④
【答案】B
【详解】
组成原电池时,负极金属较为活泼,
①②相连时,外电路电流从②流向①,说明①为负极,活泼性①>②;
①③相连时,③为正极,活泼性①>③;
②④相连时,②上有气泡逸出,应为原电池的正极,活泼性④>②;
③④相连时,③的质量减少,③为负极,活泼性③>④;
综上分析可知活泼性:①>③>④>②;
故选B。
9.下列有关能量转换的说法正确的是
A.原电池是将电能转化为化学能的过程
B.煤燃烧是化学能转化为热能的过程
C.动物体内葡萄糖被氧化成CO 是热能转变成化学能的过程
2
D.植物通过光合作用将CO 转化为葡萄糖是太阳能转变成热能的过程
2
【答案】B【详解】
A.原电池是将化学能转化为电能的过程,A错误;
B.煤燃烧是化学能转化为热能的过程,B正确;
C.动物体内葡萄糖被氧化成CO 是化学能转变成热能的过程,C错误;
2
D.植物通过光合作用将CO 转化为葡萄糖是太阳能转变成化学能的过程,D错误;
2
答案选B。
10.分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,
乙中A为电流表。请回答下列问题:
(1)以下叙述中,正确的是_______________(填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
F.乙溶液中 向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为___________;乙为______。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,
分析原因可能是___。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反
应离子方程式:铜电极:____,总反应:___。当电路中转移0.25 mol电子时,消耗负
极材料的质量为_____g(Zn的相对原子质量65)。
【答案】CD )化学能转化为热能 化学能转化为电能 锌片不纯,在锌片上就
形成原电池 Cu2++2e-=Cu Zn+Cu2+=Zn2++Cu 8.125
【详解】
(1)A.甲不能构成原电池,只有锌和稀硫酸发生氧化还原反应,乙池中能构成原电池,
锌作负极,铜作正极,故A错误;
B. 甲池不能构成原电池,所以甲池中铜电极上没有气泡产生,故B错误;
C. 两烧杯中都是氢离子得电子生成氢气,锌失电子发生氧化反应,所以溶液的pH均增大,故C正确;
D. 形成原电池时,可以加快反应速率,所以产生气泡的速度甲中比乙中慢,故D正确;
E. 乙的外电路中电流方向Cu→Zn,故E错误;
F. 乙溶液中SO 2−向负极Zn片方向移动,故F错误;
4
答案选CD;
(2)甲中不能形成原电池,所以是将化学能转变为热能,乙池能构成原电池,所以是将
化学能转化为电能,故答案为:化学能转化为热能;化学能转化为电能;
(3)锌片有气泡产生说明锌片不纯,锌和锌片中的杂质构成原电池,杂质作正极,氢离
子在杂质上得电子生成氢气,故答案为:锌片不纯,在锌片上就形成原电池;
(4)如果将稀硫酸换成硫酸铜溶液,则正极上铜离子得电子发生还原反应,电极反应式为:
Cu2++2e−=Cu,总反应为锌置换出铜的反应即Zn+Cu2+=Cu+Zn2+,负极锌失电子所以当电
路中转移0.25mol电子时,消耗负极材料的质量为 ×65g/mol=8.125g,
故答案为:Cu2++2e−=Cu;Zn+Cu2+=Cu+Zn2+;8.125g 。
11.看图回答下列问题
(1)若烧杯中溶液为稀硫酸,则观察到的现象是__________,电流表指针_______
(填偏转或不偏转),两极反应式为:
正极_______________________;
负极________________________。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为__________(填Mg或Al),总反应方
程式为__________。
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右下图所示:A、B两个
电极均由多孔的碳块组成。该电池的正极反应式为:_____________________。
(4)如果将上述装置中通入的H 改成CH 气体,也可以组成一个原电 池装置,电池
2 4
的总反应方程式为:CH +2O +2KOH=K CO +3H O,则该电池的负极反应式为:
4 2 2 3 2
_________________。
【答案】镁逐渐溶解,铝上有气泡冒出 偏转 正极 2H++2e=H 负极 Mg —2
2
e-= Mg2+ Al 2Al +2 NaOH+2H O = 2NaAlO +3H O +2H O+4e-=4OH-
2 2 2 2 2
CH +10OH-—8e-=CO 2-+7H O
4 3 2
【详解】
(1)若烧杯中的溶液为硫酸溶液,则形成原电池,镁做负极,铝做正极,镁逐渐溶解,
铝上有气泡冒出,导线中有电流通过,电流表指针偏转。铝做正极,是溶液中的氢离
子得到电子氢气,电极反应为:2H++2e-=H ;镁做负极,镁失去电子生成镁离子,电
2
极反应为Mg—2e-= Mg2+;
(2)若溶液中氢氧化钠溶液,只有铝与氢氧化钠反应,则铝做负极,镁做正极,总反
应为铝与氢氧化钠反应生成偏铝酸钠和氢气,方程式为:2Al +2 NaOH+2H O =
2
2NaAlO +3H ↑;
2 2
(3)氧气做正极,在碱性条件下得到电子生成氢氧根离子,电极反应为:
O +2H O+4e-=4OH-;
2 2
(4)在碱性条件下,正极反应为O +2H O+4e-=4OH-,所以用总反应-正极反应就可以
2 2
得到负极反应,即负极反应为:CH +10OH-—8e-=CO 2-+7H O。
4 3 2
12.锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,
其中电解质是LiClO ,溶于混合有机溶剂中,金属锂离子(Li+)通过电解质迁移入二
4
氧化锰晶格中,生成LiMnO 。
2
回答下列问题:(1)外电路的电流方向是由________极流向________极(填字母)。
(2)电池的正极反应式为___________。
(3)是否可用水代替电池中的混合有机溶剂________(填“是”或“否”),原因是
_______。
【答案】b a MnO +e-+Li+=LiMnO 否 电极锂是活泼金属,能与水反
2 2
应
【详解】
在锂锰电池中,金属锂为负极(a极),电极反应式为Li-e- Li+;二氧化锰为正
极(b极),电极反应式为MnO +e-+Li+ LiMnO ;在其外电路中,电子由负极
2 2
(a极)流向正极(b极),而电流方向则由正极(b极)流向负极(a极);负极材料
锂是活泼的金属,能与水发生反应,不能用水代替电池中的混合有机溶剂。故答案为:
b ;a;MnO +e-+Li+=LiMnO ;电极锂是活泼金属,能与水反应。
2 2