文档内容
化学必修第二册 综合测试(1)
一、选择题(本题包括16小题,每小题3分,共48分。每小题只有一个选项符合题意)
1.下列物质不属于有机物的是( )
A.“嫦娥五号”上的“织物版”国旗使用的国产高性能材料——芳纶纤维
B.“中国天眼”传输信息用的光纤材料——光导纤维
C.“一箭四星”运载火箭发动机使用的高效固态推进剂——二聚酸二异氰酸酯
D.新冠肺炎疫情期间医用防护服使用的防水透湿功能材料——聚氨酯薄膜
2.2018年6月5日是第47个世界环境日,主题为“塑战速决”,呼吁全世界齐心协力对抗一次性塑料
污染问题。下列做法不应提倡的是( )
A.大量生产超薄塑料袋
B.将塑料垃圾回收再生
C.生产可降解绿色替代品
D.少用或不用一次性塑料制品
3.2020年5月新修订的《北京市生活垃圾管理条例》将正式实施,垃圾分类并回收利用,可以减少污
染,节约自然资源。下列垃圾投放有错误的是( )
A.废旧报纸、饮料 B.剩饭菜、瓜皮果 C.过期药品、化妆 D.一次性餐具、
瓶、电池等 壳、枯草落叶等 品、油漆等 卫生纸、灰土等
4.《内经》曰:“五谷为养,五果为助,五畜为益,五菜为充”。合理膳食,能提高免疫力。下列说
法正确的是( )
A.蔗糖水解的产物中没有葡萄糖
B.植物油中含有不饱和脂肪酸酯,能使溴的四氯化碳溶液褪色
C.淀粉通过发酵法制得的乳酸[CHCH(OH)COOH]是乙酸的同系物
3
D.食盐水可以破坏蛋白质结构,用盐水漱口可以杀灭新型冠状病毒
5.关于二氧化硫和二氧化氮叙述正确的是( )
A.两种气体都是有毒的气体,且都可用水吸收以消除对空气的污染
B.两种气体都具有强氧化性,因此都能够使品红溶液褪色
C.二氧化硫与过量的二氧化氮混合后通入水中能得到两种常用的强酸
D.两种气体溶于水都可以与水反应,且只生成相应的酸,大气中的NO 和SO 可以形成酸雨
2 2
6.下列有关实验的操作、现象和实验结论错误的是( )
选项 操作 现象 实验结论A 将SO 通入酸性KMnO 溶液 溶液褪色 SO 具有还原性
2 4 2
B 将SO 通入HS溶液 产生淡黄色沉淀 SO 具有氧化性
2 2 2
向蔗糖中加入浓硫酸,将产生 蔗糖膨胀变黑,溴水
C 浓硫酸具有脱水性和氧化性
的气体通入溴水 褪色
将淀粉与稀硫酸混合加热后,
淀粉没有水解,或水解后没
D 加入少量新制的Cu(OH) ,再 无砖红色沉淀生成
2 有葡萄糖生成
加热
7.利用太阳光在新型复合催化剂表面实现高效分解水,其主要过程如图所示:
则下列说法错误的是( )
A.过程中实现了光能转化为化学能
B.氢能资源丰富,属于可再生能源
C.过程Ⅰ吸收能量,过程Ⅱ释放能量
D.2HO=====2H↑+O↑反应的能量变化如图所示:
2 2 2
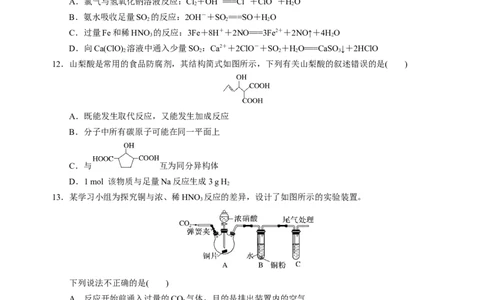
8.利用氮元素的价—类二维图可以设计氮及其化合物之间的转化路径,下列说法不正确的是( )
A.工业固氮的常用方法是由N 和H 合成NH
2 2 3
B.可利用Cu与硝酸的反应,将N元素转化为NO或NO
2
C.由氮气转化为含氮化合物的反应中,必须提供氧化剂
D.实验室可利用氢氧化钙固体与NH Cl固体混合加热制备NH
4 3
9.下列事实与带点物质表现出的性质(括号中)对应关系不正确的是( )
A. 能使含有酚酞的氢氧化钠溶液褪色(漂白性)
B.常温下,铁遇浓硫酸、浓硝酸发生钝化(强氧化性)
C.久置的浓硝酸,颜色略显黄色(不稳定性)
D.蔗糖与浓硫酸反应中有黑色物质生成(脱水性)
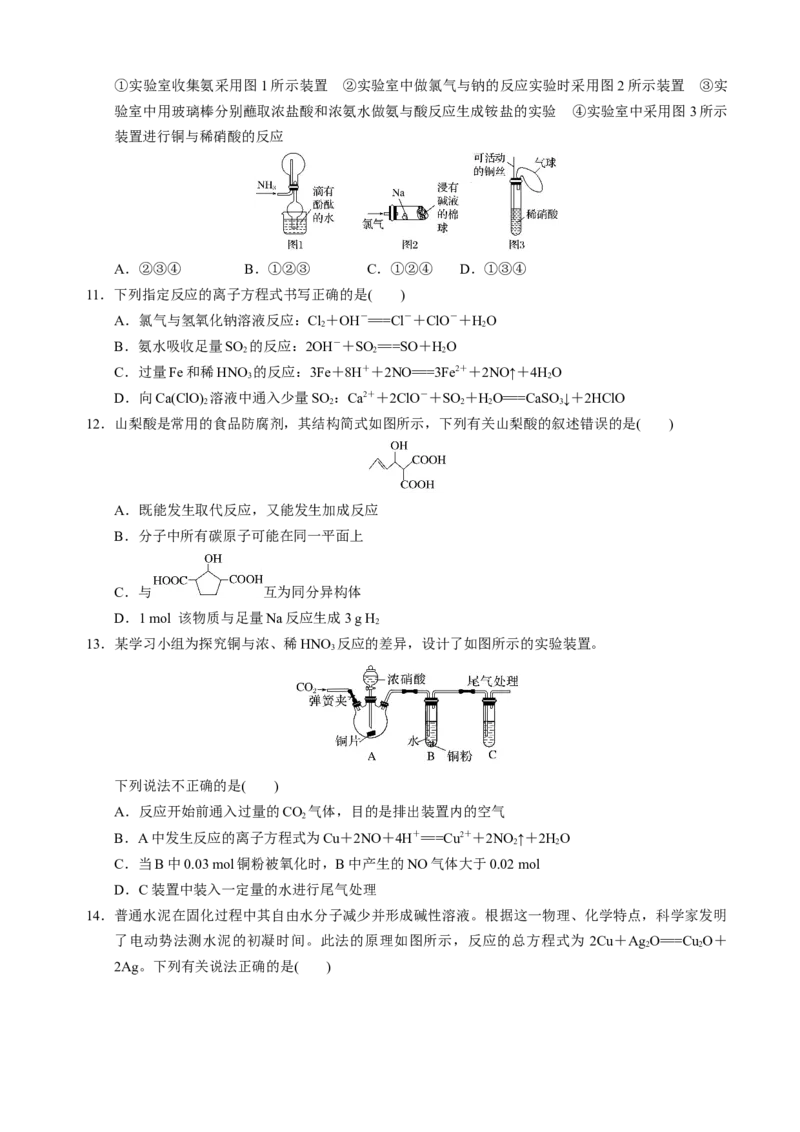
10.“绿色化学实验”已走进课堂,下列做法符合“绿色化学”要求的是( )①实验室收集氨采用图1所示装置 ②实验室中做氯气与钠的反应实验时采用图2所示装置 ③实
验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨与酸反应生成铵盐的实验 ④实验室中采用图3所示
装置进行铜与稀硝酸的反应
A.②③④ B.①②③ C.①②④ D.①③④
11.下列指定反应的离子方程式书写正确的是( )
A.氯气与氢氧化钠溶液反应:Cl+OH-===Cl-+ClO-+HO
2 2
B.氨水吸收足量SO 的反应:2OH-+SO ===SO+HO
2 2 2
C.过量Fe和稀HNO 的反应:3Fe+8H++2NO===3Fe2++2NO↑+4HO
3 2
D.向Ca(ClO) 溶液中通入少量SO :Ca2++2ClO-+SO +HO===CaSO ↓+2HClO
2 2 2 2 3
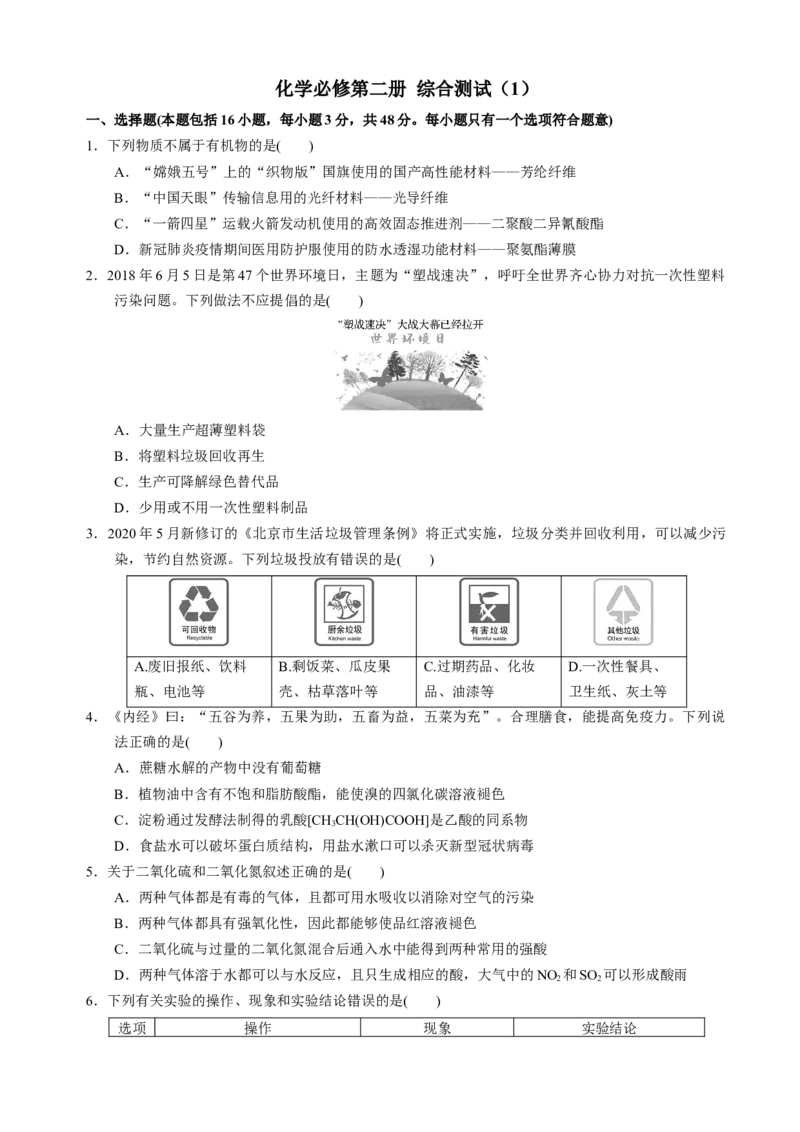
12.山梨酸是常用的食品防腐剂,其结构简式如图所示,下列有关山梨酸的叙述错误的是( )
A.既能发生取代反应,又能发生加成反应
B.分子中所有碳原子可能在同一平面上
C.与 互为同分异构体
D.1 mol 该物质与足量Na反应生成3 g H
2
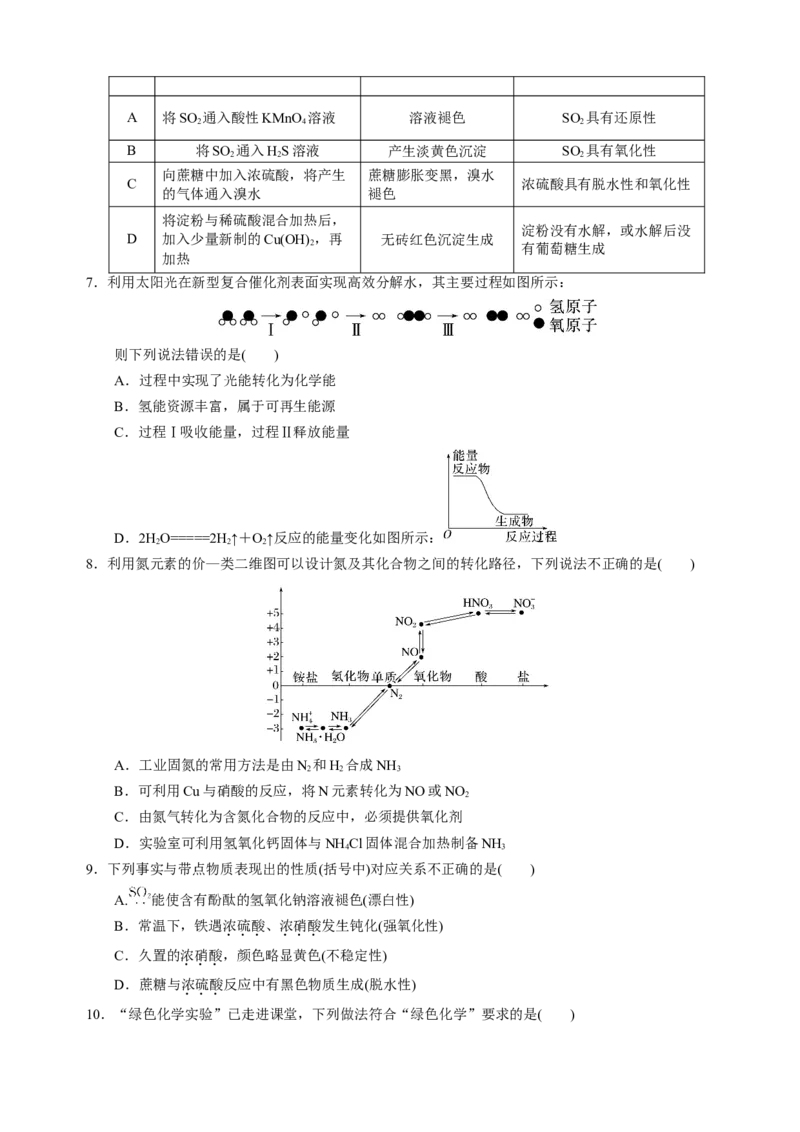
13.某学习小组为探究铜与浓、稀HNO 反应的差异,设计了如图所示的实验装置。
3
下列说法不正确的是( )
A.反应开始前通入过量的CO 气体,目的是排出装置内的空气
2
B.A中发生反应的离子方程式为Cu+2NO+4H+===Cu2++2NO ↑+2HO
2 2
C.当B中0.03 mol铜粉被氧化时,B中产生的NO气体大于0.02 mol
D.C装置中装入一定量的水进行尾气处理
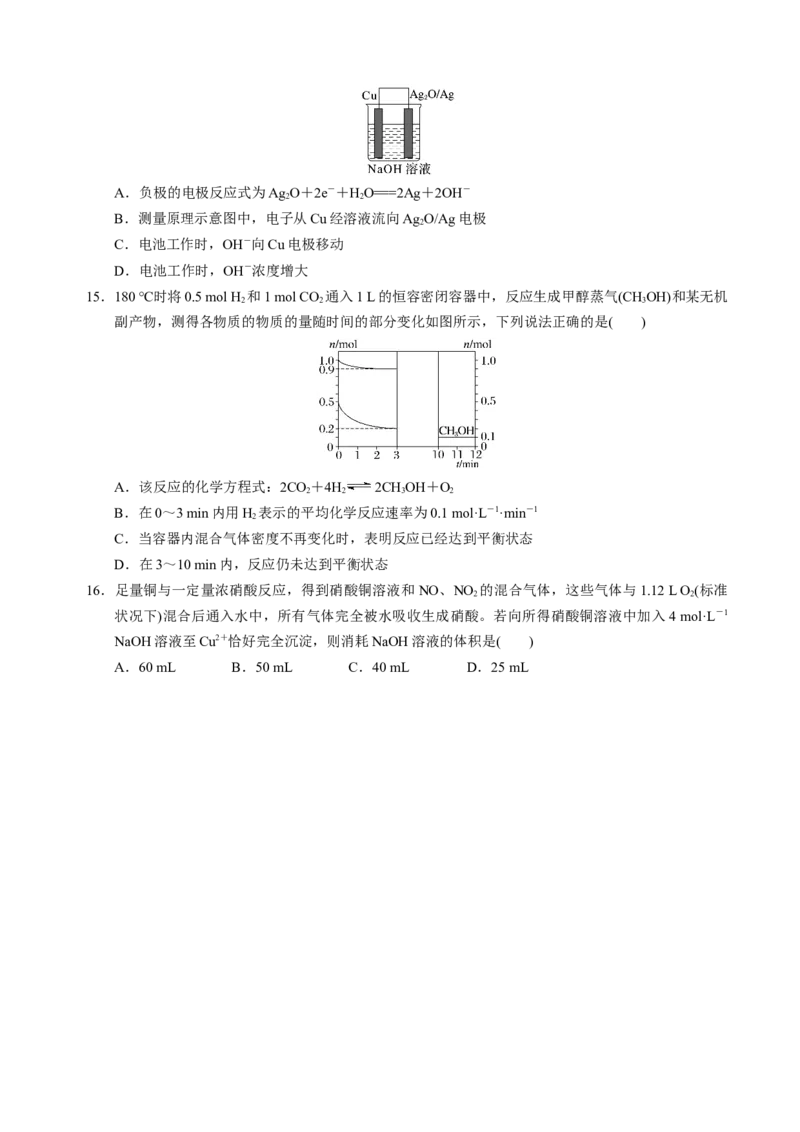
14.普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理、化学特点,科学家发明
了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为 2Cu+Ag O===Cu O+
2 2
2Ag。下列有关说法正确的是( )A.负极的电极反应式为Ag O+2e-+HO===2Ag+2OH-
2 2
B.测量原理示意图中,电子从Cu经溶液流向Ag O/Ag电极
2
C.电池工作时,OH-向Cu电极移动
D.电池工作时,OH-浓度增大
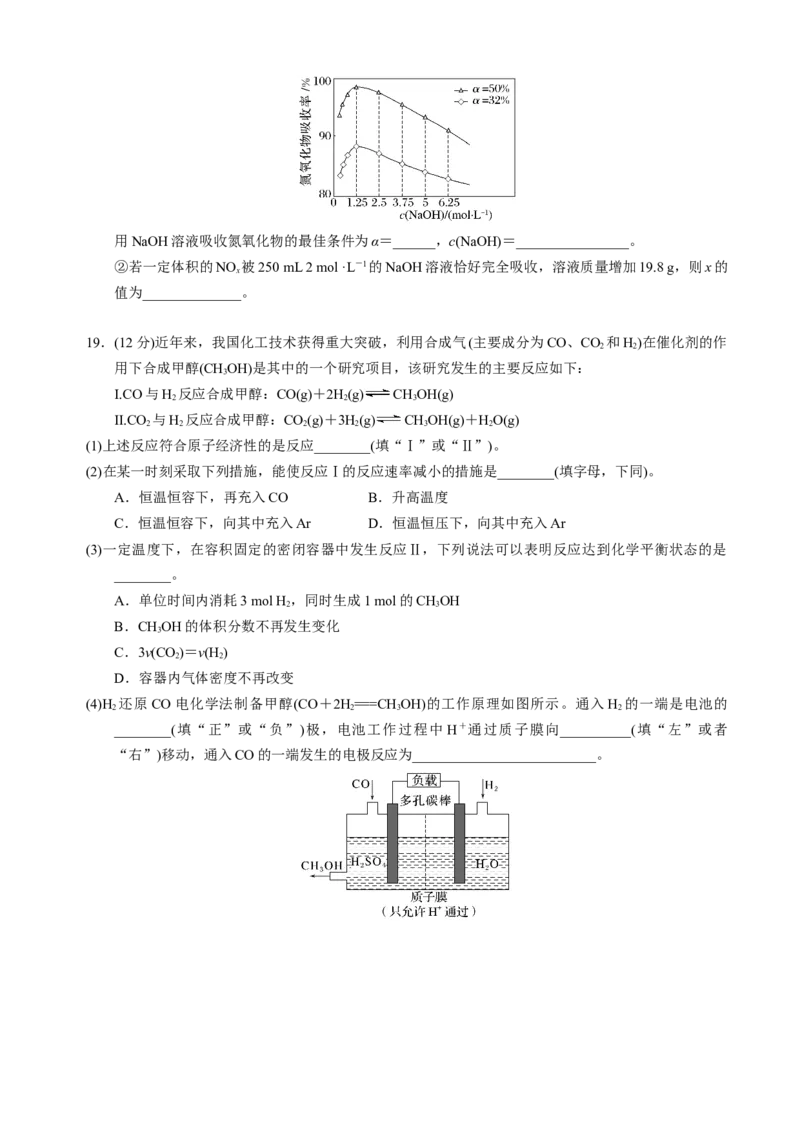
15.180 ℃时将0.5 mol H 和1 mol CO 通入1 L的恒容密闭容器中,反应生成甲醇蒸气(CHOH)和某无机
2 2 3
副产物,测得各物质的物质的量随时间的部分变化如图所示,下列说法正确的是( )
A.该反应的化学方程式:2CO+4H 2CHOH+O
2 2 3 2
B.在0~3 min内用H 表示的平均化学反应速率为0.1 mol·L-1·min-1
2
C.当容器内混合气体密度不再变化时,表明反应已经达到平衡状态
D.在3~10 min内,反应仍未达到平衡状态
16.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO、NO 的混合气体,这些气体与1.12 L O (标准
2 2
状况下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol·L-1
NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60 mL B.50 mL C.40 mL D.25 mL二、非选择题(本题包括4小题,共52分)
17.(10分)图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分物质类别的对应关
系。请回答下列问题:
(1)图2中N对应图1中物质的化学式为_________,Y与金属铜反应所得产物的化学式为__________。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为__________。
(3)碳和M的浓溶液反应生成Z的化学方程式为______________________________________。
(4)从物质分类角度分析判断,下列物质不属于酸性氧化物的是__________(填字母)。
A.SO B.SO C.SiO D.NO
2 3 2 2
(5)Na SO 溶液易变质,实验室检验NaSO 溶液是否变质的基本操作是_________________________
2 3 2 3
_______________________________________________________________________________。
18.(16分)氮氧化物(NO)是大气污染物之一,处理工业废气中的NO 对于环境保护具有重要的意义。
x x
(1)在一定条件下NH 可将NO 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装
3 2
置省略)。
①用装置A制备NH ,其中发生反应的化学方程式为__________________________________;装置
3
B内的试剂是____________。
②装置D中发生反应的离子方程式是_________________________________________,铜丝可抽动
的优点是_______________________________________。
③在装置M中NH 和NO 充分反应,生成两种对环境友好的物质,该反应中NH 和NO 的物质的量
3 2 3 2
之比为__________________。
(2)用 NaOH 溶液吸收法处理 NO(仅含 NO、NO )。已知吸收过程发生的反应有 2NaOH+NO+
x 2
NO ===2NaNO +HO;2NaOH+2NO ===NaNO +NaNO +HO。
2 2 2 2 3 2 2
①用不同浓度的NaOH溶液吸收NO 含量不同的尾气,关系如图(α表示NO 中NO 的含量):
2 x 2用NaOH溶液吸收氮氧化物的最佳条件为α=______,c(NaOH)=________________。
②若一定体积的NO 被250 mL 2 mol ·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8 g,则x的
x
值为______________。
19.(12分)近年来,我国化工技术获得重大突破,利用合成气(主要成分为CO、CO 和H)在催化剂的作
2 2
用下合成甲醇(CHOH)是其中的一个研究项目,该研究发生的主要反应如下:
3
Ⅰ.CO与H 反应合成甲醇:CO(g)+2H(g) CHOH(g)
2 2 3
Ⅱ.CO 与H 反应合成甲醇:CO(g)+3H(g) CHOH(g)+HO(g)
2 2 2 2 3 2
(1)上述反应符合原子经济性的是反应________(填“Ⅰ”或“Ⅱ”)。
(2)在某一时刻采取下列措施,能使反应Ⅰ的反应速率减小的措施是________(填字母,下同)。
A.恒温恒容下,再充入CO B.升高温度
C.恒温恒容下,向其中充入Ar D.恒温恒压下,向其中充入Ar
(3)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是
________。
A.单位时间内消耗3 mol H ,同时生成1 mol的CHOH
2 3
B.CHOH的体积分数不再发生变化
3
C.3v(CO)=v(H )
2 2
D.容器内气体密度不再改变
(4)H 还原CO电化学法制备甲醇(CO+2H===CH OH)的工作原理如图所示。通入H 的一端是电池的
2 2 3 2
________(填“正”或“负”)极,电池工作过程中 H+通过质子膜向__________(填“左”或者
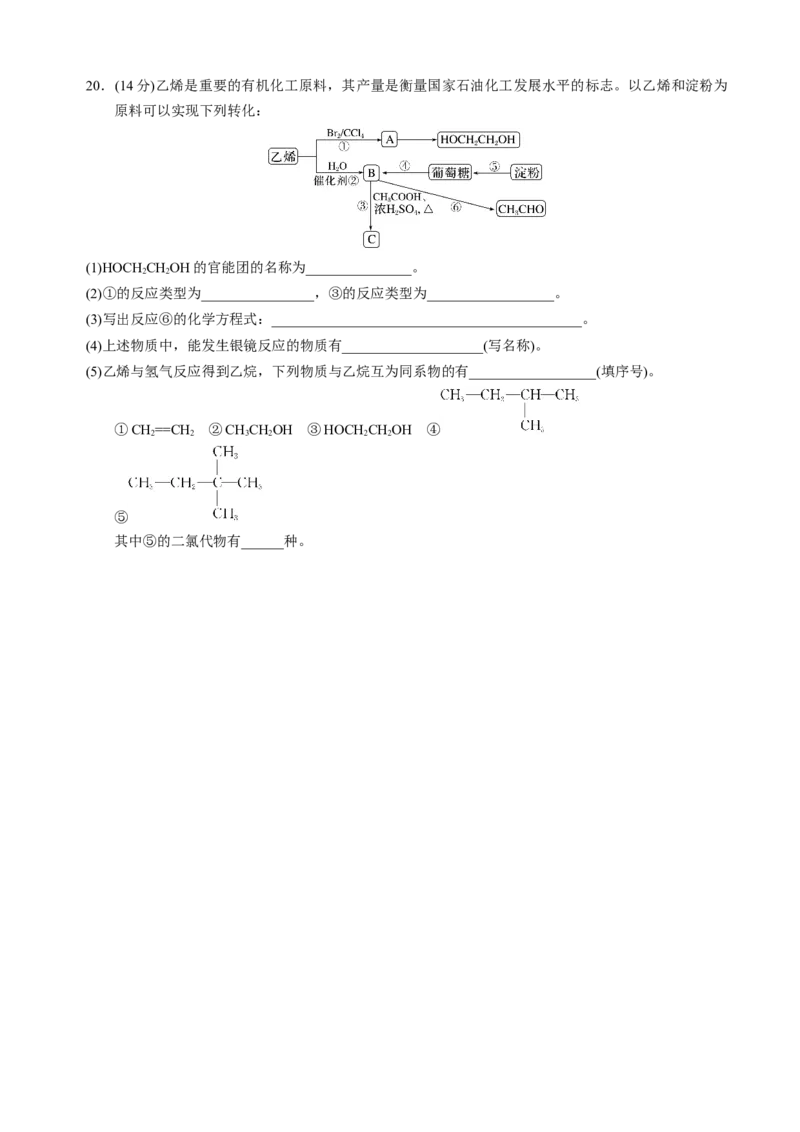
“右”)移动,通入CO的一端发生的电极反应为__________________________。20.(14分)乙烯是重要的有机化工原料,其产量是衡量国家石油化工发展水平的标志。以乙烯和淀粉为
原料可以实现下列转化:
(1)HOCHCHOH的官能团的名称为_______________。
2 2
(2)①的反应类型为________________,③的反应类型为__________________。
(3)写出反应⑥的化学方程式:____________________________________________。
(4)上述物质中,能发生银镜反应的物质有____________________(写名称)。
(5)乙烯与氢气反应得到乙烷,下列物质与乙烷互为同系物的有__________________(填序号)。
①CH==CH ②CHCHOH ③HOCH CHOH ④
2 2 3 2 2 2
⑤
其中⑤的二氯代物有______种。