文档内容
第四章单元检测试卷(解析版)
可能用到的原子量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 S 32 Fe 56 Mg 24 Al 27
第Ⅰ卷
一、选择题:本题共20个小题,每小题2分,共40分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.元素周期表是一座开放的“元素大厦”,“元素大厦”尚未客满。若发现119号元素,请在“元素
大厦”中安排好它的“房间”( )
A.第七周期0族 B.第六周期第ⅡA族
C.第八周期第ⅠA族 D.第七周期第ⅦA族
【答案】C
【解析】按目前元素周期表的编排原则,第七周期应有 32种元素,则前七个周期共有118种元素,
119号元素应位于第八周期第ⅠA族。
2.放射性元素Cn的一个原子经过6次衰变(每次衰变都放出一个相同的粒子)后,得到比较稳定的第
100号元素镄(Fm)的含153个中子的原子。下列说法中正确的是( )
A.每次衰变都放出He
B.每次衰变都放出T
C.Fm只是元素镄的一个原子,153不代表镄元素的相对原子质量
D.Cn经过3次这样的衰变是得不到镄原子的,产生的是Cn的同位素原子
【答案】A
【解析】Cn的质子数为112,该原子经过6次衰变后得到100号元素镄(Fm)的含153个中子的原子,
则放出的粒子的质子数为(112-100)÷6=2,中子数为(277-112-153)÷6=2,即放出的粒子是 α粒子
(He),A正确、B错误;根据质量数=质子数+中子数=153+100=253,应为Fm,C错误;质子数相同
中子数不同的同一元素互称同位素,Cn经过3次这样的衰变得到的原子质子数为112-2×3=106,与Cn
的质子数不相等,D错误。
3.下图中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( )
A.元素b位于ⅥA族,有+6价、-2价两种常见化合价
B.五种元素中,元素e的性质最稳定C.元素c和d的最高价氧化物对应水化物的酸性:c>d
D.元素c和e的气态氢化物的稳定性:c>e
【答案】D
【解析】图中,a为稀有气体元素氦,是5种元素中最稳定的;b是氧元素,没有+6价;c的非金属
性比d弱,因此c的最高价氧化物对应水化物的酸性比d的弱;c的非金属性比e强,因此c的气态氢化物
的稳定性比e强。
4.食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分。下列关于两种物质的说法正确的是(
)
A.炒菜时放入食盐并不破坏NaCl中的化学键
B.HCl的电子式是H+
C.NaCl熔化时破坏共价键
D.HCl的结构式是H—Cl
【答案】D
【解析】NaCl中存在离子键,NaCl溶解和熔化过程中,离子键均被破坏,故A、C错误;HCl的电子
式为 ,结构式为H—Cl,故B错误,D正确。
5.下列各组元素性质递变情况错误的是( )
A.H、Be、B原子最外层电子数依次增多
B.P、S、Cl元素最高正化合价依次升高
C.B、C、N、O、F原子半径依次增大
D.Li、Na、K、Rb的金属性依次增强
【答案】C
【解析】同周期元素(除稀有气体),从左到右核电荷数逐渐增大,原子半径逐渐减小,最高化合价逐
渐升高,非金属性逐渐增强,金属性逐渐减弱;同主族元素,从上到下电子层数逐渐增多,原子半径逐渐
增大,非金属性逐渐减弱,金属性逐渐增强。
6.根据元素周期律,由下列事实进行归纳推测,推测不合理的是( )
选项 事实 推测
A Mg与水反应缓慢, Ca与水反应较快 Ba(第ⅡA族)与水反应会更快
12 20 56
Si是半导体材料,同族的Ge也是半导体 第ⅣA族的元素的单质都可作半导体材
B
材料 料
HCl在1 500 ℃时分解,HI在230 ℃时
C HBr的分解温度介于二者之间
分解D Si与H 高温时反应,S与H 加热能反应 P与H 在高温时能反应
2 2 2
【答案】B
【解析】同主族金属元素由上至下金属性增强,与水反应剧烈程度增强,A正确;作半导体材料的元
素通常位于元素周期表中金属元素和非金属元素的交界处,第ⅣA族元素的单质并不能都作半导体材料,
B错误;同主族非金属元素由上至下非金属性减弱,气态氢化物的热稳定性减弱,C正确;同周期非金属
元素从左到右非金属性增强,与氢气化合难度减小,D正确。
7.下列物质中只含有共价键的是( )
A.NaCl、HCl、HO、NaOH B.Cl、NaS、HCl、SO
2 2 2 2
C.HBr、CO、HO、CS D.NaO、HO、HO、O
2 2 2 2 2 2 2 2 3
【答案】C
【解析】NaCl只含有离子键,HCl、HO只含有共价键,NaOH既含有离子键又含有共价键,A错误;
2
Cl 、HCl、SO 分子中只有共价键,而 NaS中只有离子键,B错误;NaO 既有离子键又有共价键,
2 2 2 2 2
HO、HO、O 分子中只有共价键,D错误。
2 2 2 3
8.几种短周期元素的原子半径和主要化合价见下表,下列说法中正确的是( )
元素代号 原子半径/nm 主要化合价
X 0.160 +2
Y 0.143 +3
Z 0.102 +6、-2
L 0.099 +7、-1
M 0.077 +4、-4
Q 0.074 -2
A.等物质的量的X、Y的单质与足量的盐酸反应,生成的H 一样多
2
B.Y与Q形成的化合物不能跟氢氧化钠溶液反应
C.Z的氢化物的稳定性强于L的氢化物的稳定性
D.在化学反应中,M原子与其他原子易形成共价键而不易形成离子键
【答案】D
【解析】由题给主要化合价可知,X位于第 ⅡA族,Y位于第ⅢA族,Z位于第ⅥA族,L位于第Ⅶ
A族,M位于第ⅣA族,Q位于第ⅥA族。在短周期元素中,结合原子半径的递变规律可知,X、Y、Z、
L、M、Q分别为Mg、Al、S、Cl、C、O。
9.短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原
子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数
是其电子层数的2倍。下列说法错误的是( )A.元素W、X的氯化物中,各原子均满足8电子的稳定结构
B.元素X与氢形成的原子比为1∶1的化合物有很多种
C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Z可与元素X形成的化合物XZ 属于共价化合物
2
【答案】A
【解析】首先根据题中条件确定各元素:根据W是制备一种高效电池的重要材料,确定W为Li元素;
根据X原子的最外层电子数是内层电子数的2倍,确定X是C元素;根据Y是地壳中含量最丰富的金属元
素,确定Y是Al元素,再根据原子序数依次增大,Z原子的最外层电子数是其电子层数的2倍,确定Z是
S元素。W为Li元素,其氯化物为LiCl,电子式为 ,显然Li原子不能满足8电子稳定结构,A
错误;C元素和H元素形成的原子个数比为1∶1的有机物有多种,如苯、苯乙烯等,B正确;金属Al与
氢氧化钠溶液或盐酸都反应,产生氢气,C正确;S元素和C元素形成的CS,属于共价化合物,D正确。
2
10.A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大。已知:A和C、B和D分别位
于同主族,且B、D质子数之和是A、C质子数之和的2倍。下列说法正确的是( )
A.原子半径的大小顺序:r(B)>r(C)>r(D)
B.C的最高价氧化物对应水化物的碱性在同周期中最强
C.E分别与A、C形成的化合物中化学键类型相同
D.B的简单气态氢化物的热稳定性比D的弱
【答案】B
【解析】有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A和C、B和D分别位于
同主族,假设A是H元素,B的原子序数小于C,则C是Na元素,且B、D质子数之和是A、C质子数之
和的2倍,则B是O元素,D是S元素,假设成立,则E是Cl元素。原子核外电子层数越多,原子半径越
大,应为Na>S>O,A错误;C为Na,在第三周期中金属性最强,最高价氧化物对应水化物的碱性在同
周期中最强,B正确;E与A、C形成的化合物分别为HCl、NaCl,分别为共价化合物和离子化合物,化
学键类型不同,C错误;非金属性O>S,非金属性越强,对应的氢化物越稳定,D错误。
11.元素X、Y、Z的原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子排布。下
列推测不正确的是( )
A.同周期元素中X的金属性最强
B.原子半径:X>Y,离子半径:X+>Z2-
C.同族元素中Z的氢化物稳定性最高
D.同周期元素中Y的最高价含氧酸的酸性最强【答案】B
【解析】由X+与Z2-具有相同核外电子排布分析:X若为K,则Z为S,根据X、Y、Z原子序数之和
为36推测Y只能为H,显然与“X、Y在同一周期”不符。所以X只能为Na,Z为O,Y为Cl,结合元素
周期律可知B项不正确。
12.X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素,其中只有Z是金属,W的单质是
黄色固体,X、Y、W在周期表中的相对位置关系如图。下列说法正确的是( )
A.五种元素中,原子半径最大的是W
B.Y与Z形成的化合物都可以和盐酸反应
C.Y的简单阴离子比W的简单阴离子还原性强
D.Z与Q形成的化合物水溶液一定显酸性
【答案】B
【解析】短周期主族元素,W的单质是黄色固体,则W为S,由X、Y、W在周期表中的相对位置可
知,Y为O,X为C,X、Y、Z、W、Q是原子序数依次增大,所以Q为Cl,其中只有Z是金属,则Z可
能为Na、Mg、Al中的一种。五种元素中,原子半径最大的是 Z,A错误;Y与Z形成的化合物为金属氧
化物,都可以和盐酸反应,B正确;氧气的氧化性比硫单质强,单质的氧化性越弱对应离子的还原性强,
所以Y的简单阴离子比W的简单阴离子还原性弱,C错误;若Z为Na,则Z与Q形成的化合物NaCl的水
溶液为中性,D错误。
13.a、b、c、d是四种短周期元素,a、b、c同周期,c、d同主族。a的原子结构示意图为 ,
b与d形成的化合物的电子式为 ,则下列叙述中正确的是( )
A.原子序数:a>b>c
B.d单质最活泼
C.原子半径:a>c>d
D.最高价氧化物对应的水化物的酸性:d>a>c
【答案】C
【解析】根据核外电子排布规律知,x=2,a为Si,由b、d形成的化合物的电子式可知b为Na,d为N,c、d同主族,则c为P。原子序数:c>a>b,A错误;N 中含有N≡N键,性质很稳定,B错误;原子
2
半径:a>c>d,C正确;最高价氧化物对应的水化物的酸性:d>c>a,D错误。
14.四种主族元素的离子 Xm+、 Yn+、Zn-和 Rm-(a、b、c、d为元素的原子序数),它们具有相同的
a b c d
电子层结构,若m>n,则下列叙述正确的是( )
①a-b=n-m ②元素的原子序数:a>b>c>d ③元素非金属性:Z>R
④最高价氧化物对应的水化物的碱性:X>Y
A.只有③ B.①②③④
C.①②③ D.②③
【答案】D
【解析】由题意知,a-m=b-n=c+n=d+m,又m >n,则①错误,②正确。主族元素简单阳离子
所带的正电荷数为其族序数,阴离子所带的负电荷数为 8-族序数,故Z、R位于X、Y的上一周期,且Z
在R后,X在Y后,故③正确,④错误。综上所述,D正确。
15.X、Y和Z是短周期的三种元素,已知X元素原子的最外层只有一个电子,Y元素原子M层上的
电子数是K层和L层电子总数的一半,Z元素原子L层上的电子数比Y元素原子L层上的电子数少2个,
则这三种元素所组成的化合物的化学式不可能是( )
A.XYZ B.XYZ
2 4 3
C.XYZ D.XYZ
3 4 4 2 7
【答案】A
【解析】由题意知,在短周期元素中,X可以是H、Li、Na三种元素中的一种;Y元素的原子结构为
,故Y是P;Z元素原子L层有6个电子,Z是O。分析各化合物化学式计算Y的化合价,其化合
价分别为+6价、+5价、+5价、+5价,而P元素无+6价,故A项不可能。
16.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知Y、W的原子序数之和是Z
的3倍,下列说法正确的是( )
A.原子半径:X<Y<Z
B.气态氢化物的稳定性:X>Z
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W【答案】C
【解析】由X、Y、Z、W四种元素的相对位置关系和Y、W的原子序数之和是Z的3倍可推出:X是
硅,Y是氮,Z是氧,W是氯。A项,原子半径:X>Y>Z。B项,气态氢化物的稳定性:X<Z。C项,
O、Cl分别与Mg形成MgO、MgCl ,它们均属于离子化合物。D项,非金属性:W(Cl)>Y(N),故最高价
2
氧化物对应水化物的酸性:W>Y。
17.下列结论正确的是( )
①离子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>HS>PH >SiH
2 3 4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl>S>Se>Te
2
⑤酸性:HSO >HPO >HCO>HClO
2 4 3 4 2 3
⑥非金属性:O>N>P>Si ⑦金属性:Be<Mg<Ca<K
A. 只有②⑤⑦ B. ②⑥⑦ C. ②④⑤⑥⑦ D. ②④⑥
【答案】C
【解析】①电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2-
>Cl->K+>Al3+,故①错误;②非金属性F>Cl>S>P>Si,氢化物稳定性:HF>HCl>HS>PH >SiH,
2 3 4
故②正确;③非金属性Cl>Br>I>S,阴离子还原性S2->I->Br->Cl-,故③错误;④非金属性Cl>S>Se
>Te,单质氧化性Cl>S>Se>Te,故④正确;⑤非金属性S>P>C,最高价含氧酸的酸性HSO >HPO
2 2 4 3 4
>HCO ,碳酸酸性比HClO酸性强,故酸性HSO >HPO >HCO >HClO,故⑤正确;⑥同周期随原子
2 3 2 4 3 4 2 3
序数增大元素非金属性增强,同主族自上而下元素非金属性减弱,故非金属性 O>N>P>Si,故⑥正确;
⑦同主族自上而下金属性增强,同周期自左而右金属性减弱,故金属性:Be<Mg<Ca<K,故正确。
18.下列有关化学用语的表示正确的是( )
A. NHCl的电子式: B. S2-的结构示意图:
4
C. 氨的电子式: D. 碳元素位于第2周期,VIA族
【答案】C的
【解析】A. NH Cl是离子化合物,电子式为 ,A错误;B. S2- 结构示意图为 ,
4
B错误;C. 氨气是共价化合物,电子式为 ,C正确;D. 碳元素位于第二周期第ⅣA族,D错误。
19.有人建议将氢元素排在元素周期表的ⅦA族。下列事实能支持这一观点的是( )
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H—H;
③与碱金属元素形成离子化合物: ;
④分子中原子间的化学键都属于非极性键。
A.①②③ B.①③④
C.②③④ D.①②③④
【答案】A
【解析】H与卤族元素得到一个电子后,最外层电子数都达到稳定结构,形成 X-,它们单质的分子
结构皆为X—X型,故①②③正确,而只要相同的非金属原子(稀有气体原子除外)就可以形成非极性键,
故④错。
20.元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是( )
A.元素原子的最外层电子数等于元素的最高化合价
B.多电子原子中,在离核较近的区域内运动的电子能量较高
C.P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强
D.元素周期表中位于金属元素和非金属元素分界线附近的元素属于过渡元素
【答案】C
【解析】O无最高正价,F和稀有气体元素没有正价,A错误;多电子原子中,能量低的电子在离核
较近的区域内运动,B错误;P、S、Cl的非金属性依次增强,得电子能力与最高价含氧酸(H PO 、
3 4
HSO 、HClO)的酸性均依次增强,C正确;过渡元素是指周期表中第3纵行到第12纵行的元素,包括了
2 4 4
七个副族与第Ⅷ族,D错误。
第Ⅱ卷
21.(12分)A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C
处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最
外层电子数的4倍。试回答:(1)这四种元素分别是A___________,B____________,C________,D________。
(2) 这 四 种 元 素 中 在 常 温 常 压 下 的 液 态 或 气 态 氢 化 物 的 稳 定 性 由 大 而 小 的 顺 序 是
________________________________________________________________________。
(3)A与B形成的三原子分子的电子式是________,B与D形成的原子个数比为1∶1的化合物的电子式是
________。
(4)A元素某氧化物与D元素某氧化物反应生成单质的化学方程式是____________________。当有0.1mol单
质生成的时,反应转移电子的物质的量为
【答案】(1)C O Si Na (2)H O>CH>SiH (3)
2 4 4
(4)2CO +2NaO===2Na CO+O 0.2mol
2 2 2 2 3 2
【解析】已知A、B同一周期,A、C同主族,原子半径D>C>A>B,所以A、B、C、D在周期表中相
对位置如图所示。
A B
D C
又因为C原子最外层上的电子数是D原子最外层电子数的4倍,所以C为第三周期ⅣA族,D为第三
周期ⅠA族,从而可知C为硅,D为钠,进而可推知,A为碳。由于C原子核内质子数等于A、B原子核
内质子数之和,14=6+B,因此B为8,即为氧。
22.(12分)下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
① ⑩ ② ③
④ ⑤ ⑦ ⑧ ⑨
⑥
(1)在这10种元素中,原子半径较小的是_____(填元素符号,稀有气体除外),化学性质最不活泼的元
素是__(填“元素名称”)。
(2)元素⑧的离子结构示意图为________,请用电子式表示化合物④和⑧的形成过程________。
(3)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:_______________________。
(4)元素⑧单质的水溶液中通入元素⑦的某种氧化物,该氧化物被氧化为元素⑦的最高价氧化物的水化
物,反应的化学方程式为_______________________________________。
【答案】(1). F (2). 氩 (3).(4).
(5). 2Al+2NaOH+2HO===2NaAlO +3H↑ (6). Cl +SO +2HO===H SO +2HCl
2 2 2 2 2 2 2 4
【解析】(1)同周期元素原子半径从左到右逐渐减小,同主族元素从上到下原子半径逐渐增大,所
以半径最小的在左上角,应该是F,稀有气体Ar的化学性质稳定,故答案为:F;氩。(2)元素⑧为Cl
元素,氯离子的结构示意图为 ,④和⑧形成的化合物为氯化镁,氯化镁是镁离子和氯离子之间通
过 离 子 键 形 成 的 离 子 化 合 物 , 用 电 子 式 表 示 其 的 形 成 过 程 为 :
, 故 答 案 为 : ,
。(3)元素⑤为Al元素,铝与氢氧化钠
溶液反应生成偏铝酸钠和氢气,化学方程式为:2Al+2NaOH+2H O=2NaAlO +3H ↑。(4)氯气能溶于水,
2 2 2
形成的水溶液是浅黄绿色的,氯气具有氧化性,能氧化二氧化硫,使其褪色,反应的方程式为:
SO +Cl+2H O=HSO +2HCl。
2 2 2 2 4
23.(12分)A、B、C、D、E、F、G的原子序数依次增大的元素,A、D元素的原子最外层电子数
相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D
元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性.G
是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:____________。
(2)D单质与C单质在加热条件下反应产物的电子式 _______,该物质与AC反应的离子方程式
2
________________________________________________。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性.
则甲、乙反应的化学方程式为____________。
的
(4)E 最高价氧化物对应水合物的浓溶液加入G单质,下列说法正确的是____________。
A.常温下两者不发生反应 B. 常温下无现象 ,G单质不溶解
C.受热能发生反应,开始放出氢气 D. 受热能发生反应,开始放出是SO
2的
(5)用电子式写出AC 形成过程________________________________________。
2
【答案】(1). (2).
(3). 2Na O+2H O=4Na++4OH-+O ↑ (4). NaHCO +NaOH=Na CO+H O
2 2 2 2 3 2 3 2
(5). BD (6).
【解析】由分析可知:A为H元素,B为C元素,C为O元素,D为Na元素,E为S元素,F为Cl元
素,G为Fe元素。
(1)S为16号元素,有3个电子层,最外层有6个电子,原子结构示意图为 。
(2)钠在加热条件下与氧气反应生成过氧化钠,过氧化钠是由钠离子与过氧根离子通过离子键结合
而成的离子化合物,电子式为 ,过氧化钠与水反应生成氢氧化钠和氧气,离子方程
式为2NaO+2H O=4Na++4OH-+O ↑。
2 2 2 2
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性,
符合条件的甲、乙两物质为碳酸氢钠和氢氧化钠,反应的化学方程式为NaHCO +NaOH=Na CO+H O
3 2 3 2
(4)S的最高价氧化物对应水合物的浓溶液为浓HSO ,浓硫酸具有很强的氧化性,铁的表面会生成
2 4
一层致密的氧化物薄膜,发生钝化现象,铁和冷的浓硫酸发生钝化,是发生了化学反应;浓硫酸具有很强
的氧化性,因此铁和浓硫酸在加热的条件下反应开始放出的气体是SO ,随着反应的进行,硫酸的浓度变
2
小,才可能有氢气放出,所以BD正确,故答案为BD。
(5)HO为共价化合物,各原子达到稳定结构,用电子式表示形成过程为
2
。
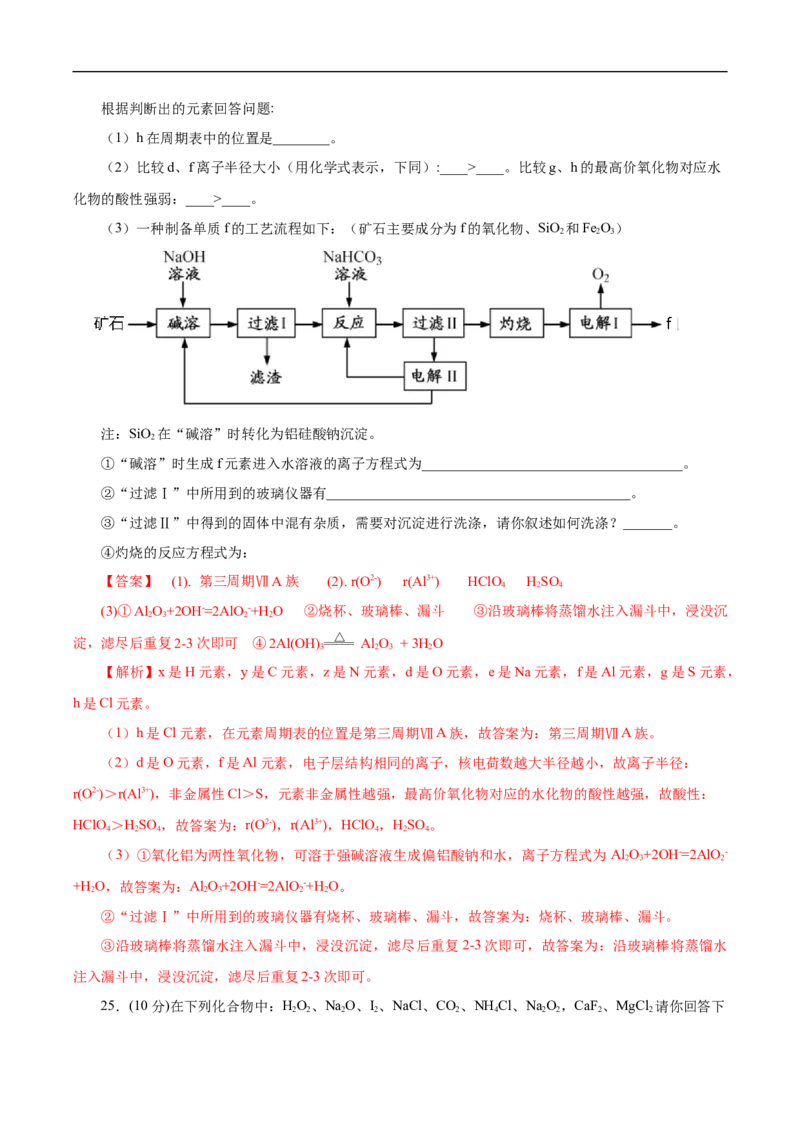
24.(14分)随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最
低负价的变化如下图所示。根据判断出的元素回答问题:
(1)h在周期表中的位置是________。
(2)比较d、f离子半径大小(用化学式表示,下同):____>____。比较g、h的最高价氧化物对应水
化物的酸性强弱:____>____。
(3)一种制备单质f的工艺流程如下:(矿石主要成分为f的氧化物、SiO 和Fe O)
2 2 3
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
①“碱溶”时生成f元素进入水溶液的离子方程式为_____________________________________。
②“过滤Ⅰ”中所用到的玻璃仪器有___________________________________________。
③“过滤Ⅱ”中得到的固体中混有杂质,需要对沉淀进行洗涤,请你叙述如何洗涤?_______。
④灼烧的反应方程式为:
【答案】 (1). 第三周期ⅦA族 (2). r(O2-) r(Al3+) HClO H SO
4 2 4
(3)①Al O+2OH-=2AlO -+H O ②烧杯、玻璃棒、漏斗 ③沿玻璃棒将蒸馏水注入漏斗中,浸没沉
2 3 2 2
△
淀,滤尽后重复2-3次即可 ④2Al(OH)===== Al O + 3H O
3 2 3 2
【解析】x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,
h是Cl元素。
(1)h是Cl元素,在元素周期表的位置是第三周期ⅦA族,故答案为:第三周期ⅦA族。
(2)d是O元素,f是Al元素,电子层结构相同的离子,核电荷数越大半径越小,故离子半径:
r(O2-)>r(Al3+),非金属性Cl>S,元素非金属性越强,最高价氧化物对应的水化物的酸性越强,故酸性:
HClO>HSO ,故答案为:r(O2-),r(Al3+),HClO,HSO 。
4 2 4 4 2 4
(3)①氧化铝为两性氧化物,可溶于强碱溶液生成偏铝酸钠和水,离子方程式为 Al O+2OH-=2AlO -
2 3 2
+H O,故答案为:Al O+2OH-=2AlO -+H O。
2 2 3 2 2
②“过滤Ⅰ”中所用到的玻璃仪器有烧杯、玻璃棒、漏斗,故答案为:烧杯、玻璃棒、漏斗。
③沿玻璃棒将蒸馏水注入漏斗中,浸没沉淀,滤尽后重复2-3次即可,故答案为:沿玻璃棒将蒸馏水
注入漏斗中,浸没沉淀,滤尽后重复2-3次即可。
25.(10分)在下列化合物中:HO、NaO、I、NaCl、CO、NH Cl、NaO,CaF 、MgCl 请你回答下
2 2 2 2 2 4 2 2 2 2列问题:
①I 的电子式为_________________;CaF 的电子式为_________________;
2 2
②只有极性共价键的共价化合物是________________;
③既有离子键又有非极性键的化合物是____________。
④既有离子键又有极性键的化合物是____________。
【答案】(1). (2). CO (3). Na O (4)NH Cl
2 2 2 4
【解析】①I 是由共价键构成的单质,碘原子间形成1对共用电子对,电子式为 ,CaF 为离子
2 2
化合物,钙离子直接用离子符号表示,氟离子需要标出所带电荷及最外层电子,其电子式为
。②只含共价键的化合物是共价化合物,不同非金属元素之间形成极性共价
键 符合条件的是CO 。③活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非
2
极性共价键 则符合条件的是NaO。④既有离子键又有极性键的化合物是NH Cl
2 2 4