文档内容
1.2.2 离子方程式 练习(原卷版)
1.下列反应属于离子反应的是( )
A.氢气还原氧化铜 B.胆矾失去结晶水
C.酸碱中和反应 D.二氧化硫与氧化钙的反应
2.关于离子方程式Cu2++2OH-===Cu(OH) ↓的说法正确的是( )
2
A.可表示所有铜盐和强碱的反应
B.可表示某一个具体的反应,也可以表示一类反应
C.离子方程式中的OH-可代表弱碱或强碱
D.该反应可看到Cu(OH) 白色沉淀
2
3.下列实验设计及其对应的离子方程式均正确的是( )
A.把铁片插入CuSO 溶液中,验证古代湿法冶铜:2Fe+3Cu2+===2Fe3++3Cu
4
B.某气体使澄清石灰水先变浑浊后变澄清,验证该气体是CO:
2
Ca2++2OH-+CO===CaCO ↓+HO CaCO +CO+HO===Ca2++2HCO
2 3 2 3 2 2
C.在小苏打溶液中加入醋酸,验证醋酸比碳酸的酸性强:HCO+H+===CO ↑+HO
2 2
D.若要求用两种单质和一种溶液来测定Zn、Cu、Ag三种金属的活动性顺序,可用Zn、Cu和AgNO
3
溶液:Zn+2Ag+===Zn2++2Ag
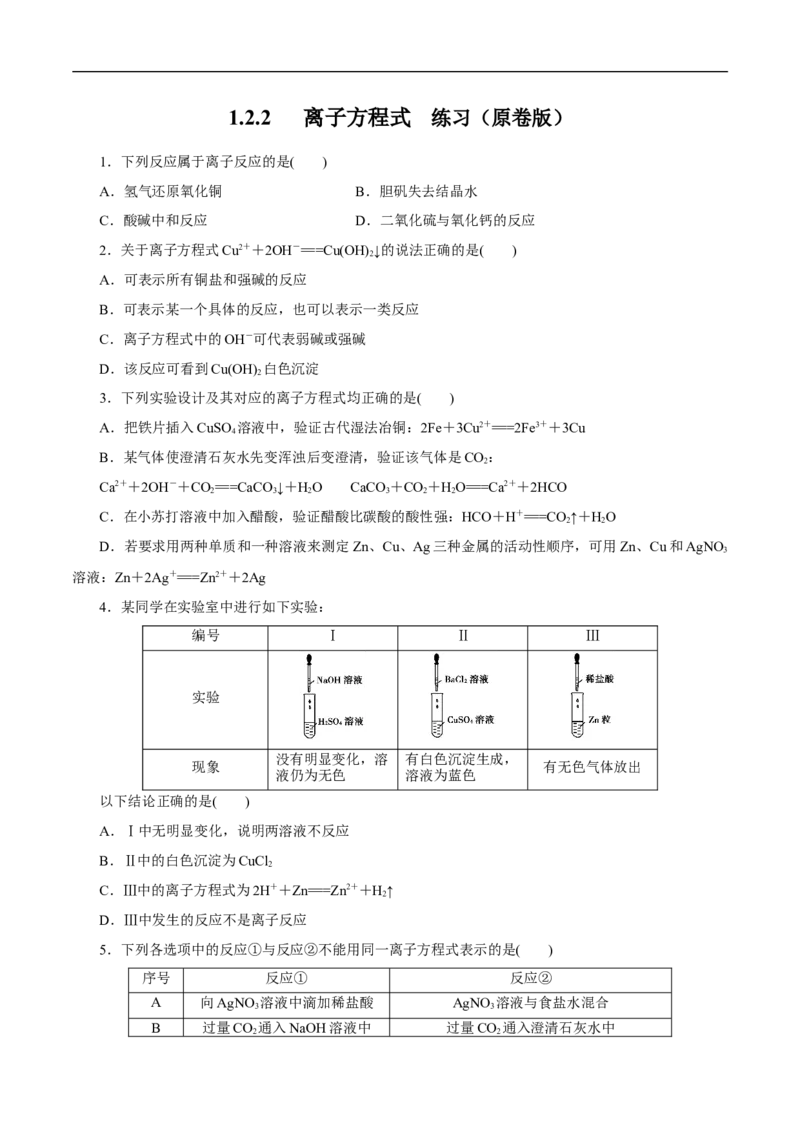
4.某同学在实验室中进行如下实验:
编号 Ⅰ Ⅱ Ⅲ
实验
没有明显变化,溶 有白色沉淀生成,
现象 有无色气体放出
液仍为无色 溶液为蓝色
以下结论正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为CuCl
2
C.Ⅲ中的离子方程式为2H++Zn===Zn2++H↑
2
D.Ⅲ中发生的反应不是离子反应
5.下列各选项中的反应①与反应②不能用同一离子方程式表示的是( )
序号 反应① 反应②
A 向AgNO 溶液中滴加稀盐酸 AgNO 溶液与食盐水混合
3 3
B 过量CO 通入NaOH溶液中 过量CO 通入澄清石灰水中
2 2C 向烧碱溶液中滴加稀盐酸 向HSO 溶液中滴加KOH溶液
2 4
D 向BaCl 溶液中滴加稀HSO 向Ba(OH) 溶液中滴加CuSO 溶液
2 2 4 2 4
6.实验室有三缸废液,分别含有NaCO、Ca(OH) 和HCl。且它们的物质的量之比为1∶1∶2。要让三缸
2 3 2
废液混合后,所得溶液的溶质只有NaCl,应选择的混合顺序是( )
A.先将NaCO 废液和Ca(OH) 废液混合,再与HCl废液混合
2 3 2
B.先将NaCO 废液和HCl废液混合,再与Ca(OH) 废液混合
2 3 2
C.先将Ca(OH) 废液和HCl废液混合,再与NaCO 废液混合
2 2 3
D.将NaCO 废液和Ca(OH) 废液同时慢慢倒入HCl废液中
2 3 2
7.能正确表示下列化学反应的离子方程式是( )
A.氢氧化钡溶液与硝酸的反应OH-+H+ HO
2
B.澄清的石灰水与稀盐酸反应Ca(OH) +2H+ Ca2++2H O
2 2
C.铜片插入硝酸银溶液中Cu+Ag+ Cu2++Ag
D.碳酸钡溶于稀盐酸中C +2H+ HO+CO↑
O2- 2 2
3
8.下列各组中的离子,能在溶液中大量共存的是( )
A.Mg2+、H+、Cl-、OH-
B.Na+、Ba2+、C 、N
O2- O-
3 3
C.Na+、H+、Cl-、C
O2-
3
D.K+、Cu2+、N 、S
O- O2-
3 4
9.在某无色溶液中含有大量的Ba2+、H+、Cl-,该溶液中还可能大量存在的离子是( )
A.N B.OH- C.S D.Cu2+
H+ O2-
4 4
10.已知NaHSO 在溶液中完全电离为金属阳离子、H+和酸根离子:
4
(1)写出NaHSO 在水溶液中电离的方程式:________________。
4
(2)NaHSO 属于“酸”“碱”“盐”中的________,你的选择理由是__________________________。
4
(3) ① 若将 NaHSO 与 Ba(OH) 在溶液中按物质的量比为 2∶1 混合,反应的离子方程式是
4 2
_______________________________________________________________________________。
②若将 NaHSO 与 Ba(OH) 在溶液中按物质的量比 1∶1 混合,反应的离子方程式是:
4 2
____________________________________________________________________________________。11.有一固体混合物,可能由NaCO 、NaSO 、CuSO 、CaCl 、NaCl等混合而成,为检验它们,做
2 3 2 4 4 2
了以下实验:
①将固体混合物溶于水中,搅拌后得无色透明溶液;
②往此溶液中滴加硝酸钡溶液,有白色沉淀产生;
③过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解。
根据上述实验事实,回答下列问题:
(1)原固体混合物中一定含有的物质是________,一定不含有的物质是________,可能含有的物质是
________( 以 上 空 格 均 填 写 化 学 式 ) 。 对 可 能 含 有 的 物 质 , 可 采 用 向 滤 液 中 滴 加
________________________________________________________________________
溶液的方法来检验。
(2)写出步骤③中的离子方程式
________________________________________________________________________。
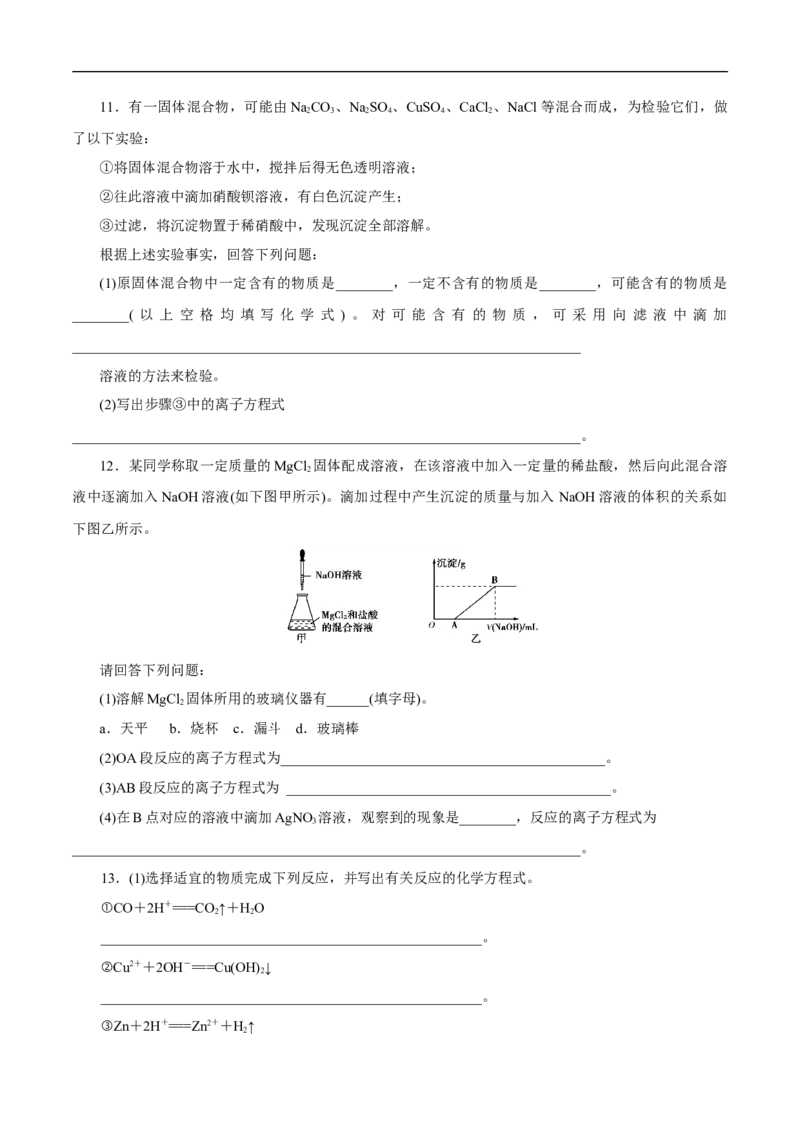
12.某同学称取一定质量的MgCl 固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶
2
液中逐滴加入NaOH溶液(如下图甲所示)。滴加过程中产生沉淀的质量与加入 NaOH溶液的体积的关系如
下图乙所示。
请回答下列问题:
(1)溶解MgCl 固体所用的玻璃仪器有______(填字母)。
2
a.天平 b.烧杯 c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为______________________________________________。
(3)AB段反应的离子方程式为 ______________________________________________。
(4)在B点对应的溶液中滴加AgNO 溶液,观察到的现象是________,反应的离子方程式为
3
________________________________________________________________________。
13.(1)选择适宜的物质完成下列反应,并写出有关反应的化学方程式。
①CO+2H+===CO ↑+HO
2 2
______________________________________________________。
②Cu2++2OH-===Cu(OH) ↓
2
______________________________________________________。
③Zn+2H+===Zn2++H↑
2_____________________________________________________。
(2)完成离子反应,并改写成化学方程式。
①________+Ag+===________+Ag
_____________________________________________________。
②Fe O+________===Fe3++________
2 3
_____________________________________________________。
③CaCO +________===CO ↑+________+________
3 2
_____________________________________________________。