文档内容
第三章� 第 1节 铁及其化合物课时作业2022-2023学年高
中化学人教版(2019)必修第一册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.纯净铁的物理性质有
①光亮的银白色 ②黑色 ③在潮湿的空气中易被腐蚀 ④有延展性 ⑤能导电导热
⑥硬而脆 ⑦能被磁铁吸,引易被磁化
A.①③④⑤⑦ B.①④⑤⑦ C.①③⑤⑦ D.全部
2.下列物质之间的转化,不能由化合反应一步完成的是
A. B.
C. D.
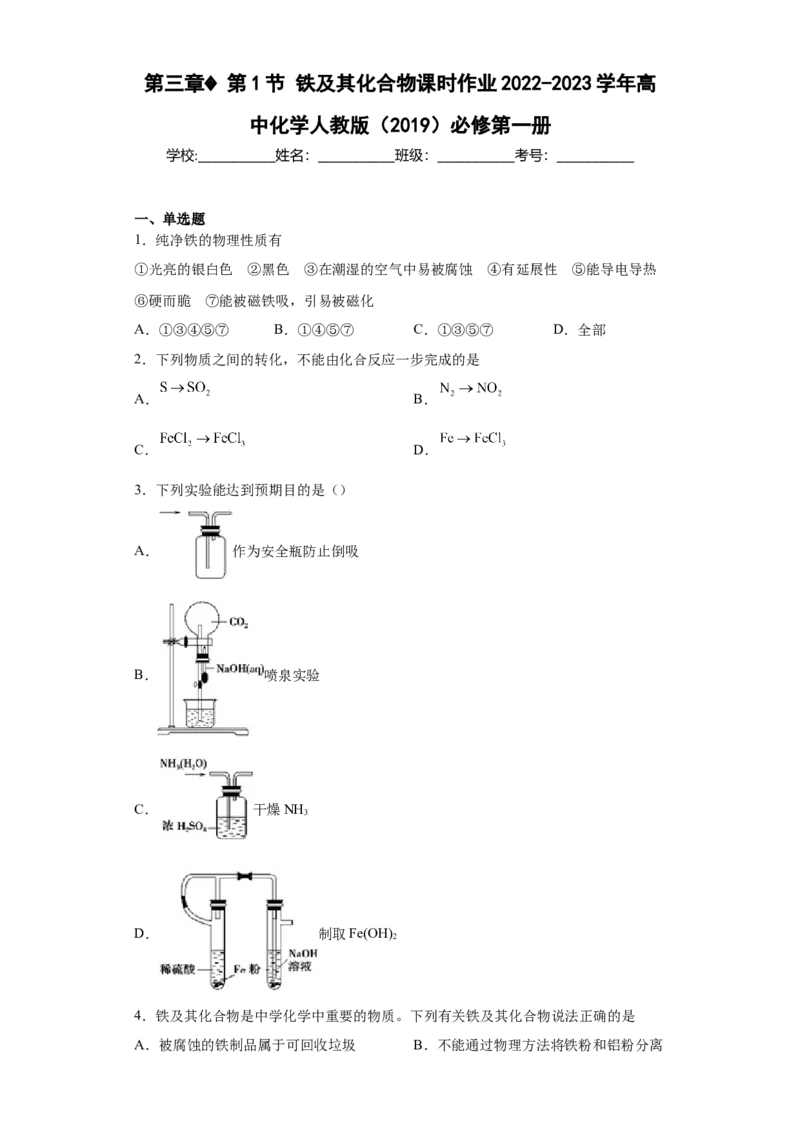
3.下列实验能达到预期目的是()
A. 作为安全瓶防止倒吸
B. 喷泉实验
C. 干燥NH
3
D. 制取Fe(OH)
2
4.铁及其化合物是中学化学中重要的物质。下列有关铁及其化合物说法正确的是
A.被腐蚀的铁制品属于可回收垃圾 B.不能通过物理方法将铁粉和铝粉分离C.铁锈的主要成分是 D.指南针中因含有 而可以指定方位
5.下列铁的化合物可以分别通过化合反应、置换反应、复分解反应生成的是
A.FeCl B.Fe O C.Fe(OH) D.Fe (SO )
3 3 4 3 2 4 3
6.关于铁及其化合物下列说法正确的是
A.铁是地壳含量最高的金属元素
B.四氧化三铁是一种红棕色难溶于水的固体
C.铁与灼热水蒸气反应生成氧化铁和氢气
D.铁在氯气蒸汽中燃烧可生成FeCl
3
7.向FeI 溶液中滴加适量氯水,将反应后溶液分3份,甲试管中滴加淀粉溶液,乙试
2
管滴加KSCN溶液,丙试管中滴加酸性高锰酸钾溶液,下列说法正确的是
A.若甲试管溶液呈蓝色,则乙试管溶液一定呈血红色
B.若甲试管溶液呈蓝色,则乙试管溶液可能无明显现象
C.乙试管溶液呈血红色,则甲试管溶液不可能呈蓝色
D.甲试管溶液呈蓝色,丙试管中紫红色褪去,说明滴加氯水后的溶液中一定存在
Fe3+和Fe2+
8.下列反应的离子方程式正确的是
A.将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+
B.将磁性氧化铁溶于盐酸:Fe O+8H+=3Fe3++4H O
3 4 2
C.FeCl 酸性溶液放在空气中变质:2Fe2++4H++O =2Fe3++2H O
2 2 2
D.将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H ↑
2
9.下列离子方程式书写正确的是( )
A.将氯气通入氯化亚铁溶液:2Fe2++Cl═2Fe3++2Cl﹣
2
B.在 NaSiO 溶液中加入盐酸:NaSiO + 2H+ = 2Na+ + H SiO↓
2 3 2 3 2 3
C.氢氧化钡溶液与稀硫酸:Ba2++OH﹣+H++SO ═BaSO ↓+H O
4 2
D.用食醋除水垢的原理:2H++CaCO =Ca2++H O+CO↑
3 2 2
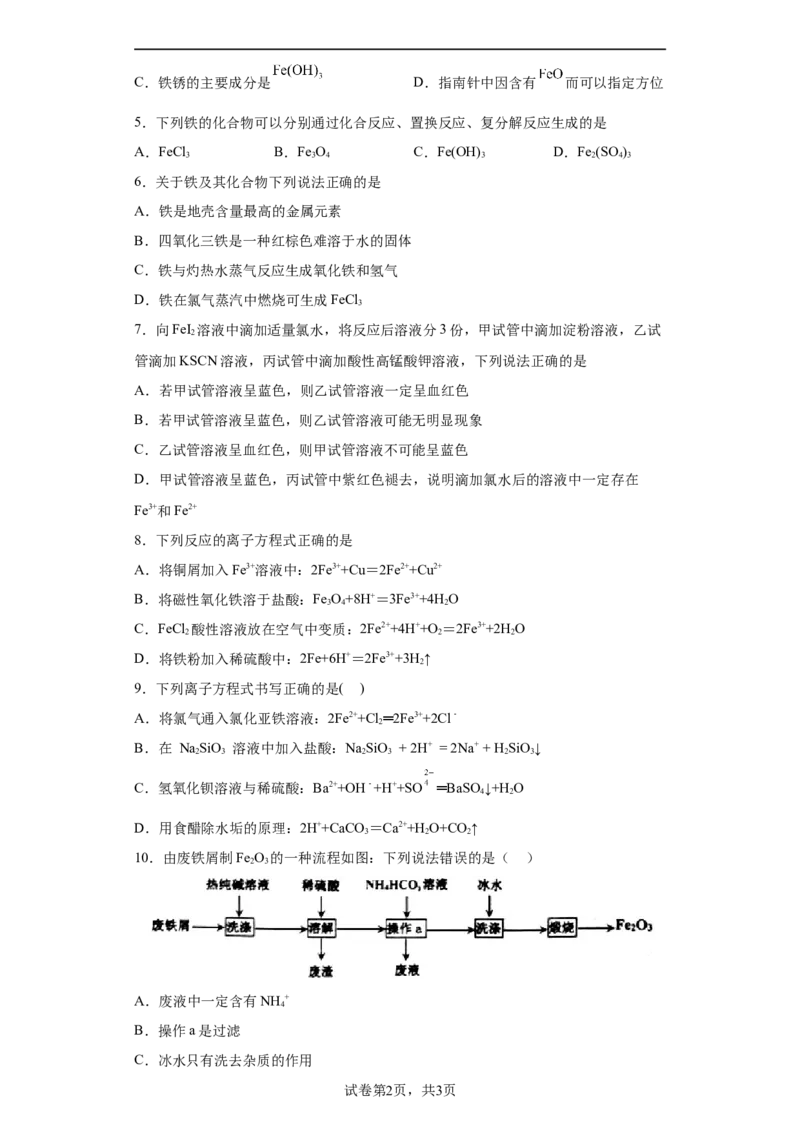
10.由废铁屑制Fe O 的一种流程如图:下列说法错误的是( )
2 3
A.废液中一定含有NH +
4
B.操作a是过滤
C.冰水只有洗去杂质的作用
试卷第2页,共3页D.Fe O 俗名铁红,可用作红色颜料
2 3
11.下列说法不正确的是
A.工业上利用电解熔融氯化钠的方法来制备金属钠
B.可用丁达尔效应区分胶体和溶液
C.工业上利用焦炭与二氧化硅在高温下反应可直接制得高纯度的硅
D.医疗上硫酸亚铁可用于生产防治缺铁性贫血的药剂
12.某红色粉末样品可能含有 和 中的一种或两种,为探究其组成,研究组同
学取少量样品加入过量稀硫酸进行实验。(已知: )
下列有关说法正确的是
A.若固体部分溶解,则样品中一定含有 ,一定不含有
B.若固体全部溶解,则发生的离子反应只有:
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红,则样品中
为2∶1
D.另取ag样品在空气中充分加热至质量不再变化,称其质量为bg(b>a),则混合物中
的质量分数为
二、填空题
13.铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
(1)铁元素有三种常见的氧化物,分别是 FeO、Fe O、Fe O 其中具有磁性的是
2 3 3 4.
_______,可作为红色颜料的是_______。
(2)某补铁口服液中含有 Fe2+,为检验其是否被氧化变质,可取少量该口服液,向其中
滴加 KSCN 溶液,若溶液变为_______色,则说明其已变质。向该口服液中加入维生
素 C 可防止其被氧化变质,此过程中利用了维生素 C 的_______性。
(3)FeCl 可作为铜电路板的腐蚀液,其反应原理为Cu与FeCl 溶液反应生成FeCl 和
3 3 2
CuCl ,该反应的化学方程式为_______。向反应后的溶液中加入_______,可回收
2
Cu,并得到FeCl 溶液。
2
14.(1)人体内的铁元素以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还
原成Fe2+,有利于人体吸收。这句话说明维生素C在这一反应中起的作用是_______。
(填“氧化剂”或者“还原剂”)
(2)实验室可用KMnO 和浓盐酸反应制取氯气:2KMnO +16HCl(浓)=2KCl+2MnCl +
4 4 2
5Cl↑+8HO
2 2
①用双线桥标出电子转移的方向和数目__________________。
②将上述配平的化学方程式改写为离子方程式__________________。
③浓盐酸在反应中显示出来的性质是_________。
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
④若产生 0.5 molCl ,则被氧化的HCl______mol,转移的电子的数目约为_____个。
2
(3)根据反应Cu+4HNO (浓)=Cu(NO)+2NO↑+2H O,回答下列问题:
3 3 2 2 2
①还原产物是______________。
②氧化剂与氧化产物的物质的量之比是____________。
③如果反应中转移了0.15 mol电子,则产生的气体在标准状况下体积为_________L。
三、实验题
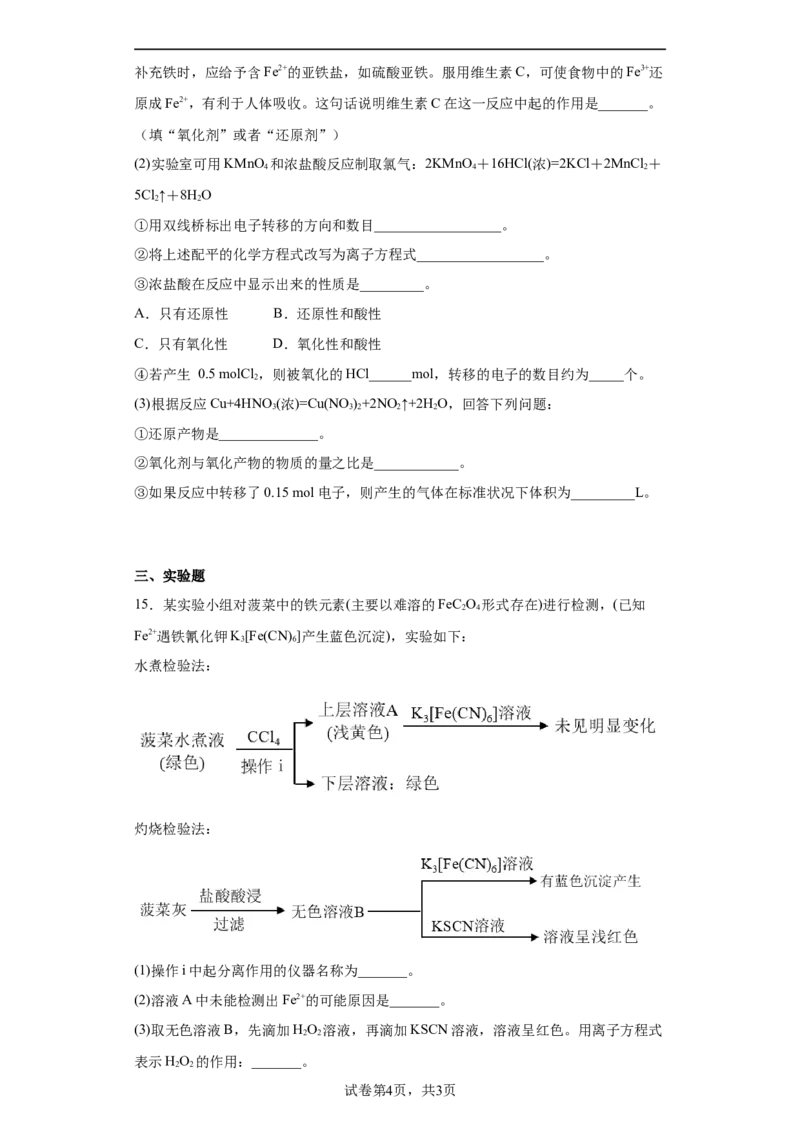
15.某实验小组对菠菜中的铁元素(主要以难溶的FeC O 形式存在)进行检测,(已知
2 4
Fe2+遇铁氰化钾K[Fe(CN) ]产生蓝色沉淀),实验如下:
3 6
水煮检验法:
灼烧检验法:
(1)操作i中起分离作用的仪器名称为_______。
(2)溶液A中未能检测出Fe2+的可能原因是_______。
(3)取无色溶液B,先滴加HO 溶液,再滴加KSCN溶液,溶液呈红色。用离子方程式
2 2
表示HO 的作用:_______。
2 2
试卷第4页,共3页(4)甲同学取少量无色溶液B,滴加酸性KMnO 溶液,振荡后,溶液紫色消失,因此得
4
出结论,溶液B合有Fe2+。乙同学认为甲同学的实验方法不严谨,设计并完成如下实
验:用稀硝酸溶解菠菜灰,产生的无色气体使澄清石灰水变浑浊,得到的无色溶液中
滴加AgNO 溶液,产生白色沉淀(Ag C O)。甲同学反思自己的方法不严谨,理由是
3 2 2 4
_______。
四、有机推断题
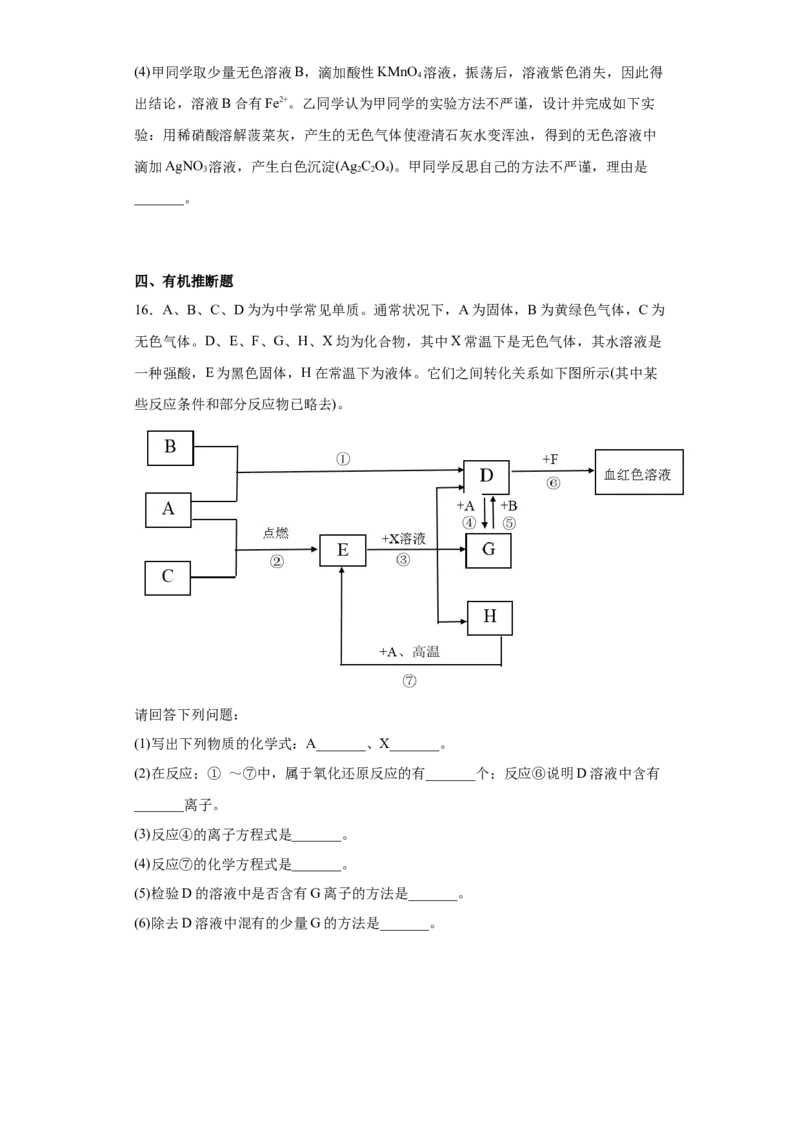
16.A、B、C、D为为中学常见单质。通常状况下,A为固体,B为黄绿色气体,C为
无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是
一种强酸,E为黑色固体,H在常温下为液体。它们之间转化关系如下图所示(其中某
些反应条件和部分反应物已略去)。
请回答下列问题:
(1)写出下列物质的化学式:A_______、X_______。
(2)在反应;① ~⑦中,属于氧化还原反应的有_______个;反应⑥说明D溶液中含有
_______离子。
(3)反应④的离子方程式是_______。
(4)反应⑦的化学方程式是_______。
(5)检验D的溶液中是否含有G离子的方法是_______。
(6)除去D溶液中混有的少量G的方法是_______。参考答案:
1.B
【详解】纯净的铁为银白色固体,具有很强的抗腐蚀能力,具有延展性,能导电导热,能
被磁铁吸,引易被磁化;只有①④⑤⑦符合题意,故答案选B。
2.B
【详解】A.硫在氧气中燃烧生成二氧化硫,可以由化合反应一步完成,A不符合题意;
B.氮气和氧气在放电条件下生成一氧化氮,不可以由化合反应一步完成,B符合题意;
C.氯化亚铁和氯气反应生成氯化铁,可以由化合反应一步完成,C不符合题意;
D.铁和氯气反应生成氯化铁,可以由化合反应一步完成,D不符合题意;
故选B。
3.B
【详解】 作为安全瓶防止倒吸时,进气管不能伸入安全瓶太长,或图中装置中都用短导
管,故A错误;
B.二氧化碳易与碱反应而在碱液中的溶解度很大,挤压胶头滴管中的碱液能引发喷泉实验,
故B正确;
C.氨气能与浓硫酸反应生成硫酸铵,不能用浓硫酸干燥,故C错误;
D.由图可知,左端反应生成氢气和硫酸亚铁,而左端导管太短,产生的氢气无法将硫酸亚
铁溶液压入右端试管中,则不能制取氢氧化亚铁,故D错误;
故选B.
4.A
【详解】A.金属可以回收再利用,因此被腐蚀的铁制品属于可回收垃圾,故A正确;
B.铁能被磁铁吸引,因此可以通过物理方法将铁粉和铝粉分离,故B错误;
C.铁锈的主要成分是 ,故C错误;
D.指南针中因含有 而可以指定方位,故D错误。
综上所述,答案为A。
5.A
【详解】A.FeCl 可以由Fe和Cl 直接化合生成,也可以有Cl 和FeBr 通过置换反应生成,
3 2 2 3
也可以用氢氧化铁与盐酸通过复分解反应生成,故A符合题意;
B.Fe O 可由Fe与氧气化合生成,也可由Fe与水蒸气通过置换反应生成,不能通过复分
3 4
解反应得到,故B不符合题意;C.氢氧化铁不能由置换反应得到,故C不符合题意;
D.硫酸铁不能由置换反应得到,故D不符合题意;
答案为A。
6.D
【详解】A.地壳中含量最高的金属是铝,铁是地壳含量第二的金属元素,故A错误;
B.四氧化三铁是一种黑色晶体,红棕色难溶于水的固体是三氧化二铁,故B错误;
C.铁与灼热水蒸气反应生成四氧化三铁和氢气,故C错误;
D.铁在氯气蒸汽中燃烧,生成红棕色的烟,然后可产物为FeCl ,故D正确;
3
答案选D。
【点睛】铁是目前应用最广泛的金属,但不是地壳中含量最高的金属,为易错点。
7.B
【详解】试题分析:A、还原性I->Fe2+,氯气先氧化I-,后氧化Fe2+,所以若甲试管溶液呈
蓝色,说明氯气和反应生成碘,如果氯水少量,则Fe2+可能未被氧化,则乙试管溶液不一
定呈血红色,A错误;B、若甲试管溶液呈蓝色,则乙试管溶液可能无明显现象,B正确;
C、如果乙试管溶液呈血红色,说明Fe2+已被氧化,则I-一定完全被氧化为碘单质,则甲试
管溶液一定呈蓝色,C错误;D、甲试管溶液呈蓝色,说明I-被氧化生成碘,丙试管中紫红
色褪去,溶液中有Fe2+,但不一定有Fe3+,D错误。答案选B。
考点:氧化还原反应
8.A
【详解】A.题中离子方程式符合实验事实,原子、电荷均守恒,A项正确;
B.该离子方程式中电荷不守恒,Fe O 中Fe有两种价态:+2、+3,所以产物中有Fe2+、
3 4
Fe3+,正确的离子方程式为:Fe O+8H+=2Fe3++Fe2++4H O,B项错误;
3 4 2
C.该离子方程式中电荷不守恒,得失电子不守恒,正确的离子方程式为:4Fe2++4H++O =
2
4Fe3++2H O,C项错误;
2
D.离子方程式不符合客观事实,将铁粉加入稀硫酸中反应后只能产生Fe2+和H,正确的
2
离子方程式为:Fe+2H+=Fe2++H ↑,D项错误;
2
答案选A。
9.A
【详解】A. 将氯气通入氯化亚铁溶液得到氯化铁溶液,则离子方程式为:2Fe2++Cl═2Fe3+
2
+2Cl﹣,A正确;
答案第2页,共2页B. 在 NaSiO 溶液中加入盐酸得到硅酸沉淀和氯化钠溶液,则离子方程式: + 2H+
2 3
=H SiO↓,B不正确;
2 3
C. 氢氧化钡溶液与稀硫酸生成硫酸钡和水,则离子方程式:Ba2++2OH﹣+2H++SO
═BaSO ↓+2H O,C不正确;
4 2
D. 用食醋除水垢,生成可溶性的醋酸钙、水和二氧化碳,则离子方程式:
2CHCOOH+CaCO =Ca2++ +H O+CO↑,D不正确;
3 3 2 2
答案选A。
10.C
【分析】根据流程:用热的纯碱溶液可去除废铁屑表面的油污,再加入稀硫酸将铁转化为
亚铁离子,加入碳酸氢铵促进亚铁离子水解得到沉淀,通过过滤、冰水洗涤、煅烧得到氧
化铁,据此分析作答。
【详解】A.根据上述分析可知,加入碳酸氢铵促进亚铁离子水解得到沉淀,所以废液中一
定含有NH +,故A正确;
4
B.加入碳酸氢铵得到沉淀和溶液,所以操作a为过滤 故B正确;
C.冰水既可洗去杂质又可减少固体的溶解,故C错误;
D. Fe O 俗称铁红,可用作红色颜料, 故D正确;
2 3
答案:C。
11.C
【详解】A.金属钠是活泼金属,则可利用电解熔融氯化钠的方法来制备金属钠,故A正
确;
B.胶体能产生丁达尔效应,溶液不能,故B正确;
C.利用焦炭与二氧化硅在高温下反应可制得粗硅,故C错误;
D.硫酸亚铁能治疗缺铁性贫血,可用于生产防治缺铁性贫血的药剂,故D正确;
答案选C。
12.D
【详解】A.固体若是 和 的混合物,放入足量稀硫酸中会有Cu生成,Cu能将
Fe3+还原为Fe2+剩余铜,A错误;B.固体全部溶解,若固体是 和 的混合物,放入足量稀硫酸中会有Cu生成,Cu
恰好能将Fe3+还原为Fe2+, 、 、
,B错误;
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红色,因为 溶于硫酸生成Cu和
CuSO ,而硫酸不能溶解Cu,所以混合物中必须有 存在,使其生成的Fe3+溶解产生的
4
Cu,反应的有关离子方程式为 、 、
,说明样品中 为1∶1,C错误;
D. , ,故混合物中Cu O的质量分数为:
2
,D正确;
故选D。
13. Fe O Fe O 红 还原 Cu+2FeCl =2FeCl +CuCl 铁
3 4 2 3 3 2 2
粉
【详解】(1)铁元素有三种常见的氧化物,分别是 FeO、Fe O、Fe O。其中Fe O 又叫做
2 3 3 4 3 4
磁性氧化铁,具有磁性的是Fe O,可作为红色颜料的是Fe O,如红色油漆中就是加入了
3 4 2 3
氧化铁;
(2)若Fe2+变质,则生成Fe3+,可使用KSCN溶液检验,若变红色,则证明其被氧化变质;
向该口服液中加入维生素 C 可防止其被氧化变质,也就是说维生素C能将Fe3+转化为
Fe2+,从而说明维生素 C 具有还原性;
(3)Cu与FeCl 溶液反应生成FeCl 和CuCl ,该反应的化学方程式为
3 2 2
Cu+2FeCl =2FeCl +CuCl ;想从溶液中还原出铜,同时得到FeCl 溶液,只能加入铁粉。
3 2 2 2
答案第4页,共2页14. 还原剂
B 1
NO 2:1 3.36
2
【详解】(1)维生素C可使食物中的Fe3+还原成Fe2+,Fe元素的化合价降低,作氧化剂,则
维生素C具有还原性,作还原剂;
(2) ①元素化合价的变化分别为:Mn元素由KMnO 的+7价变成MnCl 中的+2价,化合价
4 2
降低,所以KMnO 是氧化剂,一个KMnO 得5个电子生成MnCl ,Cl元素由 HCl中的−1
4 4 2
价变成Cl 中的0价,化合价升高,所以 HCl是还原剂,生成一个Cl 分子需失2个电子,
2 2
所以双线桥法表示该反应的电子转移的方向和数目为:
;
②反应2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8HO中,钾离子的浓度反应前后未
4 2 2 2
变,而氯离子部分参加离子反应,所以离子反应的方程式为:
;
③通过以上分析知,16molHCl,其中有10molHCl起还原剂的作用,发生氧化反应;还有
6molHCl价态没变,生成了氯化锰、氯化钾,生成了盐起了酸的作用;
故答案为:B;
④此反应中氯元素的化合价升高被氧化是还原剂,得到的氯气是氧化产物,产生1mol
Cl,则转移的电子的物质的量为2mol,则生成0.5mol Cl ,被氧化的HCl是1mol,则转移
2 2的电子的物质的量为1mol,数目约是 ;
(3)①硝酸中氮元素的化合价由+5价降到+4价,化合价降低被还原,发生还原反应,对应
的产物NO 是还原产物;
2
②反应Cu+4HNO (浓)=Cu(NO)+2NO↑+2H O中,硝酸中氮元素化合价降低作氧化剂,铜
3 3 2 2 2
元素化合价升高对应的的硝酸铜是氧化产物,依据电子守恒得:氧化剂与氧化产物的物质
的量之比是2:1;
③设二氧化氮的物质的量是xmol,则x (5-4)=0.15mol,解得x=0.15mol,其在标准状况下
的体积是0.15mol 22.4L/mol=3.36L。 ×
15. 分液×漏斗 铁元素主要以难溶的FeC
2
O
4
形式存在,Fe2+的浓度小,
所以溶液A中未能检测出Fe2+ 酸性条件下,
HC O 和Cl-都可能将MnO -还原
2 2 4 4
【分析】菠菜水煮液和四氯化碳溶液分液后,向上层溶液中加入K[Fe(CN) ]无明显现象,
3 6
表明不含Fe2+;菠菜灰经过盐酸酸浸后的滤液,向滤液中加入K[Fe(CN) ],有蓝色沉淀,
3 6
表明溶液中有Fe2+,向滤液中加入KSCN溶液,溶液呈浅红色表明溶液中有Fe3+。
【详解】(1)操作i是分离互不相容的液体,操作名称是分液,使用的仪器是分液漏斗;
(2)铁元素主要以难溶的FeC O 形式存在,Fe2+的浓度小,所以溶液A中未能检测出Fe2+;
2 4
(3)H O 把Fe2+氧化为Fe3+,反应的离子方程式是: ;
2 2
(4)用盐酸溶解菠菜灰得到的溶液B含有HC O 和Cl-,酸性条件下,HC O 和Cl-都可能将
2 2 4 2 2 4
MnO -还原,所以滴加酸性KMnO 溶液,振荡后,溶液紫色消失,不能证明溶液B含有
4 4
Fe2+。
16. Fe HCl 5 Fe3+ 2Fe3++Fe=3Fe2+ 3Fe+4HO(g)
2
Fe O+4H 取少量D的溶液,向其中加入几滴酸性KMnO 溶液,若紫红色褪去,
3 4 2 4
则含有Fe2+,若紫红色不褪去,则不含Fe2+。(或用六氰合铁酸钾) 向混合液中通入足量
的氯气(或加入足量的HO)
2 2
【分析】A为固体,B为黄绿色气体,说明B为Cl,D与F反应得到血红色溶液,结合转
2
化关系可知,固体A为Fe,D为FeCl ,F为KSCN,由D与G之间的相互转化,可知G
3
答案第6页,共2页为FeCl ,Fe与无色气体C反应得到E,E与X反应得到D、G、H,且X常温下是无色气
2
体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体,可推知C为O,E为
2
Fe O,X为HCl,H为HO,据此解答。
3 4 2
【详解】(1)由上述分析可知,A为Fe,X为HCl,故答案为Fe;HCl;
(2)在反应①~⑦中,①为铁和氯气发生的氧化还原反应,②为铁和氧气发生的氧化还原反
应,③为四氧化三铁和盐酸发生的复分解反应,不是氧化还原反应,④为氯化铁和铁发生
的氧化还原反应,⑤为氯化亚铁和氯气发生的氧化还原反应,⑥是氯化铁和硫氰酸盐发生
的复分解反应,不是氧化还原反应,反应⑦是铁与水在高温下的置换反应,是氧化还原反
应,所以属于氧化还原反应的有①②④⑤⑦,共5个,反应⑥遇KSCN溶液呈血红色,说
明D溶液中有Fe3+,故答案为5;Fe3+;
(3)反应④的离子方程式是:2Fe3++Fe=3Fe2+,故答案为2Fe3++Fe=3Fe2+;
(4)反应⑦是铁在水蒸气中发生的反应生成四氧化三铁和氢气,反应的化学方程式为:
3Fe+4H O(g) Fe O+4H ,故答案为3Fe+4H O(g) Fe O+4H ;
2 3 4 2 2 3 4 2
(5)检验FeCl 溶液中是否有FeCl 的方法是:向溶液中滴加高锰酸钾溶液,看紫色高锰酸钾
3 2
溶液是否褪色,如果褪色则说明溶液有亚铁离子,否则没有,故答案为向溶液中滴加高锰
酸钾溶液,看紫色高锰酸钾溶液是否褪色,如果褪色则说明溶液有亚铁离子,若紫红色不
褪去,则不含Fe2+;
(6)除去FeCl 溶液中混有的少量FeCl 的方法是:向混合溶液中通入足量的氯气,故答案为
3 2
向混合溶液中通入足量的氯气。答案第8页,共2页