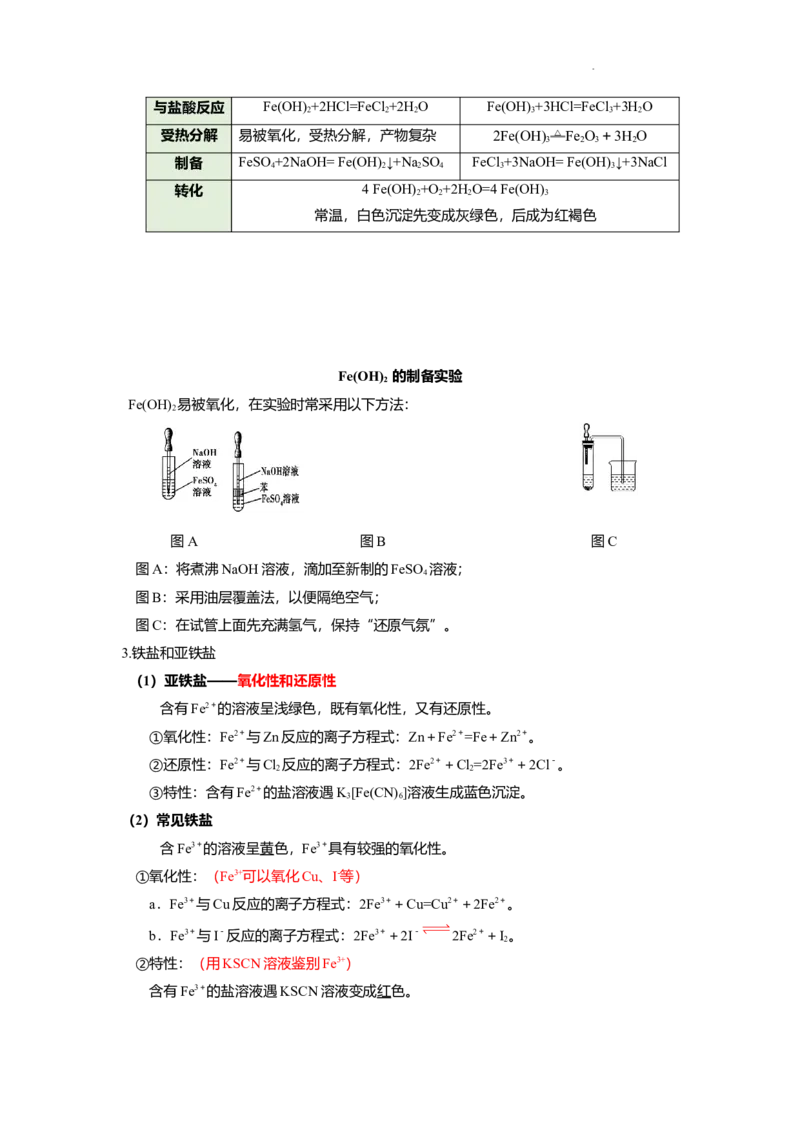
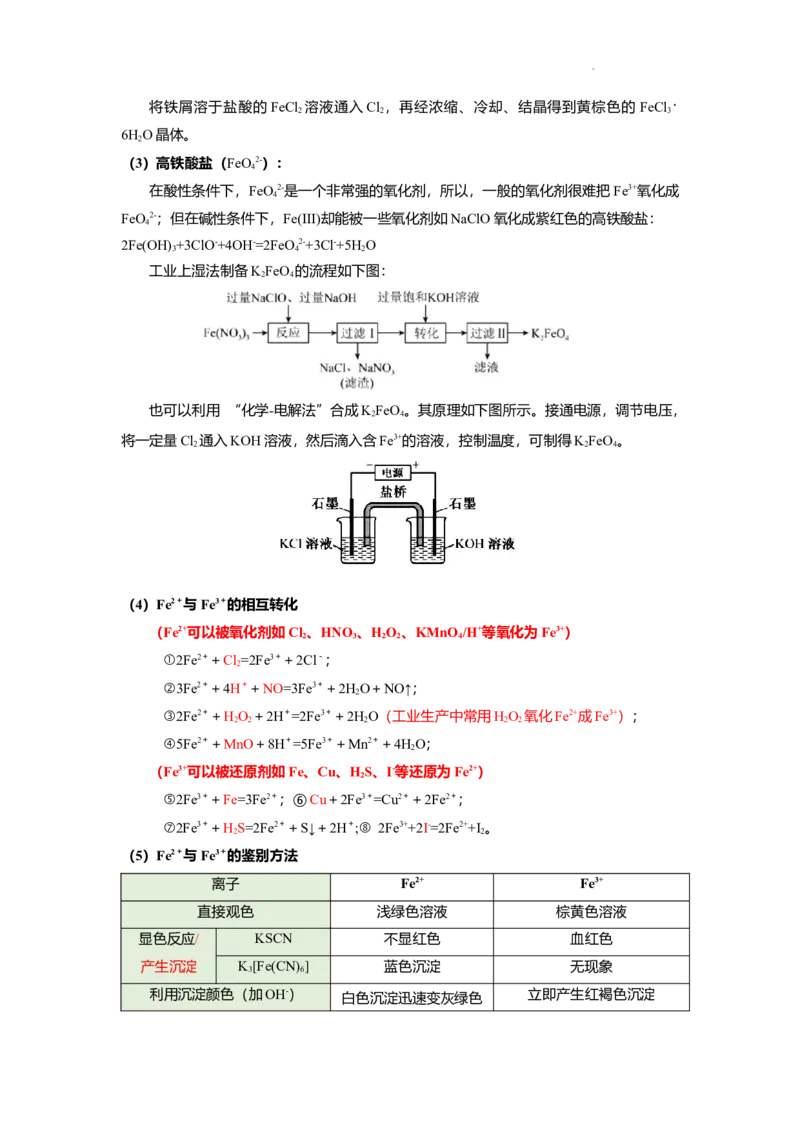
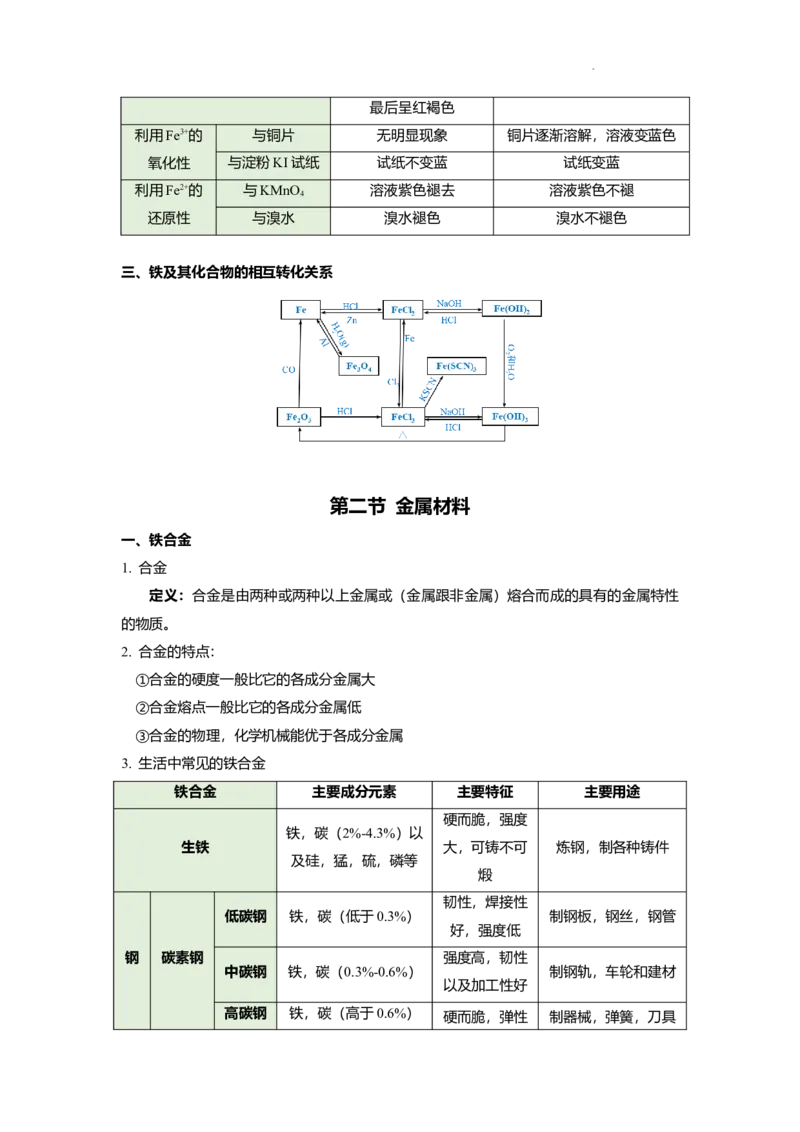
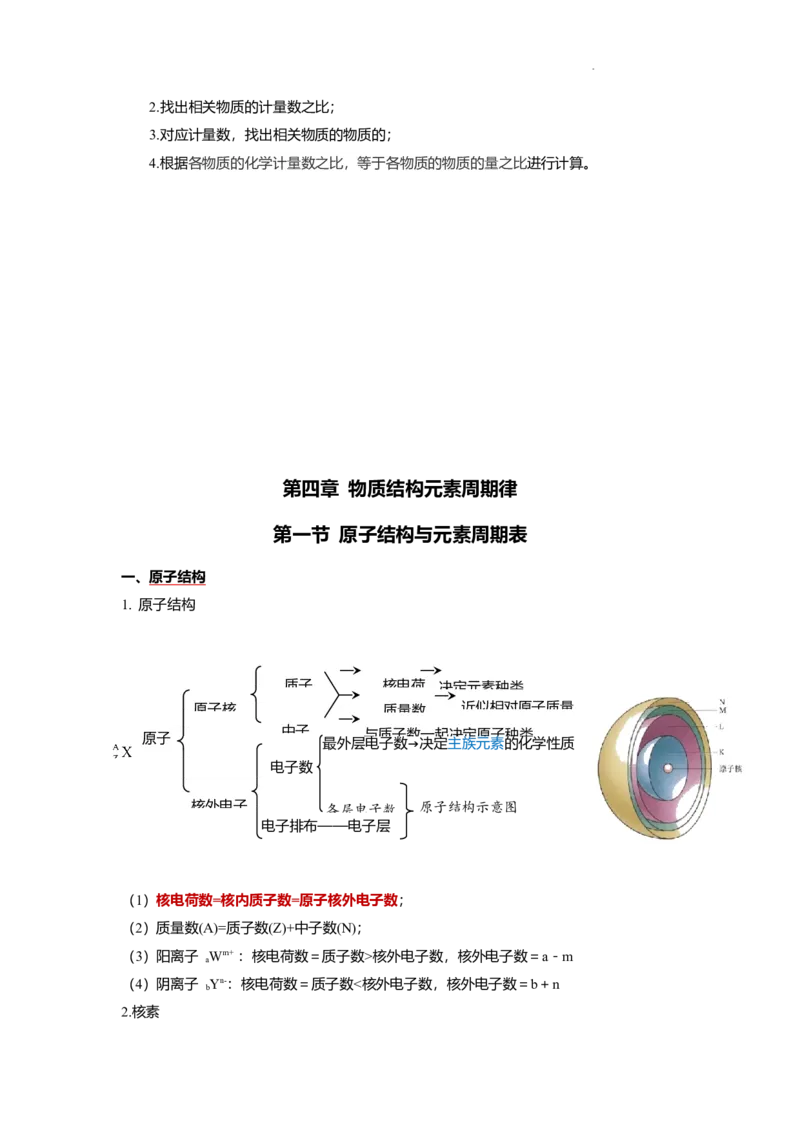
文档内容
高中化学人教版(2019)必修1知识点
第一章 物质及其变化
第一节 物质的分类及转化
一、物质的分类
1.根据物质的组成和性质分类
任何物质都是由元素组成的,每一种元素都可以形成单质,有的单质有多种形态,如
金刚石、石墨和C 都属于碳单质,像这样,由同一种元素形成的性质不同的几种单质,
60
叫做这种元素的同素异形体。
2.树状分类法
混合物:溶液(混合物可以理解为无法书写化学式的物质)
物 质 金属单质
单质 非金属单质
稀有气体 金属氧化物
氧化物
非金属氧化物
纯净物
无机
一元酸(如HNO 、H BO 、H PO (次磷酸))
化合物 非金二属元氧酸化(物 如H SO 3 、H 3 PO 3 (亚 3 磷酸 2 ))
酸 2 4 3 3
多元酸(如H PO )
3 4
氧化物
化合物 碱
盐
有机化合物
3.分散系及其分类
(1)由一种或几种物质以粒子的形式分散到另一种物质里形成的体系叫做分散系。
(2)分散系中被分散成粒子的物质叫分散质;粒子分散在其中的物质叫分散剂。
例如:在NaCl溶液中,溶质NaCl是分散质,溶剂水是分散剂。
根据分散质粒子直径大小分为以下几种:
溶液:分散质粒子直径小于1 nm
分散系 胶体:分散质粒子直径大于 1 nm小于100 nm
浊液:分散质粒子直径大于100 nm
学科网(北京)股份有限公司气溶胶:以气体作为分散剂的分散体系(如,烟、云、雾)
液溶胶:以液体作为分散剂的分散体系(如,Fe(OH) 胶体、Al(OH) 胶体、
3 3
硅酸胶体、豆浆、牛奶,血液、淀粉胶体)
胶体
固溶胶:以固体作为分散剂的分散体系(如,有色玻璃、玛瑙)
4.胶体的性质
①介稳定(稳定性:浊液<胶体<溶液)
②丁达尔效应:由于胶体粒子对光线散射(光波偏离原来的方向而分散传播)形成光亮的
“通路”的现象。(区别胶体和溶液的方法)
鉴别胶体的步骤:把该鉴别物置于暗处,用激光笔照射,在与光束垂直的方向观察是
否有光亮的“通路”。
③电泳:由于胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里作定向移动,这
种现象叫做电泳。
应用:电泳除尘
④聚沉
向胶体中加入少量电解质溶液时,由于加入的阳离子(或阴离子)中和了胶体粒子所
带的电荷,使胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂里析出,这个过程叫
做聚沉。(“三角洲”的形成)
聚沉的方法:加入电解质;与带相反电荷的胶体粒子混合;加热
应用:FeCl 溶液止血;“卤水点豆腐”
3
二、物质的转化
1.酸、碱、盐的性质
酸:电离时产生的阳离子全都是H+的化合物。
碱:电离时产生的阴离子全都是OH-的化合物。
盐:电离时产生的阳离子都是金属离子(铵根离子),阴离子都是酸根离子的化合物
氧化物:由氧元素与其他元素形成的二元化合物
金属氧化物:由氧元素与金属元素形成的二元化合物
非金属氧化物:由氧元素与非金属元素形成的二元化合物
酸性氧化物:能与水作用生成酸或与碱作用只生成一种盐和水(除了盐和水以外不包
括其它物质)的氧化物,非金属氧化物大多是酸性氧化物。(如,MnO 、NO 为酸性氧
2 7 2 5
化物;NO 不是酸性氧化物)
2
碱性氧化物:溶于水而只生成一种碱或与酸反应只成一种盐和水(除了盐和水以外不
包括其它物质)的氧化物。(如,NaO为碱性氧化物;NaO 为过氧化物,非碱性氧化物,
2 2 2
学科网(北京)股份有限公司Al O 为两性氧化物,非碱性氧化物)
2 3
2.物质的转化
根据物质的组成和性质,通过化学变化可以实现物质之间的相互转化。
第二节 离子反应
一、电解质的电离
1.电解质和非电解质
电解质:在水溶液里或熔融状态下能导电的化合物,如HNO ,NaOH,CHCOOH,
3 3
NaCl等;
非电解质:在水溶液里和熔融状态下都不导电的化合物,如C HOH,蔗糖,NH ,CO
2 5 3 2
等。
2.强电解质和弱电解质
强电解质:在水溶液中完全电离的电解质,如HNO,NaOH,NaCl等;
3
弱电解质:在水溶液中部分电离的电解质,如HCO,NH ·H O,HO等。
2 3 3 2 2
2.电离方程式的书写
电离:电解质溶于水或受热熔化,形成自由移动的离子的过程。
电离的过程可以用电离方程式表示出来。
强酸:①HCl=H++Cl-②H SO =2H++SO2-
2 4 4
强碱:③NaOH=Na++OH-
盐类:④NaHCO =Na++HCO-
3 3
⑤NaHSO 在水溶液中的电离方程式:NaHSO=Na++H++SO2-
4 4 4
NaHSO 在熔融状态中的电离方程式:NaHSO=Na++HSO -
4 4 4
水:⑥H
2
O⇌H++OH-
弱酸:⑦CH
3
COOH⇌CH
3
COO-+H+ ⑧H
2
CO 3⇌HCO
3
-+H+ HCO
3
- ⇌CO
3
2-+H+
弱碱:⑨NH
3
∙H
2
O⇌NH
4
++OH- ⑩Fe(OH) 3⇌Fe3++3OH-
二、离子反应
1.离子反应发生的条件
(1)定义:在水溶液中有离子参加或生成的化学反应。如酸、碱、盐之间的复分解反应,
学科网(北京)股份有限公司溶液中的置换反应等。
(2)发生条件
①发生复分解反应
生成沉淀,如CaCO 、BaSO、AgCl 等;
3 4
生成气体,如CO 等;
2
生成弱电解质,如HO、弱酸、弱碱等。
2
②发生氧化还原反应
氧还性离子与还原性离子发生氧化还原反应后导致溶液中离子浓度改变
2.离子方程式
(1)定义:用实际参加反应的离子符号表示反应的式子。
(2)离子方程式的书写
方法一:以NaSO 溶液与Ba(OH) 溶液的反应为例,说明离子方程式的书写步骤。
2 4 2
第一步,写:写出反应的化学方程式
第二步,拆:把易溶于水、易电离的物质写成离子形式,难溶或难电离的物质以及气
体等仍用化学式表示。上述化学方程式可改写成
第三步,删:删去方程式两边不参加反应的离子
第四步,查:检查离子方程式两边各元素的原子个数和电荷数是否相等
方法二:根据离子反应的实质直接写出离子反应方程式。
以NaSO 溶液与Ba(OH) 溶液的反应为例说明。
2 4 2
第一步:分析物质在水溶液中的电离程度,如果是强电解质就以离子书写。所以NaSO
2 4
溶液与Ba(OH) 溶液对应电离为Na+、SO 2-、Ba2+、OH-。
2 4
第二步:按离子反应条件找到反应的离子。Ba2+与SO 2-能生成沉淀,所以这组离子反应
4
离子反应。
第三步:书写离子方程式。要符合电荷守恒、原子守恒。如果是氧化还原反应的话也要
符合电子守恒。离子方程式写成:
三、离子共存问题
溶液中的离子若发生反应或违背题目限制条件则不能大量共存,否则能大量共存。
学科网(北京)股份有限公司常见离子不能相互共存的原因有以下几种:
1. 发生复分解反应不共存
(1)有气体生成
①H+与 、 生成CO 不能大量共存;
2
②H+与 、 生成SO 不能大量共存;
2
③H+与 、 生成HS不能大量共存。
2
(2)有沉淀生成
①Ca2+与 生成CaCO 不能大量共存;
3
②Ag+与 生成AgCl不能大量共存;
③Ba2+与 生成BaSO 不能大量共存;
4
④Ba2+与 生成BaCO 不能大量共存;
3
⑤Mg2+、Al3+、Fe2+、Fe3+、Cu2+与 生成Mg(OH) 、Al(OH) 、Fe(OH) 、Fe(OH) 、
2 3 2 3
Cu(OH) 不能大量共存。
2
(3)有弱电解质(弱酸、弱碱、水)生成
① 与H+生成HO不能大量共存;
2
② 与 生成HO不能大量共存。
2
③HCO-与H+生成HCO 不能大量共存;
3 2 3
④ 与NH +生成NH ·H O不能大量共存。
4 3 2
2. 发生氧化还原反应不共存:
(1)溶液有
MnO−
4 (
H+
)/ Cr O2﹣(
H+
)不能与
S2−
、
SO
3
2−
、
I−
、
Fe2+
、
Br−
、
Cl−
2 7 共存。
ClO− S2− SO2− I− Fe2+
(2)溶液有 不能与 、 3 、 、 共存。
NO− H+ S2− SO2− I− Fe2+
3 ( ) 、 3 、 、
(3)溶液有 不能与 共存。
Fe3+ S2− SO2− I−
(4)溶液有 不能与 、 3 、 共存。
3. 形成络合物不共存
Fe3+ SCN− CN− C H O− Ag+ NH ⋅H O
与 、 、 6 5 ; 和 3 2 等形成络合物而不共存
4. 发生双水解反应不共存
学科网(北京)股份有限公司该不共存类型是发生了双水解,而且反应发生的比较彻底,所以不能共存。并不是只
要发生了双水解就一定不共存,如NH +与CO2-能发生双水解,但反应是不完全的,反应
4 3
后仍有离子剩余,则二者可以认为共存。
5. 复合条件
当题目中出现以下物质时,要注意该物质进入水溶液后体现什么性质,与水反生反应
的产物体现什么性质。因避免这些性质导致的不共存。以下总结了常见的添加物质所引入
的性质。
加入物质 体现性质
氧化性
NaO
2 2
碱性
氧化性
氯水 酸性
Cl﹣
酸性
SO / HSO 氧化性
2 2 3
还原性
6. 限定条件
题目中会给出限定条件下的离子反应,所以除了考虑给出的离子是否共存外,也应注
意限定条件的影响。
(1)限制溶液酸性的条件:pH<7的溶液;使紫色石蕊变红;加镁粉放氢气;
(2)限制溶液碱性的条件:pH>7的溶液;使红色石蕊变蓝;使酚酞呈红色;
(3)可酸可碱的条件: 离子不能大量存在的溶液。
(4)有色离子:Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、 (紫红色)等。
四、常见的离子检验
1. 常见的阳离子的检验
(1)Na+、K+的检验
采用试剂:铂丝、HCl溶液
操作步骤和反应现象:用稀盐酸洗净铂丝,放在酒精灯外焰上灼烧,直到与原来火焰
颜色相同,然后用铂丝蘸取少许待测溶液在酒精灯外焰上灼烧,若火焰呈黄色则证明溶液
中含有Na+;若火焰不呈黄色则证明溶液中不含有Na+;透过蓝色钴玻璃观察若有紫色火焰
则证明溶液中含有K+,若没有观察到紫色火焰则证明溶液中不含有K+。
学科网(北京)股份有限公司(2) NH +的检验
4
采用试剂及用品:NaOH溶液、红色石蕊试纸
操作步骤和反应现象:取待测液少许于试管中,加入过量的浓氢氧化钠溶液,加热,
用湿润的红色石蕊试纸检验产生的气体,若试纸变蓝则证明溶液里含有NH,反之则溶液
里不含NH。
(3) Mg2+的检验
采用试剂:NaOH溶液;
操作步骤和反应现象:取可能含有Mg2+、Al3+待测液少许于试管中,向其中加入
NaOH溶液时生成白色沉淀,若再加入过量的NaOH溶液时白色沉淀不溶解或不完全溶解
则证明溶液里含有Mg2+,反之则溶液里不含Mg2+。
(4)Al3+的检验
采用试剂:NaOH溶液;
操作步聚和反应现象:取可能含有Mg2+、Al3+待测液少许于试管中,向其中滴加少量
NaOH溶液产生白色沉淀,再加入过量NaOH溶液若沉淀溶解则证明溶液里含有Al3+,反
之则溶液里不含Al3+
(5)Ag+的检验
采用试剂:HNO 酸化的NaCl溶液;
3
操作步骤和反应现象:取少许待测液于试管中,加入 HNO 酸化的NaCl溶液,若白色
3
沉淀生成,则证明溶液里含有Ag+,反之则溶液里不含Ag+。
(6)Fe2+的检验
①采用试剂:K[Fe(CN) ]溶液;
3 6
操作步骤和反应现象:取少许待测液于试管中,滴加K[Fe(CN) ]溶液若有蓝色沉淀生
3 6
成则证明溶液里含有Fe2+,反之则证明溶液里不含Fe2+。
②采用试剂:KSCN溶液、氯水;
操作步骤和反应现象:取少许待测液于试管中,先滴加几滴KSCN溶液无明显现象;
再滴加新制的氯水,若溶液变成血红色则证明溶液里含有Fe2+,反之,则证明溶液里不含
Fe2+。
(7)Fe3+的检验
采用试剂:KSCN溶液 ;
操作步骤和反应现象:取少许待测液于试管中,滴入几滴KSCN溶液,若溶液变成血
学科网(北京)股份有限公司红色,则证明溶液里含有Fe3+,反之则证明溶液里不含Fe3+。
(8)Cu2+的检验
采用试剂:NaOH溶液;
操作步骤和反应现象:取少许待测液于试管中,加入NaOH溶液,若蓝色絮状沉淀生
成,则证明溶液里含有Cu2+,反之则溶液里不含Cu2+。
2. 常见的阴离子的检验
(1)Cl﹣的检验
采用试剂:稀硝酸、AgNO 溶液;
3
操作步骤和反应现象:取少许待测液于试管中,先加稀硝酸无明显现象;再滴加
AgNO 溶液若产生白色沉淀则证明溶液里含有Cl-,反之则证明溶液里不含Cl-。
3
(2)Br﹣的检验
①采用试剂:AgNO 溶液、稀硝酸;
3
操作步骤和反应现象:取少许待测液于试管中,先加 AgNO 溶液产生淡黄色沉淀,再
3
滴加稀硝酸,若产生淡黄色沉淀不溶解则证明溶液里含有Br﹣,反之则证明溶液里不含
Br﹣。
②采用试剂:CCl 溶液、氯水;
4
操作步骤和反应现象:取少许待测液于试管中,先加CCl 溶液,溶液分层,下层溶液
4
无色;再滴加氯水,振荡、静置,若下层溶液变为橙红色则证明溶液里含有Br﹣,反之则
证明溶液里不含Br﹣。
(3)I﹣的检验
①采用试剂: AgNO 溶液、稀硝酸;
3
操作步骤和反应现象:取少许待测液于试管中,先加 AgNO 溶液产生黄色沉淀,再滴
3
加稀硝酸,若产生黄色沉淀不溶解则证明溶液里含有I﹣,反之则证明溶液里不含I﹣。
②采用试剂:CCl 溶液、氯水;
4
操作步骤和反应现象:取少许待测液于试管中,先加CCl 溶液,溶液分层,下层溶液
4
无色;再滴加氯水,振荡、静置,若下层溶液变为紫红色,则证明溶液里含有I﹣,反之则
证明溶液里不含I﹣。
③采用试剂:淀粉、氯水;
操作步骤和反应现象:取少许待测液于试管中,先加淀粉,溶液无明显现象;再滴加
氯水,若溶液变成蓝色则证明溶液里含有I﹣,反之则证明溶液里不含I﹣。
学科网(北京)股份有限公司(4) CO 2﹣的检验
3
采用试剂:氯化钡溶液、稀盐酸、澄清石灰水;
操作步骤和反应现象:取少许待测液于试管中,先加入氯化钡溶液有沉淀生成;过滤,向
滤渣中加入稀盐酸,滤渣溶解同时生成无色无味气体,再将气体通入澄清石灰水,澄清石
灰水变浑浊,则证明溶液里含有CO2﹣,反之则证明溶液里不含CO2﹣。
3 3
(5)SO 2﹣的检验
4
采用试剂:稀盐酸、氯化钡溶液;
操作步骤和反应现象:取少许待测液于试管中,先加过量稀盐酸无明显现象(若有沉
淀)则静置后取上层清液继续实验);再加入氯化钡溶液,若产生白色沉淀则证明溶液里含
有SO,反之则证明溶液里不含SO。
(6)NO ﹣的检验
3
采用试剂:稀硫酸、Cu屑;
操作步骤和反应现象:取少许待测液于试管中,先加稀硫酸无明显现象;再加入铜屑,
若先产生无色无味气体,后气体变成红棕色则证明溶液里含有NO ﹣,反之则证明溶液里不
3
含NO ﹣。
3
(7)S2﹣的检验:
采用试剂:CuSO 溶液;
4
操作步骤和反应现象:取少许待测液于试管中,加入CuSO 溶液,有黑色沉淀产生;
4
再加入稀HSO 溶液,若沉淀不溶解则证明溶液里含有S2﹣,反之则证明溶液里不含S2﹣。
2 4
(8)SO2﹣的检验:
2 3
采用试剂:稀盐酸;
操作步骤和反应现象:取少许待测液于试管中,加入稀盐酸,若有黄色沉淀析出,同
时有刺激性气体产生则证明溶液里含有SO2﹣,反之则证明溶液里不含SO2﹣。
2 3 2 3
第三节 氧化还原反应
一、氧化还原反应
1. 基本概念
氧化反应和还原反应
氧化反应:物质所含元素化合价升高,失电子的反应;
还原反应:物质所含元素化合价降低,得电子的反应。
氧化还原反应:氧化反应和还原反应在一个反应中同时发生的化学反应。
学科网(北京)股份有限公司氧化剂和还原剂
氧化剂:得到电子(或电子对偏向)的物质,在反应时所含元素化合价降低;
还原剂:失去电子(或电子对偏离)的物质,在反应时所含元素化合价升高。
氧化产物和还原产物
氧化产物:还原剂失去电子(或电子对偏离)后的产物,表现为化合价升高;
还原产物:氧化剂得到电子(或电子对偏向)后的产物,表现为化合价降低。
氧化性和还原性
氧化性:氧化剂在反应中表现出来的性质,是物质得电子的能力。越容易得电子的物
质,氧化性越强,氧化剂和氧化产物都具有氧化性;
还原性:还原剂在反应中表现出来的性质,是物质失电子的能力。越容易失电子的物
质,还原性越强,还原剂和还原产物都具有还原性。
2. 氧化还原反应的本质和判断依据
氧化还原反应的本质是电子的转移(电子的得失或共用电子对的偏移)。
氧化还原反应的特征是元素的化合价是否发生改变(升高或降低)。
3. 电子转移表示方法
①双线桥法
表示同一元素反应前后电子转移情况时,分别将氧化剂与其还原产物、还原剂与其氧
化产物中相应的变价元素用直线连接起来,箭头从反应物指向产物,线上标出得失电子总
数,该方法称为“双线桥法”。
得2e-
Fe + CuSO == FeSO + Cu
4 4
失
②单线桥法
单线桥法在表示氧化剂和还原剂之间元素的电子转移情况时,将氧化剂中降价元素与
还原剂中升价元素用直线连接起来,箭头从还原剂指向氧化剂,线上标出电子转移总数,
该方法称为“单线桥法”。
2e-
Fe + CuSO == FeSO + Cu
4 4
学科网(北京)股份有限公司4. 氧化还原反应与四种基本反应类型的关系
分解
化合 氧化还原反应
置换
复分
二、氧化剂和还原剂
1.常见的氧化剂和还原剂
常见的氧化剂
活泼非金属单质 F、Cl、Br 、I、O、O
2 2 2 2 2 3
Fe3+、Cu2+ 、Ag+、H+、
元素处于高价态时候的离子
ClO-(H+)、(H+)MnO-
、Cr O2-(H+)
4 2 7
金属氧化物 CuO、Fe O
2 3
含氧酸 浓HSO 、HNO、HClO
2 4 3
过氧化物 NaO、HO
2 2 2 2
常见的还原剂
非金属单质 H、C、 S
2
金属单质 Na、Mg、Al、Zn、Fe
元素处于低价态时候的离子
Fe2+ 、I- 、S2−、HS−、SO2- 、HSO-
3 3
非金属氧化物 SO 、CO
2
低价态的化合物 HS、HBr、HI、NH
2 3
三、氧化还原反应的配平
1. 配平原则
(1) 电子守恒原则:反应中还原剂失去电子的总数与氧化剂得到电子的总数相等;
(2 ) 电荷守恒原则:若为离子反应,反应前后离子所带正负电荷总数相等;
(3) 质量守恒原则:反应前后各元素的原子个数相等。
2. 配平步骤
学科网(北京)股份有限公司化合价升降法是最重要也是最基本的配平方法,以
为例配平:
标变价:找出变价元素。
变价元素为Mn,C1
找升降:找到变价元素化合价的升降
Mn下降2 ,Cl上升1
定总数:调整系数,使化合价升降总数相等,也就是找到得、失电子数的最小公倍数。
Mn得2e-×1=2e- , Cl 失e-×2=2e-
配系数:根据得失电子总数确定发生氧化还原反应的物质的系数,进而利用元素守恒,
配平没有参加氧化还原反应的物质的系数。
查相等:检查方程式两边各原子的个数是否相等,离子方程式还要检查方程式两边的
离子所带的电荷数是否相等。
四、常见的氧化还原反应
1. 普通氧化还原
还原剂+ 氧化剂氧化产物+还原产物
例如:
2.部分氧化还原反应
参加反应的还原剂(氧化剂)只有部分被氧化(被还原),有关元素的化合价只有部分发生
变化。除氧化还原反应外,还伴随着非氧化还原反应的发生。
例如:
3.自身氧化还原反应
在该类反应中,电子的转移可以发生在同种物质中的不同元素或同种元素不同价态之
间。
例如:
4.归中反应
此类反应的特点是同一种元素在不同的反应物中有两种不同的价态,反应后转化为中
间价态。
学科网(北京)股份有限公司5.歧化反应
在反应中,若氧化作用和还原作用发生在同一分子中的同一元素上,使该元素的原子
(或离子)一部分被氧化,另一部分被还原。这种自身的氧化还原反应称为歧化反应。
例如:Cl
2
+H
2
O⇌HClO+HCl
五、氧化还原反应的一般规律
1. 价态律
最高价元素只有氧化性,最低价元素只有还原性。价态在中间的元素既有氧化性又有
还原性。
2. 强弱律
得e-,化合价降低
被还原,发生还原反应
还原剂+ 氧化剂 氧化产物 + 还原产物
被氧化,发生氧化反应
失e-,化合价升高
氧化性:氧化剂>氧化产物 还原性:还原剂>还原产物
例如: 氧化性:Cl>Fe3+ 还原性:Fe2+>Cl-
2
氧化性:Fe3+>Fe2+ 还原性:Fe>Fe2+
3. 难易律
越易失电子的物质,失电子后就越难得电子;越易得电子的物质,得电子后就越难
失去电子。
K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb>H>Cu>Hg>Ag>Pt>Au
金属活动性逐渐减弱(还原性逐渐减弱)
K+核外电子数,核外电子数=a-m
a
(4)阴离子 Yn-:核电荷数=质子数<核外电子数,核外电子数=b+n
b
2.核素
学科网(北京)股份有限公司(1)定义:
核素:人们把具有一定数目质子和一定数目中子的一种原子称为核素。
同位素:质子数相同而中子数不同的同一元素的不同核素(原子)互为同位素。
(2)元素、核素、同位素
元素 核素 同位素
具有相同质子数和不同中子数
具有相同的核电荷数的具有一定数目的质子和一
定义 的同一元素的不同原子之间的
同一类原子的总称 定数目中子的一种原子。
互称
元素是宏观概念,只表
示种类。元素的种类由 同位素的化学性质几乎完全相
质子数决定,而与中子 同,物理性质不一定相同;稳
备注
数、核外电子数无关, 定同位素的原子个数百分比不
因此同种元素可以有若 变。
干种不同的同位素
、 、 中的H均 、 、 三个核素互为
实例 是一种核素
为氢元素 同位素
3.原子核外电子排布
(1)由里到外,分为K、L、M、N、O、P、Q共7层,电子分层排布,且能量由低到高;
(2)各电子层最多容纳的电子数为2n2个(n为层数);
(3)K为最外层时,最多容纳电子数是2,除K层外的其他各层为最外层时,最多容纳电
子数是8个;
(4)次外层最多容纳电子数18个,倒数第三层电子数不得超过32个。
4.原子结构示意图
学科网(北京)股份有限公司二、元素周期表
1. 元素周期表的结构
(1)周期:元素周期表中有7个横行,叫做周期。周期有短周期、长周期之分。
(2)族:元素周期表有18个纵行,除第8、9、10三个纵行叫做第VIII 族外,其余每个纵
行各为一族。族有主族和副族之分。稀有气体单为一族,为0族。
(3)元素周期表的结构
短周期:含有元素较少的第一、二、三周期叫短周期。短周期共有18种元素。
长周期:除短周期外的周期叫长周期。
镧系:第6周期第IIIB族,共15种元素。 锕系:第7周期第IIIB族,共15种元素。
主族:由短周期元素和长周期元素构成的族。用族序数(罗马数字)后加字母A表示,
如第VII A族。共7个(从I A 到VII A,分别位于1,2,13,14,15,16,17列 )。
副族:完全由长周期元素构成的族。用族序数后加字母B表示,如第II B族。共7个
(从ⅢB 到VII B,分别位于3、4、5、6、7列, ⅠB 、II B位于 11、12列 )。
第VIII族:包括8、9、10三列。
0族:稀有气体元素所在的列即第18列为0族。
2.元素位置的表示方法
(1)周期数通常用中文数字表示,如Na在第三周期。
(2)族数必须用罗马数字表示,即:I II III IV V VI VII VIII,且必须注意用
学科网(北京)股份有限公司A、B分别表示主族和副族,如Na在第I A族。
(3)另外要注意第VIII族没有A、B之分;0族的0需要使用阿拉伯数字。
3.位置和结构的关系
(1)原子序数=核电荷数=质子数=核外电子数
(2)周期数=原子核外电子层数
(3)主族序数=最外层电子数
四、原子结构与元素的性质
1.碱金属元素的递变规律
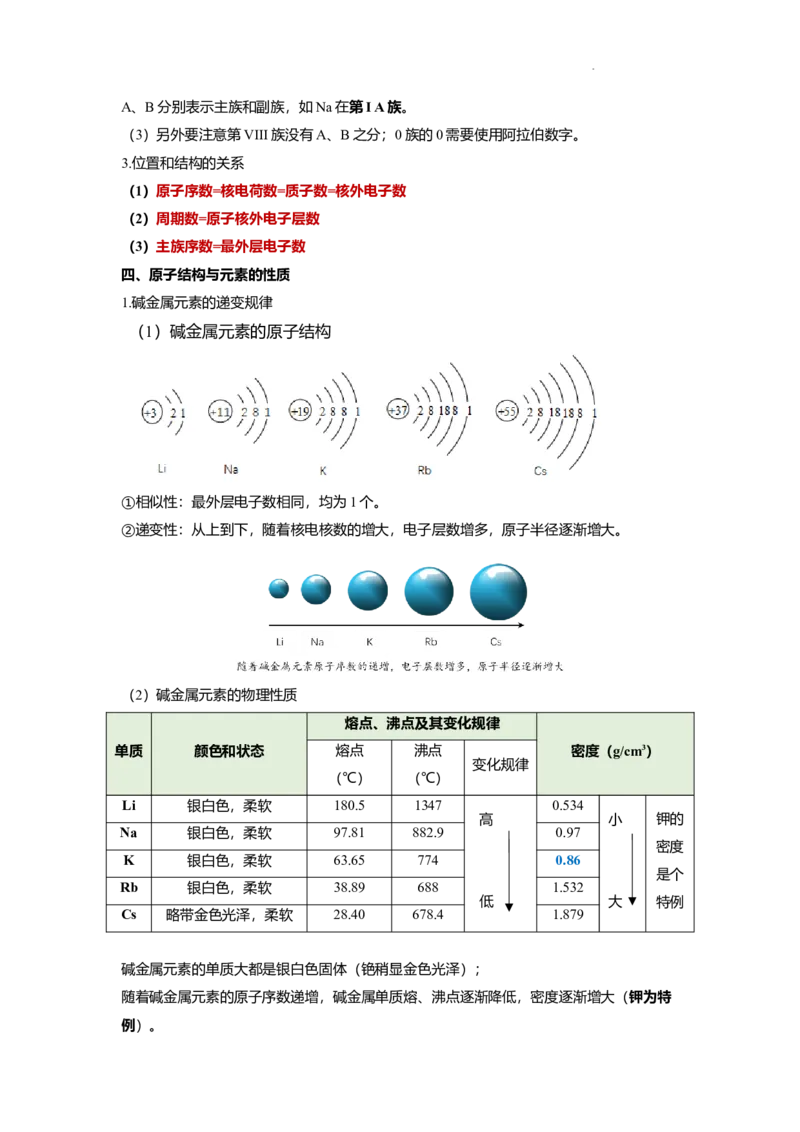
(1)碱金属元素的原子结构
①相似性:最外层电子数相同,均为1个。
②递变性:从上到下,随着核电核数的增大,电子层数增多,原子半径逐渐增大。
(2)碱金属元素的物理性质
熔点、沸点及其变化规律
单质 颜色和状态 熔点 沸点 密度(g/cm3)
变化规律
(℃) (℃)
Li 银白色,柔软 180.5 1347 0.534
高 小 钾的
Na 银白色,柔软 97.81 882.9 0.97
密度
K 银白色,柔软 63.65 774 0.86
是个
Rb 银白色,柔软 38.89 688 1.532
低 大 特例
Cs 略带金色光泽,柔软 28.40 678.4 1.879
碱金属元素的单质大都是银白色固体(铯稍显金色光泽);
随着碱金属元素的原子序数递增,碱金属单质熔、沸点逐渐降低,密度逐渐增大(钾为特
例)。
学科网(北京)股份有限公司(3)碱金属元素的化学性质
①碱金属元素单质的相似性
a.碱金属元素单质能与O 反应生成相应的氧化物,如LiO、NaO等,反应通式为
2 2 2
b.碱金属元素单质能与HO反应,并能置换出HO中的氢,反应通式为
2 2
②碱金属元素单质的递变性
a.碱金属元素单质与 O 的反应越来越剧烈,产物更加复杂,如 Li与O 反应只能生成
2 2
LiO,Na与O 反应还可以生成NaO ,而K与O 反应能够生成超氧化钾(KO )等,Rb和
2 2 2 2 2 2
Cs遇空气立即燃烧生成更为复杂的氧化物。
b.碱金属元素单质与HO的反应由Li~Cs越来越剧烈,如K与HO反应可能会发生轻微爆
2 2
炸,Rb与Cs遇水发生剧烈爆炸。LiOH~CsOH的碱性也越来越强。
随着原子序数的递增,碱金属单质的还原性依次增强,即还原性:Li<Na<K<Rb<Cs。
在元素化学中我们将元素原子失电子的能力,称为金属性。即从上到下,元素金属性逐渐
增强。
2.卤族元素的递变规律
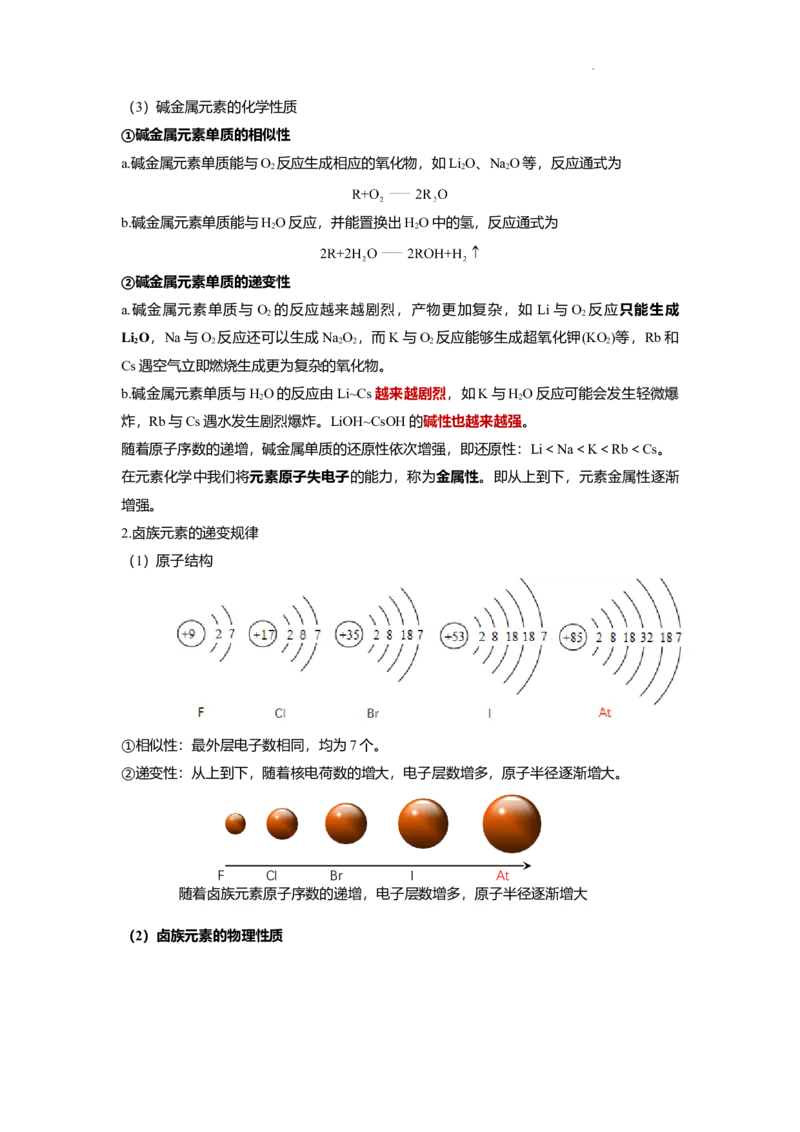
(1)原子结构
①相似性:最外层电子数相同,均为7个。
②递变性:从上到下,随着核电荷数的增大,电子层数增多,原子半径逐渐增大。
F Cl Br I At
随着卤族元素原子序数的递增,电子层数增多,原子半径逐渐增大
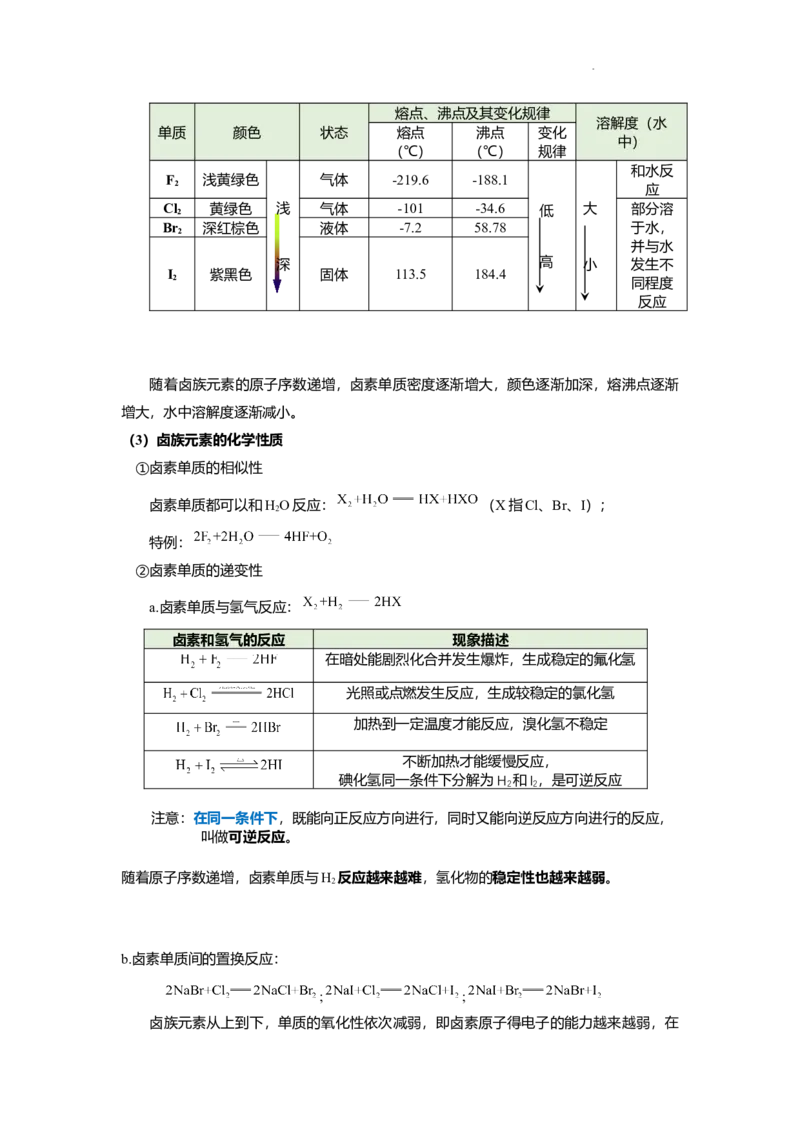
(2)卤族元素的物理性质
学科网(北京)股份有限公司熔点、沸点及其变化规律
溶解度(水
单质 颜色 状态 熔点 沸点 变化
中)
(℃) (℃) 规律
和水反
F 浅黄绿色 气体 -219.6 -188.1
2
应
Cl 2 黄绿色 浅 气体 -101 -34.6 低 大 部分溶
Br 深红棕色 液体 -7.2 58.78 于水,
2
并与水
深 高 小 发生不
I 紫黑色 固体 113.5 184.4
2 同程度
反应
随着卤族元素的原子序数递增,卤素单质密度逐渐增大,颜色逐渐加深,熔沸点逐渐
增大,水中溶解度逐渐减小。
(3)卤族元素的化学性质
①卤素单质的相似性
卤素单质都可以和HO反应: (X指Cl、Br、I);
2
特例:
②卤素单质的递变性
a.卤素单质与氢气反应:
卤素和氢气的反应 现象描述
在暗处能剧烈化合并发生爆炸,生成稳定的氟化氢
光照或点燃发生反应,生成较稳定的氯化氢
加热到一定温度才能反应,溴化氢不稳定
不断加热才能缓慢反应,
碘化氢同一条件下分解为H 和I ,是可逆反应
2 2
注意:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,
叫做可逆反应。
随着原子序数递增,卤素单质与H 反应越来越难,氢化物的稳定性也越来越弱。
2
b.卤素单质间的置换反应:
; ;
卤族元素从上到下,单质的氧化性依次减弱,即卤素原子得电子的能力越来越弱,在
学科网(北京)股份有限公司元素化学中,我们将元素原子得电子的能力,称为非金属性。即从上到下,非金属性逐渐
减弱。
第二节 元素周期律
一、元素性质的周期性变化规律
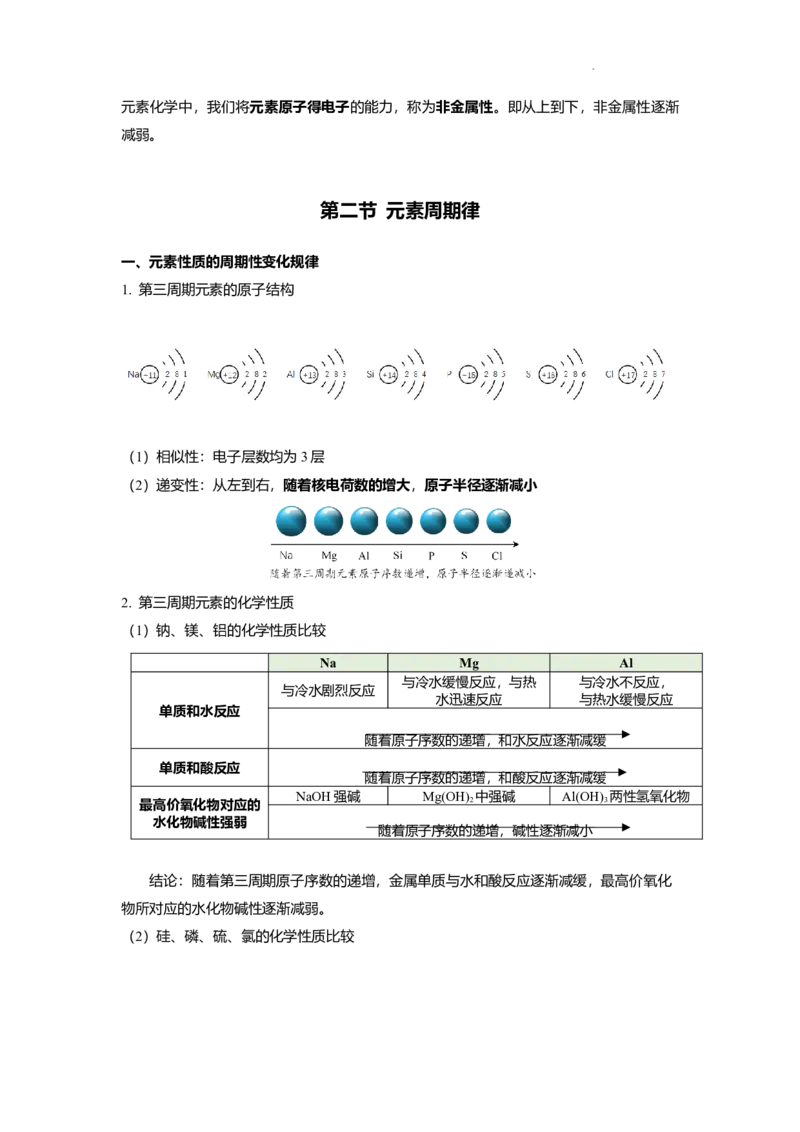
1. 第三周期元素的原子结构
(1)相似性:电子层数均为3层
(2)递变性:从左到右,随着核电荷数的增大,原子半径逐渐减小
2. 第三周期元素的化学性质
(1)钠、镁、铝的化学性质比较
Na Mg Al
与冷水缓慢反应,与热 与冷水不反应,
与冷水剧烈反应
水迅速反应 与热水缓慢反应
单质和水反应
随着原子序数的递增,和水反应逐渐减缓
单质和酸反应
随着原子序数的递增,和酸反应逐渐减缓
NaOH强碱 Mg(OH) 中强碱 Al(OH) 两性氢氧化物
最高价氧化物对应的 2 3
水化物碱性强弱
随着原子序数的递增,碱性逐渐减小
结论:随着第三周期原子序数的递增,金属单质与水和酸反应逐渐减缓,最高价氧化
物所对应的水化物碱性逐渐减弱。
(2)硅、磷、硫、氯的化学性质比较
学科网(北京)股份有限公司Si P S Cl
高温 磷蒸气与氢气能反应 加热 光照或点燃发生爆炸
单质和氢气
随着原子序数的递增,反应条件逐渐减弱
反应的条件
SiH PH H S HCl
4 3 2
生成的氢化 很不稳定 不稳定 较稳定 稳定
物稳定性
随着原子序数的递增,稳定性逐渐加强
最高价氧化 H 2 SiO 3 H 3 PO 4 H 2 SO 4 HClO 4
物对应的水 弱酸 中强酸 强酸 强酸,酸性大于硫酸
化物酸性强 随着原子序数的递增,酸性逐渐加强
弱
结论:随着第三周期原子序数的递增,非金属单质与氢气反应条件逐渐减弱,最高价
氧化物所对应的水化物酸性逐渐增强。
(3)第三周期元素金属性和非金属性比较
Na Mg Al Si P S Cl
随着原子序数的递增,元素金属性逐渐减弱,非金属性逐渐增强
对其他周期元素性质进行研究,也得到了类似的结论。
二、元素周期表和元素周期律的应用
1. 元素周期律
(1)从锂(Li)到铯(Cs),随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原
子核对核外电子的吸引能力逐渐减弱,失电子能力逐渐增强,金属性逐渐增强。
(2)从氟(F)到碘(I),随着核电荷数的增加,卤族元素原子的电子层数逐渐增多,原子核
对核外电子的吸引能力逐渐减弱,得电子能力逐渐减弱,非金属性逐渐减弱。
(3)从钠(Na)到氯(Cl),随着核电荷数的增加,第三周期元素原子的最外层电子数逐渐
增多,原子核对核外电子的吸引能力逐渐增强,原子的非金属性逐渐增强,金属性逐渐减
弱。
元素的最高正价与最低负价的绝对值的代数和为8。
我们把元素的性质随着原子序数的递增而显周期性的变化,叫元素周期律。
2. 元素周期律与金属性、非金属性的关系
(1)元素金属性指元素原子失电子的能力,非金属性指元素原子得电子的能力。
①同一周期从左到右,电子层数不变,核电荷数递增,原子半径减小,失电子越来越
难,得电子越来越容易,元素金属性减弱,非金属性增强;
②同一主族从上到下,电子层数递增,核电荷数增加,原子半径增大,失电子越来
越容易,得电子越来越难,元素金属性增强,非金属性减弱。
学科网(北京)股份有限公司(2)元素金属性的比较
①根据元素所在周期表中的位置判断。
②根据元素化合物的性质来判断。
(3)元素非金属性的比较
①根据元素所在周期表中的位置判断。
②根据元素化合物的性质来判断。
比较非金属单质与氢气反应生成氢化物的难易和气态氢化物的稳定性,反应越容易,
气态氢化物越稳定,非金属性越强。
比较最高价氧化物的水化物酸性的强弱,酸性越强,非金属性越强
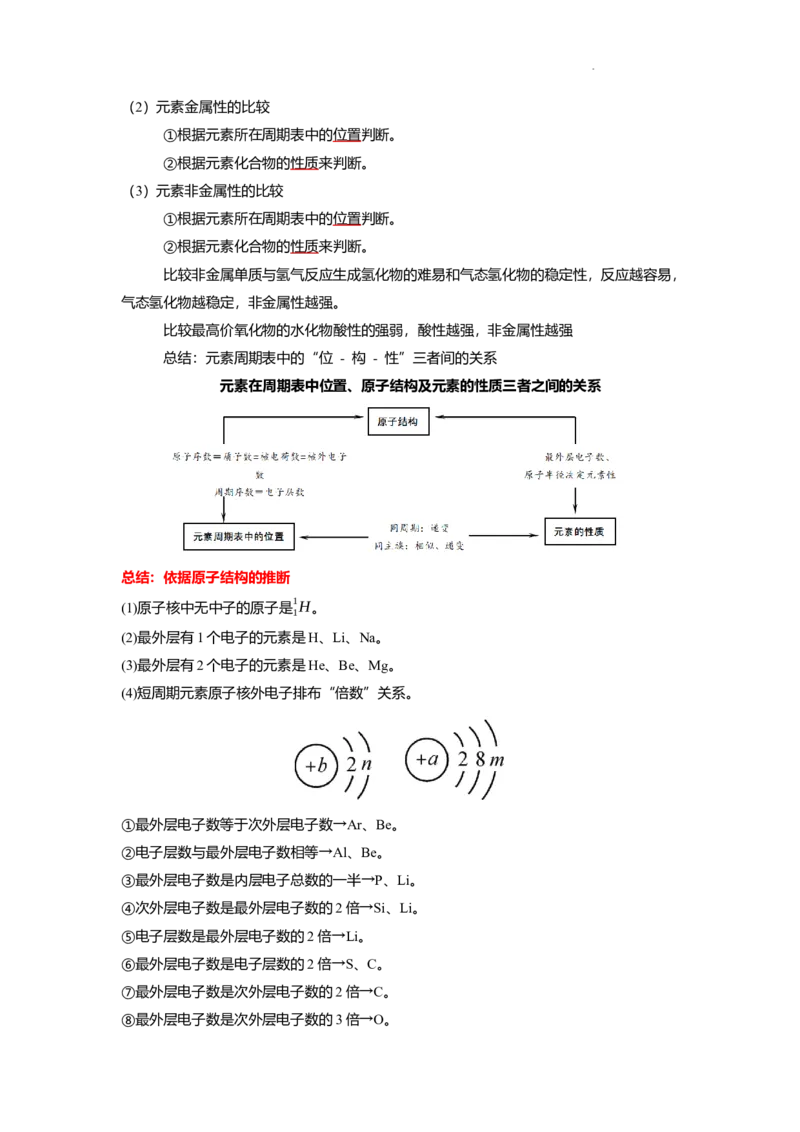
总结:元素周期表中的“位 - 构 - 性”三者间的关系
元素在周期表中位置、原子结构及元素的性质三者之间的关系
总结:依据原子结构的推断
(1)原子核中无中子的原子是
1H。
1
(2)最外层有1个电子的元素是H、Li、Na。
(3)最外层有2个电子的元素是He、Be、Mg。
(4)短周期元素原子核外电子排布“倍数”关系。
①最外层电子数等于次外层电子数→Ar、Be。
②电子层数与最外层电子数相等→Al、Be。
③最外层电子数是内层电子总数的一半→P、Li。
④次外层电子数是最外层电子数的2倍→Si、Li。
⑤电子层数是最外层电子数的2倍→Li。
⑥最外层电子数是电子层数的2倍→S、C。
⑦最外层电子数是次外层电子数的2倍→C。
⑧最外层电子数是次外层电子数的3倍→O。
学科网(北京)股份有限公司⑨最外层电子数是次外层电子数的4倍→Ne。
第三节 化学键
一、 化学键
1.定义:相邻原子之间强烈的相互作用称为化学键。
(1)成键原子必须直接相邻。
(2)“原子”是广义的原子,不仅指中性原子,还包括阴、阳离子。
2.分类 离子键——原子间发生电子转移,形成阴阳离子
化学键 极性共价键
共价键 ——原子间形成共用电子对
非极性共价键
3.化学反应的实质:旧化学键断裂,新化学键形成的过程。
二、离子键
1.离子键:带相反电荷离子之间的相互作用叫做离子键。
相反电荷离子:指的是阴阳离子。
相互作用:静电作用(包含吸引和排斥)
2.成键过程:阴、阳离子接近到某一定距离时,吸引和排斥力达到平衡,就形成了离子键。
3.离子键的影响因素:离子所带的电荷数越多,离子半径越小,则离子键越强。
4.形成条件:一般含金属阳离子或铵根离子+酸根离子。
5.离子化合物:像NaCl这种含有离子键的化合物的化合物叫做离子化合物。
(1)活泼金属(IA,IIA)与活泼非金属(VIA,VIIA)形成的化合物。如NaCl、NaO、
2
KS等
2
(2)强碱:如NaOH、KOH、Ba(OH) 、Ca(OH) 等
2 2
(3)大多数盐和大部分金属氧化物:如NaCO、BaSO、MgO
2 3 4
(4)铵盐:如NH Cl
4
三、电子式
1.定义:电子式是用“元素符号+最外层电子”来表示的,一般要求要表明成对的电子与未
成对电子,并注意对称。
2.原子的电子式:在元素符号周围用小点“.”或小叉“×”来表示其最外层电子数。
例如:
学科网(北京)股份有限公司3.离子的电子式:
(1)阳离子的电子式:简单阳离子的电子式就是它的离子符号,复杂阳离子(NH +)例
4
外。离子化合物中的阳离子可以是金属阳离子和非金属形成的铵根离子,但不能是氢离子;
例如:Na+
(2)阴离子的电子式:不但要画出最外层电子数,而且还要用中括号“[ ]“括起来,并
在右上角标出所带电荷“n-”。离子化合物中的阴离子可以是单核阴离子(O2- 、F- 、Cl-
2
、S2-)、双核阴离子(OH- 、CN-、O2 、HS- 、ClO-)
例如:
4.用电子式可以直观地看到原子结构特点与键之间的关系,也可以表示出原子或离子之间
是怎样结合的,例如:氯化钠的形成过程:
5.电子式形成过程:
(1)左边为原子的电子式;右边为NaCl的电子式,中间用“→”连接, 不能把“→”写
成“=”;箭头左边的弧线表示电子的转移方向(也可不标);
(2)左边离子化合物的电子式中注意:简单阳离子的电子式即是离子符号,阴离子的电子
式加方框和电荷;阴阳离子的电子式挤在一起即为物质的电子式;
(3)相同的原子可以合并写,相同的离子要单个写。
四、共价键
1.共价键:原子之间通过共用电子对所形成的相互作用,叫做共价键。
2.用电子式表示共价键的形成:Cl、HCl分子的形成
2
(1)Cl 的形成: +
2
(2)HCl的形成 + H
3.形成条件:非金属元素与非金属元素之间。
4.共价键的类型
(1)非极性共价键(非极性键)
同种非金属元素形成的单质中的化学键: 如:H、Cl、N、O、O、P 等。
2 2 2 2 3 4
(2)极性共价键(极性键)
不同种非金属元素之间形成的化学键:
学科网(北京)股份有限公司①非金属氧化物、氢化物等:HO、 CO 、SiO、 HS、NH 等
2 2 2 2 3
②酸中的化学键(全部是共价键):HNO、HCO、HSO 、HClO、CHCOOH 等。
3 2 3 2 4 3
5.共价化合物:只含有共价键的化合物。
(1)非金属的氢化物。如HS、NH 等
2 3
(2)酸:如HNO、HCO、HSO 、HClO、CHCOOH等
3 2 3 2 4 3
(3)非金属氧化物:如HO、 CO 、SiO
2 2 2
五、常见物质电子式的书写
1.书写电子式的步骤:
(1)分清键型(是离子键还是共价键)
(2)形成离子键时,要标电荷;形成共价键时不标电荷
(3)成键后的原子或离子,一般为8电子稳定结构
2.常见物质的电子式
(1)原子
(2)离子
(3)单质分子
(4)共价化合物
学科网(北京)股份有限公司(5)离子化合物
六、分子间作用力与氢键
分子间作用力 氢键
分子之间一种把分子聚集在一起 氢键不是化学键,是一种比化学键弱
定义
的作用力,又称范德华力。 比分子间作用力强的力的作用。
分子间作用力小于化学键,对物
质的熔、沸点、溶解性等物理性 分子间形成的氢键会使物质的熔沸点
质有影响。 升高。
特点
组成和结构相似的物质,相对分 通常N、O、F这三种元素的氢化物易
子质量越大,分子间作用力越 形成氢键。
大,物质的熔沸点也越高。
举例 沸点:F<Cl<Br <I HO、HF、NH 、CHOH等。
2 2 2 2 2 3 3
学科网(北京)股份有限公司