文档内容
天津市耀华中学 2025 届高三年级第二次月考
化学试卷
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分,考试时间60分钟。
第Ⅰ卷1至4页,第Ⅱ卷5至8页。
答卷前,考生务必将姓名、班级、考号填在答题卡上。答卷时,考生务必将答案涂写在答题
卡上,答在试卷上的无效。考试结束后,将答题卡交回。
祝各位考生考试顺利!
第Ⅰ卷(共36分)
注意事项:
1.每题选出答案后,用铅笔将答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,
再选涂其他答案标号。
2.本卷共12题,每题3分,共36分。在每题给出的四个选项中,只有一项是最符合题目要
求的。
以下数据可供解题时参考:
相对原子质量:
1.劳动人民的发明创造是中华优秀传统文化的组成部分。下列化学原理描述错误的是( )
发明 关键操作 化学原理
A 制墨 松木在窑内焖烧 发生不完全燃烧
B 造纸 草木灰水浸泡树皮 促进纤维素溶解
C 陶瓷 黏土高温烧结 形成新的化学键
D 火药 硫黄、硝石和木炭混合,点燃 发生氧化还原反应
2.下列说法不正确的是( )
A. 见光易分解,应保存在棕色试剂瓶中
B. 能与 反应产生 ,可作供氧剂
C. 有还原性,能被氧化成
D. 呈两性,不能用于治疗胃酸过多
3.下列实验操作正确且能达到实验目的的是( )A.用甲装置做喷泉实验 B.用乙装置制备氯气
C.用丙装置提纯 气体 D.用丁装置干燥
4.下列离子方程式正确的是( )
A.用 溶液除 气体:
B. 溶液中滴加 溶液:
C. 溶液中通入少量 :
D.将少量 通入 溶液:
5.化学烫发巧妙利用了头发中蛋白质发生化学反应实现对头发的“定型”,其变化过程示意图如下。下
列说法不正确的是( )
A.药剂 具有还原性
B.①→②过程若有 键断裂,则转移 电子
C.②→③过程若药剂 是 ,其还原产物为
D.化学烫发通过改变头发中某些蛋白质中 键位置来实现头发的定型
6. 为阿伏加德罗常数的值,下列说法正确的是( )
A. 中含有 键数目最多为
B. 中含有氧原子数为
C.向 溶液通氨气至中性,铵根离子数为
D.标准状况下, 通入水中,溶液中氯离子数为
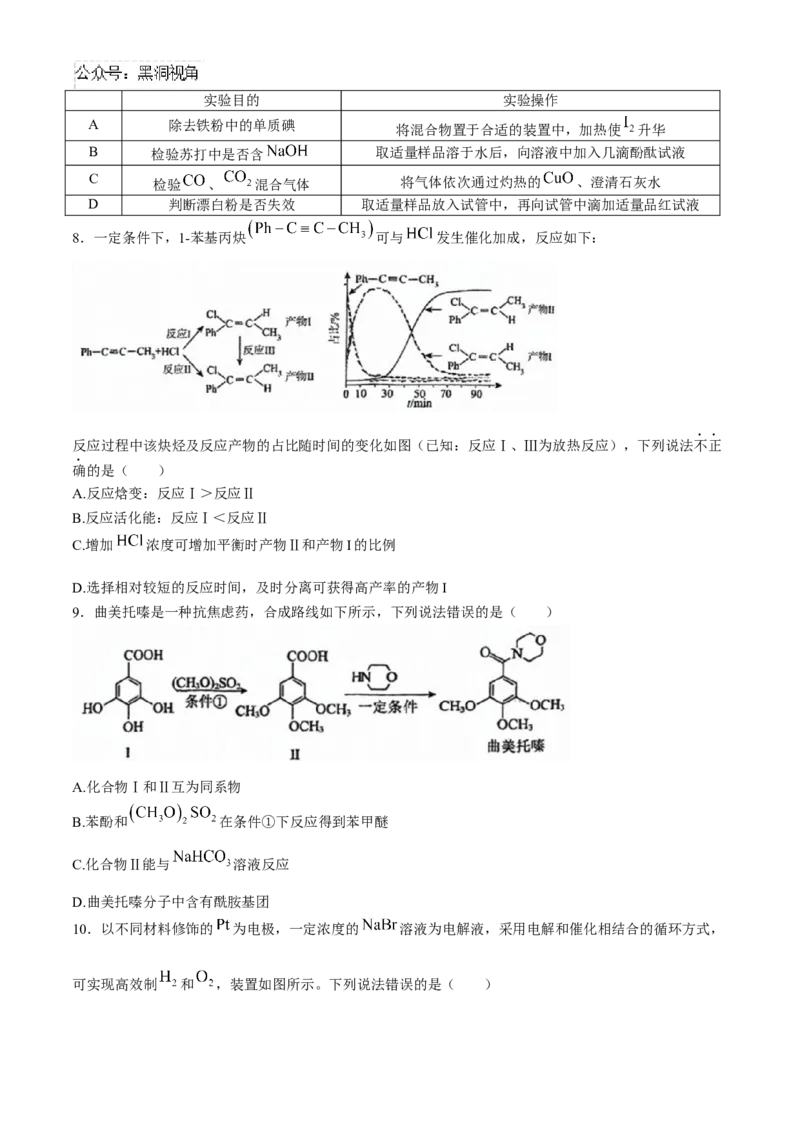
7.下列实验操作能达到相应实验目的的是( )实验目的 实验操作
A 除去铁粉中的单质碘
将混合物置于合适的装置中,加热使 升华
B 检验苏打中是否含 取适量样品溶于水后,向溶液中加入几滴酚酞试液
C 检验 、 混合气体 将气体依次通过灼热的 、澄清石灰水
D 判断漂白粉是否失效 取适量样品放入试管中,再向试管中滴加适量品红试液
8.一定条件下,1-苯基丙炔 可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应Ⅰ、Ⅲ为放热反应),下列说法不正
确的是( )
A.反应焓变:反应Ⅰ>反应Ⅱ
B.反应活化能:反应Ⅰ<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物I
9.曲美托嗪是一种抗焦虑药,合成路线如下所示,下列说法错误的是( )
A.化合物Ⅰ和Ⅱ互为同系物
B.苯酚和 在条件①下反应得到苯甲醚
C.化合物Ⅱ能与 溶液反应
D.曲美托嗪分子中含有酰胺基团
10.以不同材料修饰的 为电极,一定浓度的 溶液为电解液,采用电解和催化相结合的循环方式,
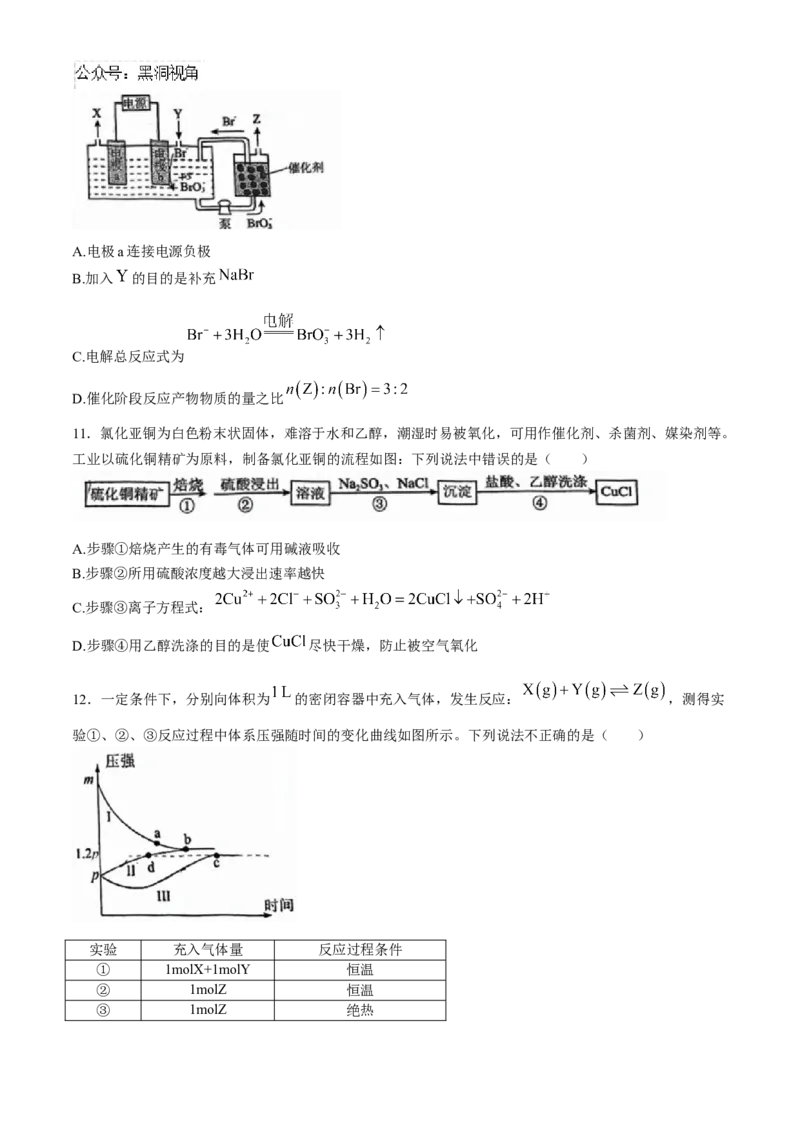
可实现高效制 和 ,装置如图所示。下列说法错误的是( )A.电极a连接电源负极
B.加入 的目的是补充
C.电解总反应式为
D.催化阶段反应产物物质的量之比
11.氯化亚铜为白色粉末状固体,难溶于水和乙醇,潮湿时易被氧化,可用作催化剂、杀菌剂、媒染剂等。
工业以硫化铜精矿为原料,制备氯化亚铜的流程如图:下列说法中错误的是( )
A.步骤①焙烧产生的有毒气体可用碱液吸收
B.步骤②所用硫酸浓度越大浸出速率越快
C.步骤③离子方程式:
D.步骤④用乙醇洗涤的目的是使 尽快干燥,防止被空气氧化
12.一定条件下,分别向体积为 的密闭容器中充入气体,发生反应: ,测得实
验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是( )
实验 充入气体量 反应过程条件
① 1molX+1molY 恒温
② 1molZ 恒温
③ 1molZ 绝热A.曲线I对应实验① B.正反应为放热反应
C.气体的总物质的量: D.C点的平衡常数:
第Ⅱ卷(共64分)
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题卡上。
2.本卷共4题,共64分。
13.Ⅰ.我国科研工作者发现并制备了一系列主要由 、 、 、 等元素组成的导电材料。回答下列
问题:
(1)O、P、S三种元素中,电负性最小的元素名称是_____;键角: _____ (填“>”、
“<”或“=”)。
(2)肼( )分子中孤电子对与 键的数目之比为_______,肼的相对分子质量与甲醇相同,
但沸点远高于甲醇的原因是______。
(3)正硝酸钠( )是一种重要的化工原料。 阴离子的空间结构为_______,其中心原子
杂化方式为_______杂化。
(4)基态硒原子的价层电子排布式为______; 晶体的熔点为350℃,加热易升华,固态 属于
_______晶体。
Ⅱ.甲硅烷 可用于制备多种新型无机非金属材料。
(5)①热稳定性: _______ (填“>”“<”或“=”)。原因是_______。
② 中H一Si一H的键角大于 中H一N一H的键角,其键角差异的原因是______。
(6)利用 与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子
位于立方体的内部。
①碳化硅晶体中每个Si原子周围距离最近的C原子数目为_____。②已知碳化硅的晶胞边长为 ,阿伏加德罗常数为 ,晶胞中相邻两个碳原子的最短
距离为_____nm,碳化硅晶体的密度为_____ (列出计算式)。
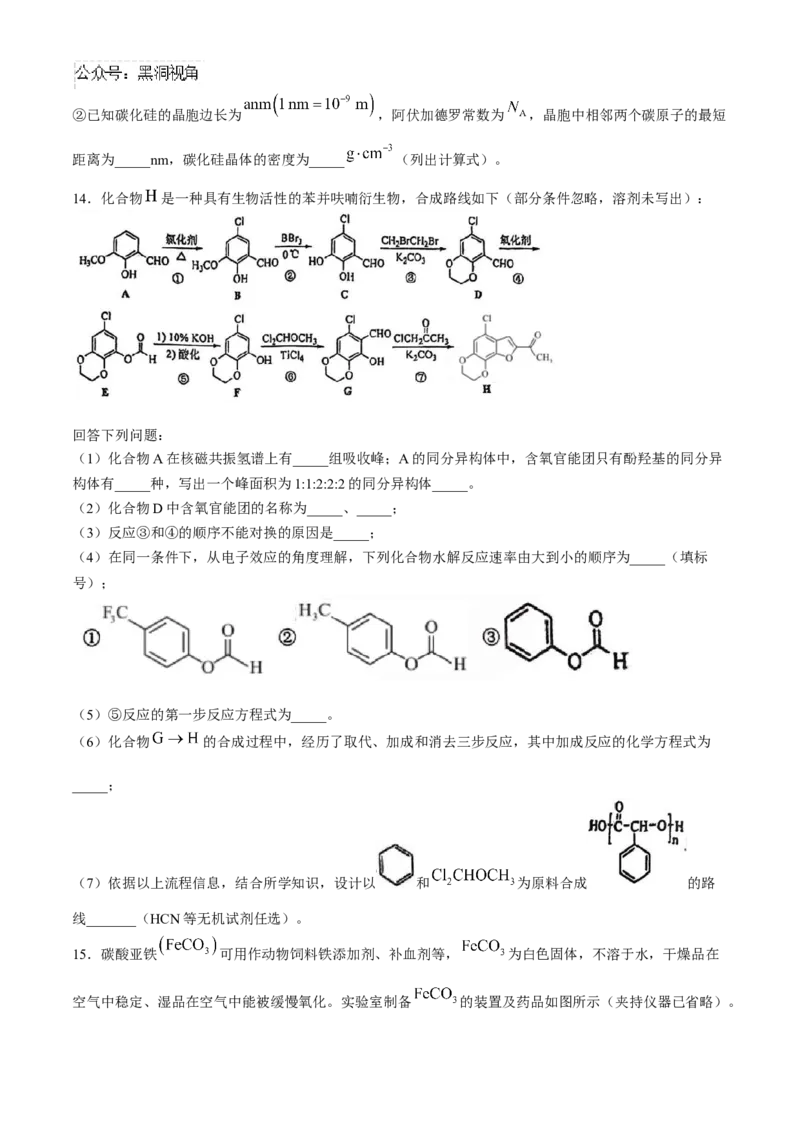
14.化合物 是一种具有生物活性的苯并呋喃衍生物,合成路线如下(部分条件忽略,溶剂未写出):
回答下列问题:
(1)化合物A在核磁共振氢谱上有_____组吸收峰;A的同分异构体中,含氧官能团只有酚羟基的同分异
构体有_____种,写出一个峰面积为1:1:2:2:2的同分异构体_____。
(2)化合物D中含氧官能团的名称为_____、_____;
(3)反应③和④的顺序不能对换的原因是_____;
(4)在同一条件下,从电子效应的角度理解,下列化合物水解反应速率由大到小的顺序为_____(填标
号);
(5)⑤反应的第一步反应方程式为_____。
(6)化合物 的合成过程中,经历了取代、加成和消去三步反应,其中加成反应的化学方程式为
_____;
(7)依据以上流程信息,结合所学知识,设计以 和 为原料合成 的路
线_______(HCN等无机试剂任选)。
15.碳酸亚铁 可用作动物饲料铁添加剂、补血剂等, 为白色固体,不溶于水,干燥品在
空气中稳定、湿品在空气中能被缓慢氧化。实验室制备 的装置及药品如图所示(夹持仪器已省略)。回答下列问题:
(1)仪器B的名称是_____,实验时,先关闭活塞2,再打开活塞1和3,加入适量稀硫酸反应一段时间,
待装置 中反应速率明显变慢时,接下来应进行的操作是_____。
(2)装置C中反应需要控制温度在35°C以下,其原因是_____;写出生成 的离子方程式:_____。
(3)装置D的作用是_____。
(4)反应结束后,将装置 中所得沉淀过滤、洗涤、干燥。
①“过滤”时宜选用减压过滤,减压过滤的优点是_____。
②“洗涤”时,证明沉淀已洗涤干净的实验操作是_____。
(5)将 样品溶于足量的酸中,配成 溶液,取 溶液,然后用 的酸性
标准液滴定,消耗标准液体积为 ,上述过程中所用的酸可以是_____(填字母),样品中铁
元素的质量分数为_____。
a.氢碘酸 b.稀硫酸 c.稀硝酸 d.浓盐酸
16.研究 与 的反应对减缓燃料危机和减弱温室效应具有重大意义。
与 发生反应Ⅰ:
在反应过程中还发生反应Ⅱ:
(1)已知部分化学键的键能数据如下:
化学键 H-O H-H C=O
键能(
413 436 803 1076
)
则 _____ 。
(2)在刚性密闭容器中充入一定量的 与 ,下列能判断反应 达到平衡状态的是_____(填标号)。
A.在绝热容器中,温度保持不变B.恒温时,混合气体的密度保持不变
C.恒温时,混合气体中 与 的物质的量浓度相等
D.恒温时, 和 的物质的量之和保持不变
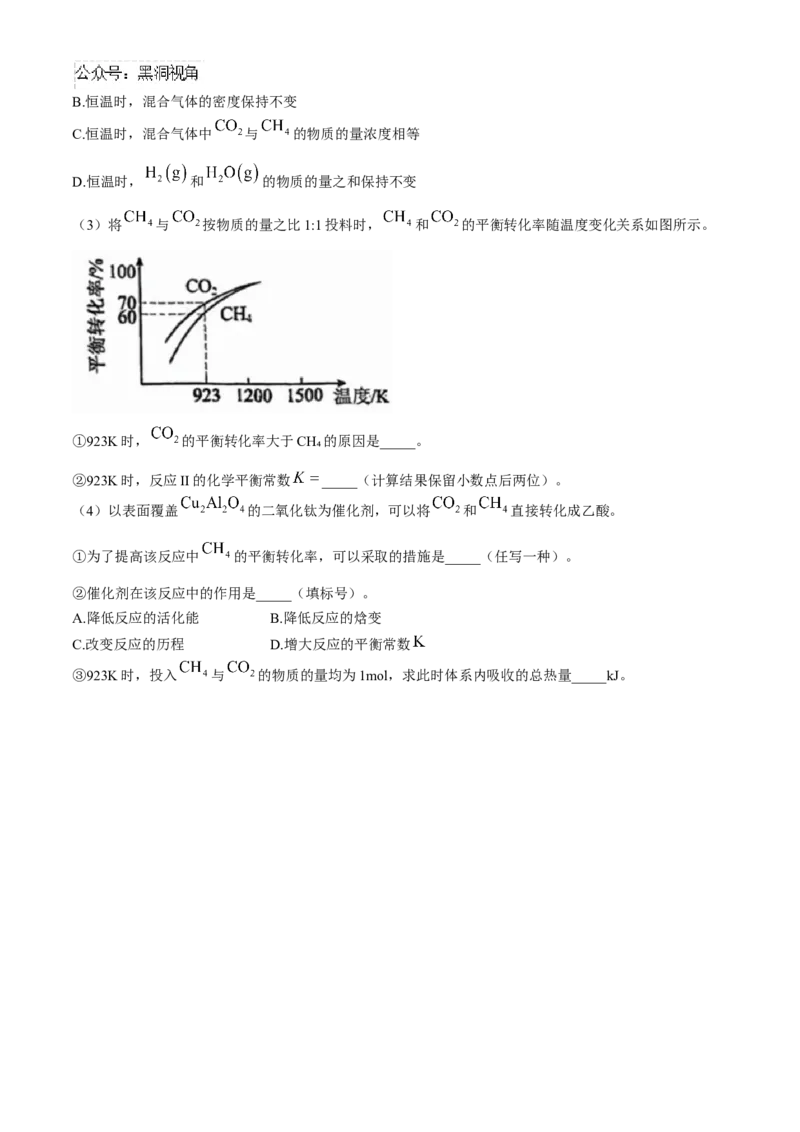
(3)将 与 按物质的量之比1:1投料时, 和 的平衡转化率随温度变化关系如图所示。
①923K时, 的平衡转化率大于CH₄的原因是_____。
②923K时,反应II的化学平衡常数 _____(计算结果保留小数点后两位)。
(4)以表面覆盖 的二氧化钛为催化剂,可以将 和 直接转化成乙酸。
①为了提高该反应中 的平衡转化率,可以采取的措施是_____(任写一种)。
②催化剂在该反应中的作用是_____(填标号)。
A.降低反应的活化能 B.降低反应的焓变
C.改变反应的历程 D.增大反应的平衡常数
③923K时,投入 与 的物质的量均为1mol,求此时体系内吸收的总热量_____kJ。天津市耀华中学 2025 届高三年级第二次月
考参考答案
1 2 3 4 5 6 7 8 9 10 11 12
B D A D C A D C A B B C
13(16分)
(1)磷 >
(2)2:5 肼分子与甲醇都能形成分子间氢键,但肼分子的分子间氢键多
(3)正四面体形 (4) 分子
(5)< Si的半径大于 键长大于 键长,则 键能小于 键能( 的非金属
性比硅大)。
分子中 原子没有孤对电子, 分子中 原子有1对孤对电子,孤对电子越多,对成键电子对的
斥力越大,键角越小(2分)
(6)4 (2分) 其余每空1分
14(18分)
(1)6(1分) 6(1分) 略 (2)醛基 醚键
(3)先进行反应③再进行反应④可以防止酚羟基被氧化
(4)①③② (5)略
(6)
(7)
15(16分)
(1)蒸馏烧瓶(1分) 关闭活塞3,打开活塞2
(2)碳酸氢铵受热易分解
(3)液封隔绝空气,防止 进入三颈烧瓶中氧化(4)过滤速率快,防止 被氧化
取最后一次洗涤液少许于试管中,滴加稀盐酸酸化,无现象,再滴加氯化钡溶液,若无白色沉淀生成,说
明沉淀已经洗涤干净
(5)b(1分) 其余每空2分
16(14分)
(1)+140 (2)AD (3)反应 中 和 的转化率相同, 又发生反应Ⅱ,转化率增
大 0.39 154.4
(4)增大浓度、增大压强等 AC