文档内容
江苏省泰州中学 2024~2025 学年度第一学期期中考试
高二化学试题
(考试时间:75分钟;总分:100分)
命题人:智莹 审题人:石清泉
可能用到的相对原子质量:H-1 C-12 O-16
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
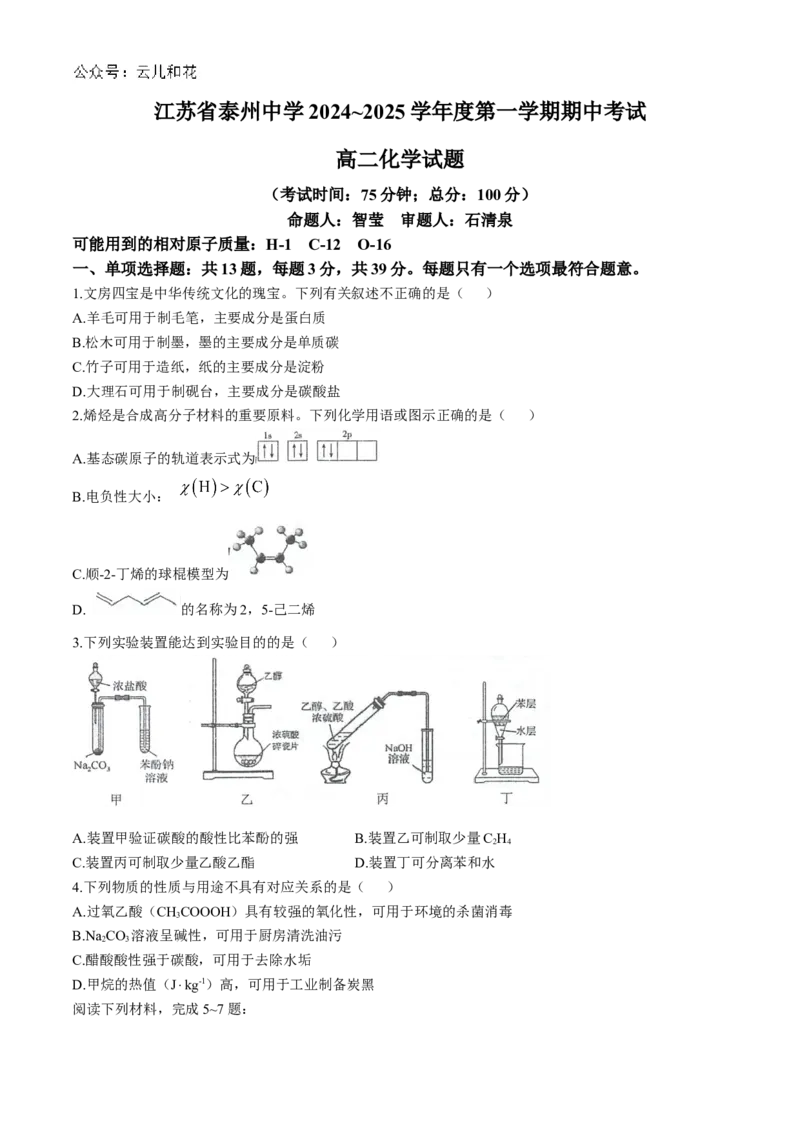
1.文房四宝是中华传统文化的瑰宝。下列有关叙述不正确的是( )
A.羊毛可用于制毛笔,主要成分是蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是淀粉
D.大理石可用于制砚台,主要成分是碳酸盐
2.烯烃是合成高分子材料的重要原料。下列化学用语或图示正确的是( )
A.基态碳原子的轨道表示式为
B.电负性大小:
C.顺-2-丁烯的球棍模型为
D. 的名称为2,5-己二烯
3.下列实验装置能达到实验目的的是( )
A.装置甲验证碳酸的酸性比苯酚的强 B.装置乙可制取少量C H
2 4
C.装置丙可制取少量乙酸乙酯 D.装置丁可分离苯和水
4.下列物质的性质与用途不具有对应关系的是( )
A.过氧乙酸(CHCOOOH)具有较强的氧化性,可用于环境的杀菌消毒
3
B.Na CO 溶液呈碱性,可用于厨房清洗油污
2 3
C.醋酸酸性强于碳酸,可用于去除水垢
D.甲烷的热值(J⋅kg-1)高,可用于工业制备炭黑
阅读下列材料,完成5~7题:碳元素被誉为“生命的核心元素”, 、 和 是碳元素的3种常见核素。CO 是常见的含碳化合物,
2
近年来由于温室效应日益加剧,科学家提出了很多捕集CO 的新手段。在催化剂作用下,CO 可以和H 反
2 2 2
应生成CHOH、CHOCH (二甲醚)、HCOOH、 (尿素)等多种物质。
3 3 3
5.下列说法正确的是( )
A. 、 和 互为同素异形体
B.CO 与H 反应转化为CHOH、CHOCH 、HCOOH,CO 都发生了还原反应
2 2 3 3 3 2
C.HCOOH分子中既有极性键也有非极性键
D.CO 与H 反应生成二甲醚时,使用催化剂降低了反应的焓变
2 2
6.下列化学反应表示不正确的是( )
A.载人航天器内,用LiOH固体吸收过量CO:
2
B.CH 与CO 重整制氢:
4 2
C.NH 和CO 反应生成尿素:
3 2
D.CO 和H 制 :
2 2
7.下列有关描述正确的是( )
A.CO、CHOH、HCOOH中碳原子的杂化轨道类型相同
2 3
B.HCOOH由于H—O键极性比CHCOOH中H—O键极性大,所以酸性更强
3
C. 中 键为6mol
D.CHOH催化氧化为HCHO,CHOH断裂C—O键
3 3
8.各相关物质的燃烧热数据如表。下列热化学方程式正确的是( )
物质
-1559.8 -1411 -285.8
A.
B.
C.
D.
9.有关有机物的检验,下列说法正确的是( )A.用溴水可以鉴别溴乙烷、乙醇和乙醛
B.苯和液溴在FeBr 催化下反应时,直接将生成的气体通入AgNO 溶液,产生浅黄色沉淀,可判断反应中
3 3
一定生成了HBr
C.麦芽糖与稀硫酸共热后加NaOH溶液调至碱性,再加入新制 并加热,产生砖红色沉淀,可判
断麦芽糖发生了水解
D.向电石中滴加饱和食盐水,将生成的气体通入酸性KMnO 溶液中,酸性KMnO 溶液褪色,可判断产生
4 4
的气体一定是乙炔
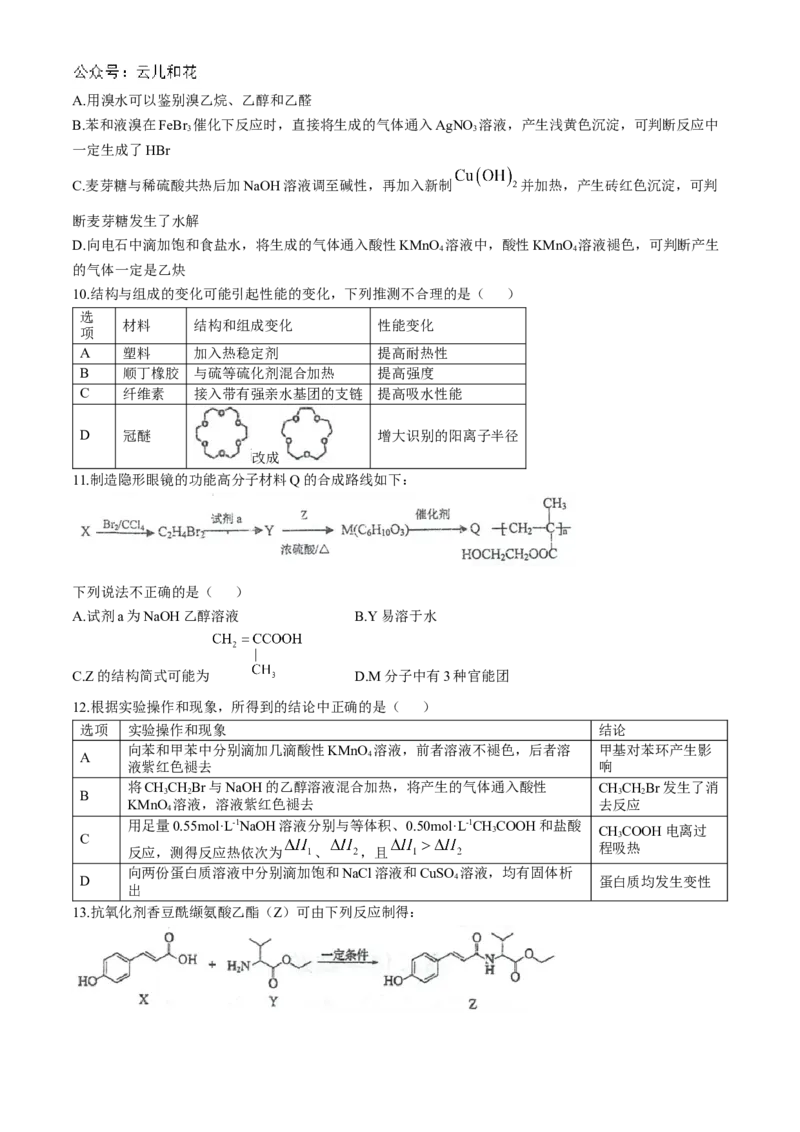
10.结构与组成的变化可能引起性能的变化,下列推测不合理的是( )
选
材料 结构和组成变化 性能变化
项
A 塑料 加入热稳定剂 提高耐热性
B 顺丁橡胶 与硫等硫化剂混合加热 提高强度
C 纤维素 接入带有强亲水基团的支链 提高吸水性能
D 冠醚 增大识别的阳离子半径
改成
11.制造隐形眼镜的功能高分子材料Q的合成路线如下:
下列说法不正确的是( )
A.试剂a为NaOH乙醇溶液 B.Y易溶于水
C.Z的结构简式可能为 D.M分子中有3种官能团
12.根据实验操作和现象,所得到的结论中正确的是( )
选项 实验操作和现象 结论
向苯和甲苯中分别滴加几滴酸性KMnO 溶液,前者溶液不褪色,后者溶 甲基对苯环产生影
A 4
液紫红色褪去 响
将CHCHBr与NaOH的乙醇溶液混合加热,将产生的气体通入酸性 CHCHBr发生了消
B 3 2 3 2
KMnO 溶液,溶液紫红色褪去 去反应
4
用足量0.55mol·L-1NaOH溶液分别与等体积、0.50mol·L-1CH
3
COOH和盐酸
CHCOOH电离过
C 3
程吸热
反应,测得反应热依次为 、 ,且
向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO 溶液,均有固体析
D 4 蛋白质均发生变性
出
13.抗氧化剂香豆酰缬氨酸乙酯(Z)可由下列反应制得:下列说法不正确的是( )
A.X分子中所有原子可能共平面 B.1molX最多可以消耗4molH
2
C.Y分子存在对映异构体 D.1molZ最多可以消耗4molNaOH
二、非选择题:共4题,共61分。
14.(13分)“碳中和”目标如期实现的关键技术之一是CO 的再资源化利用。
2
(1)天然气中普遍含有HS,需回收处理并加以利用。
2
①已知下列反应的热化学方程式:
反应Ⅰ.
反应Ⅱ.
反应Ⅲ.
计算HS热分解反应Ⅳ: 的 ______。
2
②较普遍采用处理HS的方法是克劳斯工艺,即利用反应Ⅰ和Ⅱ生成硫单质。相比克劳斯工艺,利用反应
2
Ⅳ处理HS的优点是______,缺点是______。
2
(2)CO 和H 在催化剂作用下可合成CH,已知:
2 2 4
化学键 C—H H—H C=O H—O
键能(kJ·mol-1) a b c d
则反应 的 ______。
(3)工业上以CO 和NH 为原料在一定温度和压强下合成尿素。
2 3
反应分两步:
ⅰ.CO 和NH 生成NH COONH;
2 3 2 4
ⅱ.NHCOONH 分解生成尿素。
2 4
反应过程中能量变化如图所示:
①反应ⅰ为______反应;反应ⅱ为______反应。(填“吸热”或“放热”)
②写出CO 和NH 合成尿素总反应的热化学方程式______。
2 3
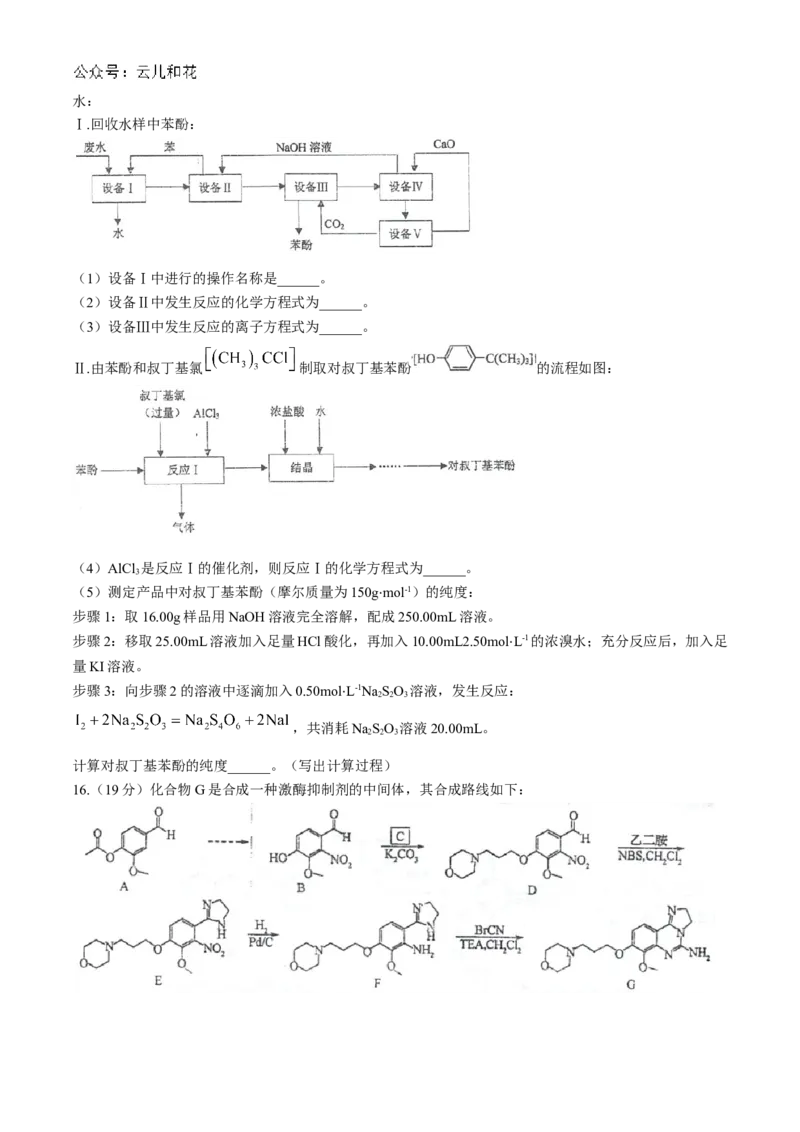
15.(14分)酚类化合物有毒,被列为须重点控制的水污染物之一。某工厂采用下列方法处理含苯酚的废水:
Ⅰ.回收水样中苯酚:
(1)设备Ⅰ中进行的操作名称是______。
(2)设备Ⅱ中发生反应的化学方程式为______。
(3)设备Ⅲ中发生反应的离子方程式为______。
Ⅱ.由苯酚和叔丁基氯 制取对叔丁基苯酚 的流程如图:
(4)AlCl 是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为______。
3
(5)测定产品中对叔丁基苯酚(摩尔质量为150gmol-1)的纯度:
步骤1:取16.00g样品用NaOH溶液完全溶解,配成250.00mL溶液。
⋅
步骤2:移取25.00mL溶液加入足量HCl酸化,再加入10.00mL2.50mol L-1的浓溴水;充分反应后,加入足
量KI溶液。
⋅
步骤3:向步骤2的溶液中逐滴加入0.50molL-1NaSO 溶液,发生反应:
2 2 3
⋅
,共消耗NaSO 溶液20.00mL。
2 2 3
计算对叔丁基苯酚的纯度______。(写出计算过程)
16.(19分)化合物G是合成一种激酶抑制剂的中间体,其合成路线如下:(1)物质A中采用sp3和sp2杂化的碳原子的个数比是______。
(2)反应A→B涉及的反应物有:a.KOH溶液;b.盐酸;c.浓硝酸、浓硫酸。
①加入反应物的正确顺序是:c、______、______(填字母)。
②写出在物质A中加入c时发生反应的化学方程式______。
(3)C的分子式为C H ONCl,其结构简式为______。
7 14
(4)已知乙二胺的结构简式为HNCH CHNH ,D→E需经历D→X→E的过程。D→X为加成反应,则
2 2 2 2
X→E的反应类型为______。
(5)已知F→G中存在: 。TEA为 ,是一种有机碱,
能促进反应进行的原因是______。 、 、 三者中碱性最强的
是______(填结构简式),原因是______。
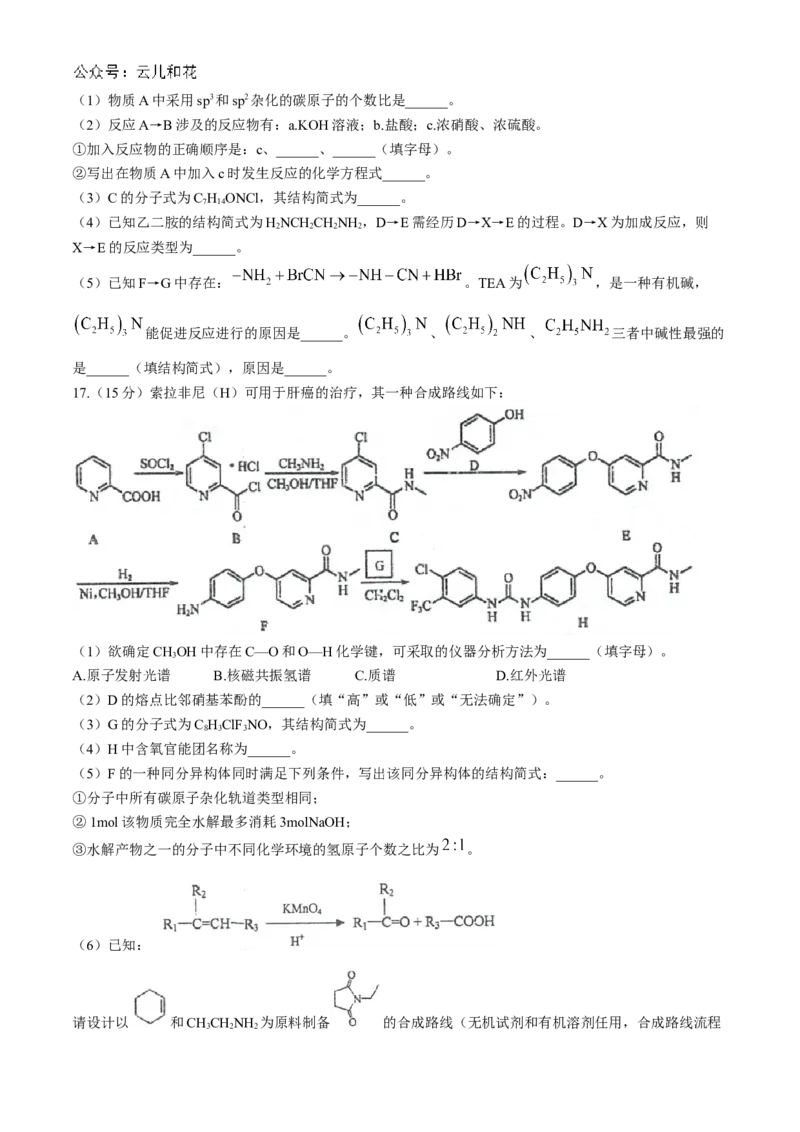
17.(15分)索拉非尼(H)可用于肝癌的治疗,其一种合成路线如下:
(1)欲确定CHOH中存在C—O和O—H化学键,可采取的仪器分析方法为______(填字母)。
3
A.原子发射光谱 B.核磁共振氢谱 C.质谱 D.红外光谱
(2)D的熔点比邻硝基苯酚的______(填“高”或“低”或“无法确定”)。
(3)G的分子式为C HClF NO,其结构简式为______。
8 3 3
(4)H中含氧官能团名称为______。
(5)F的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______。
①分子中所有碳原子杂化轨道类型相同;
②1mol该物质完全水解最多消耗3molNaOH;
③水解产物之一的分子中不同化学环境的氢原子个数之比为 。
(6)已知:
请设计以 和CHCHNH 为原料制备 的合成路线(无机试剂和有机溶剂任用,合成路线流程
3 2 2图示例见题干)。江苏省泰州中学 2024~2025 学年度第一学期期中考试
高二化学试题参考答案
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1 2 3 4 5 6 7
C C D D B A B
8 9 10 11 1 13
2
B A D A C D
二、非选择题:共4题,共61分。
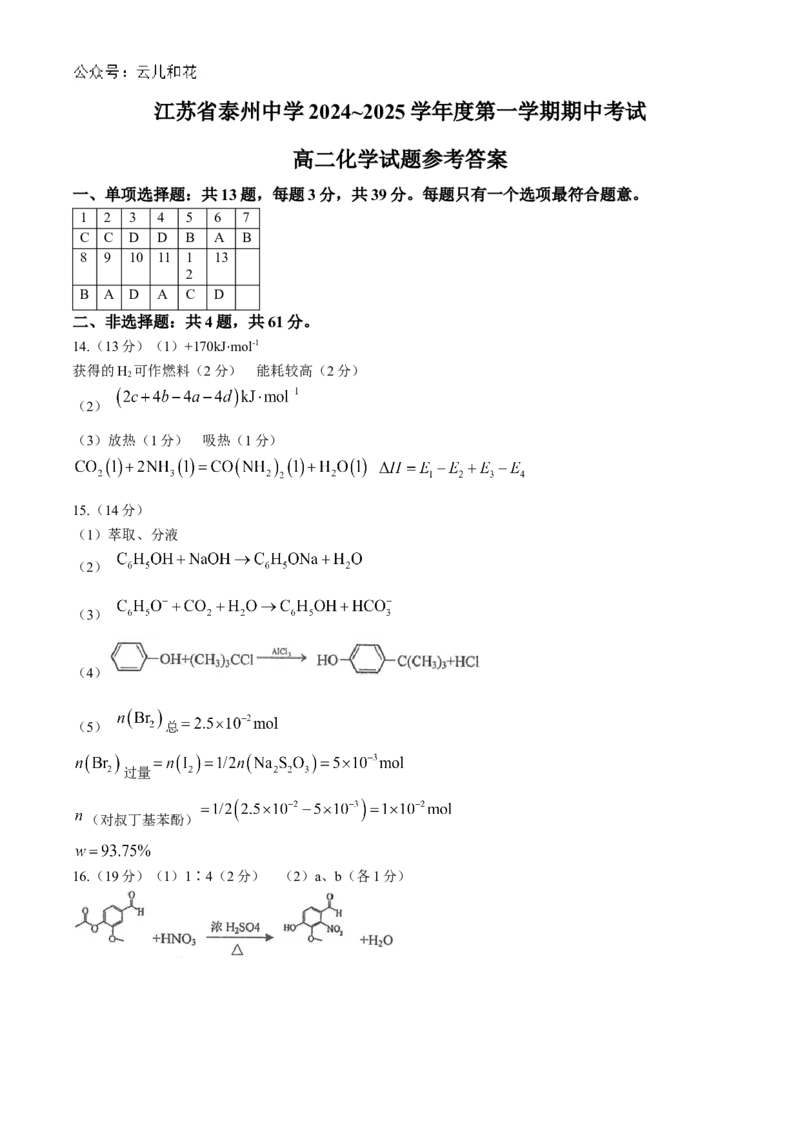
14.(13分)(1)+170kJmol-1
获得的H 可作燃料(2分) 能耗较高(2分)
2 ⋅
(2)
(3)放热(1分) 吸热(1分)
15.(14分)
(1)萃取、分液
(2)
(3)
(4)
(5) 总
过量
(对叔丁基苯酚)
16.(19分)(1)1∶4(2分) (2)a、b(各1分)(3)
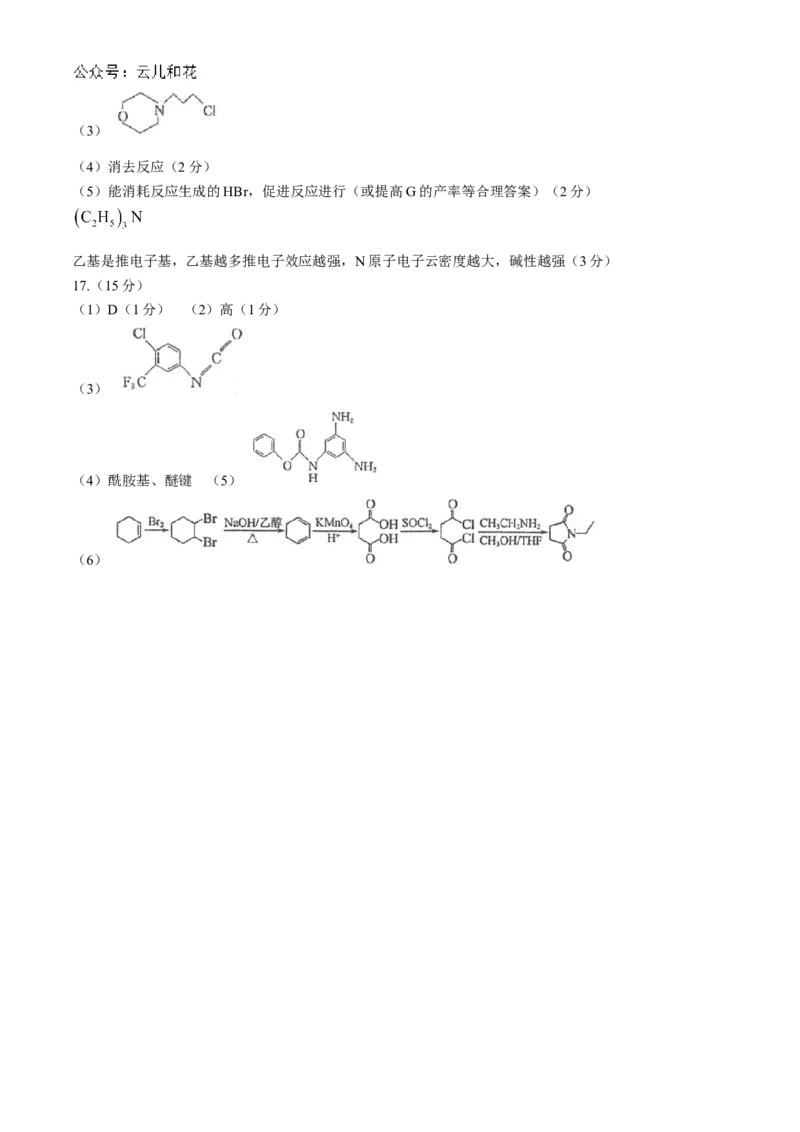
(4)消去反应(2分)
(5)能消耗反应生成的HBr,促进反应进行(或提高G的产率等合理答案)(2分)
乙基是推电子基,乙基越多推电子效应越强,N原子电子云密度越大,碱性越强(3分)
17.(15分)
(1)D(1分) (2)高(1分)
(3)
(4)酰胺基、醚键 (5)
(6)