文档内容
阿克苏市实验中学
B.稀氨水吸收足量 :
2023-2024 学年第一学期高三年级第二次月考化学试卷
C.Na与HO反应:
2
( 试卷分值:100分 所需时间:90分钟 )
D.向NaHCO 溶液中加入少量氢氧化钡溶液:
3
相关原子量:H:1 C:12 O:16 Na:23 Fe:56 Cu:65 Zn:64 S:32 Al:27 Ag:108 Cl:35.5 7、设计如下实验探究草酸(HCO) 性的质(已知:室温时,0.1 mol/L HCO 的pH为1.3),
2 2 4 2 2 4
一、选择题(每题只有一个正确选项,每题2分,共计42分) 由以下对草酸的描述得到的结论及解释正确的是( )
1、化学与生产生活密切相关,下列生产生活项目中蕴含的化学知识错误的是( )
实验 装置 试剂a 现象
选项 生产生活项目 化学知识
Ca(OH) 溶液(含酚
A 明矾作净水剂 明矾水解生成Al(OH) 胶体,吸附杂质 ① 2 溶液褪色,产生白色沉淀
3 酞)
B 船舶外壳镶嵌锌块 形成电解池,牺牲阳极锌块,保护船体
② 少量NaHCO 溶液 产生气泡
C 用碳酸钠溶液处理水垢中的硫酸钙 微溶的CaSO 转化为更难溶的CaCO 3
4 3
D 用排饱和食盐水收集氯气 增大c(Cl﹣),降低氯气在水中的溶解
③ 酸性KMnO 溶液 紫色溶液褪色
4
度
2、下列有关物质的性质和用途说法不正确的是( ) ④ C 2 H 5 OH和浓硫酸 加热后产生有香味物质
A.利用高纯单质硅的半导体性能,可以制成光电池
A. 草酸有酸性:
B.国庆节天安门广场燃放烟花,色彩绚丽, 利用了某些金属元素的焰色试验
B. HCO 酸性强于HCO:
C.NaO 与CO 反应放出氧气,可用于制作呼吸面具 2 2 4 2 3
2 2 2
D.用氯化铁溶液刻蚀覆铜板制作印刷电路板, 铜与FeCl 发生置换反应
3
C. 草酸具有还原性:
3、下列化学用语或图示表达正确的是( )
A.基态N原子的价层电子排布式:2s32p2 B.SO 的分子空间构型:三角锥型
3 D. 草酸能发生酯化反应生成具有香味的酯类物质,浓硫酸在此过程中仅为脱水剂
C.HClO的电子式: D.顺﹣2﹣丁烯的结构简式: 8.部分含Fe物质的分类与相应化合价关系如图所示。下列说法不正确的是( )
4、设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 标准状况下,11.2LCH 含有 键数目为3N
2 4 A
B. 0.1 mol/L CHCOONa溶液中,含CHCOO-的数目小于0.1N
3 3 A
C. 常温下, 含0.2 mol HSO 的浓硫酸与足量的铁反应,转移的电子数大于0.2N
2 4 A
D.2molNO与1molO 在密闭容器中充分反应后的分子数小于2N
2 A
A.存在a→f→d→e的转化 B.a可与水蒸气反应生成b
5、下列“类推”合理的是( )
A.Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H C.g的溶液可用于检验苯酚 D.c常用作涂料
2 2 2 3 2
B.SO 可与水反应生成HSO,则SiO 可与水反应生成HSiO
2 2 3 2 2 3 9下列物质间的转化能实现的是( )
C.铁与硫加热反应生成FeS,则铜与硫加热反应生成CuS
2
D.Cl 2 与H 2 O反应生成HCl和HClO,则F 2 与H 2 O反应生成HF和HFO A.Al 2 O 3 N → aOHNaAlO 2 通入 → CO 2Al(OH) 3 B.SiO 2→ HClH 2 SiO 3 NaO → H溶液Na 2 SiO 3
6、下列化学反应的离子方程式正确的是( )
A.向NaClO溶液中通入NH 3 会有N 2 生成:
C.饱和NaCl
→
CO 2NaHCO
3 →
Δ Na
2
CO
3
D.Fe点
→
燃Fe
2
O
3
盐
→
酸FeCl
3
NaO
→
H溶液Fe(OH)
3
胶体
10、常温下,下列各组离子在指定溶液中可能大量共存的是( )
第11页 共24页 ◎ 第12页 共24页
学科网(北京)股份有限公司A.无色溶液中:SO2-、NH+、MnO¯、Na+、
4 4 4
B.0.1mol•L﹣1的KNO 溶液中:H+、Fe2+、Cl﹣、SO2-
3 4
C.酸性溶液中:Fe3+、SO2-、Na+、Cl¯
4
D.水电离出的c(H+)=1×10﹣13mol•L﹣1的溶液中:Na+、K+、HCO¯、NO¯
3 3
11、已知反应:KClO+6HCl(浓)=KCl+3Cl↑+3HO,据此判断下列说法正确( )
3 2 2
A.KCl为还原产物 B.HCl全部发生氧化反应
C.反应表明氧化性KClO 比Cl 强 D.1mol KClO 在反应中得到6mole-
3 2 3
12、如表实验操作能达到实验目的的是( )
选项 实验操作 实验目的
A 向足量酸性KMnO 溶液中滴加少量FeCl 溶液,振荡 验证Fe2+具有还原性
4 2
B 用洁净的铂丝蘸取KCl溶液在酒精灯外焰上灼烧 观察钾元素的焰色
其中实验 和 (填实验序号)可以鉴别NaCO 和NaHCO
2 3 3。
C 将FeCl 固体溶于浓盐酸后再稀释 配制FeCl 溶液
3 3
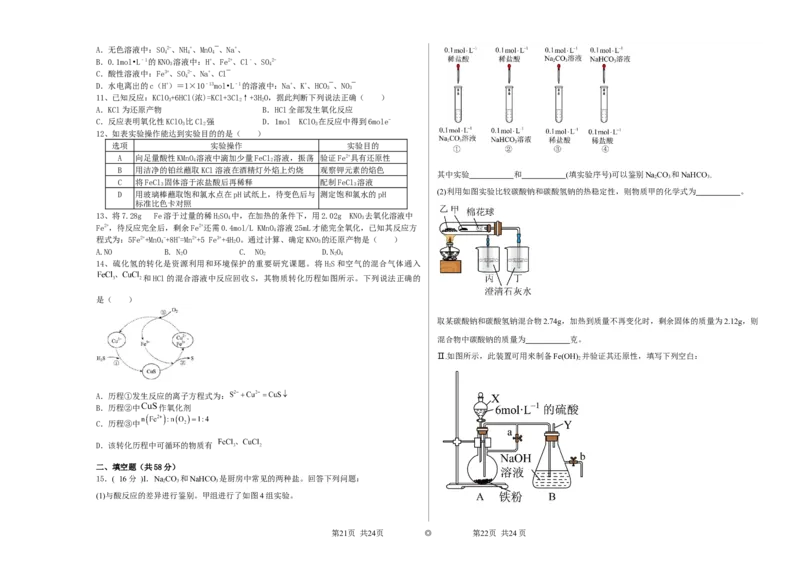
(2)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为 。
D 用玻璃棒蘸取饱和氯水点在pH试纸上,待变色后与 测定饱和氯水的pH
标准比色卡对照
13、将7.28g Fe溶于过量的稀HSO 中,在加热的条件下,用2.02g KNO 去氧化溶液中
2 4 3
Fe2+,待反应完全后,剩余Fe2+还需0.4mol/L KMnO 溶液25mL才能完全氧化,已知其反应方
4
程式为:5Fe2++MnO-+8H+=Mn2++5 Fe3++4HO。通过计算、确定KNO 的还原产物是( )
4 2 3
A.NO B. NO C. NO D.NO
2 2 2 4
14、硫化氢的转化是资源利用和环境保护的重要研究课题。将HS和空气的混合气体通入
2
和HCl的混合溶液中反应回收S,其物质转化历程如图所示。下列说法正确的
是( )
取某碳酸钠和碳酸氢钠混合物2.74g,加热到质量不再变化时,剩余固体的质量为2.12g,则
混合物中碳酸钠的质量为 克。
Ⅱ.如图所示,此装置可用来制备Fe(OH) 并验证其还原性,填写下列空白:
2
A.历程①发生反应的离子方程式为:
B.历程②中 作氧化剂
C.历程③中
D.该转化历程中可循环的物质有
二、填空题(共58分)
15.( 16分 )I.NaCO 和NaHCO 是厨房中常见的两种盐。回答下列问题:
2 3 3
(1)与酸反应的差异进行鉴别。甲组进行了如图4组实验。
第21页 共24页 ◎ 第22页 共24页
学科网(北京)股份有限公司(5)已知胆矾的溶解度随温度变化如图所示。
(3)制备Fe(OH) :
2
仪器X的名称为 ,实验开始时先将止水夹“a”打开,滴入HSO 和铁粉反应。
2 4
一段时间后关闭止水夹a,使A中溶液流入B中进行反应。
(4)验证Fe(OH) 还原性:
2
实验完毕,打开b处止水夹,充入一部分空气,此时B瓶中发生的反应为(写化学方程式)
,现象: 。
(5)某同学欲用36.5%浓盐酸(密度1.2g/mL)配制480mL上述实验所需盐酸。 从CuSO 溶液中提取胆矾,采用“一系列操作”包括蒸发浓缩、 、过滤、洗涤、
4
配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果 (填写“偏大”、“偏
低温干燥。
小”、“不变”)。
16.(12分)胆矾(或蓝矾)在日常生活中有广泛应用,如配制农药波尔多液、作游泳池的消
17.(12分)明矾[KAl(SO)•12H O]是一种常用的净水剂,以废易拉罐(主要成分为铝和少
4 2 2
毒剂。某小组以辉铜矿粉(主要成分是Cu S) 为原料制备胆矾及副产品的简易流程如下:
2 量不溶于碱性溶液的物质)为原料制取明矾晶体的实验流程如图:
回答下列问题:
(1)“碱溶”步骤中发生反应的化学方程式为 。
请回答下列问题: (2)“沉铝”步骤在煮沸条件下进行,生成Al(OH) 、NH 和NaHCO 。检验“沉铝”所得滤液
3 3 3
(1)反应1中被氧化的元素为 (填元素符号);
中主要阳离子的定性分析操作为 (填操作名称)。
在上述反应1~6中属于氧化还原反应的有 个(填数字)。
(3)由浓硫酸配制250mL“酸溶”所需的9mol•L-1HSO 溶液需要用到的玻璃仪器有烧杯、玻璃
2 4
(2)反应3的化学方程式为: 。
棒、量筒、 、 。
(3)反应6的离子方程式为: 。
(4)“酸溶”步骤在如图所示的装置中进行,导管的作用是 。圆底烧瓶中发生反应的
(4)Na SO 在空气中易氧化变质生成 (填化学式)。
2 3 离子方程式为 。
第31页 共24页 ◎ 第32页 共24页
学科网(北京)股份有限公司色的晶体,如 晶体为淡绿色。将 溶于水,一定条件下结晶析出暗
绿色晶体。称取5.33g该暗绿色晶体溶于水配成暗绿色溶液,加入足量的 溶液,得到
2.87g白色沉淀。
① 中存在的化学键有_____(填序号)。
a.配位键 b.氢键 c.离子键 d.金属键
②该暗绿色晶体的化学式为_____ 。
18、(18分)三氯化铬( )是常用的催化剂,易潮解,易升华,高温下易被氧化。某化
学小组采用如下流程制备无水三氯化铬并探究三氯化铬六水合物的结构。
已知: 沸点为8.2℃,有毒,易水解
回答下列问题:
(1)基态铬原子核外电子排布式为 ,三氯化铬固体的晶体类型为
(2)“热分解”发生反应的化学方程式为__ ___
(3)“热反应”制无水 的实验装置如图所示(AD中加热装置略)。
①实验装置连接顺序为:b→_____,_____→_____,_____→_____,_____→_____(填仪器
接口字母)
②加热反应前通 的目的是 。
③A中仪器x的名称是__ _ __,其作用是 ___ _ _。
④E中收集的物质含有 __ _ _ _(写化学式)。
⑤尾气经_ _ _ _ _ 处理后可循环使用。
(4)已知 配合物(Mr=266.5,配位数为6)有多种异构体,不同条件下析出不同颜
第41页 共24页 ◎ 第42页 共24页
学科网(北京)股份有限公司第 5 页 共 5 页
学科网(北京)股份有限公司