文档内容
2025年高二下学期化学入学考试试题
一、单选题(共48分)
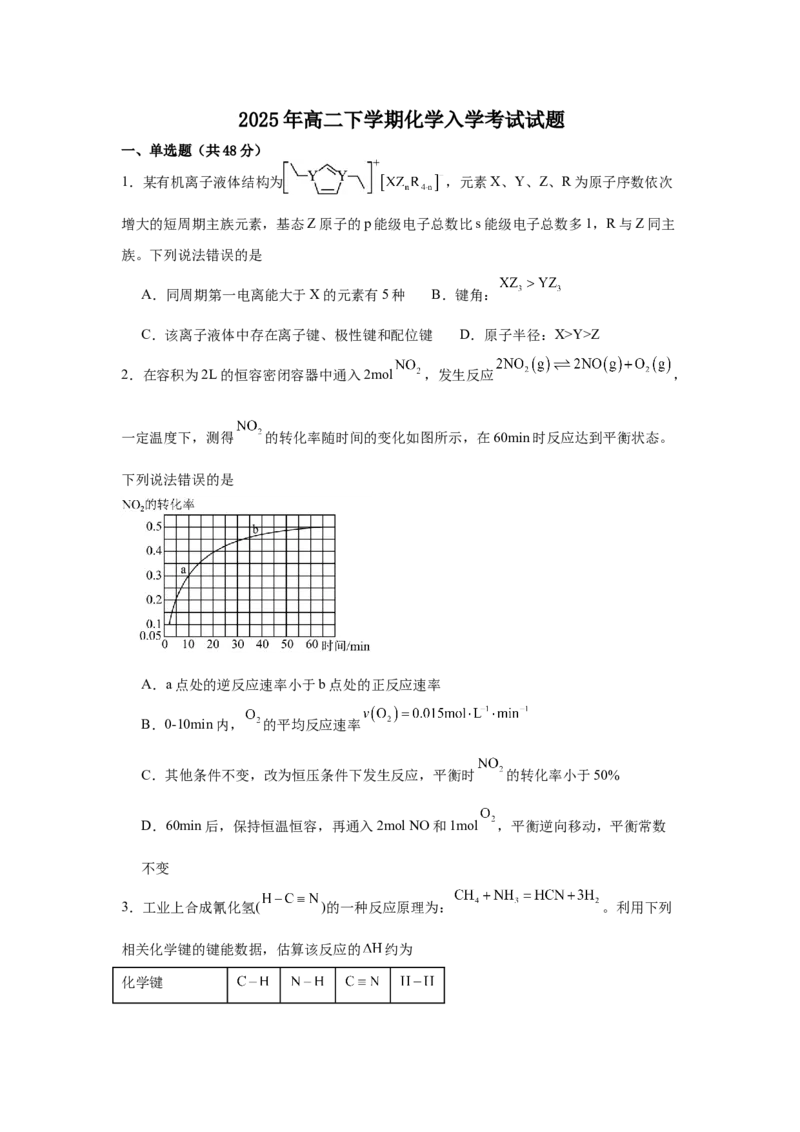
1.某有机离子液体结构为 ,元素X、Y、Z、R为原子序数依次
增大的短周期主族元素,基态Z原子的p能级电子总数比s能级电子总数多1,R与Z同主
族。下列说法错误的是
A.同周期第一电离能大于X的元素有5种 B.键角:
C.该离子液体中存在离子键、极性键和配位键 D.原子半径:X>Y>Z
2.在容积为2L的恒容密闭容器中通入2mol ,发生反应 ,
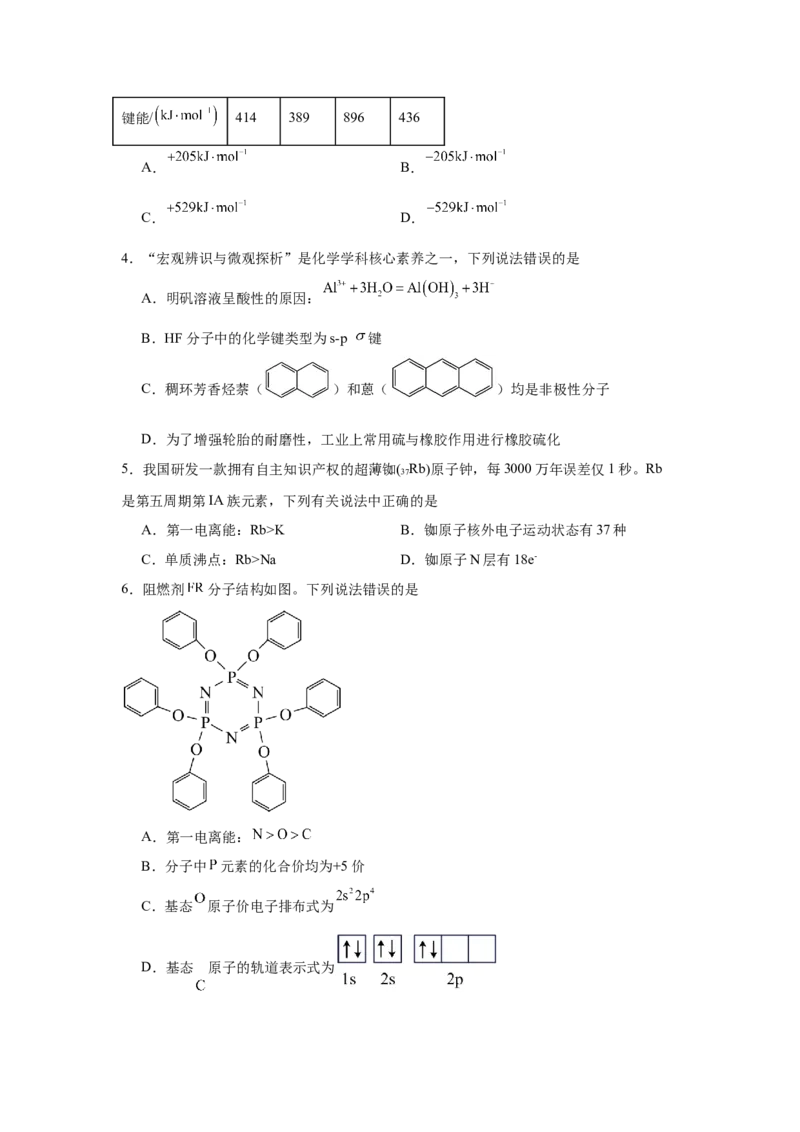
一定温度下,测得 的转化率随时间的变化如图所示,在60min时反应达到平衡状态。
下列说法错误的是
A.a点处的逆反应速率小于b点处的正反应速率
B.0-10min内, 的平均反应速率
C.其他条件不变,改为恒压条件下发生反应,平衡时 的转化率小于50%
D.60min后,保持恒温恒容,再通入2mol NO和1mol ,平衡逆向移动,平衡常数
不变
3.工业上合成氰化氢( )的一种反应原理为: 。利用下列
相关化学键的键能数据,估算该反应的 约为
化学键键能/ 414 389 896 436
A. B.
C. D.
4.“宏观辨识与微观探析”是化学学科核心素养之一,下列说法错误的是
A.明矾溶液呈酸性的原因:
B.HF分子中的化学键类型为s-p 键
C.稠环芳香烃萘( )和蒽( )均是非极性分子
D.为了增强轮胎的耐磨性,工业上常用硫与橡胶作用进行橡胶硫化
5.我国研发一款拥有自主知识产权的超薄铷 Rb原子钟,每3000万年误差仅1秒。Rb
37
是第五周期第IA族元素,下列有关说法中正确的是
A.第一电离能:Rb>K B.铷原子核外电子运动状态有37种
C.单质沸点:Rb>Na D.铷原子N层有18e-
6.阻燃剂 分子结构如图。下列说法错误的是
A.第一电离能:
B.分子中 元素的化合价均为+5价
C.基态 原子价电子排布式为
D.基态 原子的轨道表示式为7.镍为新材料的主角之一,鉴定 的特征反应为
下列说法错误的是
A.基态Ni原子核外占据最高能层电子的电子云轮廓图形状为球形
B.氮原子的杂化方式均为 杂化
C.鲜红色沉淀中存在的作用力主要有共价键、配位键、氢键
D.丁二酮肟中所有原子可能共平面
8.常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=13的溶液中:Na+、 、Al3+、ClO-
B. =1×10-6的溶液中:K+、Fe3+、Cl-、
C.水电离出来的c(H+)=1×10-12mol/L的溶液中: 、K+、 、Fe2+
D.c(H+)=1×10-2mol/L的溶液中:Na+、K+、 、Cl-
9.LiFePO 常作为锂离子电池的正极材料,电池充电时,LiFePO 脱出部分 形成
4 4
。下列说法正确的是
A.Fe元素位于元素周期表第ⅦB族
B.第三周期元素中,第一电离能介于Al和P之间的元素有2种
C.基态氧原子的核外电子的空间运动状态有5种
D.充电时阳极反应式为
10.下列指定反应的离子方程式书写正确的是
A.向 溶液中滴加 溶液至溶液呈中性:B.少量 通入NaClO溶液中:
C.铜在氨水中被腐蚀:
D.用淀粉KI溶液检验 :
11.为增强铝的耐腐蚀性,以铅蓄电池为外电源,以Al作阳极、Pb作阴极电解稀硫酸,
使铝表面的氧化膜增厚。电解过程中,下列判断正确的是
选项 铅蓄电池 电解池
移向Pb电极 移向Pb电极
电极增重64 g 铝电极增重16 g
负极: 阳极:
硫酸浓度减小 硫酸浓度不变
A.A B.B C.C D.D
12.物质的结构决定物质的性质,下列性质差异与结构因素匹配错误的是
性质差异 结构因素
A 水溶性: 分子极性
B 熔点:金刚石( )高于碳化硅( ) 共价键强度
C 键角: ( )大于 ( ) 中心原子的杂化方式
D 常温下状态: (气体), (液体) 分子间作用力
A.A B.B C.C D.D
13.已知 、 下 。在反应器中
按 投料后,在不同温度下,反应达到平衡时,得到混合物中 的质
量分数随压强的变化曲线a、b、c如图所示。下列说法正确的是A.图中M、N、Q点平衡常数K的大小关系为
B.从Q到M,平衡向左移动
C.M、N、Q达到平衡所需时间关系为
D.该条件下,向反应器中充入 和 ,则反应达平衡时放出热量小于
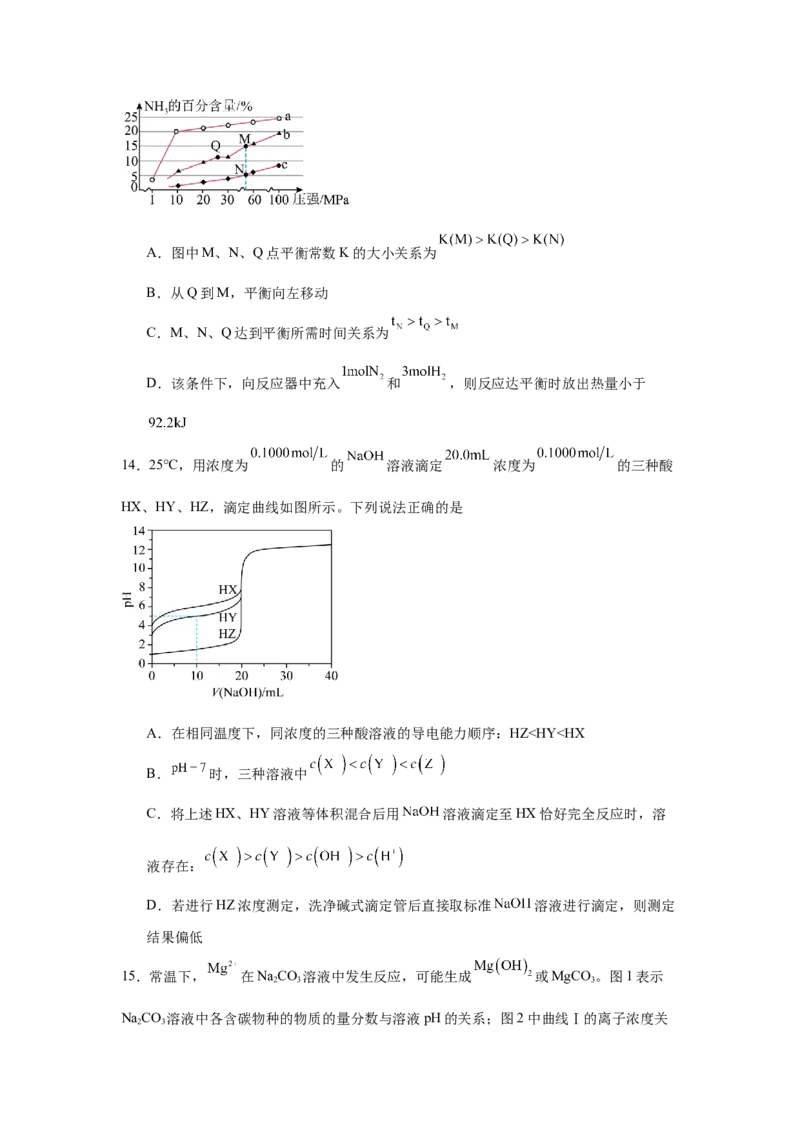
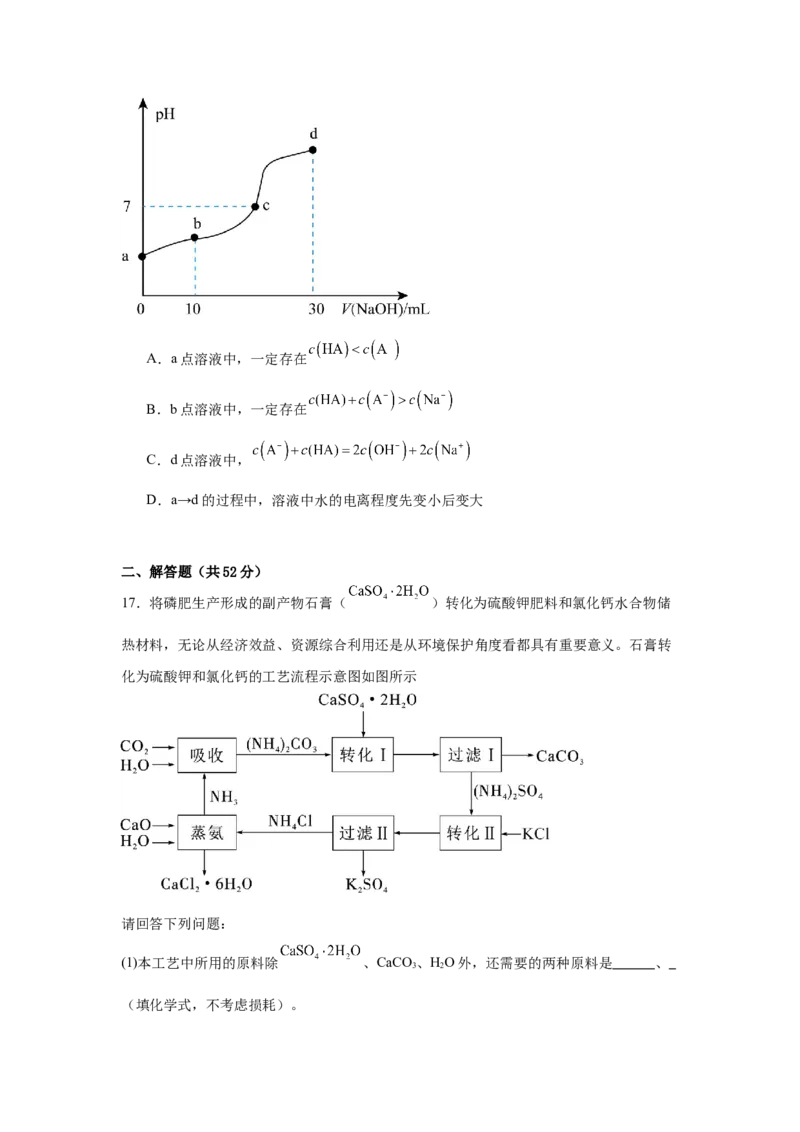
14.25℃,用浓度为 的 溶液滴定 浓度为 的三种酸
HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ”、“<”或“=”),该溶液中所有微粒
(水分子除外)的物质的量浓度由小到大的顺序为 。
(3)转化Ⅰ是将难溶的CaSO(s)转化为更难溶的CaCO (s),将一定量的 加
4 3
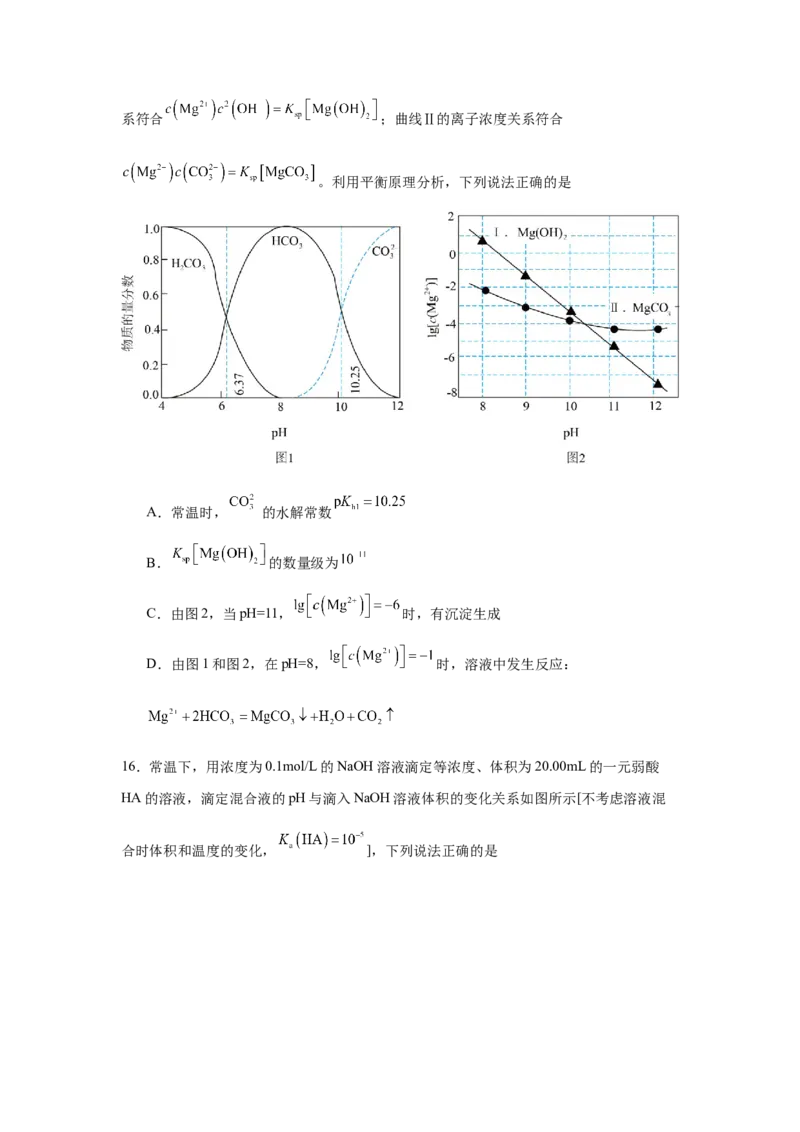
入过量的CaSO 悬浊液中,充分反应后,测得溶液中 ,此时溶液中
4
的 。[已知: 、 ]
(4)已知不同温度下KSO 在100 g水中达到饱和时溶解的量如下表:
2 4
温度/℃ 0 20 40 60 75
KSO 溶解的量/g 7.7 11.1 14.7 18.1 20.5
2 4
75℃的KSO 饱和溶液482 g冷却到20℃,可析出KSO 晶体 g。
2 4 2 4
(5)写出“蒸氨”过程中的化学方程式: 。
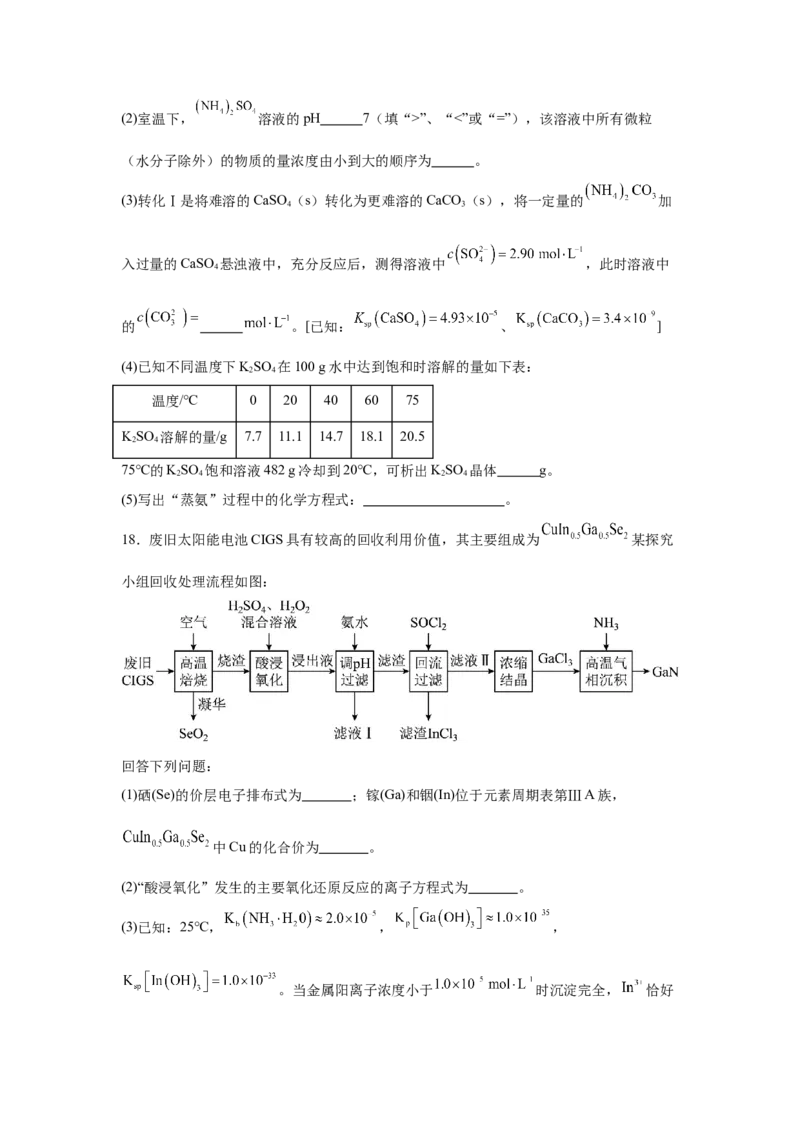
18.废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为 某探究
小组回收处理流程如图:
回答下列问题:
(1)硒(Se)的价层电子排布式为 ;镓(Ga)和铟(In)位于元素周期表第ⅢA族,
中Cu的化合价为 。
(2)“酸浸氧化”发生的主要氧化还原反应的离子方程式为 。
(3)已知:25℃, , ,
。当金属阳离子浓度小于 时沉淀完全, 恰好完全沉淀时溶液的pH约为 (保留一位小数);为探究 在氨水中能否溶解,
计算反应 的平衡常数 。(已知:
,K'= )
(4)“回流过滤”中加入的 是一种液态化合物,极易与水反应,写出 与水反应的
化学反应方程式 ; 有两个作用一是将氢氧化物转化为氯化物,另一个是
。
(5)“高温气相沉积”过程中发生的化学反应方程式为 。
19.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(1)生成氢气:将水蒸气通过红热的炭即产生水煤气。 ;
,该反应在低温下 (“能”或“不
能”)自发进行。该反应的平衡常数表达式 。
(2)已知在400℃时, 的 。相关化学键键能数据为
化学键
键能
946 436 390.8
回答下列问题:
①在400℃时, 的 。该反应的平衡常数表达
式 。
②若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡 (填
“向左”“向右”或“不”)移动;使用催化剂 (填“增大”“减小”或“不改
变”)反应的 。
20.萘类物质的加成反应,可以合成多种环状结构的异构体,并在工业中有重要应用,利用1-甲基萘( )制备四氢萘类物质( ,包括 和 )。反应过程中伴有生
成十氢萘( )的副反应,涉及反应如图:
请回答下列问题:
(1)已知一定条件下反应 的焓变分别为 ,则反应 的焓变
(用含 的代数式表示)。
(2)根据 和 的结构及命名方式, 和 的一种同分异构体
的名称为 。
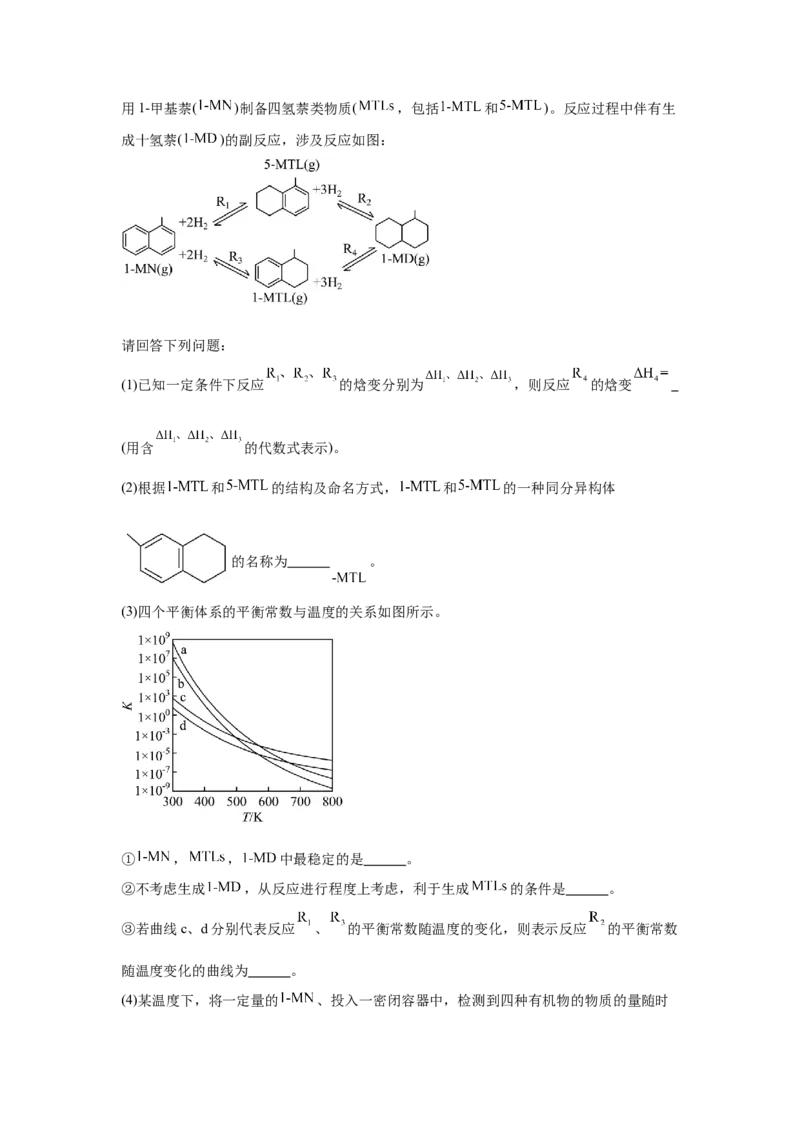
(3)四个平衡体系的平衡常数与温度的关系如图所示。
① , , 中最稳定的是 。
②不考虑生成 ,从反应进行程度上考虑,利于生成 的条件是 。
③若曲线c、d分别代表反应 、 的平衡常数随温度的变化,则表示反应 的平衡常数
随温度变化的曲线为 。
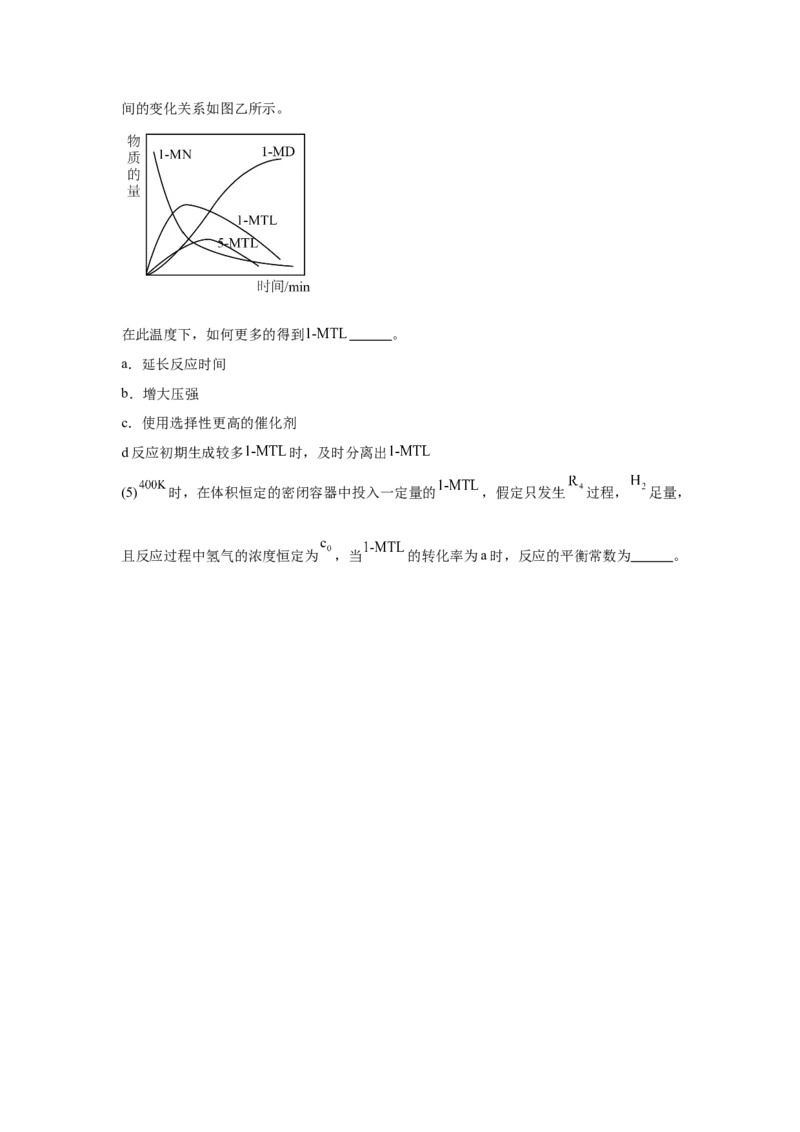
(4)某温度下,将一定量的 、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
在此温度下,如何更多的得到 。
a.延长反应时间
b.增大压强
c.使用选择性更高的催化剂
d反应初期生成较多 时,及时分离出
(5) 时,在体积恒定的密闭容器中投入一定量的 ,假定只发生 过程, 足量,
且反应过程中氢气的浓度恒定为 ,当 的转化率为a时,反应的平衡常数为 。题号 1 2 3 4 5 6 7 8 9 10
答案 A C A A B D D D C A
题号 11 12 13 14 15 16
答案 B C D B D B
17.(1) KCl NH
3
(2) <
(3)
(4)37.6
(5)
18.(1) 4s24p4 +1
(2)
(3) 4.7
(4) 作溶剂
(5)
19.(1) 不能
(2) 向左 不改变
20.(1)
(2)6
(3) 1-MD 低温高压 b
(4)cd(5)