文档内容
2024 级高二第一学期第一次限时练习化学试卷
命题人: 审题人: 满分:100分 考试时间:75分钟
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23
一、选择题:本题共20个小题,每小题3分,共60分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列科技成果中蕴含的化学知识叙述正确的是( )
A.高效光解水催化剂能降低化学反应的焓变
B.建造“福厦高铁”跨海大桥所采用的免涂装耐候钢属于合金
C.运载火箭所采用的“液氢液氧”推进剂可把化学能全部转化为热能
D.利用海洋真菌可降解聚乙烯等多种塑料,且温度越高降解速率越快
2.下列反应中,生成物的总焓大于反应物总焓的是( )
A.硫在氧气中燃烧 B.氢氧化钡晶体与氯化铵混合
C.NaOH溶液与HSO 溶液混合 D.Al在高温条件下与Fe O 反应
2 4 2 3
3.下列事实中,不能用勒夏特列原理解释的是( )
A.夏天,打开啤酒瓶时会从瓶口逸出气泡
B.使用催化剂可加快SO 转化为SO 的速率
2 3
C.将盛有二氧化氮和四氧化二氮混合气体的密闭容器置于冷水中,混合气体颜色变浅
D.用饱和食盐水除去氯气中的氯化氢气体
4.已知:25℃、101kPa时,0.5mol 完全燃烧生成液态水放出142.9kJ的热量,下列能表达 燃烧热
的热化学方程式中书写正确的是( )
A.
B.
C.
D.
5.以NO 为新型硝化剂的硝化反应具有反应条件温和、选择性高、无副反应发生、过程无污染等优点。
2 5
NO 可通过NO 臭氧化法制备。
2 5 2 4
已知:①NO(g)===2NO(g) ΔH
2 4 2 1
②2O (g)===3O (g) ΔH
3 2 2
③2NO(s)===4NO(g)+O(g) ΔH
2 5 2 2 3
则NO(g)+O(g)===N O(s)+O(g)的ΔH为( )
2 4 3 2 5 2
A.ΔH+ΔH-ΔH B.2ΔH-ΔH+ΔH
1 2 3 1 2 3
C.ΔH+ΔH-ΔH D.2ΔH+ΔH+ΔH
1 2 3 1 2 3
6.反应A(g)+3B(g)⇌2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是( )
A.v(A)=0.15mol•L-1•min-1 B.v(B)=0.01mol•L-1•s-1
C.v(C)=0.0075mol•L-1•s-1 D.v(D)=0.40mol•L-1•min-1
7.已知化学反应A(g)+B (g) 2AB(l)的能量变化如图所示,判断下列叙述中正确的是( )
2 2
A.每生成2mol气态AB放出bkJ热量
B.向密闭容器中充入1molA 和1molB 充分反应,吸收的热量为(a-b)kJ
2 2
C.向密闭容器中充入一定量的A 和B ,生成2molAB(g)吸收的热量小于(a-b)kJ
2 2D.AB(l)分解为A(g)和B (g)的反应为放热反应
2 2
8.将8molA气体和4molB气体置于2L的密闭容器中,学生如下反应2A(g)+B(g) 2C(g)。若经20s后测
得C的浓度为3.6mol/L,下列不正确的是( )
⇌
A.20s内,用物质A表示的反应速率为
B.20s时,物质A的转化率为45%
C.20s内,用物质B表示的反应速率为5.4 mol·L-1·min-l
D.20s时物质B的浓度为0.2mol/L
9.下列装置与设计不能达到实验目的的是( )
选项 A B
装置与设
计
目的 测定锌与稀硫酸反应生成氢气的速率 探究催化剂对反应速率的影响
选项 C D
装置与设
计
目的 证明铝片与盐酸的反应为放热反应 探究温度对化学平衡的影响
10.某温度下,容积一定的密闭容器中进行以下反应: ,下列叙
述中正确的是( )
A.在容器中加入氩气,反应速率不变
B.加入少量W,逆反应速率增大
C.升高温度,正反应速率增大,逆反应速率减小
D.将容器的容积缩小,可增大活化分子的百分数,有效碰撞次数增多
11.某温度下,往密闭容器中加入一定量的A和B,发生 的反应。C的物质的浓度
随反应时间(t)的变化如下表。下列说法中不正确的是( )
t/s 2 4 6 8 10 12
C的浓度/( ) 0.22 0.36 0.42 0.46 0.46 0.46
A.在0~6s内,平均反应速率v(A)为0.14
B.0~8s正反应速率大于逆反应速率
C.8s后反应物消耗完,反应停止
D.8~12s该反应处于化学平衡状态
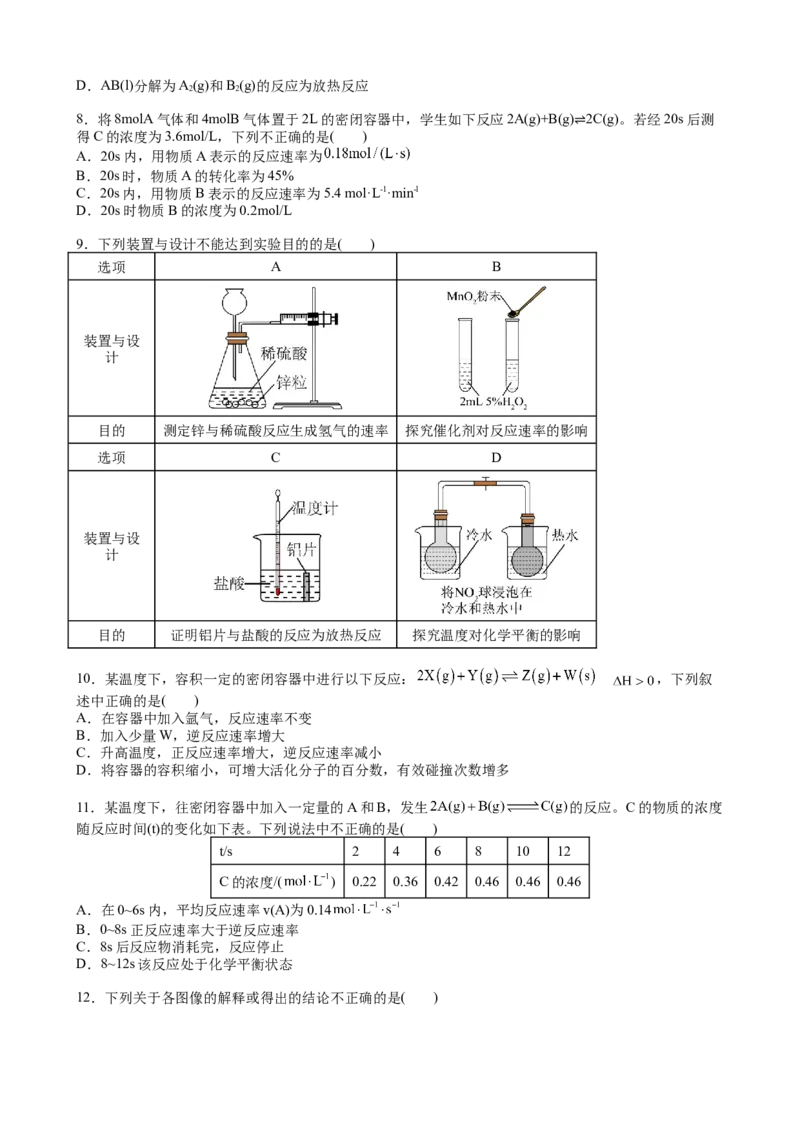
12.下列关于各图像的解释或得出的结论不正确的是( )A.由甲图可知,反应在 时刻可能改变了压强或使用了催化剂
B.由乙图可知,反应在m点可能达到了平衡状态
C.由丙图可知,C点:
D.由丁图可知,交点A表示反应一定处于平衡状态,此时
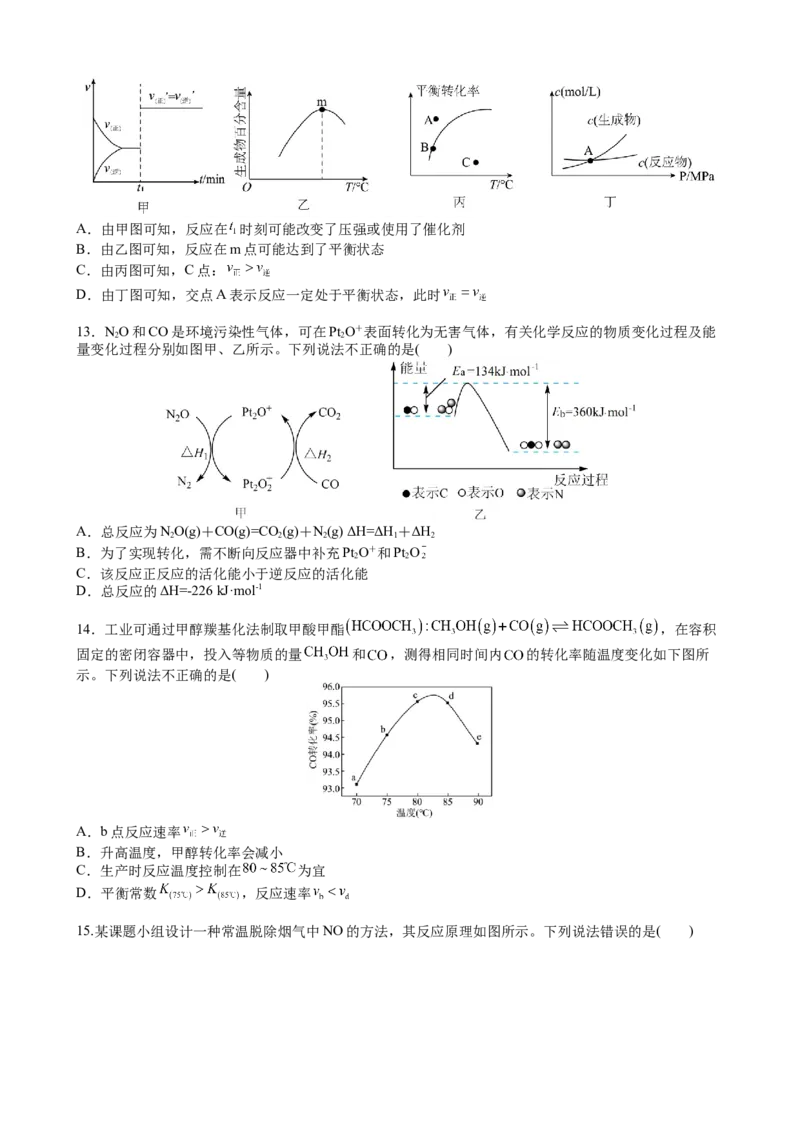
13.NO和CO是环境污染性气体,可在Pt O+表面转化为无害气体,有关化学反应的物质变化过程及能
2 2
量变化过程分别如图甲、乙所示。下列说法不正确的是( )
A.总反应为NO(g)+CO(g)=CO(g)+N(g) ΔH=ΔH +ΔH
2 2 2 1 2
B.为了实现转化,需不断向反应器中补充Pt O+和Pt O
2 2
C.该反应正反应的活化能小于逆反应的活化能
D.总反应的ΔH=-226 kJ·mol-1
14.工业可通过甲醇羰基化法制取甲酸甲酯 ,在容积
固定的密闭容器中,投入等物质的量 和 ,测得相同时间内 的转化率随温度变化如下图所
示。下列说法不正确的是( )
A.b点反应速率
B.升高温度,甲醇转化率会减小
C.生产时反应温度控制在 为宜
D.平衡常数 ,反应速率
15.某课题小组设计一种常温脱除烟气中NO的方法,其反应原理如图所示。下列说法错误的是( )A.整个过程的总反应方程式为
B. 在整个反应中起到催化作用
C.反应过程中有极性键的断裂与形成
D.该反应原理涉及的总反应的
16.恒温恒压下,对于反应:A(g)+3B(g) 3C(g),达到平衡状态的标志是( )
A.v (A)=3v (C)
正 逆
B.密闭容器内气体的密度不再改变
C.单位时间内消耗3n molC的同时,生成3n molB
D.密闭容器内A、B、C气体的浓度之比为1:3:2
17.下列反应低温有利于自发进行的是( )
A.
B.
C.
D.
18.下列有关实验操作、现象和解释或结论都正确的组合是( )
选
实验操作 现象 解释或结论
项
取0.1mol·L-1 溶液,向其中加入0.1mol·L-1的
温度越高,反应
A 硫酸,再分别在20℃、30℃下,发生反应 30℃下先出现浑浊
速率越快
铁粉与 反
应,降低了
B 向 和 的混合溶液中加入少量铁粉 血红色溶液颜色变浅
的浓度,使得平
衡正向移动
两支试管中各盛有2mL0.1mol·L-1酸性高锰酸钾溶液, 加入0.2mol·L-1草酸溶 反应物浓度越
C 分别加入5mL0.1mol·L-1草酸溶液和5mL0.2 mol·L-1草 液的试管中,高锰酸 大,反应速率越
酸溶液 钾溶液褪色更快 快
D 向紫色石蕊溶液中通入 溶液紫色逐渐变浅 具有漂白性
A.A B.B C.C D.D
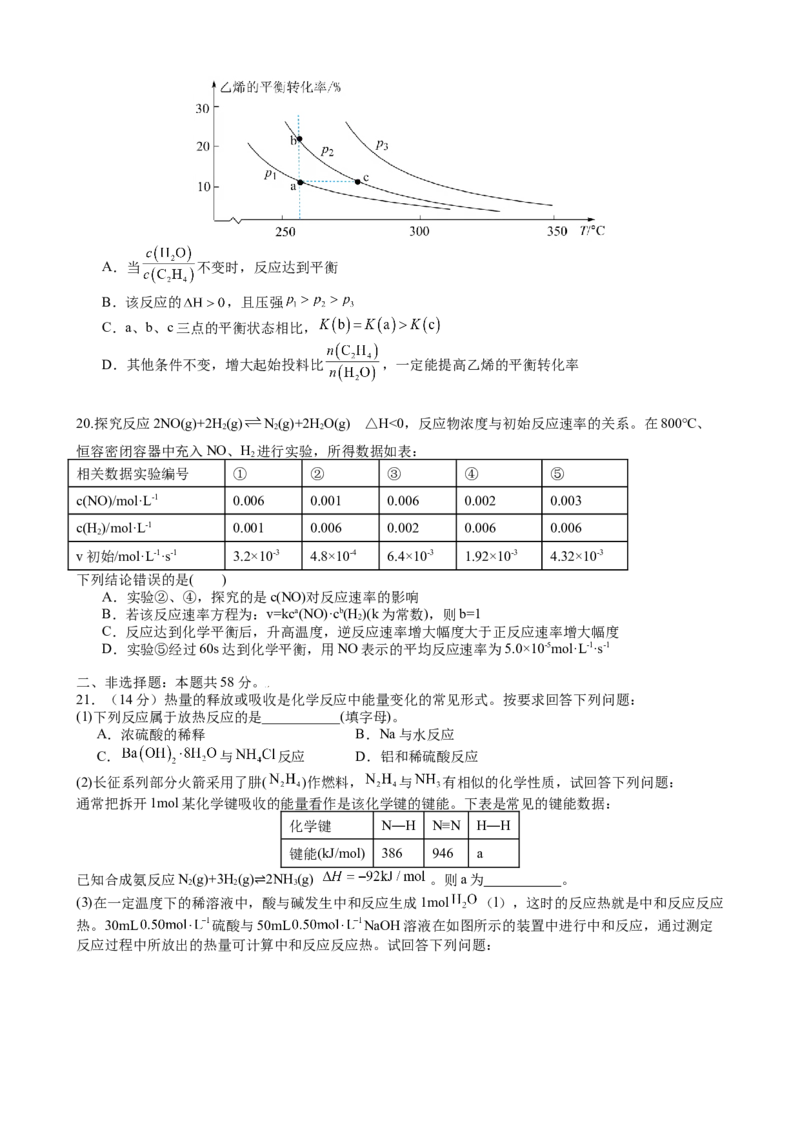
19.乙烯直接水合法生产乙醇的反应为 。在容积为3L的密闭容器中,
投料比 时,乙烯的平衡转化率与温度、压强的关系如图。下列说法正确的是( )A.当 不变时,反应达到平衡
B.该反应的 ,且压强
C.a、b、c三点的平衡状态相比,
D.其他条件不变,增大起始投料比 ,一定能提高乙烯的平衡转化率
20.探究反应2NO(g)+2H (g) N(g)+2HO(g) △H<0,反应物浓度与初始反应速率的关系。在800℃、
2 2 2
恒容密闭容器中充入NO、H 进行实验,所得数据如表:
2
相关数据实验编号 ① ② ③ ④ ⑤
c(NO)/mol·L-1 0.006 0.001 0.006 0.002 0.003
c(H)/mol·L-1 0.001 0.006 0.002 0.006 0.006
2
v初始/mol·L-1·s-1 3.2×10-3 4.8×10-4 6.4×10-3 1.92×10-3 4.32×10-3
下列结论错误的是( )
A.实验②、④,探究的是c(NO)对反应速率的影响
B.若该反应速率方程为:v=kca(NO)·cb(H )(k为常数),则b=1
2
C.反应达到化学平衡后,升高温度,逆反应速率增大幅度大于正反应速率增大幅度
D.实验⑤经过60s达到化学平衡,用NO表示的平均反应速率为5.0×10-5mol·L-1·s-1
二、非选择题:本题共58分。
21.(14分)热量的释放或吸收是化学反应中能量变化的常见形式。按要求回答下列问题:
(1)下列反应属于放热反应的是___________(填字母)。
A.浓硫酸的稀释 B.Na与水反应
C. 与 反应 D.铝和稀硫酸反应
(2)长征系列部分火箭采用了肼( )作燃料, 与 有相似的化学性质,试回答下列问题:
通常把拆开1mol某化学键吸收的能量看作是该化学键的键能。下表是常见的键能数据:
化学键 N―H N≡N H―H
键能(kJ/mol) 386 946 a
已知合成氨反应N(g)+3H(g) 2NH (g) 。则a为 。
2 2 3
(3)在一定温度下的稀溶液中,酸与碱发生中和反应生成1mol (l),这时的反应热就是中和反应反应
⇌
热。30mL 硫酸与50mL NaOH溶液在如图所示的装置中进行中和反应,通过测定
反应过程中所放出的热量可计算中和反应反应热。试回答下列问题:①从实验装置上看,图中尚缺少一种玻璃仪器是 。
②实验中要使用50mL NaOH溶液,至少需要称量NaOH固体 g。
③测得的实验数据如图:
温度 起始温度 /℃
终止温度 /℃ 温度差 /℃
实验次
NaOH 平均值
数
1 26.2 26.0 26.1 30.1
2 27.0 27.4 27.2 33.3
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度均近似为 ,中和后生成的溶液比热
容c=4.18J/(g·℃)。则生成1mol水时的反应热 kJ·mol(取小数点后一位)。
④用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和反应反应热的数值会
(填“偏大”“偏小”或“无影响”)。
22.某研究性学习小组利用HC O 溶液和酸性KMn0 溶液之间的反应来探究“外界条件改变对化学反应速
2 2 4 4
率的影响”,实验如下:
参加反应的物质
溶液颜色褪至无色时所需时
实验序 实验温度 KMn0 4 溶液(含硫 HC O 溶液 HO 间/s
号 /K 酸) 2 2 4 2
V/mL c/mol/L V/mL c/mol/L V/mL
A 293 2 0.02 4 0.1 0 t
1
B T 2 0.02 3 0.1 V 8
1 1
C 313 2 0.02 V 0.1 0 t
2 2
(1) 通过实验A、B,可探究 的改变对反应速率的影响,其中V= ,T= ;
1 1
通过实验 (填序号)可探究出温度变化对化学反应速率的影响。
(2)若t<8,则由此实验可以得出的结论是 。
1
(3)在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应较慢,溶液变色不明显;但不
久突然褪色,反应明显加快。某同学认为是反应放热导致溶液温度升高所致,重做B组实验,测定反应
过程中不同时间溶液的温度,结果如表:
时间/s 0 2 4 6 8 10
2 2
温度/℃ 20 21 21.5 22
1 2
从影响化学反应速率的因素看,你认为还可能是 的影响。若用实验证明你的猜想,除了酸性高锰
酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 (填字母)。
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
23.氨气是重要的基础化工品,请结合信息回答问题。(1)尿素[CO(NH)]是首个由无机物人工合成的有机物,在尿素合成塔中发生的反应可表示为
2 2
第一步: ΔH=-119.2kJ/mol;
1
第二步: ΔH=+15.5kJ/mol;
2
①已知第一步反应为快速反应,第二步反应为慢速反应,其中活化能较大的是第 步,则
ΔH= kJ/mol;第二步能自发进行的条件是
3
。(填“高温”或“低温”或“任何温度”)
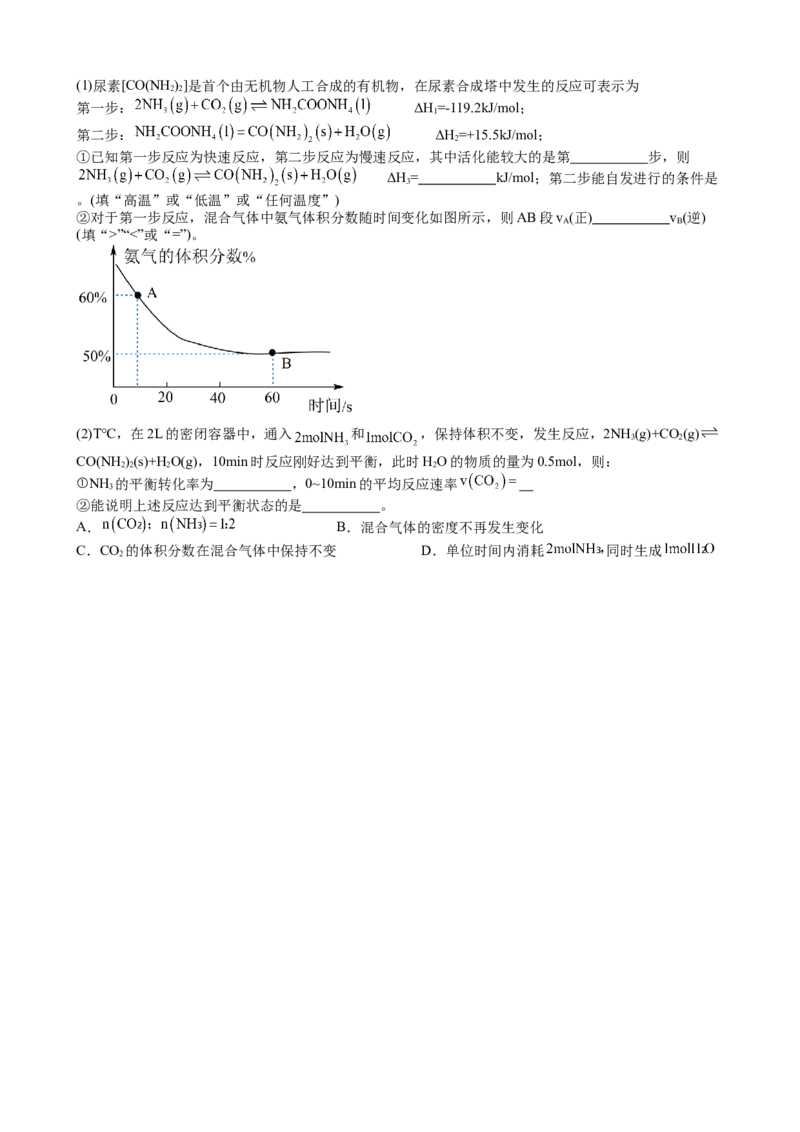
②对于第一步反应,混合气体中氨气体积分数随时间变化如图所示,则AB段v (正) v (逆)
A B
(填“>”“<”或“=”)。
(2)T℃,在2L的密闭容器中,通入 和 ,保持体积不变,发生反应,2NH (g)+CO (g)
3 2
CO(NH)(s)+HO(g),10min时反应刚好达到平衡,此时HO的物质的量为0.5mol,则:
2 2 2 2
①NH 的平衡转化率为 ,0~10min的平均反应速率
3
②能说明上述反应达到平衡状态的是 。
A. B.混合气体的密度不再发生变化
C.CO 的体积分数在混合气体中保持不变 D.单位时间内消耗 同时生成
2