文档内容
2024-2025 学年第二学期高二第一次教学质量检测化学试题
考试时间:75分钟 满分:100分
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自
己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案标号涂
黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:人教版选择性必修2。
5.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 B-11 F-19 P-31 S-32 Cl-35.5 Ca-40 Cu-64
Pb-207
第I卷(选择题)
一、选择题:本题共16个小题,1-10每小题2分,11-16每小题4分,共,44分。在每小题
给出的四个选项中,只有一项是符合题目要求的。
1.中国科学家对量子材料的研究处于国际领先水平,近年来对石墨烯、硅烯、锗烯等低维
量子材料的研究发展迅速。下列说法不正确的是
A.石墨烯是只有一个碳原子直径厚度的单层石墨
B.第一电离能:
C.X射线衍射实验可确定石墨烯的晶体结构
D.硅和锗都位于金属和非金属元素分界线处,属于过渡元素
2.下列化学用语正确的
A.铜原子( )的电子排布式:1s22s22p63s23p63d94s2
B.基态铍原子电子占据最高能级的电子云轮廓 图:
C.基态C原子价电子轨道表示式:
D.NH Cl电子式为
4
3.基本概念和理论是化学思维的基石。下列叙述错误的是( )
A.VSEPR理论认为VSEPR模型与分子的空间结构相同
B.元素性质随着原子序数递增而呈周期性变化的规律称为元素周期律
C.泡利原理认为一个原子轨道内最多只能容纳两个自旋相反的电子
D.sp3杂化轨道由1个s轨道和3个p轨道混杂而成
4. 下列对事实的分析正确的是
选项 事实 分析
A 键角: 电负性:C CO为极性分子, 为非极性分子D 热稳定性:HF>HCl HF中存在氢键,HCl中不存在氢键
5.下列关于实验现象的解释或结论正确的是
选
实验操作 现象 解释或结论
项
A 在[Cu(NH ) ]SO 溶液中加入乙醇 析出蓝色晶体 极性:乙醇>水
3 4 4
向NaCl溶液中滴加少量AgNO 溶 先产生白色沉淀
3
B 配位键影响物质的溶解性
液,然后滴加氨水直至过量 后沉淀消失
先生成沉淀,后 稳定性:
C 向AgNO 溶液中滴加过量氨水
3
沉淀溶解 [Ag(NH ) ]+<[Ag(H O) ]+
3 2 2 2
向Co(NH ) Cl 的水溶液中滴加硝酸银 该配合物中Co2+的配位数
3 3 3
D 无明显现象
溶液 是3
6.六氟化硫(SF 6 )具有良好的高压绝缘性,在电器工业中有着广泛的用途, SF 6分子呈正
八面体结构,S 原子位于正八面体的中心.下列关于 SF 6的推测中,正确的是( )
SF SO SF
A. 6在氧气中燃烧可生成 2 B. 6晶体是原子晶体
C. SF 6是非极性分子 D. SF 6中各原子的最外电子层都达到8电子稳定结
构
7.分子的结构与性质息息相关,下列说法错误的是( )
A. I 易溶于苯、CH 难溶于水,都可用“相似相溶”原理解释
2 4
B. 二氢呋喃( )和降冰片烯( )分子中均含有手性碳原子
C. H O+ 和N H 的中心原子都是sp3杂化
3 3
D. 碘和干冰升华时克服的粒子间作用为同种类型
8. 可用作纺织及造纸工业的脱氯剂:
,还可用于NaCN中毒的治疗。下列化学用语错误的是
A. 的VSEPR模型为正四面体 B.HCl的形成过程:
C.基态N的价电子排布式为: D.Cl的一种核素为:
9.结构决定性质,性质决定用途。下列事实解释错误的是( )事实 解释
A 甘油(丙三醇)是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动
10.铁氰化钾因其特殊的氧化能力,在有机合成领域中起着重要的作用,工业上采用“氯
气氧化法”制备: 。下列说法正确的是
A. 的电子式为 , 水溶液呈碱性
B. 中铁元素化合价为+3价,配位数为6
C. 中既含离子键又含非极性键、配位键
D.HCN中碳原子的杂化轨道类型为 ,其空间结构为V形
11.一种工业洗涤剂中间体的结构如图,其中X、Y、Z、Q、W原子序数依次增大且分属
三个短周期。Y、Q元素的基态原子中均有两个未成对电子,下列说法正确的是
( )
A. 电负性大小:Q>Z>Y>X
B. 简单离子半径:QZ>Q
D. 阴离子中各原子都满足8电子稳
12.短周期主族元素X、Y、Z、W在元素周期表中的位置如图所示,Y原子最外层电子数是
其电子层数的3倍。下列关于这四种元素及其化合物的说法中正确的是
A.X、Y、Z、W中可能存在金属元素
B.化合物ZW 分子中所有原子都达到8电子稳定结构
2
C.气态氢化物的稳定性:Z>W>X>Y
D.Y、Z可形成的一种化合物能够使酸性高锰酸钾溶液褪色,体现该化合物有漂白性。
13.下列物质的结构或性质及解释均正确且具有因果关系的是 ( )
选项 物质的结构或性质 解释
A 硬度:SiC>Si 晶体类型不同
B 分解温度:CH CCl COOH 氟的电负性大于氯的电负性
3 314.下列关于配合物 的说法正确的是
A.配体是 和 ,配位数是5
B.中心离子是的
C. 该配合物中含共价键16mol
D.含 该配合物的水溶液中加入足量 溶液,生成 沉淀
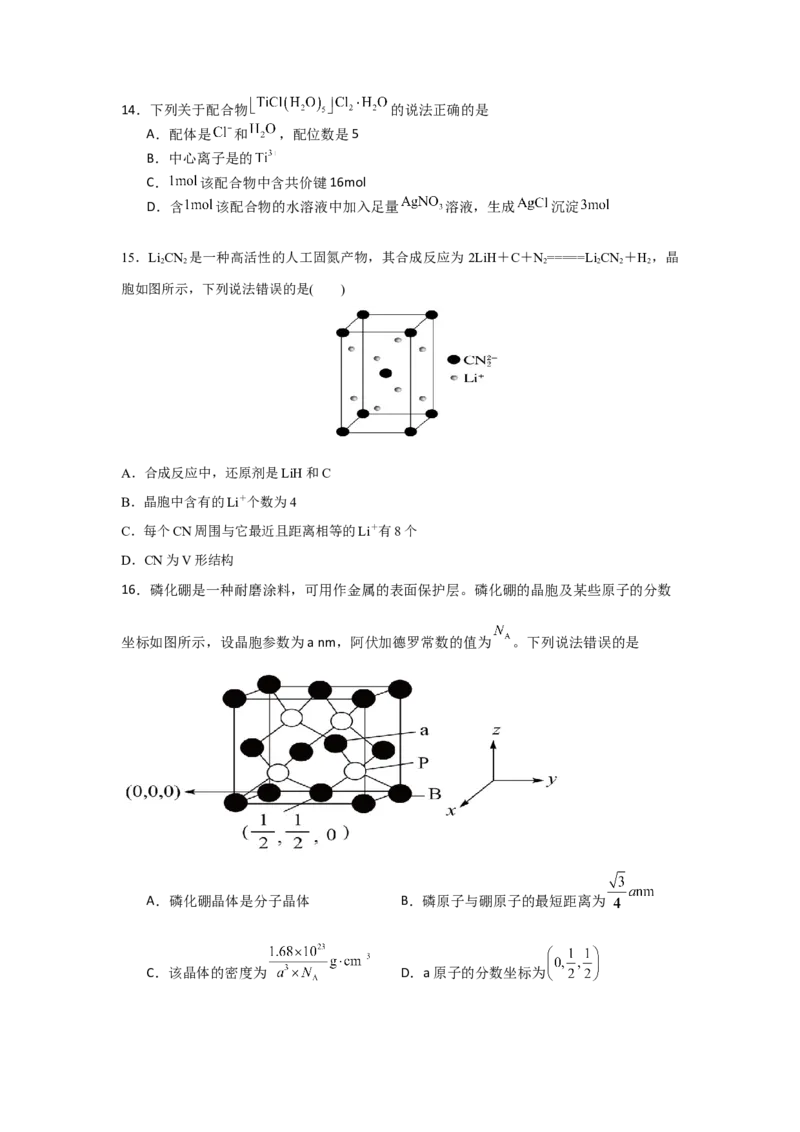
15.LiCN 是一种高活性的人工固氮产物,其合成反应为 2LiH+C+N=====LiCN +H ,晶
2 2 2 2 2 2
胞如图所示,下列说法错误的是( )
A.合成反应中,还原剂是LiH和C
B.晶胞中含有的Li+个数为4
C.每个CN周围与它最近且距离相等的Li+有8个
D.CN为V形结构
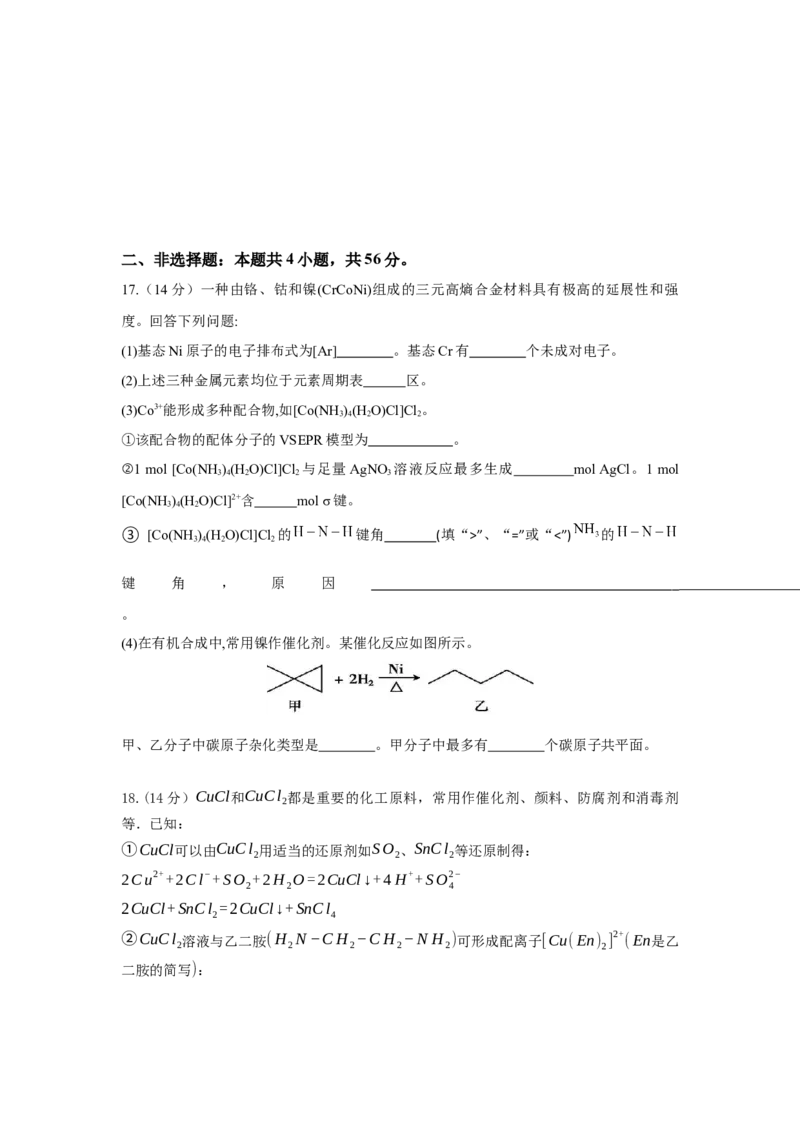
16.磷化硼是一种耐磨涂料,可用作金属的表面保护层。磷化硼的晶胞及某些原子的分数
坐标如图所示,设晶胞参数为a nm,阿伏加德罗常数的值为 。下列说法错误的是
A.磷化硼晶体是分子晶体 B.磷原子与硼原子的最短距离为
C.该晶体的密度为 D.a原子的分数坐标为二、非选择题:本题共4小题,共56分。
17.(14分)一种由铬、钴和镍(CrCoNi)组成的三元高熵合金材料具有极高的延展性和强
度。回答下列问题:
(1)基态Ni原子的电子排布式为[Ar] 。基态Cr有 个未成对电子。
(2)上述三种金属元素均位于元素周期表 区。
(3)Co3+能形成多种配合物,如[Co(NH )(H O)Cl]Cl 。
3 4 2 2
①该配合物的配体分子的VSEPR模型为 。
②1 mol [Co(NH)(H O)Cl]Cl 与足量AgNO 溶液反应最多生成 mol AgCl。1 mol
3 4 2 2 3
[Co(NH )(H O)Cl]2+含 mol σ键。
3 4 2
③ [Co(NH )(H O)Cl]Cl 的 键角 (填“>”、“=”或“<”) 的
3 4 2 2
键 角 , 原 因
。
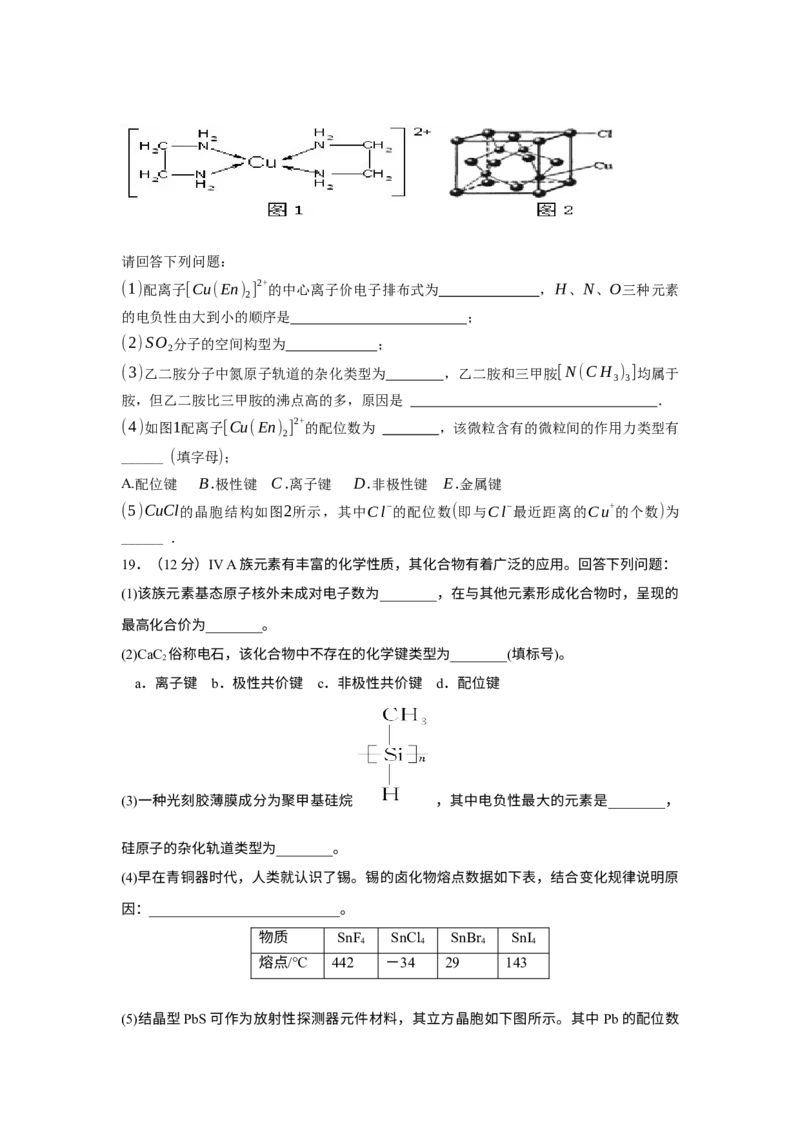
(4)在有机合成中,常用镍作催化剂。某催化反应如图所示。
甲、乙分子中碳原子杂化类型是 。甲分子中最多有 个碳原子共平面。
18.(14分)CuCl和CuCl 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂
2
等.已知:
①CuCl可以由CuCl 用适当的还原剂如SO 、SnCl 等还原制得:
2 2 2
2Cu2++2Cl−+SO +2H O=2CuCl↓+4H++SO2−
2 2 4
2CuCl+SnCl =2CuCl↓+SnCl
2 4
②CuCl 溶液与乙二胺(H N−CH −CH −N H )可形成配离子[Cu(En) ] 2+ (En是乙
2 2 2 2 2 2
二胺的简写):请回答下列问题:
(1)配离子[Cu(En) ] 2+ 的中心离子价电子排布式为 ,H、N、O三种元素
2
的电负性由大到小的顺序是 ;
(2)SO 分子的空间构型为 ;
2
(3)乙二胺分子中氮原子轨道的杂化类型为 ,乙二胺和三甲胺[N(CH ) ]均属于
3 3
胺,但乙二胺比三甲胺的沸点高的多,原因是 .
(4)如图1配离子[Cu(En) ] 2+ 的配位数为 ,该微粒含有的微粒间的作用力类型有
2
______ (填字母);
A.配位键 B.极性键 C.离子键 D.非极性键 E.金属键
(5)CuCl的晶胞结构如图2所示,其中Cl−的配位数(即与Cl−最近距离的Cu+的个数)为
______ .
19.(12分)ⅣA族元素有丰富的化学性质,其化合物有着广泛的应用。回答下列问题:
(1)该族元素基态原子核外未成对电子数为________,在与其他元素形成化合物时,呈现的
最高化合价为________。
(2)CaC 俗称电石,该化合物中不存在的化学键类型为________(填标号)。
2
a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)一种光刻胶薄膜成分为聚甲基硅烷 ,其中电负性最大的元素是________,
硅原子的杂化轨道类型为________。
(4)早在青铜器时代,人类就认识了锡。锡的卤化物熔点数据如下表,结合变化规律说明原
因:___________________________。
物质 SnF SnCl SnBr SnI
4 4 4 4
熔点/℃ 442 -34 29 143
(5)结晶型PbS可作为放射性探测器元件材料,其立方晶胞如下图所示。其中 Pb的配位数(距离最近的 S的数目)为______。设 NA为阿伏加德罗常数的值,则该晶体密度为
_____________g·cm-3(列出计算式)。
20.(16分)三卤化氮(NX )如NF 、NCl 等有广泛的用途。NF 是液晶显示器生产过程中
3 3 3 3
常用的化学清洗剂,NCl 可用于面粉的漂白和杀菌。回答下列问题:
3
(1)锑是制造液晶显示器的一种原材料,基态锑的价层电子排布式为5s25p3,可知锑在元素
周期表的位置是______________。基态锑原子中有____个未成对电子,这些未成对电子具
有________(填“相同”或“不同”)的自旋状态。
(2)元素F、O、N位于同一周期,其第一电离能由大到小的顺序是____________,原子半径
由大到小的顺序是____________。
(3)液晶显示器材料因含微量杂质元素铬(Cr)而呈浅红色。基态铬原子的价层电子排布式为
________。液晶在放电过程中会产生NO和NO,其中N原子的杂化类型分别是________,
键角:NO____NO(填“<”或“=”或“>”)。
(4)已知热稳定性NF 高于NCl ,解释其原因是__________________________________。常
3 3
温常压下NF 为无色气体,NCl 为黄色油状液体,NCl 和NF 价层电子对互斥模型均为
3 3 3 3
________,NCl 和NF 的分子空间结构均为________。
3 3
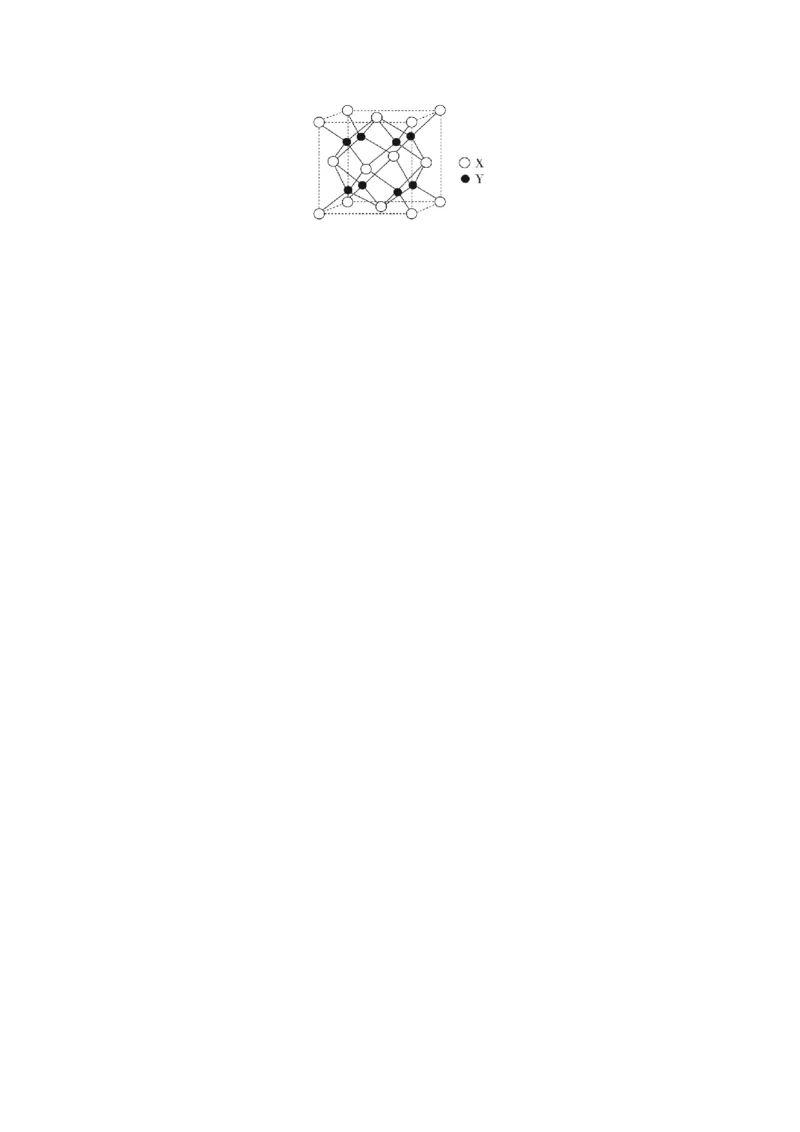
(5)CaF 的晶胞结构如图所示,X代表的离子是________;若该立方晶胞参数为a pm,
2
CaF 的摩尔质量为M g/mol,阿伏加德罗常数的值用 N 来表示,则CaF 晶体的密度=
2 A 2
________ g/cm3(写出表达式)。