文档内容
2024-2025 学年度第一学期福九联盟(高中)期中联考
高中二年化学科试卷
完卷时间:75分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Fe-56
第I卷(选择题)
一、单选题(每题3分,共45分。每小题只有一项符合题目要求)。
1. 化学与生产、生活、社会和环境等密切相关,下列有关说法正确的是
A. 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
B. 工业上用离子交换膜电解饱和食盐水时,阳极区pH升高
C. 铁表面镀锌可以增强其抗腐蚀性,镀层局部破损后仍然具有防护作用
D. 铜在酸性环境下易发生析氢腐蚀
【答案】C
【解析】
【详解】A.催化剂只影响反应速率,不影响化学平衡,不可以改变化学反应进行的方向,A错误;
B.工业上用离子交换膜电解饱和食盐水时,阳极区 ,pH减小,B错误;
C.铁表面镀锌可以隔绝空气,同时锌的活泼性强于铁,增加抗腐蚀性,C正确;
D.铜不能从酸中置换出氢气,这不是一个自发发生的氧化还原反应,D错误;
故选C。
2. 下列实验操作或实验方案,能达到目的的是
A.往Fe电极区滴入2滴铁氰化钾溶液,溶液中
B.验证 与 发生可逆反应
产生蓝色沉淀C.研究二氧化锰与三价铁盐对双氧水分解速率的
D.验证铁钉的吸氧腐蚀
影响
A. A B. B C. C D. D
【答案】D
【解析】
为
【详解】A.该装置 原电池装置,负极为锌,正极为铁,铁不参与反应,故往Fe电极区滴入2滴铁氰化
钾溶液,溶液中不能产生蓝色沉淀,A不符合题意;
B.两者发生的反应为:2Fe3++2I-=2Fe2++I ,等体积等物质的量浓度的溶液混合,Fe3+过量,加入KSCN溶
2
液会变红,不能证明该反应为可逆反应,B不符合题意;
C.研究二氧化锰与三价铁盐对双氧水分解速率的影响,不能选择Fe O,Fe O 属于金属氧化物,不属于
2 3 2 3
三价铁盐,C不符合题意;
D.铁发生吸氧腐蚀时消耗氧气,氧气传感器会发生相应变化,能达到实验目的,D符合题意;
故选D。
3. 下列说法错误的是
A. 恒容绝热容器中,发生反应H(g)+I (g) 2HI(g),当压强不变时反应达到平衡状态
2 2
B. ∆H<0、∆S>0,2NO(g) 4NO (g)+O(g)的反应在任何温度下都能自发进行
2 5 2 2
C. ∆H>0,T 温度下的平衡常数为K,T 温度下的平衡常数为K,若KT
1 1 2 2 1 2 1 2
D. S(g)+O(g)=SO(g) ΔH ;S(s)+O (g)=SO(g) ΔH ,则ΔH<ΔH
2 2 1 2 2 2 1 2
【答案】C
【解析】
【详解】A.恒压绝热容器中发生,反应放热导致温度升高,容器内的压强不再变化,说明反应温度不变,
说明反应达到化学平衡状态,A正确;
B.当∆H<0、∆S>0时,则ΔG=ΔH-TΔS永远小于0,反应在任何温度下都能自发进行,B正确;C.该反应的正反应是吸热反应,升高温度,平衡向正反应移动,平衡常数增大,C错误;
D.S(g)+O(g)=SO(g) ΔH ;S(s)+O (g)=SO(g) ΔH ,气态S燃烧放热多,则ΔH<ΔH ,D正确;
2 2 1 2 2 2 1 2
故选C。
4. 二氧化碳甲烷化的研究对缓解能源危机意义重大。以LaNiO 催化二氧化碳甲烷化的反应机理如图所示
3
(LaNiO 与H 作用生成LaO 和Ni),下列说法正确的是
3 2 2 3
A. H→2H∙放出能量
2
B. LaOCO 在反应中为催化剂
2 2 3
C. 若H+CO→ 是反应的决速步,则该步的化学反应速率最快
2
D. 图示过程的总反应式可表示为
【答案】D
【解析】
【详解】A. 为断键过程,吸收能量,A错误;
B.由图中反应可知,LaOCO 生成又被消耗,为中间产物,B错误;
2 2 3
C.活化能大的一步是决速步骤,此时反应慢,则若H+CO→ 是反应的决速步,则该步的化学反
2
应速率最慢,C错误;
D.上图过程的总反应为氢气和二氧化碳在催化剂作用下生成水和甲烷,方程式可表示为:,D正确;
故选D。
5. 在一定体积的密闭容器中,进行如下化学反应:CO(g)+H(g) CO(g)+HO(g),平衡常数K和温度关
2 2 2
系如表,下列说法错误的是
83
t/℃ 700 800 1000 1200
0
K 0.6 0.9 1.0 1.7 2.6
A. 反应的化学平衡常数表达式为K=
B. 该反应为吸热反应
C. 700℃时,CO(g)+HO(g) CO(g)+H(g)化学平衡常数K=1.67
2 2 2
D. 某温度下,各物质的平衡浓度符合如下关系:3c(CO)·c(H)=5c(CO)·c(HO),此时的温度为830℃
2 2 2
【答案】D
【解析】
【详解】A.根据反应方程式,反应 的化学平衡常数表达式为K= ,A正确;
B.由表格可知,平衡常数随温度的升高而增大,故该反应为吸热反应,B正确;
C.700℃时,CO(g)+HO(g) CO(g)+H(g)化学平衡常数K= ,C正确;
2 2 2
D.温度为830℃时K=1.0,某温度下,各物质的平衡浓度符合如下关系:3c(CO)·c(H)=5c(CO)·c(HO),
2 2 2
此时K= ,两者不相等,故温度不是830℃,D错误;
故选D。
6. 已知如下热化学方程式:
①②
③
④
高氯酸铵是发射火箭的固体能源,发生爆炸的反应如下:
可表示为
A. B.
C. D.
【答案】A
【解析】
【详解】根据盖斯定律,③ ④ -① -②等于目标反应,对应反应热也有类似的加和关系,得:
,A正确,故选A。
7. 汽车尾气净化的主要原理为2NO(g)+2CO(g) N(g)+2CO (g),∆H<0。若该反应在绝热、恒容的密闭体
2 2
系中进行,下列示意图正确且能说明反应在进行到t 时刻达到平衡状态的是
1
A. ③④ B. ①②③ C. ②③④ D. ①③
【答案】A
【解析】
【详解】①到达平衡后正、逆速率相等,不再变化,t 时刻v 最大,之后随反应进行速率发生变化,未到
1 正达平衡;
②t 时刻时,CO、CO的物质的量的变化量之比不等于1∶1,未达到平衡状态;
1 2
③t 时刻之后,NO的质量分数不再改变,说明t 时刻反应处于平衡状态;
1 1
④该反应是放热反应,在绝热容器中进行,随着反应进行,容器温度上升,t 时刻之后随反应进行温度不
1
再发生变化,说明反应达到平衡状态;
正确的是③④;
故选A。
8. 在一定温度下,在2个容积均为2L的恒容密闭容器中,加入一定量的反应物,发生反应:2NO(g)
+2CO(g) N(g)+2CO (g) ∆H<0,相关数据见表。下列说法不正确的是
2 2
起始物质的量/mol 平衡物质的量/mol
容器编号 温度/℃
NO(g) CO(g) CO(g)
2
Ⅰ 0.4 0.4 0.2
Ⅱ 0.4 0.4 0.24
A. T 温度下,平衡常数K=5
1
B. Ⅰ中反应达到平衡时,CO的转化率为50%
C. 达到平衡所需要的时间:II>I
D. 对于Ⅰ,平衡后向容器中再充入0.4molCO和0.2molCO,平衡逆向移动
2
【答案】D
【解析】
【 详 解 】 A . 在 温 度 为 T 时 , 根 据 三 段 式 : ,
1
,A正确;B.根据以上分析,Ⅰ中反应达到平衡时,CO的转化率为 ,B正确;
C.温度为T, , ,
2
所以温度 ,反应速率 ,达到平衡所需要的时间:II>I,C正确;
D.对于Ⅰ,平衡后向容器中再充入0.4molCO和0.2molCO,
2
, ,平衡正向移动,D错误;
故选D。
9. 随着各地“限牌”政策的推出,电动汽年成为汽车届的“新宠”。特斯拉全电动汽车使用的是钴酸锂(
)电池,其工作原理如图,A极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一
种能传导 的高分子材料,隔膜只允许特定的离子通过,电池反应式
。下列说法不正确的是A. 据题意分析可知该隔膜只允许 通过,放电时 从左边流向右边
B. 放电时,正极锂的化合价未发生改变
C. 充电时B作阳极,电极反应式为:
D. 废旧钴酸锂( )电池进行“放电处理”让 进入石墨中而有利于回收
【答案】D
【解析】
【分析】根据电池反应式知,放电时,负极反应式为LiC -xe-=C +xLi+、正极反应式为Li CoO+xLi++xe-
x 6 6 1-x 2
=LiCoO,充电时,阴极、阳极反应式与负极、正极反应式正好相反,所以A是负极、B是正极。
2
【详解】A.据题意分析可知该隔膜只允许Li+通过,放电时Li+往正极移动,即从左边流向右边,A正确;
B.无论放电还是充电,Li元素化合价都是+1价,所以化合价不变,B正确;
C.充电时,B电极是阳极,放电时是正极,其电极反应与正极反应相反,故电极反应式为LiCoO -xe-=
2
Li CoO+xLi+,C正确;
1-x 2
D.根据电池反应式知,充电时锂离子加入石墨中,D错误;
故答案选D。
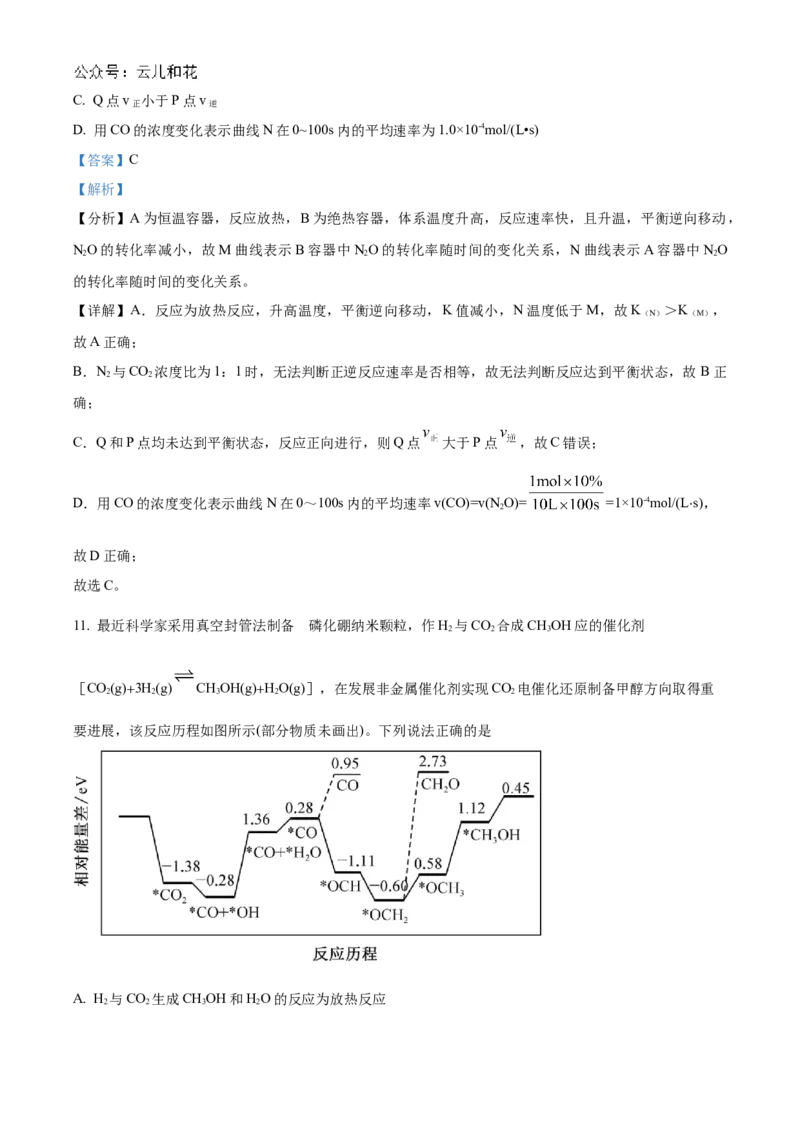
10. 在起始温度均为T/℃。容积均为10L的密闭容器A(恒温)、B(绝热)中均加入1molN O和4molCO,发
2
生反应NO(g)+CO(g) N(g)+2CO (g) ∆H<0。A、B容器中NO的转化率随时间的变化关系如图所示。
2 2 2 2
下列说法中错误的是
A. 曲线M、N的平衡常数大小为:K >K
(N) (M)
B. N 与CO 浓度比为1:1且保持不变,不能说明反应达到平衡状态
2 2C. Q点v 小于P点v
正 逆
D. 用CO的浓度变化表示曲线N在0~100s内的平均速率为1.0×10-4mol/(L•s)
【答案】C
【解析】
【分析】A为恒温容器,反应放热,B为绝热容器,体系温度升高,反应速率快,且升温,平衡逆向移动,
NO的转化率减小,故M曲线表示B容器中NO的转化率随时间的变化关系,N曲线表示A容器中NO
2 2 2
的转化率随时间的变化关系。
【详解】A.反应为放热反应,升高温度,平衡逆向移动,K值减小,N温度低于M,故K >K ,
(N) (M)
故A正确;
B.N 与CO 浓度比为1:1时,无法判断正逆反应速率是否相等,故无法判断反应达到平衡状态,故 B正
2 2
确;
C.Q和P点均未达到平衡状态,反应正向进行,则Q点 大于P点 ,故C错误;
D.用CO的浓度变化表示曲线N在0~100s内的平均速率v(CO)=v(N O)= =1×10-4mol/(L s),
2
⋅
故D正确;
故选C。
的
11. 最近科学家采用真空封管法制备 磷化硼纳米颗粒,作H 与CO 合成CHOH应的催化剂
2 2 3
[CO(g)3H(g) CHOH(g)HO(g)],在发展非金属催化剂实现CO 电催化还原制备甲醇方向取得重
2 2 3 2 2
要进展,该反应历程如图所示(部分物质未画出)。下列说法正确的是
A. H 与CO 生成CHOH和HO的反应为放热反应
2 2 3 2B. 上述反应生成的副产物中,CHO比CO多(相同条件下)
2
C. 在合成甲醇的过程中,降低*CO*OH*CO*HO能量变化,可提高反应速率
2
D. 电催化还原制备甲醇过程中,阳极的电势比阴极电势低
【答案】C
【解析】
【详解】A.根据图示,反应物总能量小于生成物总能量, 与 生成 和 的反应为吸热
反应,故A错误;
B.生成CO的活化能小于生成 的活化能,所以生成的副产物中, 比 少,故B错误;
C.在合成甲醇的过程中, 能量变化最大,即能垒最高,反应速率最慢,降低
能量变化,可提高反应速率,故C正确;
D.电催化还原制备甲醇过程中,阳极的电势比阴极的高,故D错误;
故选C。
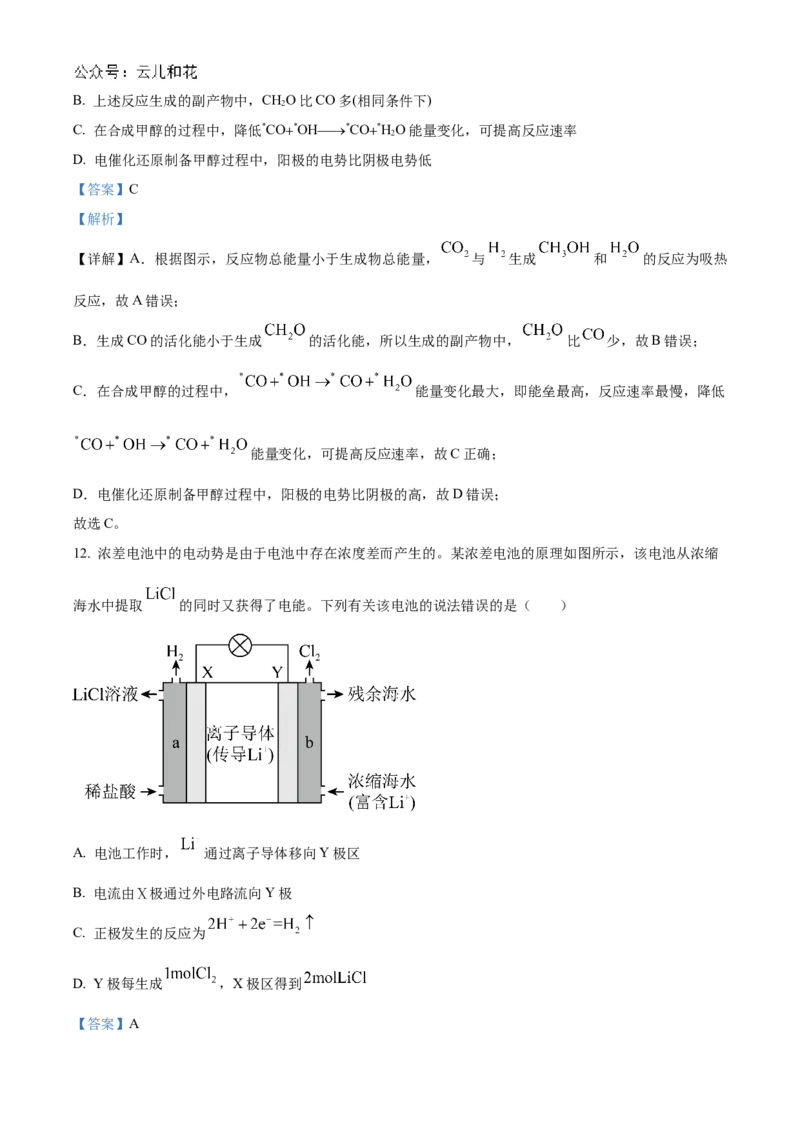
12. 浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩
海水中提取 的同时又获得了电能。下列有关该电池的说法错误的是( )
A. 电池工作时, 通过离子导体移向Y极区
B. 电流由Ⅹ极通过外电路流向Y极
C. 正极发生的反应为
D. Y极每生成 ,X极区得到
【答案】A【解析】
【详解】A. 加入盐酸,X电极上生成氢气, 发生还原反应: ,X极为正极;Y极上
生成 , 发生氧化反应:2Cl--2e-=Cl↑,Y极是负极,电池工作时, 向X极区移动,A项错误;
2
B. 在外电路,电流由正极流向负极,B项正确;
C. 由前面分析知,C项正确;
D. Y极每生成 ,则转移2mol电子,有2mol 向正极移动,则X极区得到 ,D项正确;
答案选A。
13. Burns和Dainton研究发现Cl 与CO合成COCl 的反应机理如下:
2 2
①Cl(g) 2Cl•(g) 快
2
②CO(g)+Cl•(g) COCl•(g) 快
③COCl•(g)+Cl(g) COCl (g)+Cl•(g) 慢
2 2
反应②的速率方程为v =k c(CO)c(Cl•),v =k c(COCl•)。下列说法正确的是
正 正 逆 逆
A. 反应①的活化能大于反应③的活化能
B. 反应②的平衡常数K=
C. 使用催化剂反应②的k 、k 均不发生改变
正 逆
D. 升高温度反应②的k 增加,k 减小
正 逆
【答案】B
【解析】
【详解】A.活化能越小,反应速率越快,则反应①的活化能小于反应③的活化能,A错误;
B.反应②存在v =k c(CO)c(Cl•),v =k c(COCl•),平衡时正逆反应速率相等,则K= ,B正确;
正 正 逆 逆
C.催化剂影响化学反应速率,应②的k 、k 均发生改变,C错误;
正 逆
D.升高温度正逆反应速率均增加,反应②的k 增加,k 增加,D错误;
正 逆
故选B。
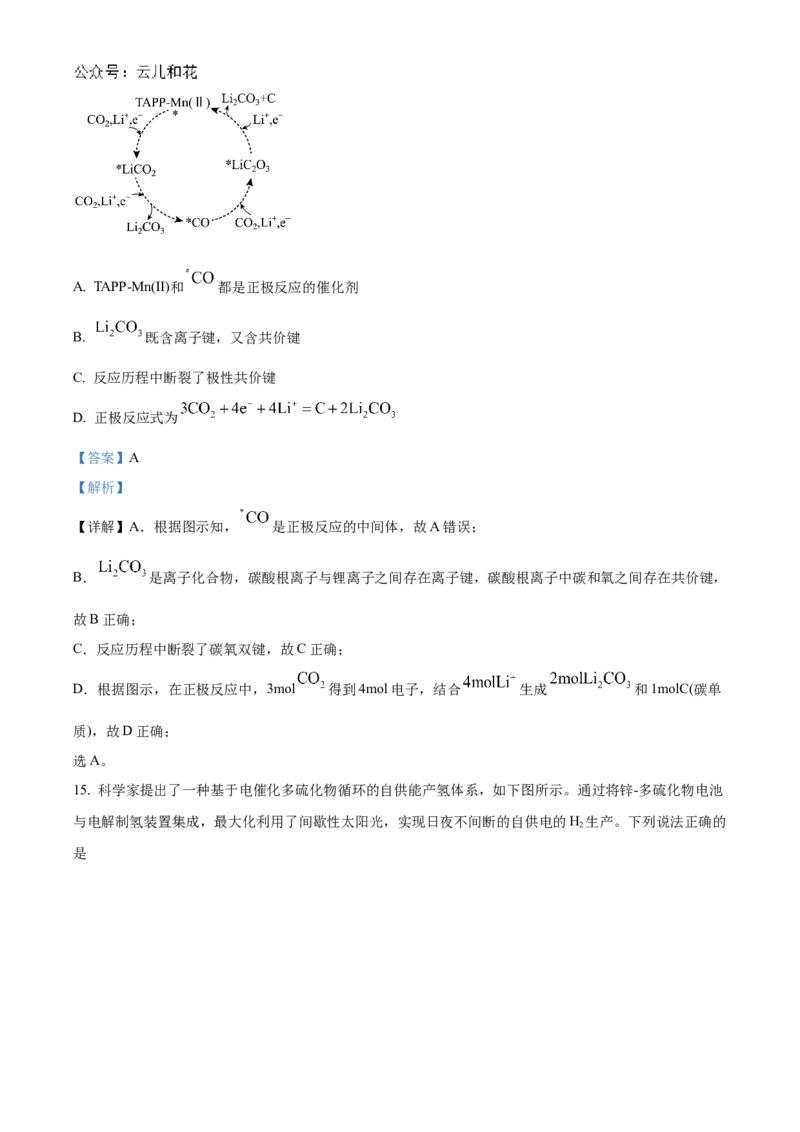
14. 在TAPP-Mn(Ⅱ)作用下,锂-二氧化碳电池的正极反应历程如图。下列说法错误的是A. TAPP-Mn(Ⅱ)和 都是正极反应的催化剂
B. 既含离子键,又含共价键
C. 反应历程中断裂了极性共价键
D. 正极反应式为
【答案】A
【解析】
【详解】A.根据图示知, 是正极反应的中间体,故A错误;
B. 是离子化合物,碳酸根离子与锂离子之间存在离子键,碳酸根离子中碳和氧之间存在共价键,
故B正确;
C.反应历程中断裂了碳氧双键,故C正确;
D.根据图示,在正极反应中,3mol 得到4mol电子,结合 生成 和1molC(碳单
质),故D正确;
选A。
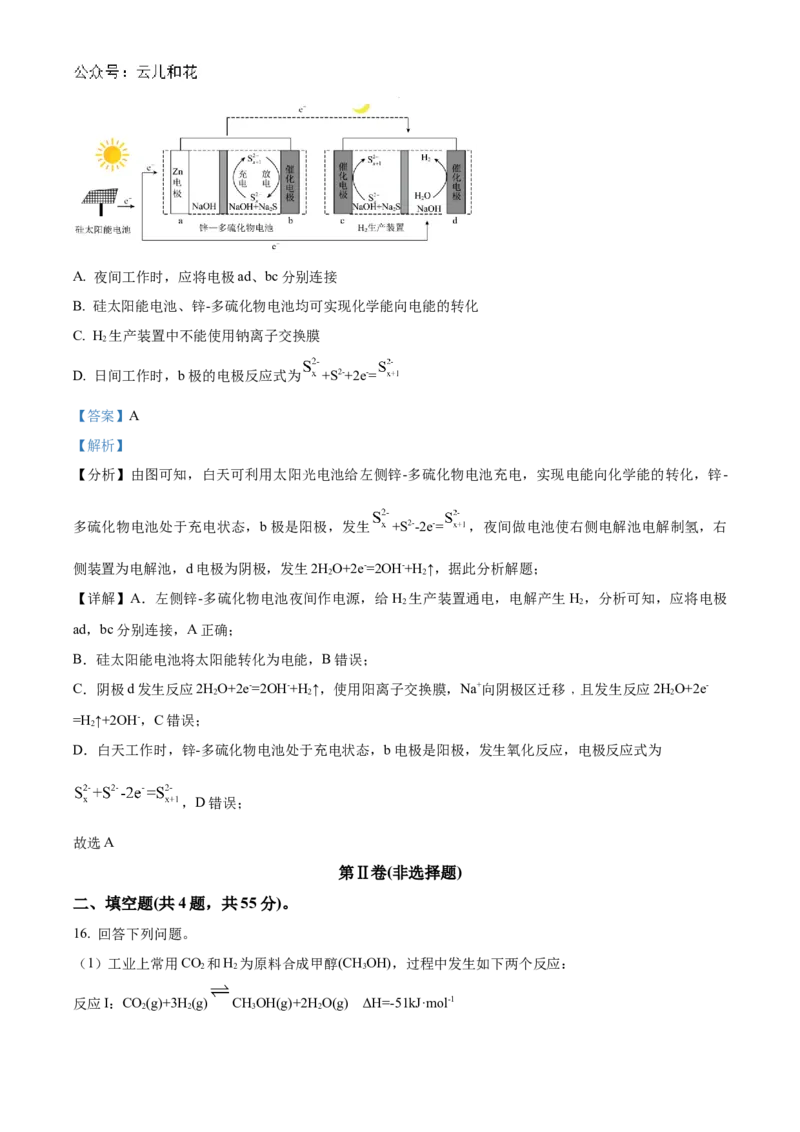
15. 科学家提出了一种基于电催化多硫化物循环的自供能产氢体系,如下图所示。通过将锌-多硫化物电池
与电解制氢装置集成,最大化利用了间歇性太阳光,实现日夜不间断的自供电的H 生产。下列说法正确的
2
是A. 夜间工作时,应将电极ad、bc分别连接
B. 硅太阳能电池、锌-多硫化物电池均可实现化学能向电能的转化
C. H 生产装置中不能使用钠离子交换膜
2
D. 日间工作时,b极的电极反应式为 +S2-+2e-=
【答案】A
【解析】
【分析】由图可知,白天可利用太阳光电池给左侧锌-多硫化物电池充电,实现电能向化学能的转化,锌-
多硫化物电池处于充电状态,b极是阳极,发生 +S2--2e-= ,夜间做电池使右侧电解池电解制氢,右
侧装置为电解池,d电极为阴极,发生2HO+2e-=2OH-+H ↑,据此分析解题;
2 2
【详解】A.左侧锌-多硫化物电池夜间作电源,给H 生产装置通电,电解产生H ,分析可知,应将电极
2 2
ad,bc分别连接,A正确;
B.硅太阳能电池将太阳能转化为电能,B错误;
C.阴极d发生反应2HO+2e-=2OH-+H ↑,使用阳离子交换膜,Na+向阴极区迁移﹐且发生反应2HO+2e-
2 2 2
=H ↑+2OH-,C错误;
2
D.白天工作时,锌-多硫化物电池处于充电状态,b电极是阳极,发生氧化反应,电极反应式为
,D错误;
故选A 。
第Ⅱ卷(非选择题)
二、填空题(共4题,共55分)。
16. 回答下列问题。
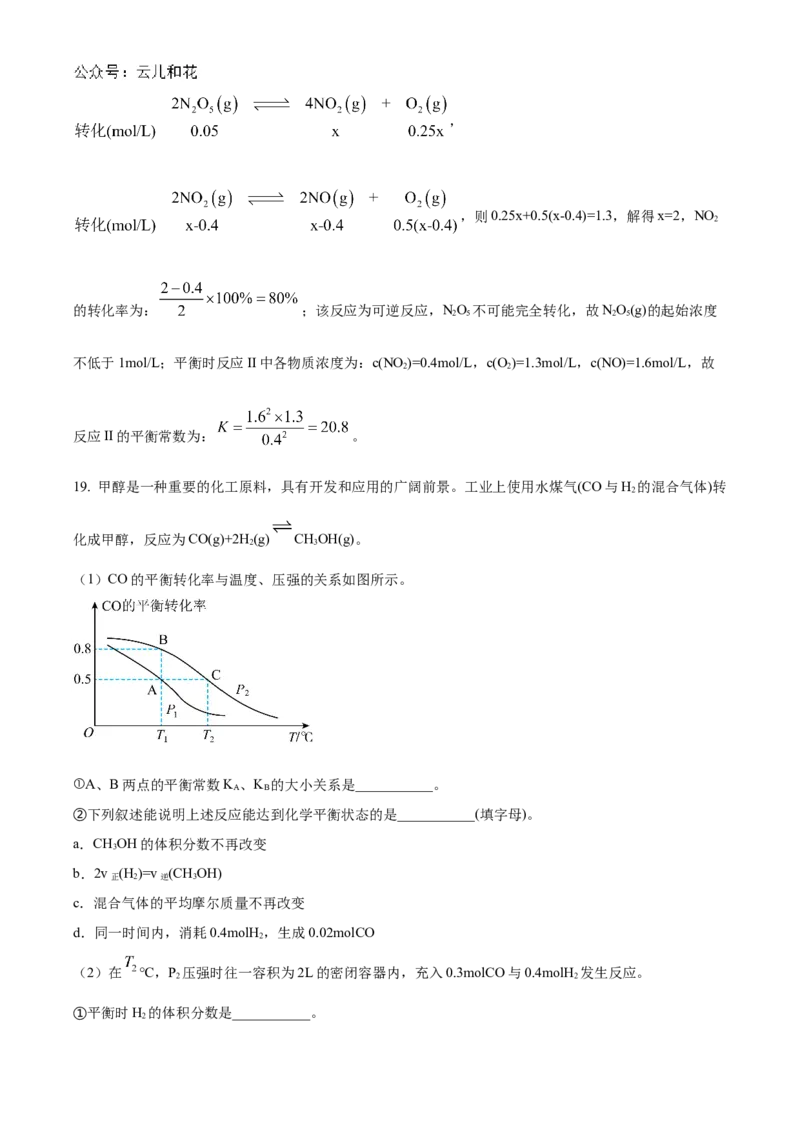
(1)工业上常用CO 和H 为原料合成甲醇(CHOH),过程中发生如下两个反应:
2 2 3
反应I:CO(g)+3H(g) CHOH(g)+2H O(g) ΔH=-51kJ·mol-1
2 2 3 2反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH=+41kJ·mol-1
2 2 2
的
①已知几种化学键 键能如下表所示,则a=___________kJ·mol-1。
化学键 C—H C—O H—O H—H C≡O(CO)
键能/
406 351 465 436 a
kJ·mol-1
②若反应Ⅱ逆反应活化能E'=124kJ·mol-1,则该反应的正反应的活化能E=___________kJ·mol-1。
a
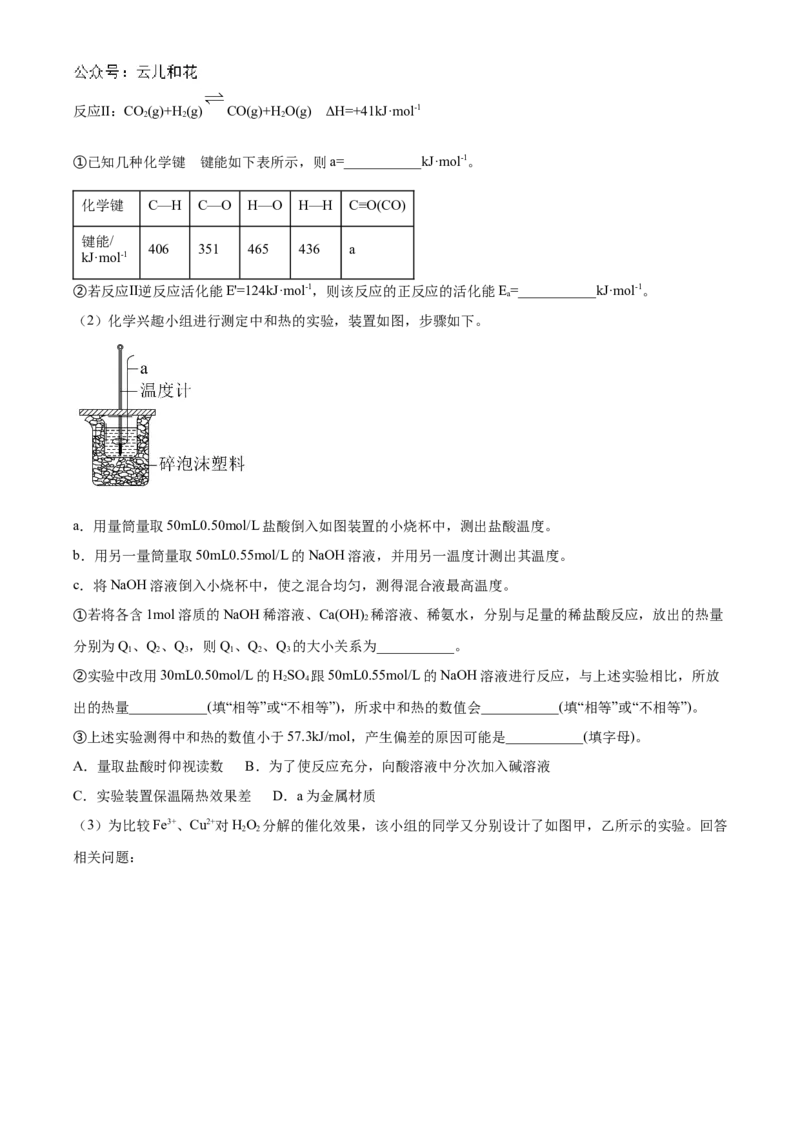
(2)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。
a.用量筒量取50mL0.50mol/L盐酸倒入如图装置的小烧杯中,测出盐酸温度。
b.用另一量筒量取50mL0.55mol/L的NaOH溶液,并用另一温度计测出其温度。
c.将NaOH溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
①若将各含1mol溶质的NaOH稀溶液、Ca(OH) 稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量
2
分别为Q、Q、Q,则Q、Q、Q 的大小关系为___________。
1 2 3 1 2 3
②实验中改用30mL0.50mol/L的HSO 跟50mL0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放
2 4
出的热量___________(填“相等”或“不相等”),所求中和热的数值会___________(填“相等”或“不相等”)。
③上述实验测得中和热的数值小于57.3kJ/mol,产生偏差的原因可能是___________(填字母)。
A.量取盐酸时仰视读数 B.为了使反应充分,向酸溶液中分次加入碱溶液
C.实验装置保温隔热效果差 D.a为金属材质
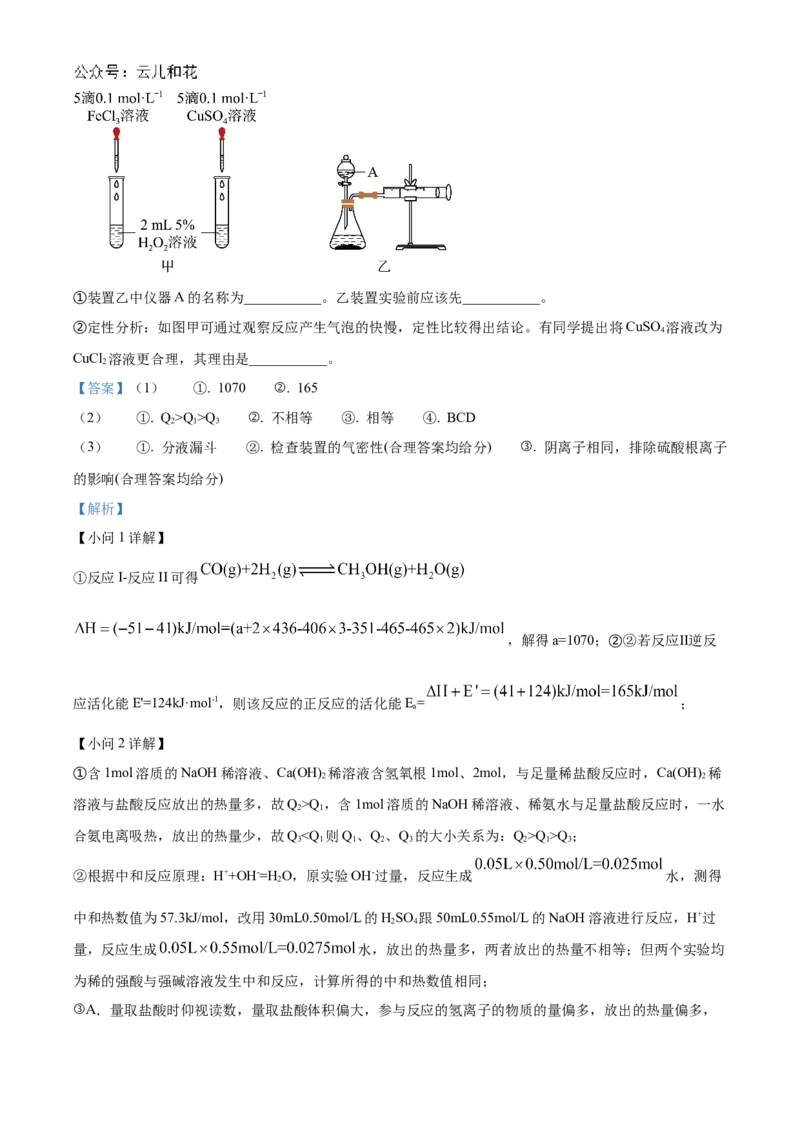
(3)为比较Fe3+、Cu2+对HO 分解的催化效果,该小组的同学又分别设计了如图甲,乙所示的实验。回答
2 2
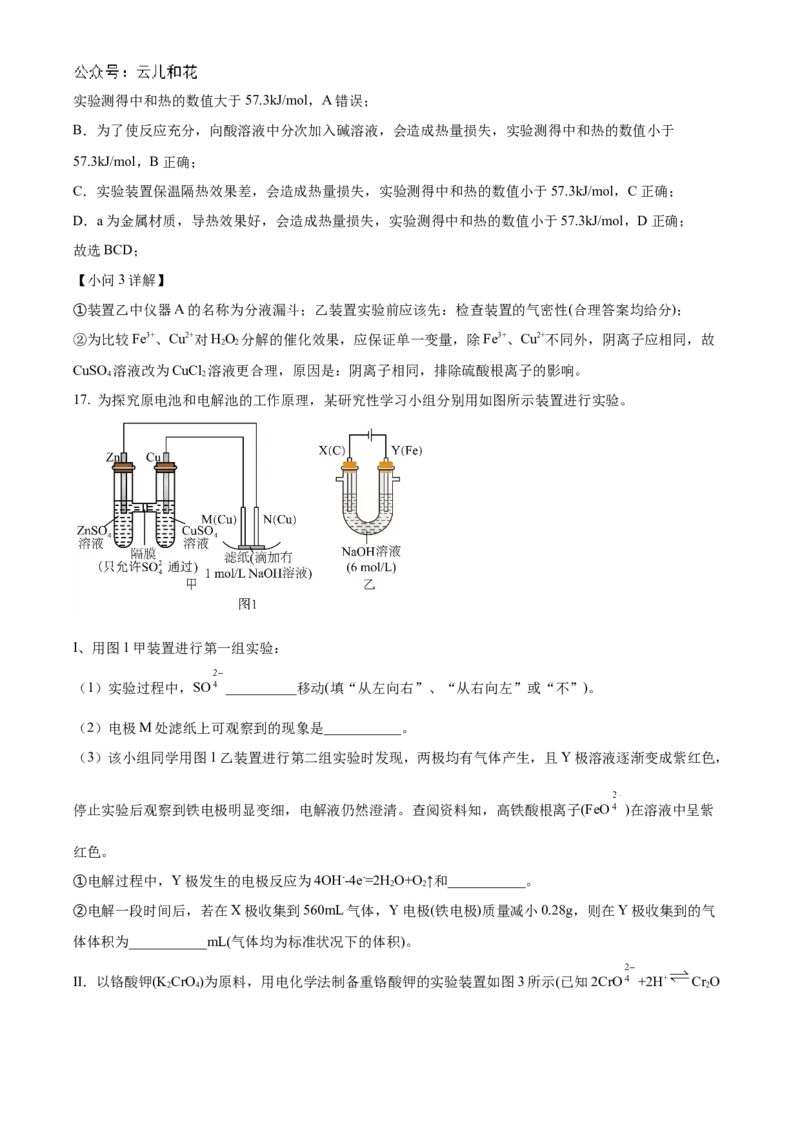
相关问题:①装置乙中仪器A的名称为___________。乙装置实验前应该先___________。
②定性分析:如图甲可通过观察反应产生气泡的快慢,定性比较得出结论。有同学提出将CuSO 溶液改为
4
CuCl 溶液更合理,其理由是___________。
2
【答案】(1) ①. 1070 ②. 165
(2) ①. Q>Q >Q ②. 不相等 ③. 相等 ④. BCD
2 1 3
(3) ①. 分液漏斗 ②. 检查装置的气密性(合理答案均给分) ③. 阴离子相同,排除硫酸根离子
的影响(合理答案均给分)
【解析】
【小问1详解】
①反应I-反应II可得
,解得a=1070;②②若反应Ⅱ逆反
应活化能E'=124kJ·mol-1,则该反应的正反应的活化能E= ;
a
【小问2详解】
①含1mol溶质的NaOH稀溶液、Ca(OH) 稀溶液含氢氧根1mol、2mol,与足量稀盐酸反应时,Ca(OH) 稀
2 2
溶液与盐酸反应放出的热量多,故Q>Q ,含1mol溶质的NaOH稀溶液、稀氨水与足量盐酸反应时,一水
2 1
合氨电离吸热,放出的热量少,故Q
Q >Q ; 3 1 1 2 3 2 1 3 ②根据中和反应原理:H++OH-=H O,原实验OH-过量,反应生成 水,测得 2 中和热数值为57.3kJ/mol,改用30mL0.50mol/L的HSO 跟50mL0.55mol/L的NaOH溶液进行反应,H+过 2 4 量,反应生成 水,放出的热量多,两者放出的热量不相等;但两个实验均 为稀的强酸与强碱溶液发生中和反应,计算所得的中和热数值相同; ③A.量取盐酸时仰视读数,量取盐酸体积偏大,参与反应的氢离子的物质的量偏多,放出的热量偏多,实验测得中和热的数值大于57.3kJ/mol,A错误; B.为了使反应充分,向酸溶液中分次加入碱溶液,会造成热量损失,实验测得中和热的数值小于 57.3kJ/mol,B正确; C.实验装置保温隔热效果差,会造成热量损失,实验测得中和热的数值小于57.3kJ/mol,C正确; D.a为金属材质,导热效果好,会造成热量损失,实验测得中和热的数值小于57.3kJ/mol,D正确; 故选BCD; 【小问3详解】 ①装置乙中仪器A的名称为分液漏斗;乙装置实验前应该先:检查装置的气密性(合理答案均给分); ②为比较Fe3+、Cu2+对HO 分解的催化效果,应保证单一变量,除Fe3+、Cu2+不同外,阴离子应相同,故 2 2 CuSO 溶液改为CuCl 溶液更合理,原因是:阴离子相同,排除硫酸根离子的影响。 4 2 17. 为探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示装置进行实验。 Ⅰ、用图1甲装置进行第一组实验: (1)实验过程中,SO __________移动(填“从左向右”、“从右向左”或“不”)。 (2)电极M处滤纸上可观察到的现象是___________。 (3)该小组同学用图1乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色, 停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(FeO )在溶液中呈紫 红色。 ①电解过程中,Y极发生的电极反应为4OH--4e-=2H O+O↑和___________。 2 2 ②电解一段时间后,若在X极收集到560mL气体,Y电极(铁电极)质量减小0.28g,则在Y极收集到的气 体体积为___________mL(气体均为标准状况下的体积)。 Ⅱ.以铬酸钾(K CrO)为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知2CrO +2H+ Cr O 2 4 2+H O) 2 (4)结合阳极电极反应式,分析阳极区能得到重铬酸钾溶液的原因:___________。 (5)电解一段时间后,测得阳极区溶液中K+物质的量由bmol变为amol,则此时铬酸钾的转化率为 ___________。 【答案】(1)从右向左 (2)有蓝色沉淀产生 (3) ①. ②. 112 (4)阳极的电极反应为 ,溶液中 浓度增大,使反应 向生成 的方向移动,部分 通过阳离子交换膜移动到阴极区,使阳极区主要成分是 (合理答案均可) (5) 或 【解析】 【分析】Ⅰ、由图可知甲为Zn-Cu-硫酸铜电池,为原电池,Zn为负极,Cu为正极,装置乙为电解池,Y作 阳极, ,X做阴极, 。 Ⅱ.左侧为阴极区发生反应: ,右侧为阳极区发生反应: ,,据此分析。 【小问1详解】 电解质溶液中的阴离子向负极Zn移动,则硫酸根离子从右向左; 【小问2详解】 M为活性电极且与电源正极相连,M作阳极,发生反应:Cu-2e-=Cu2+,生成的铜离子与电解质中氢氧根离 子结合生成氢氧化铜蓝色沉淀; 【小问3详解】 ①装置乙为电解池,Y作阳极,Y极溶液逐渐变成紫红色,结合已知信息可知Y电极上Fe失电子生成 ,电极反应为: ,该电极生成气体,说明氢氧根离子也在电极放电生 成氧气4OH--4e-=2H O+O↑; 2 2 ②X极发生反应为: ,收集到560mL氢气,物质的量为0.025mol,转移电子的物 质的量为0.05mol;Y电极(铁电极)质量减小0.28g,即消耗0.005molFe,失去电子物质的量为0.03mol,则 该电极上水放电时失去电子的物质的量为0.02mol,结合电极反应: ,则在Y极 收集到的气体物质的量为0.005mol,标准状况下气体体积为0.005mol ×22.4L/mol=0.112L=112mL; 【小问4详解】 阳极的电极反应为 ,溶液中 浓度增大,使反应 向生成 的方向移动,部分 通过阳离子交换膜移动到阴极区,使阳极区主要成分是 (合理答案均可); 【小问5详解】 由反应可知电解过程中钾离子向左侧移动,物质的量减少,钾离子的减少量与转移电子的物质的量相同, 阳极区溶液中 物质的量由bmol变为a mol,则转移电子的物质的量为(b - a)mol,根据阳极反应可知电 子转移1mol时生成1mol氢离子,则溶液中生成的氢离子的物质的量为(b - a)mol。由反应可知,生成(b - a)mol氢离子时消耗(b - a)mol mol ,原溶液中钾离子的物质的量为 bmol,则 的物质的量为 ,则此时铬酸钾的转化率为 或 ; 18. 控制、治理氮氧化物污染是改善大气质量的重要措施。 (1)火力发电厂的燃煤排烟中含大量的氮氧化物(NO ),可利用甲烷和NO 在一定条件下反应消除其污染, x x 那么CH 与NO 反应的化学方程式为___________。 4 2 (2)在一密闭容器中发生反应2NO (g) 2NO(g)+O (g) ΔH>0,反应过程中NO 的浓度随时间变化的情 2 2 2 况如下图所示。请回答: ①假设曲线A、B分别表示的是该反应在某不同条件下的反应情况,那么温度高的是曲线___________。 (填“A”或“B”) ②曲线B对应的反应平衡常数 =___________(填数值)。 ③依曲线A,反应在前3min内氧气的平均反应速率为___________。(保留三位有效数字) (3)一定温度下,密闭容器中NO 可发生以下反应: 2 5 I.2NO(g) 4NO (g)+O(g) 2 5 2 2 Ⅱ.2NO (g) 2NO(g)+O (g) 2 2 那么反应I的平衡常数表达式为K=___________。假设达到平衡时,c(NO )=0.4mol/L,c(O)=1.3mol/L,那 2 2么反应Ⅱ中NO 的转化率为___________,NO(g)的起始浓度不低于___________mol/L,反应Ⅱ的平衡常数 2 2 5 为___________(填数值)。 【答案】(1) (2) ①. B ②. 0.05 ③. (3) ①. ②. 80% ③. 1 ④. 20.8 【解析】 【小问1详解】 CH 与NO 反应转化为无污染物质,即生成CO、N 和HO,化学方程式为: 4 2 2 2 2 ; 【小问2详解】 ①B曲线2min时达到平衡,而A曲线3min时达到平衡,B的反应速率快,温度高; ②B曲线2min时达到平衡,可列出三段式: , ; ③依曲线A,反应在前3min内NO 的浓度变化量为0.07mol/L,故氧气的浓度变化量为0.035mol/L,平均 2 反应速率为: ; 【小问3详解】 反应I的平衡常数表达式为 ;设反应I中NO2的转化浓度为xmol/L,可列出三段式:, ,则0.25x+0.5(x-0.4)=1.3,解得x=2,NO 2 的转化率为: ;该反应为可逆反应,NO 不可能完全转化,故NO(g)的起始浓度 2 5 2 5 不低于1mol/L;平衡时反应II中各物质浓度为:c(NO )=0.4mol/L,c(O)=1.3mol/L,c(NO)=1.6mol/L,故 2 2 反应II的平衡常数为: 。 19. 甲醇是一种重要的化工原料,具有开发和应用的广阔前景。工业上使用水煤气(CO与H 的混合气体)转 2 化成甲醇,反应为CO(g)+2H(g) CHOH(g)。 2 3 (1)CO的平衡转化率与温度、压强的关系如图所示。 ①A、B两点的平衡常数K 、K 的大小关系是___________。 A B ②下列叙述能说明上述反应能达到化学平衡状态的是___________(填字母)。 a.CHOH的体积分数不再改变 3 b.2v (H )=v (CHOH) 正 2 逆 3 c.混合气体的平均摩尔质量不再改变 d.同一时间内,消耗0.4molH,生成0.02molCO 2 (2)在 ℃,P 压强时往一容积为2L的密闭容器内,充入0.3molCO与0.4molH 发生反应。 2 2 ①平衡时H 的体积分数是___________。 2②若P 压强恒定为p,则平衡常数K=___________(K 用气体平衡分压代替气体平衡浓度计算,分压=总压 2 p p ×气体的物质的量分数,整理出含p的最简表达式)。 (3)中国科学院应用化学研究所在甲醇(CHOH是一种可燃物)燃料电池技术方面获得新突破。甲醇燃料 3 电池的工作原理如图所示。 ①该电池工作时,甲醇燃料应从___________口通入; ②该电池负极的电极反应式:___________;该电池正极的电极反应式:___________。 ③工作一段时间后,当6.4g甲醇完全反应成产物时,有___________mol电子转移。 【答案】(1) ①. K =K ②. acd A B (2) ①. 25% ②. (3) ①. b ②. CHOH-6e-+H O=CO↑+6H+ ③. O+4H++4e-=2H O ④. 1.2 3 2 2 2 2 【解析】 【小问1详解】 ①A、B两点的温度相同,平衡常数相等,即K =K ; A B ②a.CHOH的体积分数不再改变时,说明该反应正逆反应速率相等,反应达到平衡,a正确; 3 b.当v (H )=2v (CHOH)时,该反应正逆反应速率相等,反应才达到平衡,b错误; 正 2 逆 3 c.该反应平衡前气体总质量不变,总物质的量改变,则平均摩尔质量在改变,故平均摩尔质量不变,说 明反应达到平衡,c正确; d.同一时间内,消耗0.4molH,生成0.02molCO,说明该反应正逆反应速率相等,反应达到平衡,d正确; 2 故选acd; 【小问2详解】 ①在 ℃,P 压强时,CO的平衡转化率为50%,可列出三段式: 2,平衡时H 的体积分数是: 2 ; ②平衡时H 的分压是: ,CO和CHOH的分压为: ,平衡常数 ; 2 3 【小问3详解】 该装置为燃料电池,质子向正极移动,故右侧电极为正极,c通入氧气(或空气),左侧为负极,b通入 CHOH,a处产生CO。 3 2 ①根据分析,该电池工作时,甲醇燃料应从b口通入; ②该电池负极的电极反应式:CHOH-6e-+H O=CO↑+6H+;该电池正极的电极反应式:O+4H++4e-=2H O; 3 2 2 2 2 ③工作一段时间后,当6.4g即0.2mol甲醇完全反应成产物时,根据负极电极式可知有 电子转移。