文档内容
2025 届高三第一次教学质量监测
化学参考答案
1.【详解】A.制白砂糖时用活性炭脱色为活性炭的吸附作用,属于物理变化,A错误;
B.石墨烯为碳单质,不属于有机高分子材料,B错误;
C.港珠澳大桥使用高性能富锌底漆防腐,锌作负极保护铁,依据的是牺牲阳极法,C错误;
D.采用氢能源汽车代替燃油车,减少CO 的产生和排放,有利于“碳达峰、碳中和”,D正确;
2
故选D。
2.【详解】A.H O 是共价化合物,电子式为 ,A错误;
2 2
B.由系统命名法, 的化学名称是3-甲基-2-戊烯,B正确;
C.同素异形体指的是单质,CO、CO 是化合物,C错误;
2
D.B的核电荷数为5,原子结构示意图为 ,D错误;
故选B。
3.【详解】【详解】A.同周期元素,从左到右第一电离能呈增大趋势,氮原子的2p轨道为稳定的半充满结构,
元素的第一电离能大于相邻元素,则氮元素的第一电离能大于氧元素,故A错误;
B.该反应的反应物中N 为分子晶体,故B错误;
2
C.1个N 分子中有1个σ键和2个π键,数目之比为1:2,故C正确;
2
D.碳元素的原子序数为6,基态原子的电子排布式为1s22s22p2,原子中共有4种不同空间运动状态的电子,
故D错误;
故选C。
4.【详解】A.配制溶液不能在容量瓶中直接溶解固体,故A错误;
B.NH 的密度比空气小,故采用向下排空气法收集,装置正确,故B正确;
3
C.Zn片与CuCl 溶液反应,置换出铜,能说明活动性:Zn>Cu,故C正确;
2
D.HCl与NaOH快速反应,故要考虑防倒吸,故D正确;
故选A。
5.【详解】A.标准状况下,水不是气体,22.4L H O物质的量不是1mol,故A错误;
2
B.碳酸根离子水解导致其数目小于N ,B错误;
A
C.电解精炼铜时,阳极上除了铜放电之外,还有其他金属(锌、铁等)也会放电,因此阳极质量减轻64g时,
转移电子数不是2N ,C错误;
A
D.42g丙烯为1mol,则碳原子数为3N ,D正确;
A
故选D。
6.【详解】A.丁基苯酞的化学式不饱和度为6,H原子个数为12×2+2-6×2=14,化学式为C H O ,A项错误;
12 14 2
B.丁基苯酞分子中碳原子有2种杂化方式,B项错误;
C.酯基能发生取代反应,苯环能与氢气发生加成反应,可燃烧能发生氧化反应,C项正确;
D.苯环不对称,因此苯环上一氯代物有4种,D项错误;
故选C。
7.【详解】A.氢氟酸是弱电解质,氢氟酸蚀刻玻璃的离子方程式为:SiO 4HFSiF 2H O,A错误;
2 4 2
B.Cl 制备84消毒液是将Cl 通入NaOH溶液中,离子方程式为:Cl +2OH-=Cl-+ClO-+H O,选项B正确;
2 2 2 2
C.将稀硫酸滴入Ba(OH) 溶液中,反应的离子方程式为:Ba2++SO 2-+2H++2OH-=BaSO ↓+2H O,选项
2 4 4 2
C错误;
D.金属Na先与溶液中的水反应,生成的碱与MgCl 溶液生成沉淀,反应的离子方程式为:
2
2Na+2H O+Mg2+=2Na++Mg(OH) ↓+H ↑,D错误;
2 2 2
故选B。
化学答案 第1页,共5页8.【分析】X、Y、Z、W、R为原子序数依次增大的短周期元素,由题目信息Z的单质在空气成分中体积分数占
比最大可知Z为N元素,Y、W分别为C、O;X原子核外电子只有一种运动状态,则X为H。
【详解】A.Y、Z、W分别为:C、N、O,电负性由大到小的顺序为O>N>C,A正确;
B.非金属性越强,最简单氢化物的稳定性越强,非金属性N>P,则氢化物稳定性N>P,B错误;
C.X与W形成的化合物可以为H O、H O ,都为极性分子,C错误;
2 2 2
D.分子结构中含羧基官能团,能和碱反应,D错误;
故选A。
9.【分析】净化除氯后的海水,加入硝酸银,发生反应为I-+Ag+=AgI↓,进行富集,生成含有AgI的悬浊液,
继续即加入铁粉,发生反应Fe+2AgI=2I-+2Ag+Fe2+,过滤掉析出的Ag,向FeI 中加入过量Cl ,发生反
2 2
应为2FeI +3Cl =2FeCl +2I ,得到I 。据此解答。
2 2 3 2 2
【详解】A.过滤操作用到的玻璃仪器有漏斗、烧杯、玻璃棒,故A正确;
B.将“氧化”后的溶液需要先萃取分液后再蒸馏可得单质碘,故B错误;
C.I-、Fe2+的还原性I->Fe2+,氯气首先与碘离子反应,因此先生成的氧化产物为I ,故C正确;
2
D.从流程图可知,转化生成的沉淀为单质Ag,银和硝酸反应生成硝酸银,可循环使用,故D正确;
故选B。
10.【详解】A.由图可知,该反应为反应物总能量高于生成物总能量的放热反应,降低温度,平衡向正反应方
向移动,DMF的平衡转化率增大,故A正确;
B.由图可知,该历程包含6个基元反应,故B正确;
C.由反应物和生成物的相对能量可知,反应放热为0eV-(-1.02eV)=1.02eV,1molDMF完全转化为三甲胺,
则会释放出1.02eV·N 的能量,故C错误;
A
D.由图可知,最大能垒(活化能)为1.19eV,反应的方程式为N(CH ) +OH*+H*=N(CH ) (g)+H O(g),
3 3 3 3 2
故D正确;
故选C。
11.【详解】A.将新鲜菠菜剪碎、研磨、溶解,过滤,向滤液中加入少量稀硝酸,再滴加几滴溶液,若溶液变
红,说明菠菜中含有铁元素,A正确;
B.AgNO 过量,加入0.1molL1KI,剩余的AgNO 与KI反应生成AgCl黄色沉淀,没有发生沉淀转化,
3 3
无法比较K AgCl、K (AgI),B不正确;
sp sp
C.常温下,用pH计测量0.1molL-1NaClO溶液的pH>7,说明次氯酸根离子水解使溶液呈碱性,则说明
HClO是弱酸,C正确;
D.轻金属盐的浓溶液能使蛋白质溶液发生盐析,盐析可逆,向NH SO 饱和溶液中,加入几滴鸡蛋清溶
4 2 4
液,震荡,出现沉淀,再加入蒸馏水,振荡,沉淀溶解,证明蛋白质的盐析过程是可逆的,D正确;
故选B。
12.【分析】电子从X极流出,说明X极是失去电子做负极,发生氧化反应,电极反应方程式为Li-e-=Li+。电
子从Y极流入,说明Y极是得到电子做正极,发生还原反应,电极反应方程式为:
2SOCl +4e-=SO ↑+S↓+4Cl-。外电路中电子移动形成电流,内电路中离子移动形成电流。阳离子交换膜只
2 2
允许阳离子通过。原电池中,阳离子向正极移动,阴离子向负极移动。Li+透过阳离子交换膜向Y极移动。
化学答案 第2页,共5页【详解】A.根据电子流向可知,X为负极,Y为正极,A正确;
B.Li+为阳离子,应透过阳离子交换膜向正极移动,B正确;
C.Li的性质较活泼,易与水反应,所以四氯铝酸锂LiAlCl 的SOCl 溶液不能含水,C正确;
4 2
D.正极为得到电子的一极,D错误;
故选D。
13.【详解】A.SO 中心S原子形成3个σ键,孤电子对数为0,所以S原子属于sp2杂化,空间结构为平面三角
3
形,故A正确;
4120
B. 根据晶胞图可知阴阳离子数目均为4,由密度公式可算得 a31030N g/cm3,故B正确;
A
C.根据晶胞图,可以看出Fe2紧邻的阴离子个数为6,故C错误;
D.FeS 中Fe为+2价,S为-1价;完全反应生成SO 和Fe O 后,Fe为+3价,S为+4价,有1molFe和2molS
2 2 2 3
发生电子转移,所以有1molFeS 完全反应生成SO 和Fe O ,有11mol电子发生转移,故D正确;
2 2 2 3
故答案选C。
14.【详解】A.由图可知,0.1 molL1HX的pH等于1,则HX为强酸,电离方程式为HX=H++X-,故A错误;
B.由图可知,HY的pH等于4,0.1mol/LHY溶液中c(H+)=10-4mol/L,故B错误;
C.VNaOH20 mL时,两种溶液恰好反应分别生成等量的NaX和NaY,NaY发生水解,所以溶液中
c
X-
>c
Y-
,故C错误;
D.b点为加入NaOH溶液体积为10mL,对于HY溶液中,反应恰好生成等量的HY和NaY,根据物料守
恒:c Y- +cHY=2c Na+ ,根据电荷守恒:c Y- +c OH- =c H+ +c(Na+) ,联立得:c(Y-)-
c(HY)=2[c(H+)-c(OH-)],则c(Y-)-c(HY)>c(H+)-c(OH-),故D正确;
故选:D。
15.(14分)
【分析】装置A用饱和食盐水和电石反应制取乙炔,反应方程式为:CaC +2H O=Ca(OH) +CH≡CH↑,装
2 2 2
置B的硫酸铜溶液可除去电石中产生的杂质气体H S、PH 等,装置C中C H 与浓HNO 反应生成H C O 和
2 3 2 2 3 2 2 4
NO ,装置D用来吸收二氧化氮尾气,据此分析回答。
2
【详解】(1)仪器a的名称为分液漏斗;(2)由分析可知,装置B中盛有的硫酸铜溶液用于吸收除去乙炔
气体中混用的硫化氢和磷化氢等气体杂质;
(3)装置C中C H 与浓HNO 反应发生H C O 和NO ,反应化学方程式为
2 2 3 2 2 4 2
HgNO
C H 8HNO 浓 3 2 H C O 8NO 4H O ,NO 的颜色为红棕色,a、c、d均为无色,故b正确;
2 2 3 2 2 4 2 2 2
4555℃
(4)增大气液接触面积,加快反应速率;
(5)反应方程式为:CaC +2H O=Ca(OH) +C H ↑;
2 2 2 2 2
(6)a.使用托盘天平时,应该“左物右码”,a错误;b.溶解草酸固体时需要搅拌,b正确;
c.将草酸溶液转移到容量瓶中时需要用玻璃棒引流,c错误;d.定容时,视线应该与凹液面的最低处相
平,d正确;故选ac。
(7)已知5H C O +2MnO -+6H+=10CO ↑+2Mn2++8H O,消耗的nKMnO 2.0103mol,消耗高锰酸钾
2 2 4 4 2 2 4
的草酸的物质的量为nH C O 2.5nKMnO 5.0103mol,样品中草酸晶体的质量分数为:
2 2 4 4
化学答案 第3页,共5页100
5103126 g
20
100% 90%
3.500g
参考答案:(每空2分)(1)分液漏斗 (2)除去H S、PH 等气体杂质 (3)b
2 3
(4)增大气液接触面积,加快反应速率 (5)CaC +2H O=Ca(OH) +C H ↑
2 2 2 2 2
(6)ac (7)90%
16.(15分)
【解析】炼锌废渣含有锌、铅、铜、铁、钴、锰等元素的2价氧化物及锌和铜的单质,经稀硫酸酸浸时,
铜不溶解,Zn及其它2价氧化物除铅元素转化为硫酸铅沉淀外,其他均转化为相应的+2价阳离子进入溶液;
然后通入硫化氢沉铜生成CuS沉淀;过滤后,滤液中加入Na S O 将锰离子氧化为二氧化锰除去,同时亚铁离子
2 2 8
也被氧化为铁离子;再次过滤后,用氢氧化钠调节pH=3.1~6.2,铁离子完全转化为氢氧化铁沉淀除去铁元素;第
三次过滤后的滤液中加入次氯酸钠沉钴,得到Co(OH) 。
3
(1)“酸浸”前,需将废渣磨碎,其原因是增大固体与酸反应的接触面积,提高钴元素的浸出效率。
(2)Co在元素周期表的位置是第四周期VIII族,Cu的价电子排布式为3d104s1。(3)“沉锰”步骤中,Na S O
2 2 8
将Mn2+氧化为二氧化锰除去,二氧化锰为氧化产物,故C正确;(4)“酸浸”步骤中,Cu不溶解,Zn单质
及其它元素的2价氧化物除铅元素转化为硫酸铅沉淀外,其它元素均转化为相应的+2价阳离子进入溶液,
浸渣的成分为铜和硫酸铅;“沉淀”步骤中,用NaOH调pH分离出的滤渣是Fe(OH) ,从图像分析得知Zn2+
3
不能沉淀,调节的pH的范围是3.1~6.2;(5)“酸浸”步骤中,CoO发生反应的化学方程式为:
CoO+H SO =CoSO +H O。
2 4 4 2
(6)“沉钴”后滤液的pH=5.0~5.5,溶液中有Zn元素以Zn2形式存在,当pH>12后氢氧化锌会溶解转化为
[Zn(OH) ]2,因此,从“沉钴”后的滤液中回收氢氧化锌的方法是:向滤液中滴加NaOH溶液,边加边搅拌,
4
控制溶液的pH:8≤pH<12,静置后过滤、洗涤、干燥。
参考答案:(1)增大固体与酸反应的接触面积,提高钴元素的浸出效率。(2分)
(2)第四周期VIII族(2分);3d104s1(1分) (3)C(2分)
(4)硫酸铅(或PbSO )(2分);3.1~6.2(2分)
4
(5)CoO+H SO =CoSO +H O(2分)
2 4 4 2
(6)向滤液中滴加NaOH溶液,边加边搅拌,控制溶液的pH:8≤pH<12,静置后过滤、洗涤、干燥。
(2分)
17.(14分)
【解析】主要对盖斯定律、化学平衡、反应速率、平衡图像分析平衡移动原理的综合应用、电化学的电极反
应式及相关计算进行考查。(1)应用盖斯定律①+②得H =a+bKJ/mol;(2)①氧气的初始浓度为0.5mol/L,平衡
3
时浓度为0.2mol/L,变化的浓度为(0.5-0.2)mol/L=0.3mol/L,氧气的速率为0.3/5=0.06mol/(L·min),乙烷速率
是氧气的υ(C H )=2υ(O )=0.06×2=0.12mol/(L·min);②恒温恒容,密度是个恒量,A错误;反应体系不等,压
2 6 2
强是变量,容器内压强不再变化则达到平衡,B正确;υ (O )是消耗,υ (C H )是消耗,两侧同时消耗,乙烯消
正 2 逆 2 4
耗的量是氧气的2倍,故C正确;因投料比等于系数之比,转化率之比也等于系数之比是个恒量,故D错误;
故选BC。(3)从图中可知,压强相同的情况下,随着温度升高,C H 的平衡转化率增大,因此该反应为吸热反
2 6
应,a>0。
a.600℃,0.6MPa时,C H 的平衡转化率约为20%,a错误;
2 6
b.700℃,0.7MPa时,C H 的平衡转化率约为50%,最接近40%,b正确;
2 6
c.700℃,0.8MPa时,C H 的平衡转化率接近50%,升高温度,该反应的化学平衡正向移动,C H 转化率
2 6 2 6
增大,因此800℃,0.8MPa时,C H 的平衡转化率大于50%,c错误;故答案选b。
2 6
(4)由图3可知,M极二氧化碳得到电子发生还原反应生成乙烯、N极水失去电子发生氧化反应生成氧气:
2H O-4e-=4H++O ↑;M极得到电子发生还原反应生成乙烯:2CO +12e-+12H+=C H +4H O,转移的电
2 2 2 2 4 2
子数为6N 时即为6mole-,制备得到的乙烯为0.5mol的乙烯,故标况下体积为11.2L。
A
参考答案:【每空2分】(1)a+b (2)0.12mol/(L·min), BC(错一个扣1分,扣完为止)
(3)a>0;b (4)2H O-4e-=4H++O ↑; 11.2L
2 2
化学答案 第4页,共5页18.(15分)
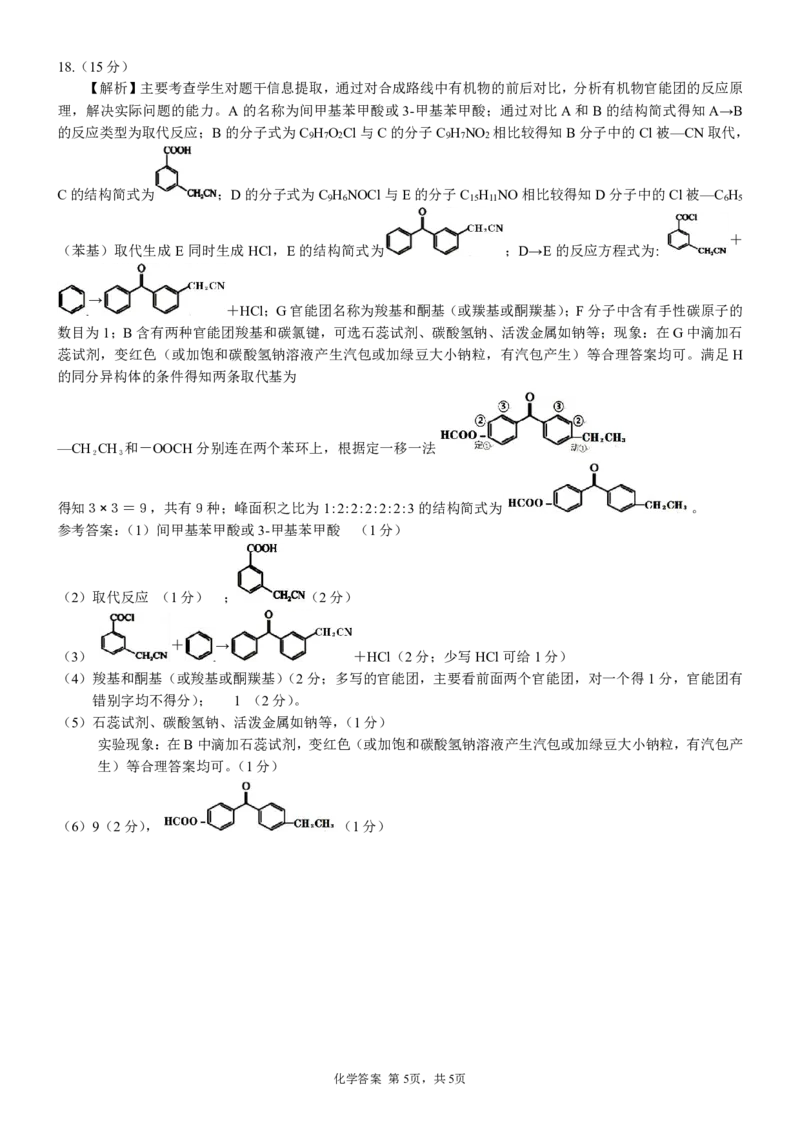
【解析】主要考查学生对题干信息提取,通过对合成路线中有机物的前后对比,分析有机物官能团的反应原
理,解决实际问题的能力。A的名称为间甲基苯甲酸或3-甲基苯甲酸;通过对比A和B的结构简式得知A→B
的反应类型为取代反应;B的分子式为C H O Cl与C的分子C H NO 相比较得知B分子中的Cl被—CN取代,
9 7 2 9 7 2
C的结构简式为 ;D的分子式为C H NOCl与E的分子C H NO相比较得知D分子中的Cl被—C H
9 6 15 11 6 5
+
(苯基)取代生成E同时生成HCl,E的结构简式为 ;D→E的反应方程式为:
→
+HCl;G官能团名称为羧基和酮基(或羰基或酮羰基);F分子中含有手性碳原子的
数目为1;B含有两种官能团羧基和碳氯键,可选石蕊试剂、碳酸氢钠、活泼金属如钠等;现象:在G中滴加石
蕊试剂,变红色(或加饱和碳酸氢钠溶液产生汽包或加绿豆大小钠粒,有汽包产生)等合理答案均可。满足H
的同分异构体的条件得知两条取代基为
—CH CH 和-OOCH分别连在两个苯环上,根据定一移一法
2 3
得知3×3=9,共有9种;峰面积之比为1:2:2:2:2:2:3的结构简式为 。
参考答案:(1)间甲基苯甲酸或3-甲基苯甲酸 (1分)
(2)取代反应 (1分) ; (2分)
+ →
(3) +HCl(2分;少写HCl可给1分)
(4)羧基和酮基(或羧基或酮羰基)(2分;多写的官能团,主要看前面两个官能团,对一个得1分,官能团有
错别字均不得分); 1 (2分)。
(5)石蕊试剂、碳酸氢钠、活泼金属如钠等,(1分)
实验现象:在B中滴加石蕊试剂,变红色(或加饱和碳酸氢钠溶液产生汽包或加绿豆大小钠粒,有汽包产
生)等合理答案均可。(1分)
(6)9(2分), (1分)
化学答案 第5页,共5页