文档内容
2024 2025 学年第一学期高二年级七校期中联考试题
∼
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用 2B 铅笔把答题卡上对
应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区
域内作答,超
.
出
.
答
.
题
.
区
.
域
.
书
.
写
.
的
.
答
.
案
.
无
.
效
.
,
.
在
.
试
.
题
.
卷
.
、
.
草
.
稿
.
纸
.
上
.
作
.
答
.
无
.
效
.
。
4.本卷命题范围:人教版选择性必修1第一章~第三章第一节。
5.可能用到的相对原子质量:H1 C12 N14 O16 P31
一、选择题(本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一项
是符合题目要求的)
1.下列物质属于强电解质的是( )
A.BaSO B.CO C.C H OH D.CH COOH
4 2 2 5 3
2.下列叙述正确的是( )
A.焓减反应一定能自发进行
B.熵增反应一定能自发进行
C.利用2CO ( g )=C ( s )+O ( g )可以消除CO污染
2
D.吸热反应2N O ( g )=4NO ( g )+O ( g )在较高温度下能自发进行
2 5 2 2
3.某温度时,在容积为4L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,由
图中数据分析,下列结论错误的是( )
A.该反应的化学方程式为2Z+Y 3X
B.3min时,Z的转化率为80%
C.该反应是由正、逆反应同时开始的,最终建立化学平衡
D.添加催化剂可能使反应在2min时达到平衡
4.铬及其化合物在催化、金属防腐等方面具有重要应用。Cr O 催化丙烷脱氢过程中,部分反应历程如图。
2 3
下列说法正确的是( )
学科网(北京)股份有限公司A.X
(
g
)→Y (
g
)的焓变为∆H
B.图示反应历程均为吸热过程
C.该反应为放热反应
D.该反应一定需要加热才能发生
5. 硫 酸 工 业 中 , 通 过 下 列 反 应 使 SO 转 化 为 SO : 2SO ( g )+O ( g ) 2SO ( g )
2 3 2 2 3
∆H =−196.6kJ⋅mol−1。下列关于该过程实际生产中条件选择的说法错误的是( )
A.选择温度为400∼500℃是综合考虑了速率和平衡
B.选择压强为常压主要是出于控制成本角度考虑
C.通入过量空气可以提高SO 、O 的转化率
2 2
D.回收利用尾气中的SO ,可以防止环境污染,同时提高其转化率
2
6.在某化学平衡状态的体系中,若下列物理量发生变化,则一定能判断平衡发生移动的是( )
A.反应混合物的浓度 B.反应的平衡常数 C.正、逆反应速率 D.反应体系的压强
高温
7.工业制氢原理:C ( s )+H O ( g ) CO ( g )+H ( g )。改变下列条件能提高产生氢气的速率且提高活
2 2
化分子百分率的是( )
将炭块改为炭粉 增大水蒸气浓度 适当升高温度 加入高效催化剂
A. B. C. D.
① ② ③ ④
8.已①知②:NH ⋅H O ( aq )与①H③SO ( aq )反应生成③1m④ol ( NH ) SO 的∆②H④=−24.2kJ⋅mol−1;强酸、强碱
3 2 2 4 4 2 4
的稀溶液生成1molH O ( l )的反应热∆H =−57.3kJ⋅mol−1。则NH ⋅H O在水溶液中电离的∆H 为( )
2 3 2
A.+45.2kJ⋅mol−1 B.−45.2kJ⋅mol−1 C.−69.4kJ⋅mol−1 D.+69.4kJ⋅mol−1
9.在恒温恒容密闭容器中投入足量CaC O ,发生反应:CaC O ( s ) CaO ( s )+CO ( g )+CO ( g )。下
2 4 2 4 2
列有关叙述正确的是( )
A.CO体积分数不变时反应达到平衡状态
B.增大CaC O 质量,反应速率会增大
2 4
C.平衡后充入等物质的量的CO和CO ,达到新平衡时其浓度均增大
2
学科网(北京)股份有限公司D.可用单位时间内CaO质量净增量比较反应快慢
10.乙烯、环氧乙烷是重要的化工原料,用途广泛。实验测得2CH =CH ( g )+O ( g ) 2< ( g )
2 2 2
∆H <0中,v =k ⋅c2( ),v =k ⋅c2( CH =CH )⋅c ( O )(k 、k 为速率常数,只与温度
逆 逆 正 正 2 2 2 正 逆
有关)。下列说法正确的是( )
A.反应平衡后,升温,k 增大、k 减小
正 逆
B.反应平衡后,降温,k 减小、k 增大
正 逆
C.反应平衡后,充入一定量的O ,k 增大、k 减小
2 正 逆
k
D.反应平衡后,升温, 正 减小
k
逆
11.常温下,加水稀释H C O 溶液,下列物理量保持不变的是( )
2 2 4
c ( H C O ) c ( H+)
2 2 4
A. B.
c
(
HC
O−)
c
(
H C O
)
2 4 2 2 4
c
(
HC
O−)
C. 2 4 D.c ( HC O−) ⋅c ( C O2−)
c ( H+) ⋅c ( C O2−) 2 4 2 4
2 4
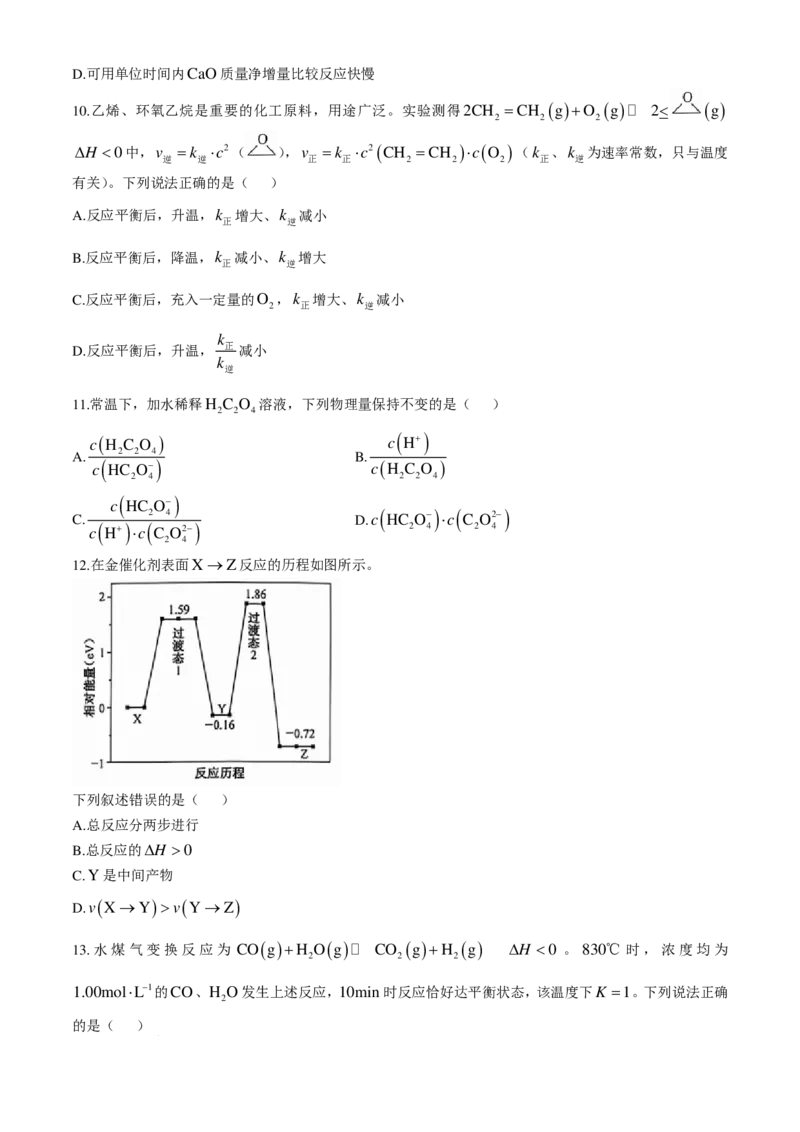
12.在金催化剂表面X→Z反应的历程如图所示。
下列叙述错误的是( )
A.总反应分两步进行
B.总反应的∆H >0
C.Y是中间产物
D.v ( X→Y )>v ( Y→Z )
13.水煤气变换反应为 CO ( g )+H O ( g ) CO ( g )+H ( g ) ∆H <0 。 830℃ 时,浓度均为
2 2 2
1.00mol⋅L−1的CO、H O发生上述反应,10min时反应恰好达平衡状态,该温度下K =1。下列说法正确
2
的是( )
学科网(北京)股份有限公司A.10min时该反应的化学反应速率为0.05mol⋅L−1⋅min−1
B.反应达到平衡时v ( CO )=v ( CO )
正 2 逆
C.平衡后升高温度,平衡逆向移动,∆H 增大
D.再充入少量CO ( g ),平衡正向移动,K值增大
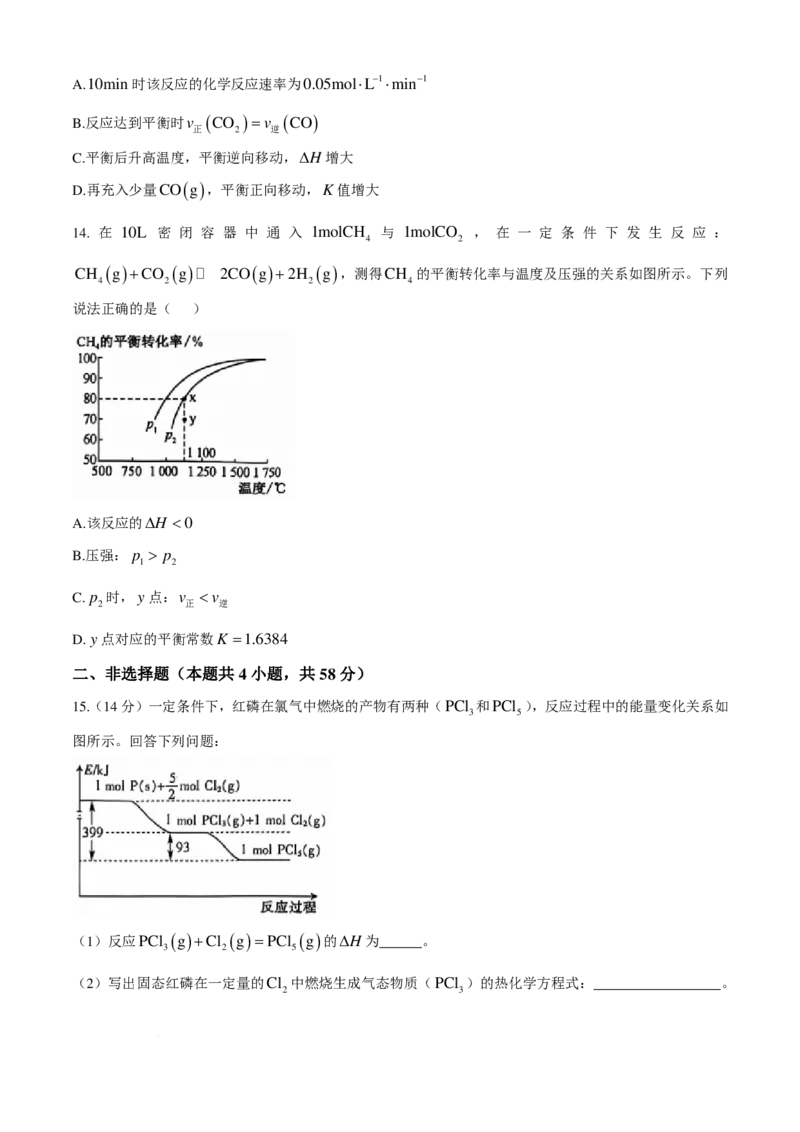
14. 在 10L 密 闭 容 器 中 通 入 1molCH 与 1molCO , 在 一 定 条 件 下 发 生 反 应 :
4 2
CH ( g )+CO ( g ) 2CO ( g )+2H ( g ),测得CH 的平衡转化率与温度及压强的关系如图所示。下列
4 2 2 4
说法正确的是( )
A.该反应的∆H <0
B.压强: p > p
1 2
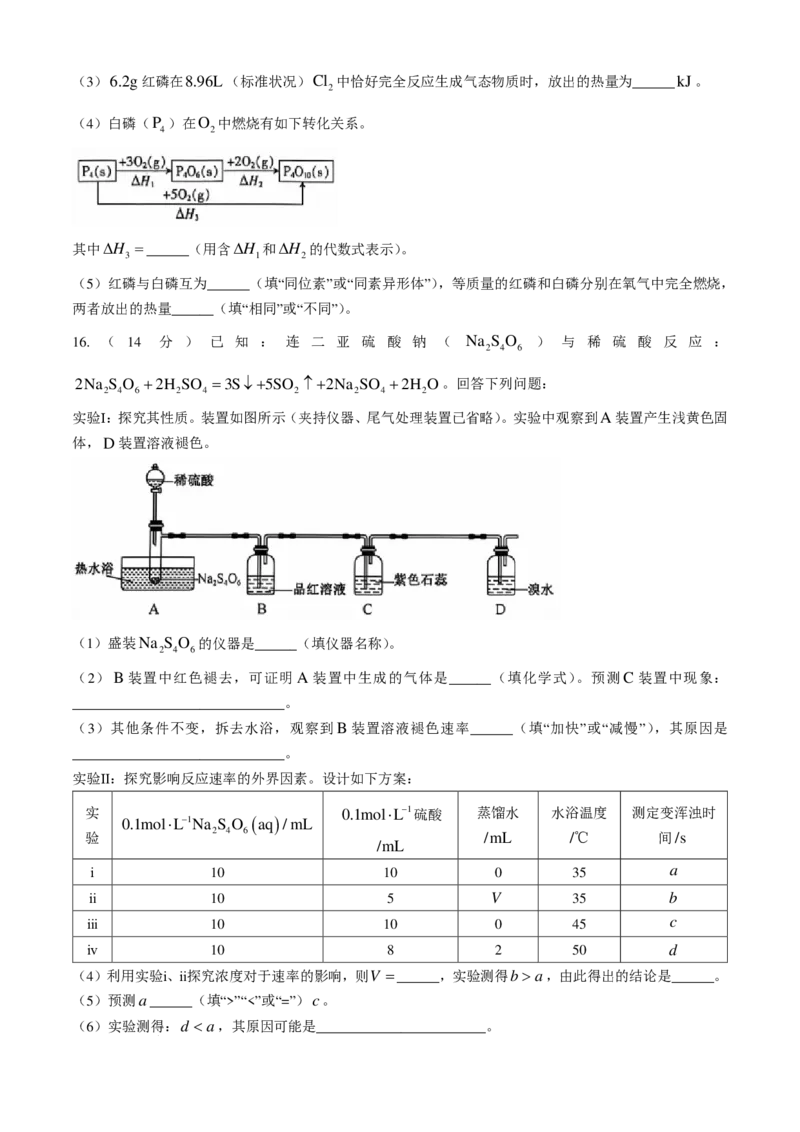
C. p 时,y点:v a,由此得出的结论是______。
(5)预测a______(填“>”“<”或“=”)c。
(6)实验测得:d 0)
2 2 3 2 1
反应Ⅱ:CH OCH ( g )+H O ( g ) 2CH OH ( g ) ∆H =+bkJ⋅mol−1(b>0)
3 3 2 3 2
反应Ⅱ:2CO ( g )+6H ( g ) CH OCH ( g )+3H O ( g ) ∆H
2 2 3 3 2 3
回答下列问题:
(1)∆H =______kJ⋅mol−1,据此判断反应Ⅲ在______(填“低温”“高温”或“任意温度”)条件下能自发进
3
行。
(2)恒温恒压条件下,在密闭容器中通入等物质的量的CO 和H 发生反应Ⅰ,能说明反应Ⅰ达到平衡状态的
2 2
是______(填字母)。
A.平衡常数保持不变
B.生成3molH−H键的同时断裂1molC−O键
C.容器内混合气体的密度保持不变
D.CO 和H O的物质的量之比保持不变
2 2
学科网(北京)股份有限公司( 3 ) T℃ 时 , 将 1mol 二 甲 醚 充 入 某 恒 容 密 闭 容 器 中 , 发 生 如 下 分 解 反 应 :
1
CH OCH
(
g
)
CH
(
g
)+H (
g
)+CO (
g
),在不同时间测定容器内的总压,所得数据如下表:
3 3 4 2
反应时间t/min 0 5 10 15 20 ∞
气体总压 p /kPa p 1.4p 1.6p 1.8p 1.9p 2p
总 0 0 0 0 0 0
由表中数据计算:反应达平衡时,二甲醚的分解率为______,该温度下的平衡常数K =______ ( kPa )2(K
p p
为用气体平衡分压代替气体平衡浓度表示的平衡常数,分压=总压×气体的物质的量分数)。
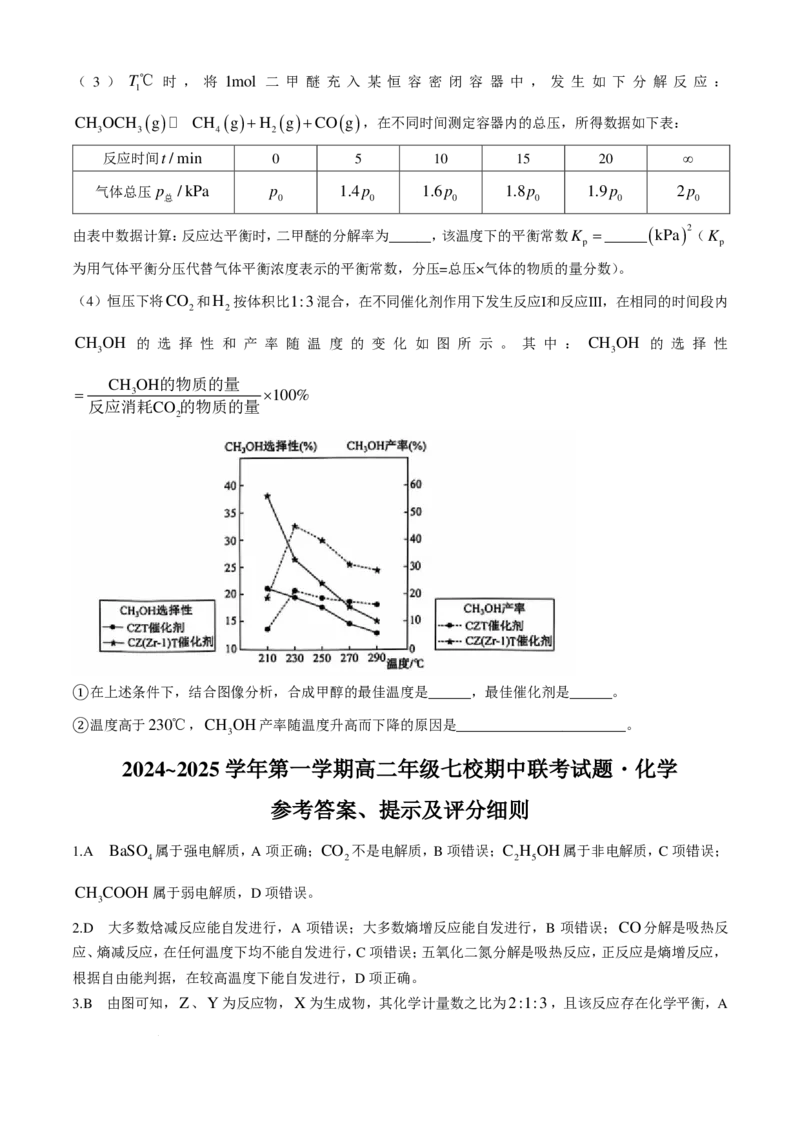
(4)恒压下将CO 和H 按体积比1:3混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅲ,在相同的时间段内
2 2
CH OH 的 选 择 性 和 产 率 随 温 度 的 变 化 如 图 所 示 。 其 中 : CH OH 的 选 择 性
3 3
CH OH的物质的量
= 3 ×100%
反应消耗CO 的物质的量
2
在上述条件下,结合图像分析,合成甲醇的最佳温度是______,最佳催化剂是______。
①温度高于230℃,CH OH产率随温度升高而下降的原因是________________________。
3
②
2024~2025 学年第一学期高二年级七校期中联考试题・化学
参考答案、提示及评分细则
1.A BaSO 属于强电解质,A项正确;CO 不是电解质,B项错误;C H OH属于非电解质,C项错误;
4 2 2 5
CH COOH属于弱电解质,D项错误。
3
2.D 大多数焓减反应能自发进行,A 项错误;大多数熵增反应能自发进行,B 项错误;CO分解是吸热反
应、熵减反应,在任何温度下均不能自发进行,C项错误;五氧化二氮分解是吸热反应,正反应是熵增反应,
根据自由能判据,在较高温度下能自发进行,D项正确。
3.B 由图可知,Z、Y为反应物,X为生成物,其化学计量数之比为2:1:3,且该反应存在化学平衡,A
学科网(北京)股份有限公司2.0−1.6
项正确;3min时Z的转化率为 ×100%=20%,B项错误;起始既有反应物又有生成物,C项正
2.0
确;添加催化剂可增大反应速率,使其更快达到平衡,D项正确。
4.B X ( g )→Y ( g )的焓变为E −E +E −E +∆H ,A项错误;图中所示反应历程中:E > E ,∆H >0,
1 2 3 4 1 2
E > E ,故各步反应均为吸热过程,B项正确;该反应E (生成物)> E (反应物),故为吸热反应,C项
3 4
错误;无论是放热还是吸热反应,都不一定需要加热,D项错误。
5.C 温度降低,平衡正向移动可以提高产率但速率会减慢,因此需要综合考虑速率和平衡,同时温度会影
响催化剂的活性,实际生产中,选择温度为400∼500℃,该温度下催化剂的活性最大,A项正确;常压下
SO 的转化率已经很高,增大压强时,转化率提升不明显,但对材料的强度和设备制造的要求均提高很多,
2
因此实际生产中采用的压强为常压,B 项正确;通入过量空气可以提高SO 的转化率,O 的转化率下降,
2 2
C项错误;回收利用尾气中的SO ,可以防止环境污染,同时提高其转化率,D项正确。
2
6.B 当反应前后气体计量数之和相等时,增大压强,反应混合物的浓度增大,正、逆反应速率均增大,但
平衡不移动,A、C、D三项均错误;平衡常数改变,化学平衡一定发生移动,B项正确。
7.C 提高活化分子百分率有两条途径:降低活化能(如加催化剂),提高反应物平均能量(如升高温度),
C项符合题意。
8.A 由题意知2NH ⋅H O ( aq )+H SO ( aq )=( NH ) SO ( aq )+2H O ( l ) ∆H =−24.2kJ⋅mol−1,
3 2 2 4 4 2 4 2
即:NH ⋅H O ( aq )+H+ = NH+( aq )+H O ( l ) ∆H =−12.1kJ⋅mol−1 ,强酸与强碱中和反应反应热
3 2 4 2
①
可 表 示 为 H+( aq )+OH−( aq )=H O ( l ) ∆H =−57.3kJ⋅mol−1 , - 可 得 :
2
② ① ②
NH ⋅H O ( aq )= NH+( aq )+OH−( aq ) ∆H =+45.2kJ⋅mol−1,A项正确。
3 2 4
9.D 分析此反应,产物中只有CO、CO 为气体,化学计量数固定,CO体积分数始终为50%,A项错误;
2
CaC O 是固体,其质量不影响反应速率,B项错误;温度不变,平衡常数不变,按比例充入CO、CO ,
2 4 2
相当于加压,达到新平衡时浓度与原来的相等,C项错误;可用单位时间内固体质量变化比较反应快慢,D
项正确。
10.D 反应平衡后,升温,k 、k 均增大,A项错误;反应平衡后,降温,k 、k 均减小,B项错误;
正 逆 正 逆
k
反应平衡后,充入一定量的O ,k 、k 不变,C项错误;反应平衡后,升温,平衡左移,K = 正 减小,
2 正 逆 原 k
逆
D项正确。
11.C 加水稀释草酸溶液,H+、HC O−、C O2−、H C O 浓度均减小,同时平衡向右移动,促进草酸电
2 4 2 4 2 2 4
学科网(北京)股份有限公司c ( H C O ) c ( H+)
离, 2 2 4 减小, 增大,c ( HC O−) ⋅c ( C O2−) 减小,所以,A、B、D 项均错误;
c ( HC O−) c ( H C O ) 2 4 2 4
2 4 2 2 4
c
( H+)
⋅c
(
C
O2−)
K = 2 4 只与温度有关,C项正确。
a2
c
(
HC
O−)
2 4
12.B 总反应历程有2个过渡态,故总反应分两步反应,A项正确;X的能量高于Z,总反应是放热反应,
B项错误;Y是第一步反应产物,是第二步反应的反应物,Y是中间产物,C项正确;X→Y的活化能小
于Y→Z的活化能,所以速率快,D项正确。
13.B 化学反应速率为一段时间内的平均速率,而不是瞬时速率,A项错误;反应达平衡时,正逆反应速率
之比等于系数之比,B项正确;温度升高,平衡逆向移动,但∆H 不变,C项错误;温度不变,平衡常数不
变,D项错误。
14.D 由图可知,随温度升高CH 的平衡转化率增大,正反应吸热,∆H >0,A项错误;反应的正反应为
4
气体分子数增大的反应,增大压强平衡向逆反应方向移动,CH 的转化率减小,由图知在相同温度下 p 时
4 1
CH 的平衡转化率大于 p 时CH 的平衡转化率,则 p < p ,B项错误;由图知,y点CH 的转化率小于
4 2 4 1 2 4
平衡时CH 的转化率,反应正向进行,v >v ,C项错误;y点的温度与x点的温度相同,y点平衡常数
4 正 逆
与x点相等,用三段式
CH ( g ) + CO ( g ) 2CO ( g ) + 2H ( g )
4 2 2
c (起始) / ( mol⋅L−1 ) 0.1 0.1 0 0
c (转化) / ( mol⋅L−1 ) 0.1×0.8=0.08 0.08 0.16 0.16
c (平衡) / ( mol⋅L−1 ) 0.02 0.02 0.16 0.16
c2( CO )⋅c2( H ) 0.162×0.162
K = 2 = =1.6384,D项正确。
c ( CH )⋅c ( CO ) 0.02×0.02
4 2
15.(1)−93kJ⋅mol−1(2分)
3
(2)P ( s )+ Cl ( g )=PCl ( g ) ∆H =−306kJ⋅mol−1(3分)
2 2 3
(3)70.5(3分)
(4)∆H +∆H (2分)
1 2
(5)同素异形体;不同(各2分)
16.(1)(具支)试管(1分)
(2)SO ;溶液变红色,不褪色(不褪色不写不扣分)(各2分)
2
(3)减慢(1分);其他条件不变,降低温度,活化分子百分数降低,反应速率减慢(2分)
(4)5(1分);其他条件相同,(硫酸)浓度减小,反应速率减慢(2分)
(5)>(1分)
学科网(北京)股份有限公司(6)升温对速率的影响大于减小浓度对速率的影响(2分)
17.(1)NH ⋅H O NH+ +OH−;2NH ⋅H O+SO =2NH+ +SO2− +H O
3 2 4 3 2 2 4 3 2
(2)HF>H CO >HClO
2 3
(3)0.1;4.0×10−8
(4)减小;增大(每空2分)
18.(1)−( 2a+b );低温
(2)CD
1
(3)50%; p2(0.25p2也可给分)
4 0 0
(4) 230℃;CZ ( Zr−1 ) T催化剂
①
反应Ⅰ为放热反应,温度升高,平衡逆向移动,使CO 转化为CH OH的平衡转化率下降(或温度升高,
2 3
催②化剂活性下降,然后速率减慢也可以给分)(每空2分)
学科网(北京)股份有限公司