文档内容
邵东三中2025年上学期高二年级期中考试化学试题卷
一、单选题(本题包括14小题,每小题3分,共42分,在每小题给出的四个选项中,只有一
项是符合题目要求的)
1.0.01molCrCl ⋅6H O在水溶液中用过量硝酸银溶液处理,生成 0.02molAgC1 沉淀。已
3 2
知该CrCl ⋅6H O中C13+形成六个配位键,则其结构是
3 2
A. [Cr(H O) ]Cl B. [Cr(H O) Cl]Cl ⋅H O
2 6 3 2 5 2 2
C. [Cr(H O) Cl]Cl ⋅2H O D. [Cr(H O) Cl ]⋅3H O
2 4 2 2 2 3 3 2
2.用N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.25∘C,1.01×105Pa时,11.2LO2所含的原子数目为NA
B.78gNa O 晶体所含阴阳离子的总数为3NA
2 2
C.0.5mol·L-1的FeCl3溶液中,含有Cl个数为1.5NA
D.9g水(D O)含有的中子数为5NA
2
3.下列关于有机物同分异构体数目的分析不正确的是
A.C6H14含四个甲基的同分异构体有2种
B.(CH3CH2)2CHCH3的一氯代物有4种
C.分子式为C4H10的有机物的二氯取代物有12种
D.“立方烷”C8H8,如图所示 ,呈正六面体结构,其六氯代物有3种
4.已知有如图晶体结构:
冰 金刚石 石墨 氯化钠
下列有关晶体的叙述中,错误的是
A.在冰中,一个水分子周围有4个紧邻的水分子
B.金刚石晶体中碳原子所连接的最小环为六元环
C.石墨晶体的二维结构,碳原子的配位数是3,采取sp2杂化
D.在NaCl晶体里,每个Na+周围有6个距离最近且相等的Na+
5.根据下表中有关短周期元素性质的数据,下列说法正确的是① ② ③ ④ ⑤ ⑥ ⑦ ⑧
原子半径(10-10m) 0.74 1.60 1.52 1.10 0.99 1.86 0.75 0.82
最高价 - +2 +1 +5 +7 +1 +5 +3
主要化合价
最低价 -2 - - -3 -1 - -3 -
A.⑤号元素最高价氧化物对应水化物的酸性最强
B.③号元素简单离子半径大于①号元素简单离子半径
C.④的简单氢化物沸点大于⑦的简单氢化物
D.⑦和⑧号元素形成的类似金刚石结构的化合物中两种原子杂化类型不同
6.在碱性溶液中,双缩脲(NH,CONHCONH)2)能与Cu2+作用形成紫红色配合物,配离子
结构如图所示。下列说法错误的是
A.双缩脲分子中σ键与π键个数比为11:2
B.该配离子与水形成氢键的原子只有N
C.该配离子中提供空轨道的微粒是Cu2+
D.基态Cu原子电子占据最高能级的电子云轮廓图为球形
7.某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相
对密度为13,在标准状况下,将22.4L混合气体通入足量溴水,溴水质量增重 14g。下列说
法错误的是
A.混合气体中一定含有甲烷 B.22.4L混合气体中含有烷烃的物质的量为0.75mol
C.此烯烃有两种同分异构体 D.混合气体中烷烃与烯烃的物质的量之比为3:1
8.下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确
的是
A.ZY、ZW的水溶液都显酸性
B.原子半径大小:W>R>X,离子半径大小:Z+>R2->W->Y-
C.W的氢化物水溶液的酸性比R的氢化物水溶液的酸性强,可证明非金属性:W>R
D.Z、X两种元素可形成的Z2X、Z2X2、ZX2等多种离子化合物
9.砷化镓(GaAs)的晶胞结构如图甲所示。将 Mn掺杂到晶体中得到稀磁性半导体材料,其晶
胞结构如图乙所示。下列说法错误的是甲 乙
A.稀磁性半导体材料中,Mn、As的原子个数比为1:2
B.图甲中,As原子位于Ga原子构成的正四面体空隙中
4❑√3
C.图甲中,若Ga-As的键长为apm,则晶胞边长为 cpm
3
D.As属于P区元素
10.我国疾控中心利用尿素(酸H N-N H )制备出了两种低温消毒剂:三聚氰
2 2
)和二氯异氰尿酸钠( )。已知:尿素分子中所有原子共平面。下
列说法错误的是
A.二氯异氰尿酸钠中元素的电负性:N>O>Na
B.二氯异氰尿酸钠中存在的化学键只有极性键、离子键
C.基态氮原子的电子的空间运动状态有5种
D.尿素分子中键角NCO与键角/HNC基本相等
11.利用反应2N H +NaClO=N H +NaCl+H O可制备N2H4。下列叙述正确的是
3 2 4 2
A.NaClO和NaCl均为离子化合物,他们所含的化学键类型相同
B.NH3分子有孤电子对,可做配体
C.一个N2H4分子中有4个σ键
D.NaCl晶体可以导电
12.20世纪20年代中期建立的量子力学理论不仅能够较圆满的解释原子光谱的实验事实,而且为
解释和预测物质结构和性质提供了全新的理论支持,已经成为现代化学理论的基础。依据该理论,
下列各项叙述中正确的是
A.所有原子任一能层的s电子云轮廓图都是球形,电子绕核运动,其轨道为球面
B.钠的焰色试验呈现黄色,是电子由激发态转化成基态时吸收能量产生的
C.4s轨道电子能量较高,总是在比3s轨道电子离核更远的地方运动
D.s轨道电子能量可能高于p轨道电子能量
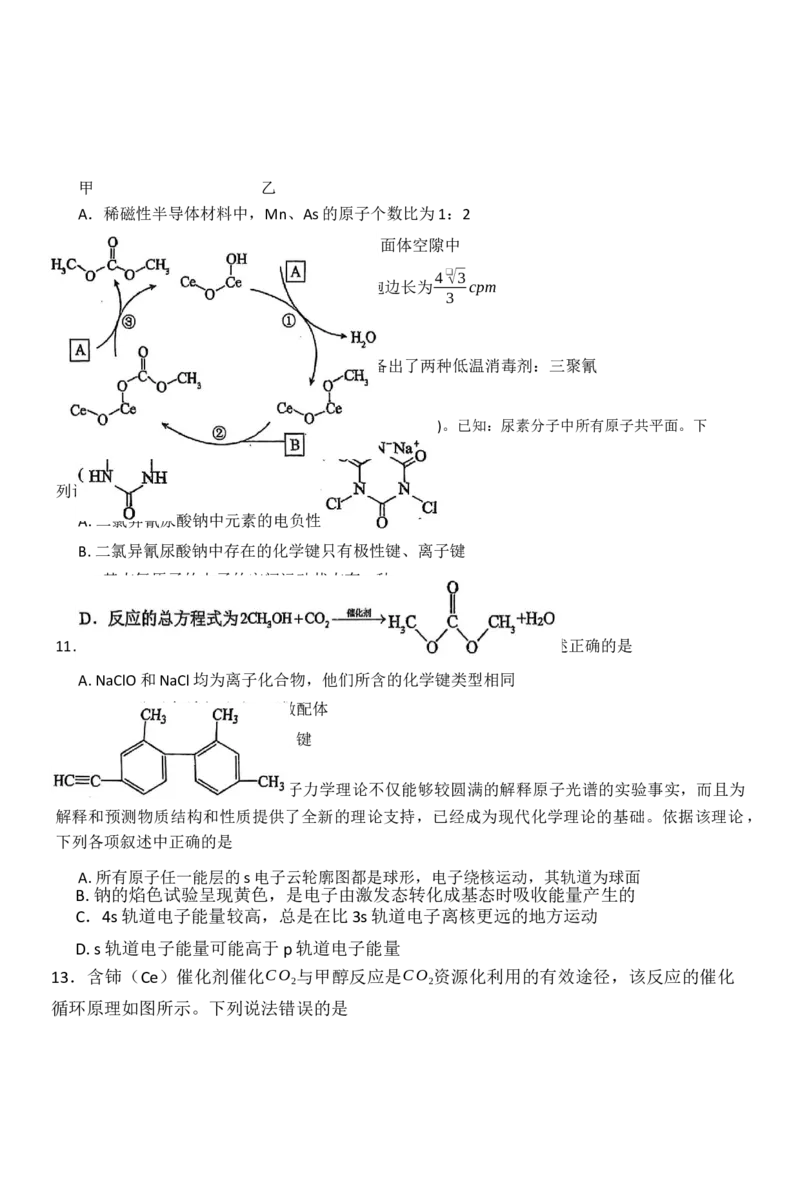
13.含铈(Ce)催化剂催化CO 与甲醇反应是CO 资源化利用的有效途径,该反应的催化
2 2
循环原理如图所示。下列说法错误的是A.物质A为CH3OH
B.反应过程涉及的物质中碳原子的杂化方式有3种
C.反应过程中断裂的化学键既有极性键又有非极性键
14.已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的烃,下列说法中正确的是( )
A.分子中至少有12个碳原子处于同一平面上 B.该烃苯环上的二氯代物共有13种
C.该烃的一氯代物共有8种 D.分子中处于同一直线上的碳原子最多有6个
二、非选择题(本题共4小题,每空2分,共58分)
15.完成下列问题。
(1)下列物质在固态时,属于分子晶体的有 - (填序号,下同),属于共价
晶体的有 ,属于离子晶体的有 。
①金刚石 ②氩 ③水晶 ④水银 ⑤氧化铝 ⑥P4⑦苯
(2)某常见固体能导电,质软,它可能属于 (填字母)。
A.分子晶体 B.共价晶体 C.离子晶体 D.金属晶体 E.混合型晶体
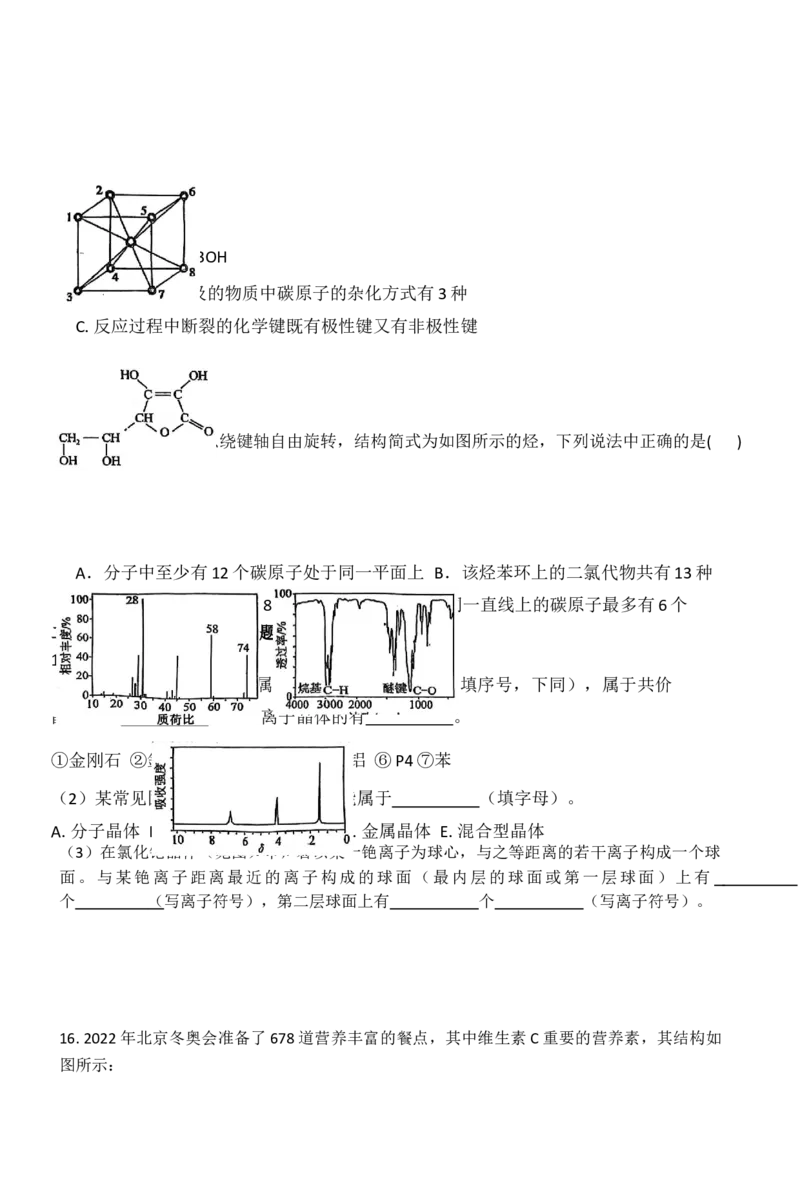
(3)在氯化铯晶体(见图)中,若以某一铯离子为球心,与之等距离的若干离子构成一个球
面。与某铯离子距离最近的离子构成的球面(最内层的球面或第一层球面)上有
个 ( 写离子符号),第二层球面上有 个 (写离子符号)。
16.2022年北京冬奥会准备了678道营养丰富的餐点,其中维生素C重要的营养素,其结构如
图所示:(1)维生素C的分子式是 。
(2)维生素C易溶于水,可能的原因是 。
(3)提取维生素C常用萃取的方法,有机物A是常用的有机萃取剂,也可以在手术时作麻醉
剂,使用现代分析仪器对其分子结构进行测定,相关结果如图:
波数/cm-
图1质谱 图2红外光谱
图3核磁共振氢谱
①利用有机物A萃取时用到的主要玻璃仪器是 。
②有机物A的相对分子质量是 。
③图3中两个峰的面积之比为2:3,有机物A的结构简式是 。
④有机物B是A的同分异构体,分子中含有一个羟基,核磁共振氢谱中含有两组峰,峰面积之
比为1:9,写出有机物B的结构简式 。
.(4)分子式为C H 的有机物中,含有乙基支链的一种同分异构体有: (写出结构简
8 18
式)
17.元素X、Y、Z、M、N均为原子序数依次增大的短周期主族元素;R在地壳金属元素中
的含量仅次于Z。已知Y原子最外层电子数与核外电子总数之比为 3:4,M原子的最外层电
子数与次外层电子数之比为3:4;N、Z3+、X+离子半径逐渐减小;化合物XN常温下为气
体,请回答下列问题:
(1)R在元素周期表中的位置是 ;Z3+的离子结构示意图是 。
(2)写出X、Y、N按原子个数之比1:1:1形成的化合物的电子式 ;M和N
气态氢化物的稳定性大小比较为 (用化学式和“>”“<”或“=”表示)。
(3)Z元素的单质能与Y和R形成的红棕色化合物在一定条件下发生反应,同时放出大量
的热,其反应的化学方程式为 。
(4)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分
反应前后的转化关系,在该转化关系中还原剂是 (填化学式),示意图中转移电
子的数目为 。18.A、B、C、D、E五种元素的原子序数依次增大。A是原子半径最小的元素;B的最外层电
子数是次外层电子数的2倍;D的L能层有两对成对电子;E+的核外有三个能层,且都外于
全满状态。试回答下列问题:
(1)基态E原子核外电子的排布式为 。
(2)B、C、D三种元素的电负性由大到小的顺序是 (填元素符号)。A、C、D
三种元素形成的常见离子化合物中阳离子的空间构型为 ,阴离子的中心原子
轨道采用 杂化。
(3)E(C A ) 2+离子的颜色是 . ;含有化学键类型是 。
3 4
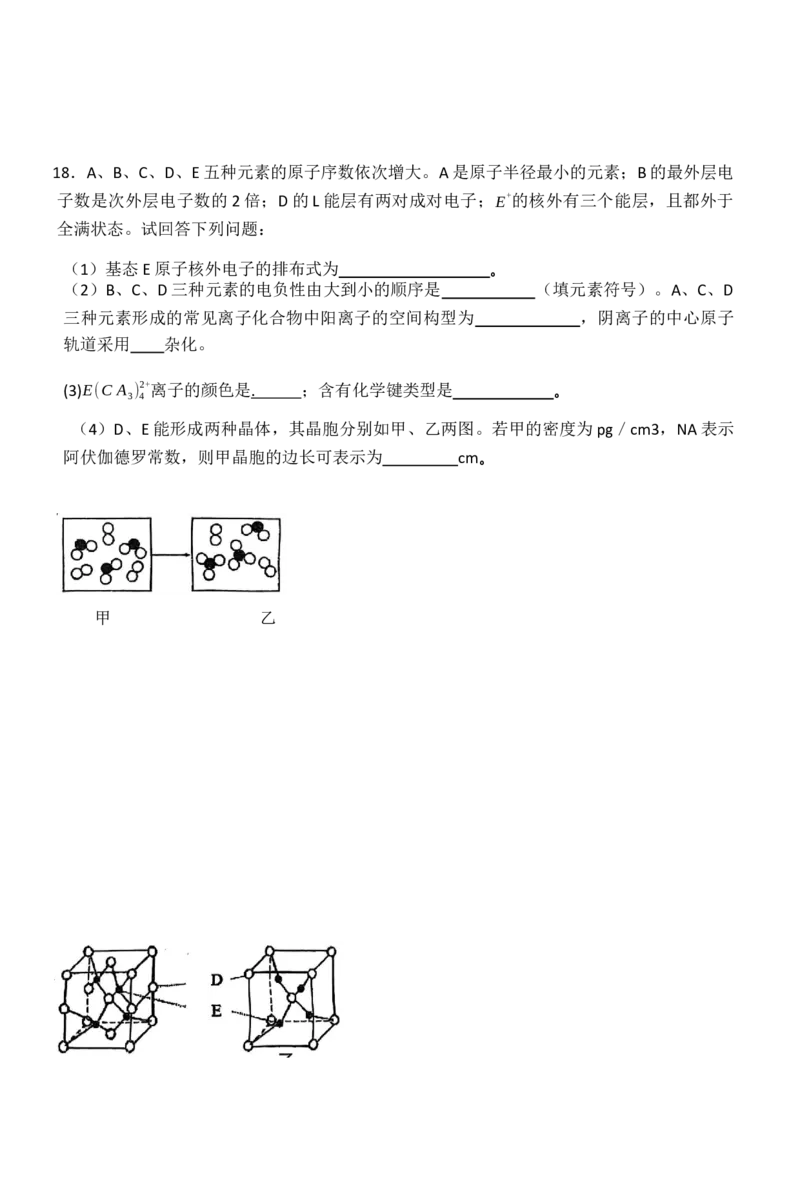
(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。若甲的密度为pg/cm3,NA表示
阿伏伽德罗常数,则甲晶胞的边长可表示为 cm。
甲 乙