文档内容
高二年级第一次月考化学试卷
一、单选题(每小题只有一个正确答案,每小题3分,共42分)
1.下列关于热化学反应的描述正确的是
A.若2H (g)+O (g)=2H O(g) ΔH ;2H (g)+O (g)=2H O(l) ΔH ,则ΔH <ΔH
2 2 2 1 2 2 2 2 1 2
B.若C(金刚石,s)=C(石墨,s) ΔH=-1.9 kJ·mol—1,则金刚石能量更高更稳定
C.若H+(aq)+OH-(aq)=H O(l) ΔH=-57.3 kJ·mol—1 ,则NaOH固体和HCl反应的反应热 ΔH=-
2
57.3 kJ·mol—1
D.若C H (g)的燃烧热ΔH=-1299.6 kJ·mol-1,则乙炔燃烧的热化学方程式为:
2 2
2C H (g)+5O (g)=4CO (g)+2H O(l) ΔH=-2599.2 kJ·mol-1
2 2 2 2 2
2.自然界中臭氧形成反应3O (g)=2O (g)的能量变化如图所示。下列说法中错误的是
2 3
A.2O =3O 为放热反应
3 2
B.氧气比臭氧稳定
C.反应物的能量低于生成物
D.反应热为E -E
3 1
3.下列有关能源与能量的说法正确的是
A.风能、太阳能、潮汐能等清洁能源的使用,有利于“碳达峰”的实现
B.化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种
C.已知
答案第1页,共2页
C ( 石 墨 , s ) C ( 金 刚 石 , s ) H 0 ,则金刚石比石墨稳定
D.所有反应的反应热都可以通过量热计直接测量
4.下列燃烧反应的反应热是燃烧热的是
A.H (g)+
2
1
2
O (g)=H O(g) △H B.C(s)+
2 2 1
1
2
O (g)=CO(g) △H
2 2
C.S(s)+O (g)=SO (g) △H D.H S(g)+
2 2 3 2
1
2
C.工业合成氨时,使用过量的
O (g)=S(s)+H O(l) △H
2 2 4
5.下列有关说法不正确的是
...
A.太阳能以光和热的形式传送到地面,人们可以直接利用这些光和热
B.反应热就是化学反应中放出的能量
C.煤中含有硫元素,大量直接燃烧煤会引起酸雨等环境问题
D.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
6.已知H—H键的键能是436.4 kJ.mol-1, Cl—Cl 键的键能是242.7 kJ.mol-1,H—Cl键的键能是
431.8 kJ.mol-1 。则H (g)+ Cl (g)=2H Cl(g)的反应热是:
2 2
A.-184.5kJ/mol B.+184.5kJ/mol C.+247.3 kJ/mol D.-247.3 kJ/mol
7.下列说法正确的是
A.热化学方程式的计量数只表示分子的个数 B.热化学方程式中只需标明生成物的状态
C.反应热指的是反应过程中放出或吸收的热量 D.有能量变化的一定是化学变化
8.化学反应速率和限度的研究对日常生活和工业生产有着重要意义。下列有关说法错误的是
A.向炉膛内鼓风、用煤粉代替煤块都可以使炉火更旺
B.将肉类食品进行低温冷藏,能使其永远不会腐败变质
N
2
,也不可能使 H
2
的转化率达到100%
D.我国西周时期已经发明了用酒曲酿酒,其原理是催化剂能改变反应速率
9.下列措施是为了增大化学反应速率的是
A.将食物放进冰箱避免变质 B.用锌粒代替镁条制备氢气
C.自行车车架镀漆避免生锈 D.工业合成氨时加入铁触媒作催化剂
10.站在对人类有益的角度,下列化学反应速率希望减慢的是
A.植物的光合作用 B.金属的腐蚀
C.氨的合成 D.汽车尾气中NO和CO转化为 N
2
和 C O
2
11.某温度下,在容积一定的密闭容器中进行如下反应2X(g)+Y(s) ⇌ Z(g) ΔH>0。下列叙述正
确的是( )
A.向容器中充入氩气,压强增大,反应速率不变 B.加入少量Y,反应速率增大
C.升高温度,正反应速率增大,逆反应速率减小 D.将容器的容积扩大,化学反应速率增
大
12. H
2
和 C O
2
反应生成 H
2
O 和 C H
4
的化学方程式为4H +CO ⇌2H O+CH 下列关于该反应的说法
2 2 2 4
不正确的是
...
A.合适的催化剂能加快反应速率 B.达到化学平衡时,H 能全部转化为H O
2 2
C.缩小体积增大压强能加快化学反应速率 D.适当升高温度会加快化学反应速率
13.一定条件下,向密闭容器中充入1molNO和1molCO进行反应:
2NO(g)+2CO(g) ⇌N (g)+2CO (g),测得化学反应速率随时间的变化关系如图所示,其中处于
2 2
化学平衡状态的点是
A.d点
B.b点
C.c点
D.a点
14.可逆反应4CO+2NO ⇌ 4CO +N 达到化学平衡时,下列说法正确的是
2 2 2
A.反应混合气体的颜色不再变化 B.CO、CO 两种物质浓度一定相等
2
C.CO和NO 全部变成CO 和N D.升高温度,正反应速率增大,逆反应速率则减小
2 2 2
二、填空题(每空2分,共58分)
15.反应A(g)+B(g) ⇌ C(g)+D(g)过程中的能量变化如图所示,回答下列问题。(共10分)
(1)正反应是 反应(填“吸热”、“放热”)。
(2)当反应达到平衡时,升高温度,A的转化率 (填“增大”、
“减小”或“不变”),原因是 。
(3)反应体系中加入催化剂对反应热是否有影响? (填“有影响”
或“无影响”)。
(4)在反应体系中加入催化剂,E 的变化是:E (填“增大”、
1 1
“减小”或“不变”)。
1
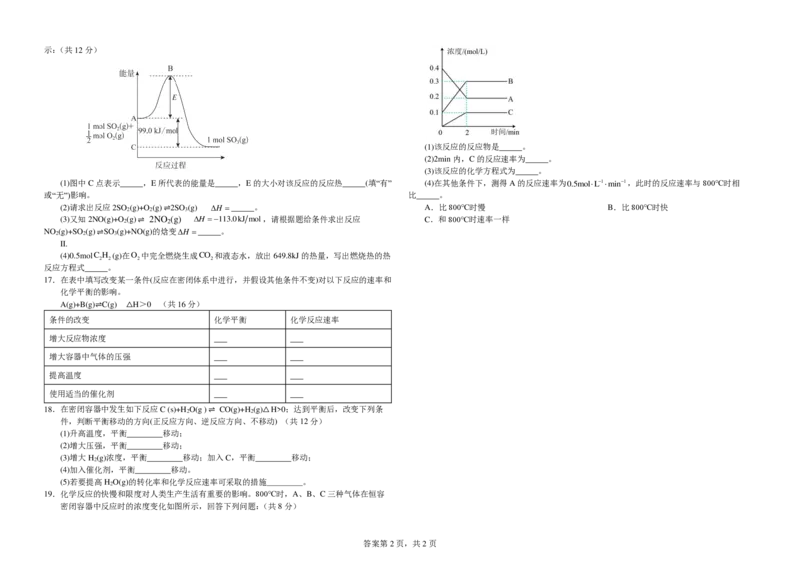
16.I. 已知SO (g)+ O (g) ⇌SO (g)反应过程的能量变化如图所
2 2 3
2
{#{QQABCYYlwgiQwMSACJ6KVQWkCggQkIChJSoMhRASKARKyQFIFAA=}#}示:(共12分)
(1)图中C点表示 ,E所代表的能量是 ,E的大小对该反应的反应热 (填“有”
或“无”)影响。
(2)请求出反应2SO (g)+O (g) ⇌2SO (g)
2 2 3
答案第2页,共2页
H 。
(3)又知2NO(g)+O (g) ⇌ 2NO (g)
2 2
H 1 1 3 .0 k J m o l ,请根据题给条件求出反应
NO (g)+SO (g) ⇌SO (g)+NO(g)的焓变H 。
2 2 3
II.
(4)0.5mol C
2
H
2
(g)在 O
2
中完全燃烧生成 C O
2
(1)该反应的反应物是 。
(2)2min内,C的反应速率为 。
(3)该反应的化学方程式为 。
(4)在其他条件下,测得A的反应速率为0.5molL1min1,此时的反应速率与800℃时相
比 。
A.比800℃时慢 B.比800℃时快
C.和800℃时速率一样
和液态水,放出649.8kJ的热量,写出燃烧热的热
反应方程式 。
17.在表中填写改变某一条件(反应在密闭体系中进行,并假设其他条件不变)对以下反应的速率和
化学平衡的影响。
A(g)+B(g)⇌C(g) △H>0 (共16分)
条件的改变 化学平衡 化学反应速率
增大反应物浓度
增大容器中气体的压强
提高温度
使用适当的催化剂
18.在密闭容器中发生如下反应C (s)+H O(g ) ⇌ CO(g)+H (g)△H>0;达到平衡后,改变下列条
2 2
件,判断平衡移动的方向(正反应方向、逆反应方向、不移动) (共12分)
(1)升高温度,平衡 移动;
(2)增大压强,平衡 移动;
(3)增大H (g)浓度,平衡 移动;加入C,平衡 移动;
2
(4)加入催化剂,平衡 移动。
(5)若要提高H O(g)的转化率和化学反应速率可采取的措施 。
2
19.化学反应的快慢和限度对人类生产生活有重要的影响。800℃时,A、B、C三种气体在恒容
密闭容器中反应时的浓度变化如图所示,回答下列问题:(共8分)
{#{QQABCYYlwgiQwMSACJ6KVQWkCggQkIChJSoMhRASKARKyQFIFAA=}#}