文档内容
第 2 章 第 3 节 课时 1 化学反应的快慢
一、化学反应速率
1.化学反应速率的概念及表示方法
(1)定义:描述化学反应快慢的物理量。
(2)表示方法:用单位时间某反应物浓度的减少量(绝对值)或某生成物浓度的增加量来表示。
(3)举例:对于在体积固定的容器中进行的化学反应 aA+bB===cC+dD,以反应物B来表
示,反应的化学反应速率为v(B)=。
(4)单位: mol·L -1 ·s -1 或mol·L-1·min-1。
2.理解化学反应速率的注意事项
(1)一个确定的化学反应涉及反应物、生成物等多种物质,因而定量表示一个化学反应的反
应速率时,必须指明是哪一种反应物或生成物表示的反应速率。
(2)同一反应,用不同物质表示的反应速率其数值可能不同,但表示的意义相同,即表示整
个化学反应的快慢。
(3)化学反应速率是不断变化的,有瞬时速率和平均速率之分,在中学阶段化学反应速率的
计算只涉及一段时间内的平均反应速率,而不是某一时刻的瞬时反应速率。
(4)各物质的化学反应速率之比等于化学方程式中各物质的化学计量数之比。如反应 aA(g)
+bB(g)===cC(g)+dD(g)中,v(A)∶v(B)∶v(C)∶v(D)=a∶b∶c∶d。
(5)固体或纯液体的浓度可视为常数,因此一般不用固体或纯液体表示化学反应速率。
3.化学反应速率大小的比较方法
(1)归一法:若单位不统一,则要换算成相同的单位;若为不同物质表示的化学反应速率,
则要换算成同一物质来表示化学反应速率;再比较数值的大小。
(2)比值法:比较化学反应速率与化学计量数的比值,如aA(g)+bB(g)===cC(g)+dD(g),比
较与,若>,则说明用A表示的化学反应速率大于用B表示的化学反应速率。
二、影响化学反应速率的因素
1.方法引导——变量控制方法
探究化学反应速率的影响因素,关键是变量控制,其大致步骤:
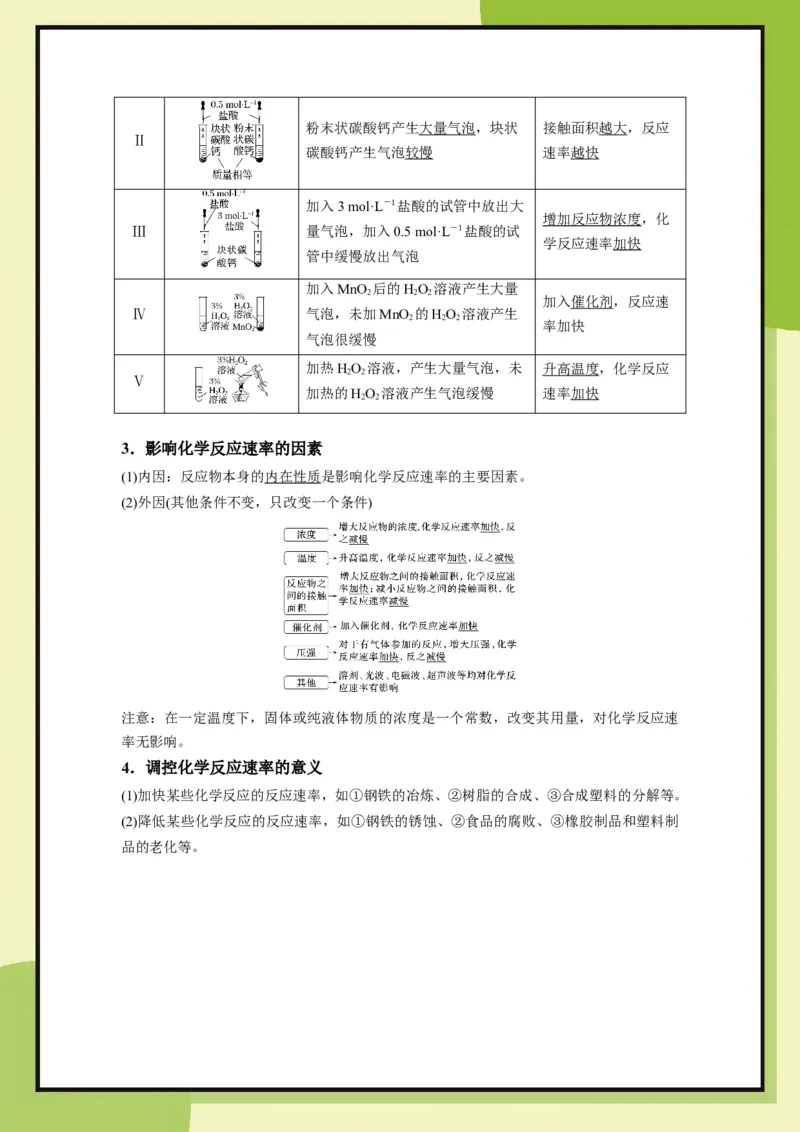
2.探究化学反应速率的影响因素
编号 实验内容 实验现象 实验结论
镁条产生大量气泡,铁片产生气泡 物质本身的内在性质
Ⅰ
较缓慢 决定化学反应速率粉末状碳酸钙产生大量气泡,块状 接触面积越大,反应
Ⅱ
碳酸钙产生气泡较慢 速率越快
加入3 mol·L-1盐酸的试管中放出大
增加反应物浓度,化
Ⅲ 量气泡,加入0.5 mol·L-1盐酸的试
学反应速率加快
管中缓慢放出气泡
加入MnO 后的HO 溶液产生大量
2 2 2
加入催化剂,反应速
Ⅳ 气泡,未加MnO 的HO 溶液产生
2 2 2
率加快
气泡很缓慢
加热HO 溶液,产生大量气泡,未 升高温度,化学反应
2 2
Ⅴ
加热的HO 溶液产生气泡缓慢 速率加快
2 2
3.影响化学反应速率的因素
(1)内因:反应物本身的内在性质是影响化学反应速率的主要因素。
(2)外因(其他条件不变,只改变一个条件)
注意:在一定温度下,固体或纯液体物质的浓度是一个常数,改变其用量,对化学反应速
率无影响。
4.调控化学反应速率的意义
(1)加快某些化学反应的反应速率,如①钢铁的冶炼、②树脂的合成、③合成塑料的分解等。
(2)降低某些化学反应的反应速率,如①钢铁的锈蚀、②食品的腐败、③橡胶制品和塑料制
品的老化等。