文档内容
2019年山东省泰安市初中学业水平考试化学试题
本卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分50分,考试时间60分钟。
相对原子质量:H—1 C—12 O—16 Na—23 Cl—35.5 Ca—40
第Ⅰ卷(选择题 共20分)
一、选择题(本题包括20小题,每小题1分,共20分。每小题只有一个选项符合题意。)
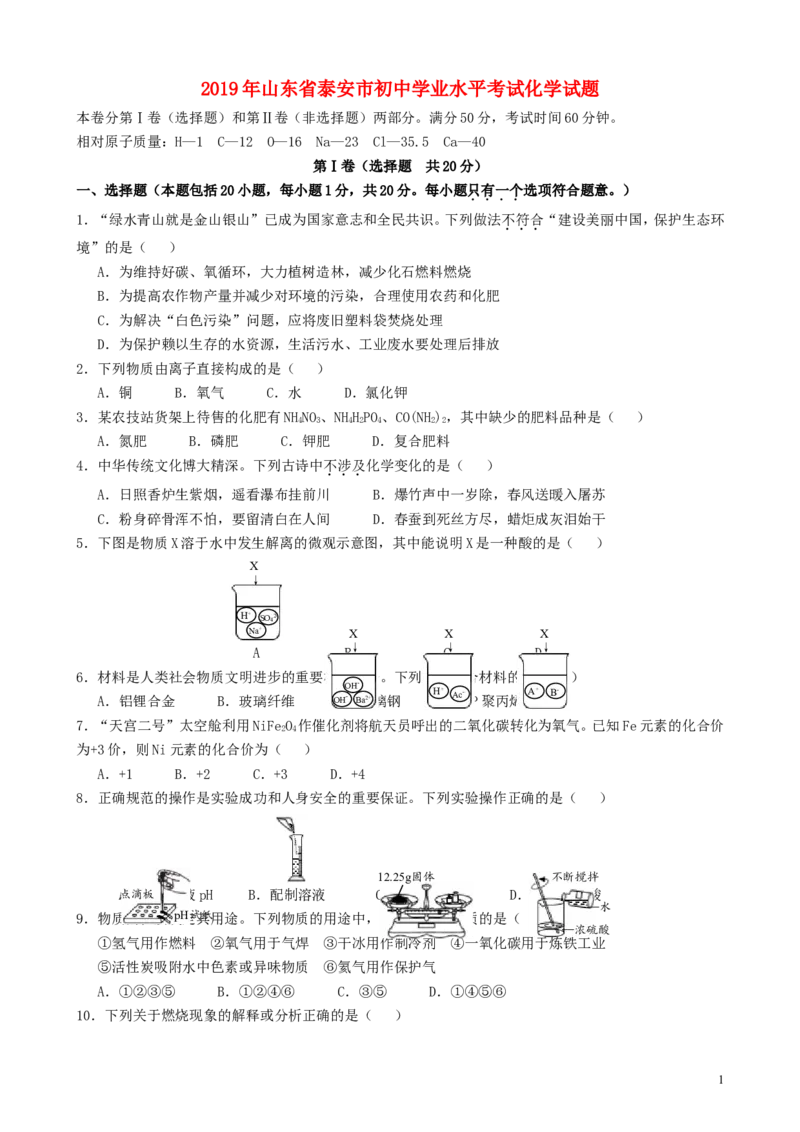
1.“绿水青山就是金山银山”已成为国家意志和全民共识。下列做法不符合“建设美丽中国,保护生态环
境”的是( )
A.为维持好碳、氧循环,大力植树造林,减少化石燃料燃烧
B.为提高农作物产量并减少对环境的污染,合理使用农药和化肥
C.为解决“白色污染”问题,应将废旧塑料袋焚烧处理
D.为保护赖以生存的水资源,生活污水、工业废水要处理后排放
2.下列物质由离子直接构成的是( )
A.铜 B.氧气 C.水 D.氯化钾
3.某农技站货架上待售的化肥有NHNO、NHHPO、CO(NH),其中缺少的肥料品种是( )
4 3 4 2 4 2 2
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
4.中华传统文化博大精深。下列古诗中不涉及化学变化的是( )
A.日照香炉生紫烟,遥看瀑布挂前川 B.爆竹声中一岁除,春风送暖入屠苏
C.粉身碎骨浑不怕,要留清白在人间 D.春蚕到死丝方尽,蜡炬成灰泪始干
5.下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
X
↓
H+ SO4 2-
Na+ X X X
A B↓ C↓ D↓
6.材料是人类社会物质文明进步的重要标志之一。下列属于复合材料的是( )
OH-
A.铝锂合金 B.玻璃纤维 OCH.- B玻a2+璃钢
H + D.Ac-
PP聚丙烯塑
A+
料
B-
7.“天宫二号”太空舱利用NiFeO 作催化剂将航天员呼出的二氧化碳转化为氧气。已知Fe元素的化合价
2 4
为+3价,则Ni元素的化合价为( )
A.+1 B.+2 C.+3 D.+4
8.正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是( )
12.25g固体 不断搅拌
点A.滴测板定溶液pH B.配制溶液 C.称量固体 D.稀释浓硫酸
—水
9.物质的性质决pH定试其纸用途。下列物质的用途中,利用其化学性质的是( )
—浓硫酸
①氢气用作燃料 ②氧气用于气焊 ③干冰用作制冷剂 ④一氧化碳用于炼铁工业
⑤活性炭吸附水中色素或异味物质 ⑥氦气用作保护气
A.①②③⑤ B.①②④⑥ C.③⑤ D.①④⑤⑥
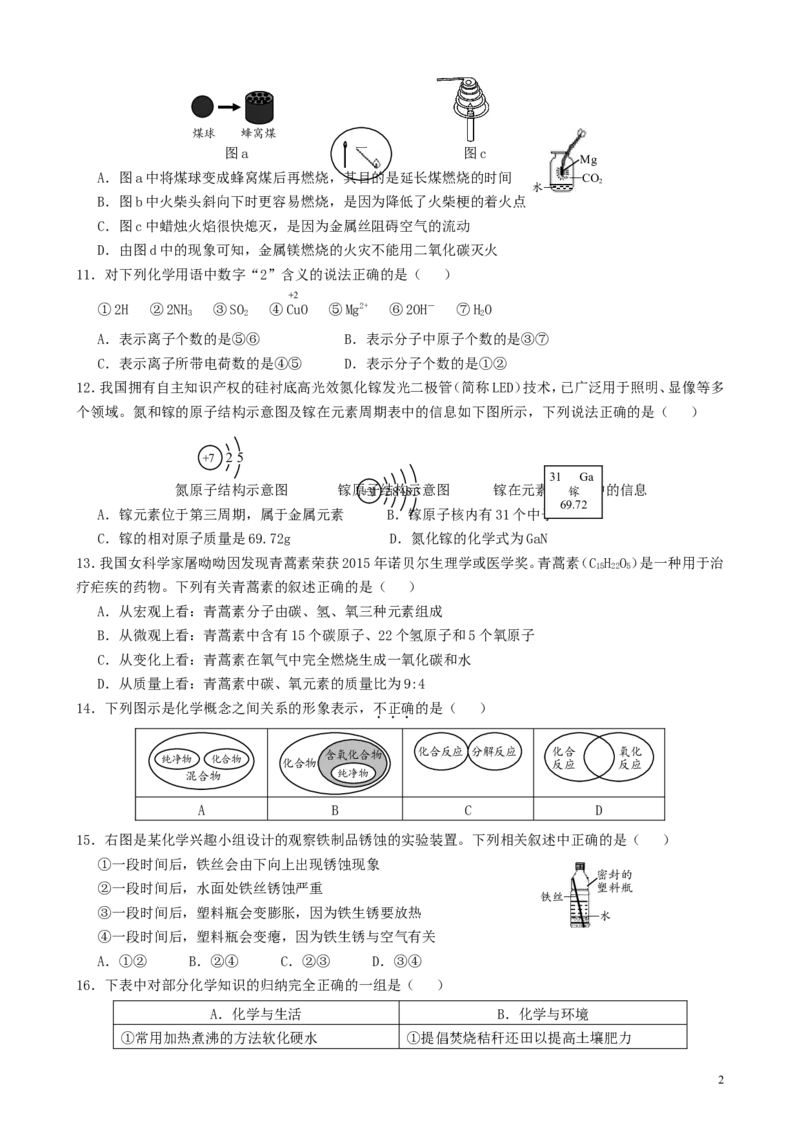
10.下列关于燃烧现象的解释或分析正确的是( )
1煤球 蜂窝煤
图a 图b 图c 图d
Mg
A.图a中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间 —CO
水— 2
B.图b中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
C.图c中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
D.由图d中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火
11.对下列化学用语中数字“2”含义的说法正确的是( )
+2
①2H ②2NH ③SO ④CuO ⑤Mg2+ ⑥2OH- ⑦HO
3 2 2
A.表示离子个数的是⑤⑥ B.表示分子中原子个数的是③⑦
C.表示离子所带电荷数的是④⑤ D.表示分子个数的是①②
12.我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显像等多
个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如下图所示,下列说法正确的是( )
+7 25
31 Ga
氮原子结构示意图 镓原+子31结2 8构 18示 3意图 镓在元素周期镓表中的信息
69.72
A.镓元素位于第三周期,属于金属元素 B.镓原子核内有31个中子
C.镓的相对原子质量是69.72g D.氮化镓的化学式为GaN
13.我国女科学家屠呦呦因发现青蒿素荣获2015年诺贝尔生理学或医学奖。青蒿素(C H O)是一种用于治
15 22 5
疗疟疾的药物。下列有关青蒿素的叙述正确的是( )
A.从宏观上看:青蒿素分子由碳、氢、氧三种元素组成
B.从微观上看:青蒿素中含有15个碳原子、22个氢原子和5个氧原子
C.从变化上看:青蒿素在氧气中完全燃烧生成一氧化碳和水
D.从质量上看:青蒿素中碳、氧元素的质量比为9:4
14.下列图示是化学概念之间关系的形象表示,不正确的是( )
含氧化合物 化合反应 分解反应 化合 氧化
纯净物 化合物 化合物 反应 反应
混合物 纯净物
A B C D
15.右图是某化学兴趣小组设计的观察铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①一段时间后,铁丝会由下向上出现锈蚀现象
密封的
②一段时间后,水面处铁丝锈蚀严重 塑料瓶
铁丝—
③一段时间后,塑料瓶会变膨胀,因为铁生锈要放热
—水
④一段时间后,塑料瓶会变瘪,因为铁生锈与空气有关
A.①② B.②④ C.②③ D.③④
16.下表中对部分化学知识的归纳完全正确的一组是( )
A.化学与生活 B.化学与环境
①常用加热煮沸的方法软化硬水 ①提倡焚烧秸秆还田以提高土壤肥力
2②病人输入葡萄糖溶液能及时补充能量 ②PM2.5是造成雾霾天气的元凶之一
C.化学与安全 D.化学与健康
①皮肤沾上浓烧碱溶液,先用水冲洗,再涂碳 ①缺乏维生素C会引起夜盲症
酸氢钠溶液 ②制作糕点时加入适量的碳酸氢钠,可使糕
②档案材料失火,可用泡沫灭火器灭火 点松软可口
17.控制变量是实验探究的重要方法。下列实验设计不能达到实验目的的是( )
10% 10% CO ↓碘 ↓ 各滴一滴红墨
硫酸 盐酸 2 碘 水
铁片— —镁片 10mL
干燥的蓝 湿润的蓝 50mL 50mL
色石蕊试纸 色石蕊试 冷水 热水
纸 水 酒精
A.探究铁、镁金属活 B.探究二氧化碳与水 C.探究不同溶剂中 D.探究温度对分子
动性强弱 是否发生反应 物质溶解性大小 运动快慢的影响
18.右图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是( )
A.t℃时,a、c两种物质饱和溶液的溶质质量分数为20%
1 溶解度/g
a
50
B.将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法
b
C.将a、b、c三种物质的饱和溶液从t℃降温至t℃,所得溶液中溶质质量
2 1 P
20
分数的大小关系为b>a=c
c
D.将150g a物质的饱和溶液从t 3 ℃降温至t 1 ℃,可析出30g a物质 0 t t t 温
1 2 3
19.某化学兴趣小组对A、B、C、D四种未知溶液的成分进行了检验,检验结果见下
度/℃
表。其中检验结果不正确的是( )
组别 溶液中检验出的离子
A K+、Na+、OH-、SO2-
4
B Ba2+、Na+、Cl-、OH-
C Cu2+、Mg2+、NO-、Cl-
3
D H+、NH+、CO2-、SO2-
4 3 4
20.A~G都是初中化学常见的物质,A可用于金属表面除锈,F可用于改良酸性土壤,D、E组成元素相同,B、C
常温下为气体。图中“—”表示能相互反应,“→”表示转化关系(部分反应物、生成物及反应条件已略
去)。下列说法错误的是( )
A.E→F是一个放热反应 —→←—
B.D可用于实验室制取氧气
C.若G为一种盐,则A不可能与G发生反应
D.B→E和C→E的反应类型可能不相同
第Ⅱ卷(非选择题 共30分)
二、(本题包括3小题,共13分)
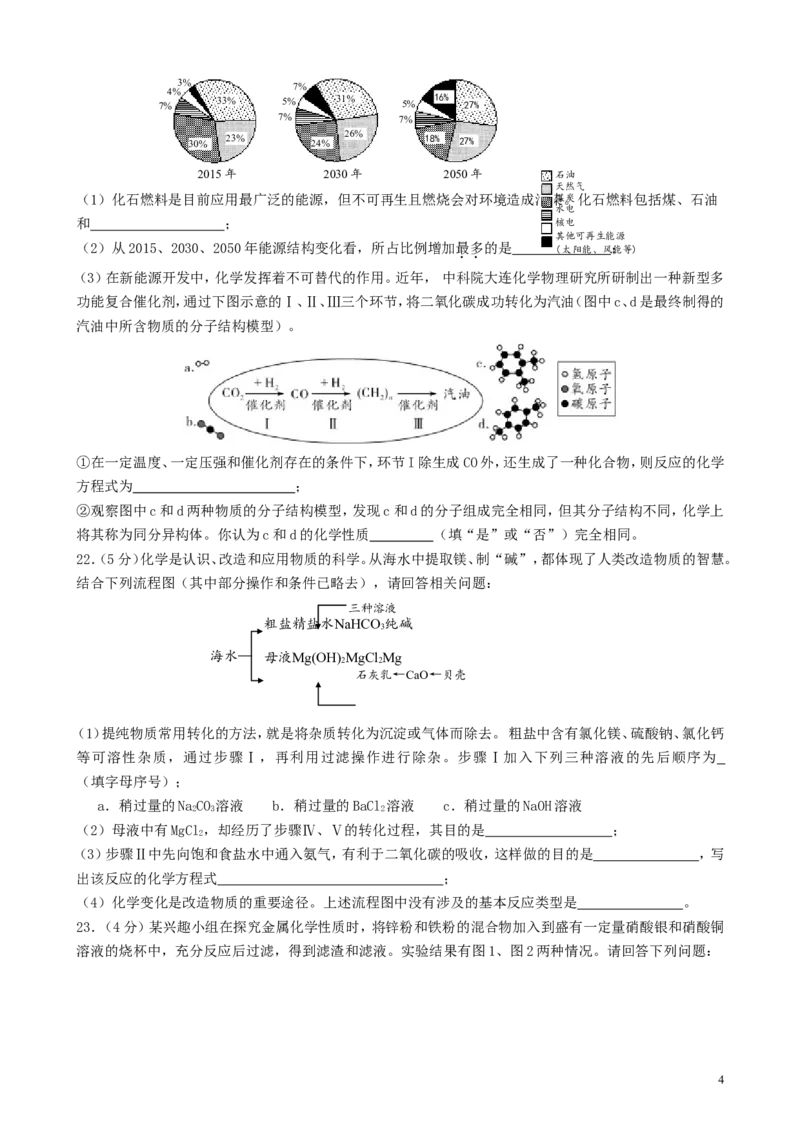
21.(4分)《2015年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。下列是我国
能源结构变化的调整图,请回答相关问题:
33% 7%
4%
7% 33% 5% 31% 5% 16% 27%
7% 7%
30% 23% 24% 26% 18% 27%
2015年 2030年 2050年 石油
天然气
(1)化石燃料是目前应用最广泛的能源,但不可再生且燃烧会对环境造成污染煤。炭化石燃料包括煤、石油
水电
和 ; 核电
其他可再生能源
(2)从2015、2030、2050年能源结构变化看,所占比例增加最多的是 ( 太 阳 能 、 风 ;能等)
(3)在新能源开发中,化学发挥着不可替代的作用。近年, 中科院大连化学物理研究所研制出一种新型多
功能复合催化剂,通过下图示意的Ⅰ、Ⅱ、Ⅲ三个环节,将二氧化碳成功转化为汽油(图中c、d是最终制得的
汽油中所含物质的分子结构模型)。
①在一定温度、一定压强和催化剂存在的条件下,环节I除生成CO外,还生成了一种化合物,则反应的化学
方程式为 ;
②观察图中c和d两种物质的分子结构模型,发现c和d的分子组成完全相同,但其分子结构不同,化学上
将其称为同分异构体。你认为c和d的化学性质 (填“是”或“否”)完全相同。
22.(5分)化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。
结合下列流程图(其中部分操作和条件已略去),请回答相关问题:
三种溶液
粗盐精盐水NaHCO 纯碱
3
海水— 母液Mg(OH) MgCl Mg
2 2
石灰乳←CaO←贝壳
(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。 粗盐中含有氯化镁、硫酸钠、氯化钙
等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为
(填字母序号);
a.稍过量的NaCO 溶液 b.稍过量的BaCl 溶液 c.稍过量的NaOH溶液
2 3 2
(2)母液中有MgCl,却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是 ;
2
(3)步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是 ,写
出该反应的化学方程式 ;
(4)化学变化是改造物质的重要途径。上述流程图中没有涉及的基本反应类型是 。
23.(4分)某兴趣小组在探究金属化学性质时,将锌粉和铁粉的混合物加入到盛有一定量硝酸银和硝酸铜
溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。实验结果有图1、图2两种情况。请回答下列问题:
4锌粉和铁粉
滤渣
滤液
AgNO和Cu(NO)
3 32
混合溶液
图1 图2
锌粉和铁粉
滤渣
(1)图1是向滤液中加入稀盐酸,观察到有白色沉淀产生。
①滤液中一定含有的金属离子为 (填离子符号);
滤液
AgNO和Cu(NO)
②写出一个产生滤渣的反应的化学方程式 3 3 2 。
混合溶液
(2)图2是向滤渣中加入稀盐酸,观察到有无色气体产生。
①滤渣中一定含有 (填化学式,下同);
②滤液中可能含有 。
三、(本题包括2小题,共12分)
24.下图是实验室,制取气体常用的装置。结合图示回答下列问题:
a
c e f g
b
A B C D E F 浓
Ⅰ 硫
(1)写出B图中仪器Ⅰ的名称 ; d 酸
(2)实验室用加热氯化铵和氢氧化钙固体混合物制取氨气,应选用的发生装置 (填装置字母序号);
(3)实验室利用大理石和稀盐酸反应制取二氧化碳,可选用B发生装置,装置中使用分液漏斗的优点是
;
(4)实验室用双氧水和二氧化锰制取一瓶干燥的氧气,仪器接口的连接顺序是 (填导管接
口的字母序号);
(5)实验室制取CO 一般有六个步骤:①检查装置的气密性;②按要求装配好仪器; ③向漏斗中注入酸液;
2
④向仪器Ⅰ中放入小块的大理石;⑤用燃着的木条靠近集气瓶口验满;⑥收集气体。则正确的操作顺序是
(填数字序号)。
25.(7分)在整理实验室时,同学发现7瓶不同的无色溶液(见下图所示),其中2、3、7号试剂瓶标签完全破
损,4、5号试剂瓶标签部分破损。查阅药品记录单可知,2、3、4、5、7号溶液分别是10% NaOH溶液、饱和石灰
水、10% NaCO 溶液、10% CaCl 溶液、10%稀盐酸中的一种。化学小组同学进行了以下实验探究。
2 3 2
酚酞
1 2 3 4 5 6 7
【实验目的】①给试剂瓶贴上正确的标签;②探究部Na分溶液混Na合发生的 N 溶 aH 反液 CO 应3 。
【查阅资料】①CaCl 溶液呈中性,能与NaCO 发生复分解反应;
2 2 3
②Ca(OH)+NaHCO===CaCO↓+NaOH+HO NaOH+NaHCO===NaCO+HO
2 3 3 2 3 2 3 2
【实验探究】
(1)分别取2、3、4、5、7号溶液于5支试管中,向其中分别滴加1号溶液, 发现3、4、5号溶液变红色,说明
这3种溶液呈 (填“酸性”、“碱性”或“中性”),由该实验可确定的溶液为 (写
出试剂瓶编号及相应的溶液名称);
5(2)分别取2号5.55g和7号3.65g溶液,混合均匀后,逐滴加入5号溶液。首先观察到有气泡冒出,然后有
沉淀析出。加入5号溶液的质量与产生气体或沉淀的质量关系如图1所示,加入5号溶液的质量与溶液pH
的变化关系如图2所示。根据图示完成下列问题:
2号 7号
2号 7号 5号
5.55g 2号溶液 3.65g 7号溶液
气体或沉淀质 pH
量/g c
①7号溶液是(填名称); 0.5 h
7
k
a
②图1中b点数据为 g; 0.22 g
③图2中h→k段发生反应的化学方程式为 0 b 。 10.6 0 5 号溶
5号溶液/g 液/g 图2
(3)取3号溶液于试管中,逐滴加入一定量的6号溶液,观察到溶液变浑浊,过滤, 则滤液中含有的溶质可
图1
能为①NaOH;②NaCO;③NaOH、NaCO;④NaOH、Ca(OH);⑤ 。
2 3 2 3 2
【实验反思】分析上述实验,下列说法不正确的是 (填字母序号)。
A.5号试剂可能是部分变质的氢氧化钠溶液
B.该实验无法确定各种试剂,没有完成实验目的①
C.图1中b→c段反应过程中溶液的pH变化情况可用图2中h→k段表示
D.碳酸氢钠既能与碱反应,又能与酸反应
四、(本题包括2小题,共5分)
26.(1分)纯净物A是打火机的常用燃料,其相对分子质量为58。在一定条件下,将一定质量的A与
10.4g B按下图所示充分反应,当B消耗完时,可生成8.8g C和4.5g D物质。A物质的化学式为 。
—氢原子
+
+ —氧原子
—碳原子
A B C D
27.(4分)长期使用的热水锅炉会产生水垢。水垢主要成分是碳酸钙和氢氧化镁。某兴趣小组为了测定水垢
中CaCO 的含量,将6g水垢粉碎放在烧杯中,然后向其中加入40g某浓度的稀盐酸,使之充分反应(水垢中
3
除碳酸钙和氢氧化镁外都不与稀盐酸反应)。实验数据记录如下:
反应时间/min 0 1 2 3 4 5 6 7 8
烧杯内所盛物
46.0 45.2 44.8 45.1 44.1 43.9 43.8 43.8 43.8
质的总质量/g
试计算:(1)表中有一数据是不合理的,该数据的测得时间是第 min;
(2)水垢中CaCO 的质量分数(计算结果精确至0.1%)。
3
62019年山东省泰安市初中学业水平考试化学试题(A)参考答案
说明:1.每小题若有其它正确答案,可参照评分标准给分。
2.化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分。
3.化学方程式未配平的,都不给分。
一、选择题(本题包括20小题,每小题1分,共20分)
1~5:CDCAC 6~10:CBABD 11~15:BDDAB 16~20:AADDC
二、(本题包括3小题,共13分)
21.(每空1分,共4分)(1)天然气 (2)其他可再生能源
(3)①H+CO==============CO+HO ②否
2 2 2
22.(每空1分,共5分)(1)cba(或bca或bac) (2)富集、提纯MgCl
2
(3)促进碳酸氢钠的生成与析出 NaCl+HO+CO+NH=== NHCl+NaHCO (4)置换反应
2 2 3 4 3
23.(每空1分,共4分)(1)①Ag+、Cu2+、Fe2+、Zn2+ ②Zn+2AgNO=== Zn(NO)+2Ag
3 3 2
或Fe+2AgNO=== Fe(NO)+2Ag (2)①Ag、Cu、Fe ②Fe(NO)
3 3 2 3 2
三、(本题包括2小题,共12分)
24.(每空1分,共5分)(1)锥形瓶 (2)A (3)可控制反应速率,节约药品
7(4)b→g→f→e (5)②①④③⑥⑤
25.(每空1分,共7分)【实验探究】(1)碱性 3号 饱和石灰水
(2)①稀盐酸 ②5.3 ③NaCO+CaCl=== CaCO↓+2NaCl (3)NaCO、NaHCO
2 3 2 3 2 3 3
【实验反思】AB
四、(本题包括2小题,共5分)
26.(1分)CH
4 10
27.(4分)(1)3(1分)
(2)解:设6g水垢中含有碳酸钙的质量为x。
CaCO+2HCl=== CaCl+HO+CO↑ 1分
3 2 2 2
100 44
x 46g-43.8g
== x=5g 1分
水垢中CaCO 的质量分数为:×100%=83.3% 1分
3
答:该水垢中CaCO 的质量分数为83.3%。
3
说明:1.计算题只写出最后结果而无运算过程的不给分
2.计算题解题过程不符合法定单位制(设未知数不符合要求或运算过程不带单位)和计算结果
不符合要求者共扣1分。
89