文档内容
2019年广州市初中毕业生学业考试化学
本试卷分为选择题和非选择题两部分,共8页,满分100分。考试时间80分钟。
注意事项:
1.答卷前,考生务必在答题卡第1面和第3面上用黑色字迹的钢笔或签字笔填写自己的
考生号、姓名;同时填写考点考场号、座位号,再用2B铅笔把对应这两个号码的标号涂
黑。
2.选择题每小题选出答案后, 用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号;不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内
的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案,改动的答案也不
能超出指定的区域;不准使用铅笔、园球笔和涂改液,不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束时,将本试卷和答题卡一并交回。
5.全卷共三大题29小题,请考生检查题数。
相对原子质量: H1 C 12 O16 Na23 Ca40 S32 C135.5 Fe56
Co59 Cu 64
第一部分 选择题 (共40分)
一、选择题(本题包括20小题,每小题2分,共40分)
注意:每道选择题有四个选项,其中只有一项符合愿意。请用铅笔在答题卡上作答。选
错、不选、多选或涂改不清的,均不给分。
1.做好垃圾分类,为绿色发展做贡献。下列可回收垃圾主要成分为有机合成材料的是
A.旧报纸 B.塑料瓶 C.铝制易拉罐 D.玻璃瓶
2.“食在广州”, 下列广州美食中富含蛋白质的是
A.增城迟菜心 B.从化荔枝 C.沙湾姜撞奶 D.沙河粉
3.空气是一种宝贵的资源,下列生产生活中用到的气体不是来自空气的是
A.作为燃料电池燃料的H B.手于生产氮肥的N
2 2
C.用于医疗急救的O D.用于飞艇的He
2
4.下列过程中,发生了化学变化的是
A.干冰变成CO 气体 B.从含SiO 的沙子中提炼高纯Si
2 2
C.海水晒盐 D.从潮湿空气中分离出水
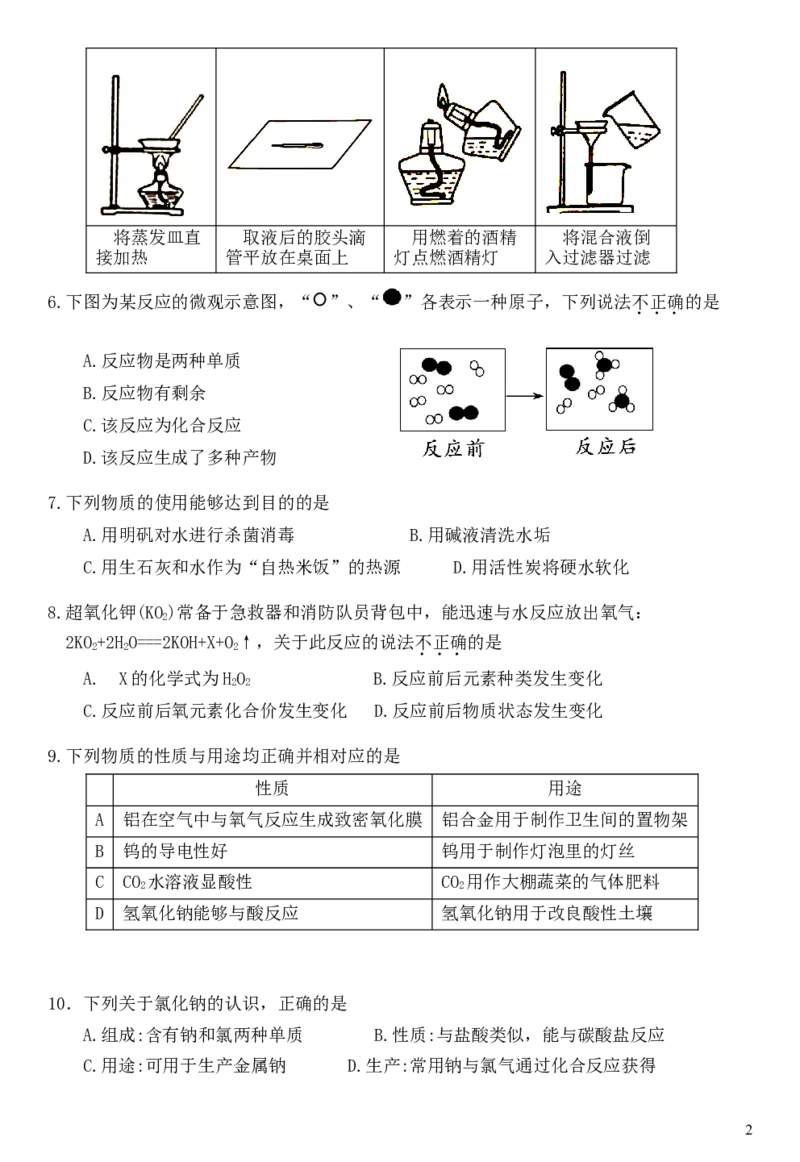
5.下列实验操 正确的是
A B C D
1将蒸发皿直 取液后的胶头滴 用燃着的酒精 将混合液倒
接加热 管平放在桌面上 灯点燃酒精灯 入过滤器过滤
6.下图为某反应的微观示意图,“ ”、“ ”各表示一种原子,下列说法不正确的是
A.反应物是两种单质
B.反应物有剩余
C.该反应为化合反应
D.该反应生成了多种产物
7.下列物质的使用能够达到目的的是
A.用明矾对水进行杀菌消毒 B.用碱液清洗水垢
C.用生石灰和水作为“自热米饭”的热源 D.用活性炭将硬水软化
8.超氧化钾(KO)常备于急救器和消防队员背包中,能迅速与水反应放出氧气:
2
2KO+2HO===2KOH+X+O↑,关于此反应的说法不正确的是
2 2 2
A. X的化学式为HO B.反应前后元素种类发生变化
2 2
C.反应前后氧元素化合价发生变化 D.反应前后物质状态发生变化
9.下列物质的性质与用途均正确并相对应的是
性质 用途
A 铝在空气中与氧气反应生成致密氧化膜 铝合金用于制作卫生间的置物架
B 钨的导电性好 钨用于制作灯泡里的灯丝
C CO 水溶液显酸性 CO 用作大棚蔬菜的气体肥料
2 2
D 氢氧化钠能够与酸反应 氢氧化钠用于改良酸性土壤
10.下列关于氯化钠的认识,正确的是
A.组成:含有钠和氯两种单质 B.性质:与盐酸类似,能与碳酸盐反应
C.用途:可用于生产金属钠 D.生产:常用钠与氯气通过化合反应获得
211.中国古代诗句中蕴含有很多化学原理,下列诗句的解释不正确的是
诗句 解释
A 吴山开,越溪涸,三金合冶成宝锷 “宝锷”的成分为合金
B 遥知不是雪,为有暗香来 分子在不停地运动
C 千淘万漉虽辛苦,吹尽狂沙始到金 金的密度比沙大
D 千锤万凿出深山,烈火焚烧若等闲 煅烧生石灰得到熟石灰
12.燃料和能源与生活息息相关,下列说法正确的是
A.石油是一种清洁能源,也是一种可再生能源
B.炒菜时油锅着火,应立即用水浇灭
C.“钻木取火”的原理是通过摩擦生热提高木材的着火点
D.燃气灶火焰出现黄色,锅底出现黑色时,可增大灶具进风口
13. 25℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是
编号 ① ② ③ ④
水的质量/g 50 50 50 50
加入固体质量/g 5 10 15 20
现象 固体完全溶解 固体完全溶解 剩余少量固体 剩余较多固体
A.实验①所得溶液质量分数为10%
B.实验说明25℃时该物质的溶解度是20g
C.实验③④所得溶液质量分数相同
D.实验④所得溶液中含溶质20g
14. 从地沟油中提炼生物柴油是垃圾资源化的方法之一。生物柴油主要成分是硬脂酸甲酯
(C H O),下列有关硬脂酸甲酯的说法正确的是
19 38 2
A.C、H、O三种元素的质量比为19:38:2
B.相对分子质量为(12×19+1×38+16×2)
C.C、H、O三种原子的个数比为12:1:16
D.氧元素的质量分数为 ×100%
15.煤和燃油的燃烧是造成空气污染的重婴原因,下列排放物能形成酸雨的是
A. SO、NO B. CO、CO C.烟尘 D.未充分燃烧的汽油
2 2 2
16.下列物质混合后能够反应,且有明显现象的是
A.向氧化铁粉末中滴入氢氧化钠溶液 B.向和硫酸中滴入稀氢氧化钾溶液
C.将硫酸铵与熟石灰混合研磨 D.向澄清石灰水中滴入氯化钡溶液
317. 某微粒M的结构示意图如下,关于该微粒的说法正确的是
A. M的原子易失电子
B.x只能为7
C. M为金属元素
D. x为8时,M为阴离子
18. 下列物质与空气充分混合后,遇明火不会发生爆炸的是
A.PO B.面粉 C.镁粉 D.CH
2 5 4
19.除去下列物质中理有的少量杂质(括号内为杂质),所用方法正确的是:
A. Zn粉(Fe):用ZnCl 溶液浸泡,过滤
2
B.碳粉(MnO):滴入HO 溶液,过滤
2 2 2
C. NaCl溶液(NaSO):加入适量MgCl 溶液过滤
2 4 2
D. CO (HO):通过盛有浓硫酸的洗气瓶
2 2
20. 下列实验中,现象正确且可得到相应结论的是
实验操作 现象 结论
硫在空气中燃烧发出淡蓝色 硫在空气中燃烧生成
把硫在空气中点燃,再伸进
A 火焰,在氧气中燃烧发出蓝紫 SO,在氧气中燃烧生
充满氧气的集气瓶里 2
色火焰 成SO
3
在电解器的玻璃管中加满 两极玻璃管中有气体生成,体
B 水是化合物,可分解
水,接通直流电源 积比是1:2
高温条件下,将CO通入 可利用CO的还原性
C 黑色粉末变为红色
FeO 粉末 来炼铁
2 3
将带火星的木条置于一瓶
D 木条不复燃 O 能支持燃烧
盛有氧气的集气瓶口上方 2
第二部分 非选择题 (共60分)
二、(本题包括5小题,共30分)
21.(3分)地球大气中存在氧气(O) 和臭氧(O)两种含氧元素的单质,其中臭氧氧主要存在
2 3
于15000-30000米的高空,能减弱高能量紫外线对地球表面的辐射。
(1) O 表示一个_____________ (填“原子”、“分子”或“离子”)
3
(2)高空中可发生转化: 2O 3O, 该变化属于_______ (填“物理”或“化
3 2
学”)变化。
(3)镁在氧气中燃烧的化学方程式是____________________________________________。
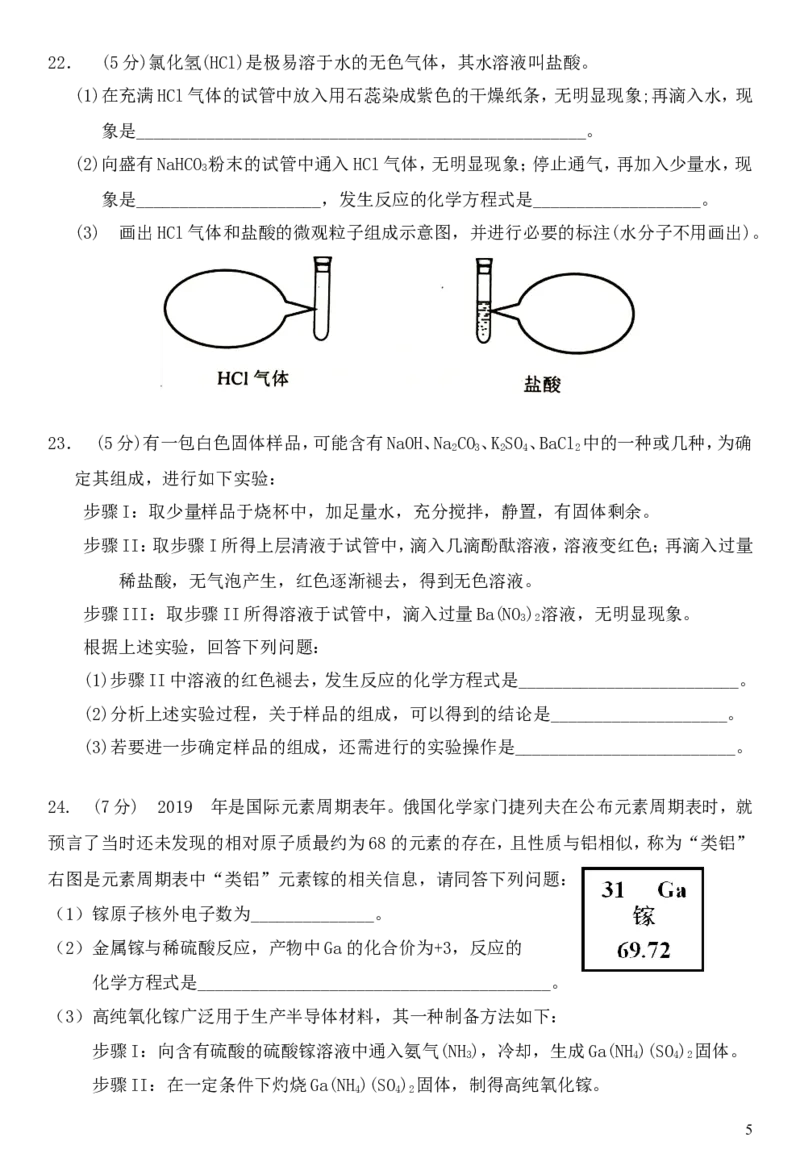
422. (5分)氯化氢(HCl)是极易溶于水的无色气体,其水溶液叫盐酸。
(1)在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水,现
象是___________________________________________________。
(2)向盛有NaHCO 粉末的试管中通入HCl气体,无明显现象;停止通气,再加入少量水,现
3
象是_____________________,发生反应的化学方程式是___________________。
(3) 画出HCl气体和盐酸的微观粒子组成示意图,并进行必要的标注(水分子不用画出)。
23. (5分)有一包白色固体样品,可能含有NaOH、NaCO、KSO、BaCl 中的一种或几种,为确
2 3 2 4 2
定其组成,进行如下实验:
步骤I:取少量样品于烧杯中,加足量水,充分搅拌,静置,有固体剩余。
步骤II:取步骤I所得上层清液于试管中,滴入几滴酚酞溶液,溶液变红色;再滴入过量
稀盐酸,无气泡产生,红色逐渐褪去,得到无色溶液。
步骤III:取步骤II所得溶液于试管中,滴入过量Ba(NO) 溶液,无明显现象。
3 2
根据上述实验,回答下列问题:
(1)步骤II中溶液的红色褪去,发生反应的化学方程式是_________________________。
(2)分析上述实验过程,关于样品的组成,可以得到的结论是____________________。
(3)若要进一步确定样品的组成,还需进行的实验操作是_________________________。
24. (7分) 2019 年是国际元素周期表年。俄国化学家门捷列夫在公布元素周期表时,就
预言了当时还未发现的相对原子质最约为68的元素的存在,且性质与铝相似,称为“类铝”
右图是元素周期表中“类铝”元素镓的相关信息,请同答下列问题:
(1)镓原子核外电子数为______________。
(2)金属镓与稀硫酸反应,产物中Ga的化合价为+3,反应的
化学方程式是________________________________________。
(3)高纯氧化镓广泛用于生产半导体材料,其一种制备方法如下:
步骤I:向含有硫酸的硫酸镓溶液中通入氨气(NH),冷却,生成Ga(NH)(SO) 固体。
3 4 4 2
步骤II:在一定条件下灼烧Ga(NH)(SO) 固体,制得高纯氧化镓。
4 4 2
5①Ga(NH)(SO) 中含有的带电的原子团(根)是___________________(填化学符号)
4 4 2
②步骤I反应的化学方程式是____________________________________________。
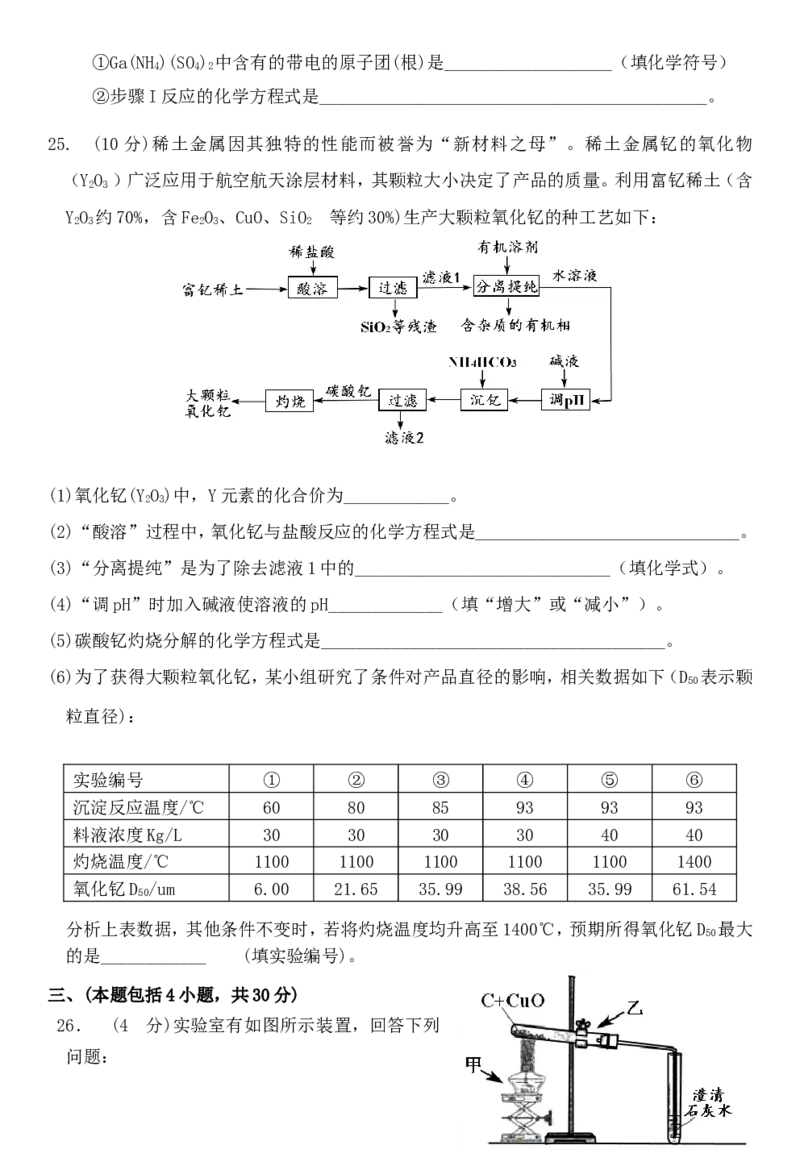
25. (10分)稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物
(YO )广泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含
2 3
YO 约70%,含FeO、CuO、SiO 等约30%)生产大颗粒氧化钇的种工艺如下:
2 3 2 3 2
(1)氧化钇(YO)中,Y元素的化合价为____________。
2 3
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是______________________________。
(3)“分离提纯”是为了除去滤液1中的_____________________________(填化学式)。
(4)“调pH”时加入碱液使溶液的pH_____________(填“增大”或“减小”)。
(5)碳酸钇灼烧分解的化学方程式是_______________________________________。
(6)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如下(D 表示颗
50
粒直径):
实验编号 ① ② ③ ④ ⑤ ⑥
沉淀反应温度/℃ 60 80 85 93 93 93
料液浓度Kg/L 30 30 30 30 40 40
灼烧温度/℃ 1100 1100 1100 1100 1100 1400
氧化钇D /um 6.00 21.65 35.99 38.56 35.99 61.54
50
分析上表数据,其他条件不变时,若将灼烧温度均升高至1400℃,预期所得氧化钇D 最大
50
的是____________ (填实验编号)。
三、(本题包括4小题,共30分)
26. (4 分)实验室有如图所示装置,回答下列
问题:
6(1)连接装置时,需根据导管的高度调节___________处的高度,再确定______处的高度 。
(填“甲”或“乙”)
(2)结束实验的操作作是:先______________,再 ______________________。
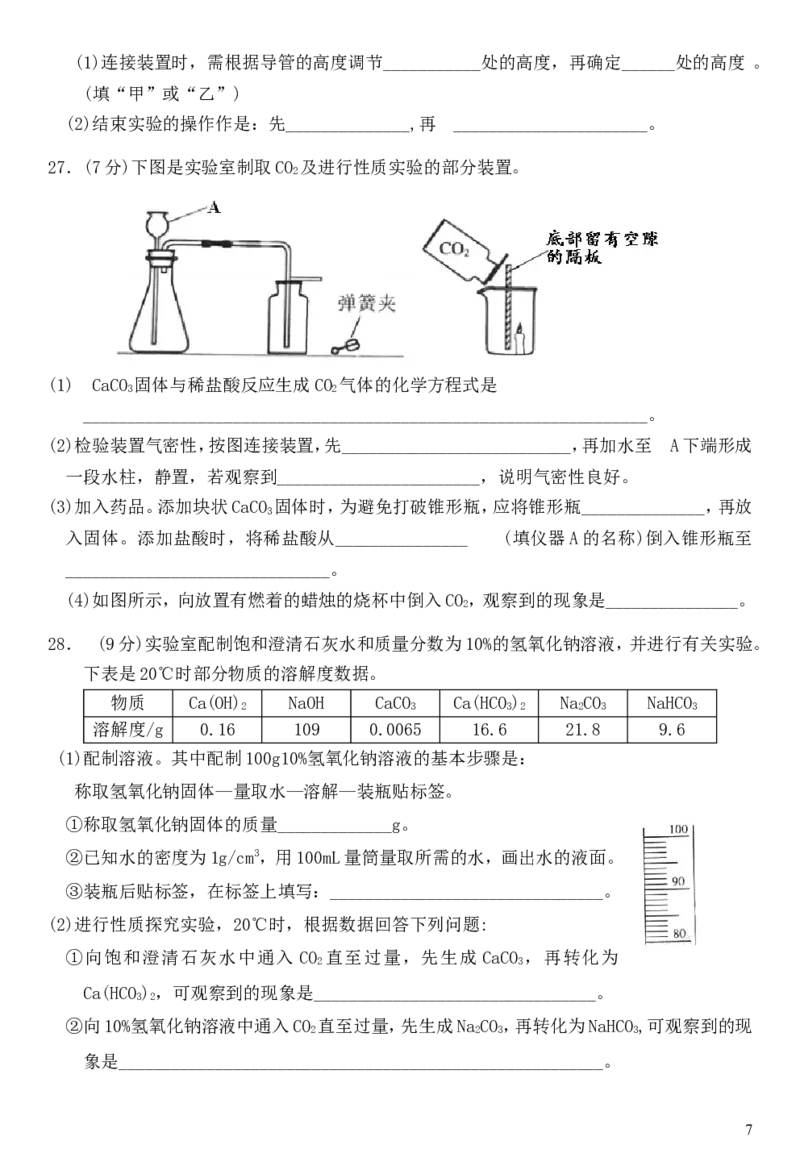
27.(7分)下图是实验室制取CO 及进行性质实验的部分装置。
2
(1) CaCO 固体与稀盐酸反应生成CO 气体的化学方程式是
3 2
________________________________________________________________。
(2)检验装置气密性,按图连接装置,先__________________________,再加水至 A下端形成
一段水柱,静置,若观察到_______________________,说明气密性良好。
(3)加入药品。添加块状CaCO 固体时,为避免打破锥形瓶,应将锥形瓶______________,再放
3
入固体。添加盐酸时,将稀盐酸从_______________ (填仪器A的名称)倒入锥形瓶至
______________________________。
(4)如图所示,向放置有燃着的蜡烛的烧杯中倒入CO,观察到的现象是_______________。
2
28. (9分)实验室配制饱和澄清石灰水和质量分数为10%的氢氧化钠溶液,并进行有关实验。
下表是20℃时部分物质的溶解度数据。
物质 Ca(OH) NaOH CaCO Ca(HCO) NaCO NaHCO
2 3 3 2 2 3 3
溶解度/g 0.16 109 0.0065 16.6 21.8 9.6
(1)配制溶液。其中配制100g10%氢氧化钠溶液的基本步骤是:
称取氢氧化钠固体—量取水—溶解—装瓶贴标签。
①称取氢氧化钠固体的质量_____________g。
②已知水的密度为1g/cm3,用100mL量筒量取所需的水,画出水的液面。
③装瓶后贴标签,在标签上填写:_______________________________。
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向饱和澄清石灰水中通入 CO 直至过量,先生成 CaCO ,再转化为
2 3
Ca(HCO),可观察到的现象是________________________________。
3 2
②向10%氢氧化钠溶液中通入CO 直至过量,先生成NaCO,再转化为NaHCO,可观察到的现
2 2 3 3
象是_______________________________________________________。
7③理论上吸收4.4gCO,需饱和澄清石灰水的质量至少为___________g,或需10%氢氧化钠
2
溶液的质量至少为__________g。(计算结果精确到个位)
29. (10分)已知金属钻(Co)的活动性与铁相似,请预测氯化钻(CoCl)的化学性质,说明预
2
测的依据,并设计实验验证。经查阅资料,钻的化合物相关性质如下:
物质 CoO Co(OH) CoCl CoSO Co(NO) CoCO
2 2 4 3 2 3
难溶于水 难溶于水 易溶于水 易溶于水 易溶于水 难溶于水
在水中溶
的灰绿色 的粉红色 形成粉红 形成粉红 形成粉红 的粉红色
的溶解性
固体 固体 色溶液 色溶液 色溶液 固体
限选试剂:CoCl 溶液、(NH)CO 溶液、NaSO 溶液、AgNO 溶液、NaOH溶液、稀硫酸、镁条、
2 4 2 3 2 4 3
铜片。
预测 预测的依据 验证预测的实验操作与预期现象
①能够与含Ag+的 CoCl 2 溶 液 中 含 取少量CoCl 2 溶液于试管中,__________,
Cl-, 如果观察到_________________,则预测成
可溶性盐反应
AgCl难溶于水。 立。
取少量CoCl 溶液于试管中,__________,
②能够与________ 2
______________ 如果观察到_________________,则预测成
(填物质类别)反应
立。
取少量CoCl 溶液于试管中,__________,
③能够与________ 2
______________ 如果观察到_________________,则预测成
(填物质类别)反应
立。
2019 广州中考化学参考答案
一、选择题
1-5 BCABA 6-10 DCBAC 11-15DDCBA 16-20 CDADB
二、(本题包括5小题,共30分)
21.(1)分子 (2)化学 (3) 2Mg+O 2MgO
2
22.(1)染有石蕊的纸条变红色;
(2)固体溶解,有气泡产生;
NaHCO +HCl===NaCl+HO+CO (3)
3 2 2
23.(1)NaOH+HCl=NaCl+HO
2
(2)该样品中一定含有BaCl 和NaOH,至少含有NaCO 和KSO 其中一种。
2 2 3 2 4
(3)取少量步骤 I 所得固体于试管中,滴加过量的稀盐酸,若固体不溶解,则样品中含
KSO ;若固体完全溶解,则样品中含 NaCO ;若部分溶解,则样品中含NaCO 和
2 4 2 3 2 3
KSO。
2 4
24.(1)31 (2)2Ga+3HSO =Ga(SO) +3H
2 4 2 4 3 2
8(3)① NH+ 、SO2− ② Ga(SO) +2NH +HSO =2Ga (NH)(SO)
4 4 2 4 3 3 2 4 4 4 2
25.(1)+3 (2) YO +6HCl=2YCl +3HO
2 3 3 2
(3)FeCl、CuCl (4)增大 (5) Y(CO) YO +3CO
3 2 2 3 3 2 3 2
(6)④
三、(本题包括4小题,共30分)
26.(1)乙;甲
(2)移出导管;熄灭酒精灯
27.(1) CaCO +2HCl=CaCl +HO+CO
3 2 2 2
(2)夹紧止水夹;长颈漏斗内水柱不下降。
(3)横放;长颈漏斗;浸没长颈漏斗下端口;
(4)蜡烛一开始持续燃烧,之后熄灭
28.(1)①10.0;②(见右图) ;③氢氧化钠 10%
(2)①先产生白色浑浊,继续通二氧化碳,溶液又变澄清;
②一段时间后出现白色沉淀;
③4632;80
29.
① 加入少量AgNO 溶液;有白色沉淀产生;
3
② 可溶性碱;CoCl 溶液中含Co2+,Co(OH) 难溶于水;加入少量NaOH溶液;有粉红色固体生成;
2 2
③含CO2-的盐(或可溶性碳酸盐);CoCl 溶液中含Co2+,CoCO 难溶于水;加入少量(NH)CO 溶
3 2 3 4 2 3
液;有粉红色固体生成。
910