文档内容
湖北省咸宁市2018年中考化学真题试题
可能用到的相对原子质量: H-1 C-12 Na -23 Cu-64 S-32 Fe-56 Zn-65
一、选择题
1. 生活中的下列变化一定属于化学变化的是
A. 雪糕融化 B. 湿衣服晾干 C. 自行车胎爆裂 D. 食物腐烂
【答案】D
【解析】A、雪糕融化的过程中没有新物质的生成,是物理变化,故错误;
B、湿衣服晾干是水分蒸发的过程,该过程中没有新物质的生成,是物理变化,故错误;
C、自行车胎爆裂是分子之间的间隙变大,故是物理变化,故错误;
D、食物腐烂是食物与空气中的氧气反应的过程,故是化学变化,故正确。故选D。
2. 下列实验现象描述正确的是
A. 镁条在空气中燃烧,发出白光,生成黑色固体
B. 细铁丝在氧气中燃烧,火星四射,生成了四氧化三铁
C. 铁锈与稀盐酸反应后溶液颜色由无色变成了黄色
D. 将紫色石蕊试液滴入到稀氢氧化钠溶液中变红
【答案】C
【解析】A. 镁条在空气中燃烧,发出白光,生成白色固体,故错误;
B. 细铁丝在氧气中燃烧,火星四射,生成了黑色固体,描述现象时,不能说明物质的名称,故错误;
C. 铁锈与稀盐酸反应后溶液颜色由无色变成了黄色,正确;
D. 石蕊遇碱变蓝,故将紫色石蕊试液滴入到稀氢氧化钠溶液中变蓝,故错误。故选C。
3. 水是我们日常生活必不可少的物质,下列有关水的说法错误的是
A. 水是由氢元素和氧元素组成的
B. 生活中可通过煮沸降低水的硬度
C. 洗菜、洗衣和淘米的水可用来浇花、拖地或冲厕所
D. 水通电分解时正极产生的氢气与负极生的氧气体积比约为2:1
【答案】D
【解析】A. 水是由氢元素和氧元素组成的,正确;
B. 煮沸可以将可溶性的钙镁化合物转化为难溶性的钙镁化合物沉淀出来,故生活中可通过煮沸降低水的硬
度,正确;
C. 洗菜、洗衣和淘米的水可用来浇花、拖地或冲厕所,正确;
D. 水通电分解时正极产生的氧气气与负极生的是氢气,气体积比约为1:2,故错误。故选D。
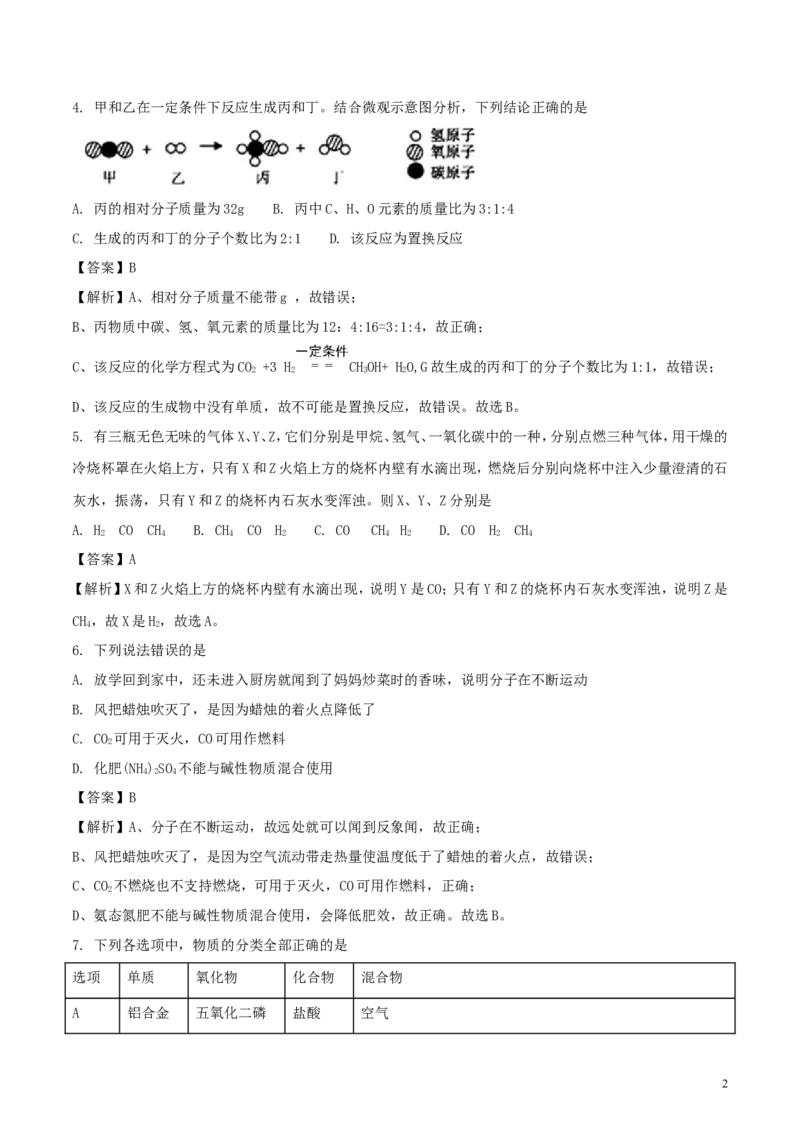
14. 甲和乙在一定条件下反应生成丙和丁。结合微观示意图分析,下列结论正确的是
A. 丙的相对分子质量为32g B. 丙中C、H、O元素的质量比为3:1:4
C. 生成的丙和丁的分子个数比为2:1 D. 该反应为置换反应
【答案】B
【解析】A、相对分子质量不能带g ,故错误;
B、丙物质中碳、氢、氧元素的质量比为12:4:16=3:1:4,故正确;
C、该反应的化学方程式为CO +3 H CHOH+ HO,G故生成的丙和丁的分子个数比为1:1,故错误;
2 2 3 2
D、该反应的生成物中没有单质,故不可能是置换反应,故错误。故选B。
5. 有三瓶无色无味的气体X、Y、Z,它们分别是甲烷、氢气、一氧化碳中的一种,分别点燃三种气体,用干燥的
冷烧杯罩在火焰上方,只有X和Z火焰上方的烧杯内壁有水滴出现,燃烧后分别向烧杯中注入少量澄清的石
灰水,振荡,只有Y和Z的烧杯内石灰水变浑浊。则X、Y、Z分别是
A. H CO CH B. CH CO H C. CO CH H D. CO H CH
2 4 4 2 4 2 2 4
【答案】A
【解析】X和Z火焰上方的烧杯内壁有水滴出现,说明Y是CO;只有Y和Z的烧杯内石灰水变浑浊,说明Z是
CH,故X是H,故选A。
4 2
6. 下列说法错误的是
A. 放学回到家中,还未进入厨房就闻到了妈妈炒菜时的香味,说明分子在不断运动
B. 风把蜡烛吹灭了,是因为蜡烛的着火点降低了
C. CO 可用于灭火,CO可用作燃料
2
D. 化肥(NH)SO 不能与碱性物质混合使用
4 2 4
【答案】B
【解析】A、分子在不断运动,故远处就可以闻到反象闻,故正确;
B、风把蜡烛吹灭了,是因为空气流动带走热量使温度低于了蜡烛的着火点,故错误;
C、CO 不燃烧也不支持燃烧,可用于灭火,CO可用作燃料,正确;
2
D、氨态氮肥不能与碱性物质混合使用,会降低肥效,故正确。故选B。
7. 下列各选项中,物质的分类全部正确的是
选项 单质 氧化物 化合物 混合物
A 铝合金 五氧化二磷 盐酸 空气
2B 水银 水 硝酸铵 冰水混合物
C 金刚石 干冰 氧化铜 生理盐水
D 钢 生石灰 火碱 煤
A. A B. B C. C D. D
【答案】C
【解析】A、盐酸是溶液,是混合物,故错误;
B、冰水混合物是同一种物质,故不是混合物,故错误;
D、煤是混合物,故错误。故选C。
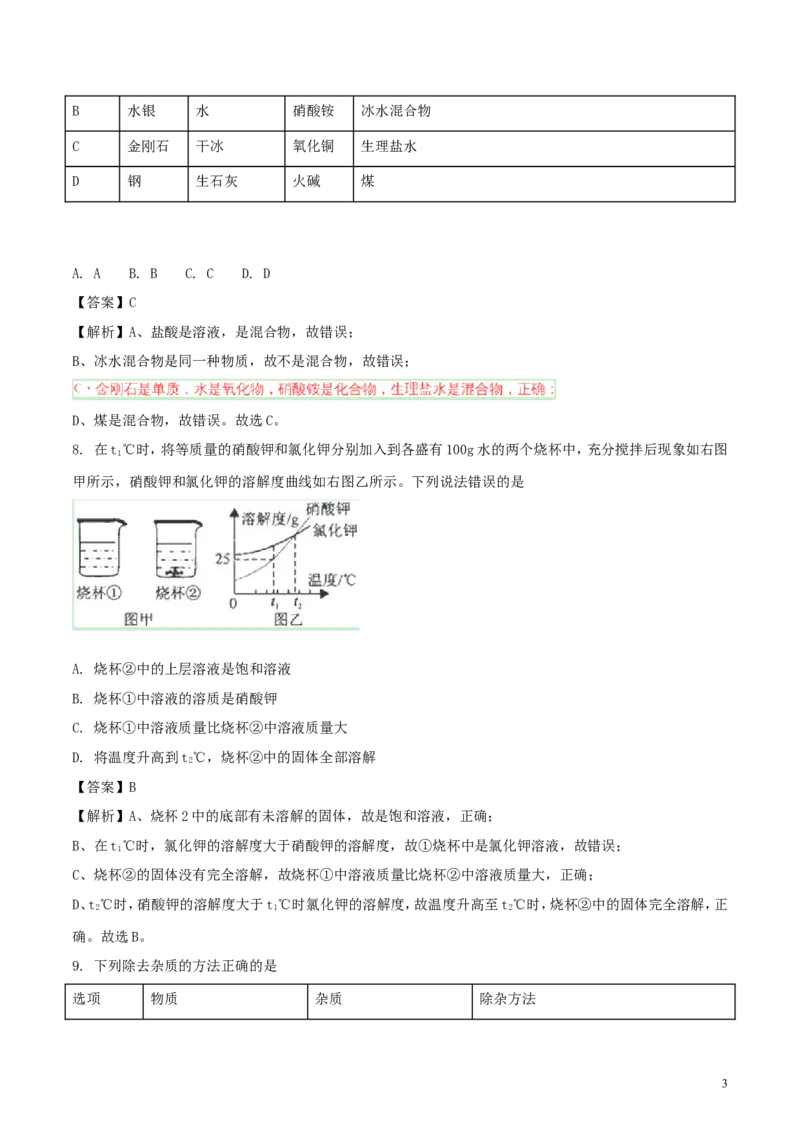
8. 在t℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如右图
1
甲所示,硝酸钾和氯化钾的溶解度曲线如右图乙所示。下列说法错误的是
A. 烧杯②中的上层溶液是饱和溶液
B. 烧杯①中溶液的溶质是硝酸钾
C. 烧杯①中溶液质量比烧杯②中溶液质量大
D. 将温度升高到t℃,烧杯②中的固体全部溶解
2
【答案】B
【解析】A、烧杯2中的底部有未溶解的固体,故是饱和溶液,正确;
B、在t℃时,氯化钾的溶解度大于硝酸钾的溶解度,故①烧杯中是氯化钾溶液,故错误;
1
C、烧杯②的固体没有完全溶解,故烧杯①中溶液质量比烧杯②中溶液质量大,正确;
D、t℃时,硝酸钾的溶解度大于t℃时氯化钾的溶解度,故温度升高至t℃时,烧杯②中的固体完全溶解,正
2 1 2
确。故选B。
9. 下列除去杂质的方法正确的是
选项 物质 杂质 除杂方法
3A CaCl 溶液 稀盐酸 加入过量的CaCO,过滤
2 3
B 盐酸 硫酸 加入过量BaCl 溶液,过滤
2
C NaNO NaCl 加入过量AgNO 溶液,过滤
3 3
D CaO Ca(OH) 加过量水,过滤
2
A. A B. B C. C D. D
【答案】A
【解析】A、加入过量的碳酸钙可以与稀盐酸反应生成氯化钙,过量的碳酸钙通过过滤除去,故正确;
B、引入了氯化钡杂质,故错误;
C、引入了过量的硝酸银杂质,故错误;
D、氧化钙可以与水反应,故错误。故选A。
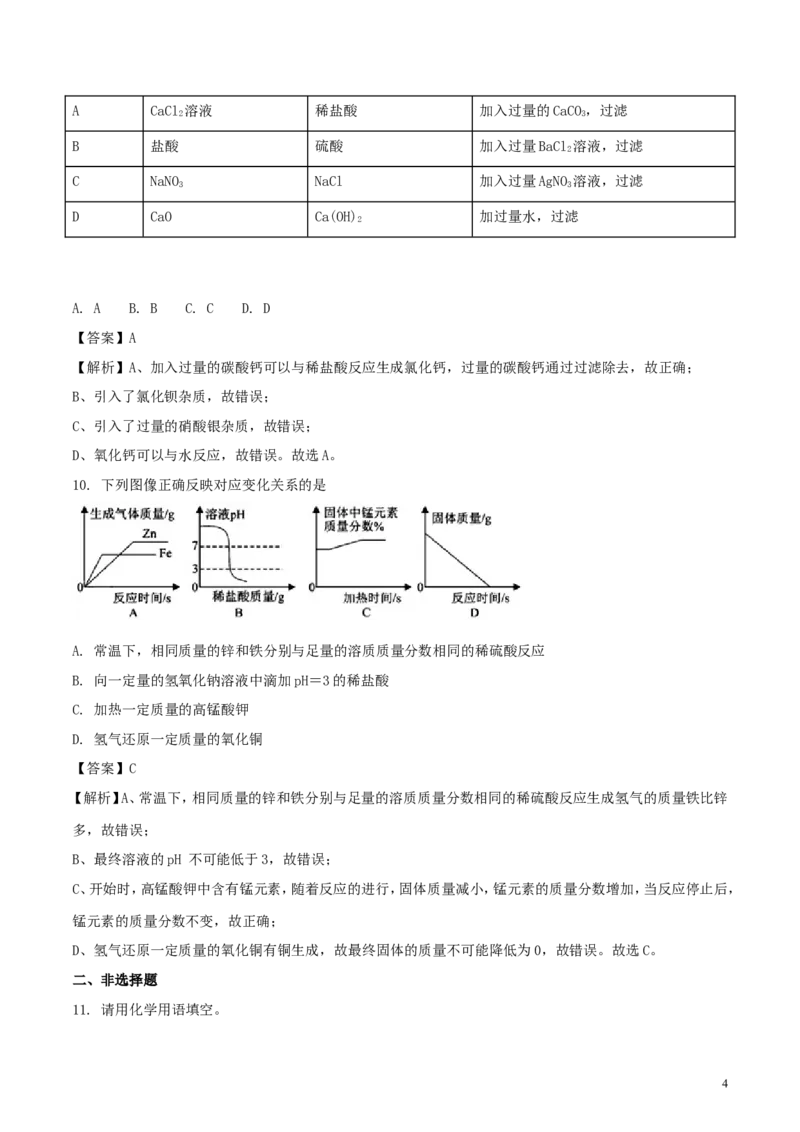
10. 下列图像正确反映对应变化关系的是
A. 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
B. 向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
C. 加热一定质量的高锰酸钾
D. 氢气还原一定质量的氧化铜
【答案】C
【解析】A、常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应生成氢气的质量铁比锌
多,故错误;
B、最终溶液的pH 不可能低于3,故错误;
C、开始时,高锰酸钾中含有锰元素,随着反应的进行,固体质量减小,锰元素的质量分数增加,当反应停止后,
锰元素的质量分数不变,故正确;
D、氢气还原一定质量的氧化铜有铜生成,故最终固体的质量不可能降低为0,故错误。故选C。
二、非选择题
11. 请用化学用语填空。
4(1)某微粒的结构示意图为 ,该微粒的符号_______________。
(2)稀有气体氦的化学式______________。
(3)保持双氧水化学性质的最小微粒_______________。
(4)写出硫酸铝的化学式并标出铝元素的化合价_______________。
【答案】 (1). Cl- (2). He (3). HO (4).
2 2
【解析】(1)该粒子结构示意图中核外电子数比核内质子数大1,故是氯离子,符号为. Cl- ;
(2)稀有气体氦的化学式是He;
(3)分子是保持物质化学性质的最小微粒,故保持双氧水化学性质的最小微粒是HO ;
2 2
(4)硫酸铝中硫酸根的化合价为-2价,根据化合价的代数和为0求得铝元素的化合价为+3价,表示为
;
12. 化学与生活密切相关。请回答下列问题。
(1)习近平总书记在“十九大”报告中指出:要加强生态文明建设,创建美丽中国。
①创建美丽中国需要向人民提供优质食品。牛奶是一种优质食品,除水外,牛奶中富含的营养素是
_______________。
②要加强生态文明建设,必须推广清洁能源的使用,国家已经在推广乙醇汽油,写出乙醇(CHOH)燃烧的化学
2 5
方程式__________________。
(2)某水样加入肥皂水后产生了较多泡沫,该水样是(选填“硬水”或“软水”)___________。
(3)配制一定溶质质量分数的氯化钠溶液,在其它操作无错误的前提下,用量筒量取水时俯视读数,则配制溶
液的溶质质量分数会(选填“偏大”、“偏小”或“不变”)_______________。
【答案】 (1). 蛋白质 (2). CHOH+3O 2CO+3HO (3). 软水 (4). 偏大
2 5 2 2 2
【解析】(1)①牛奶中富含的营养素是蛋白质;②乙醇与氧气在点燃的条件下反应生成二氧化碳和水,反应方
程式为CHOH+3O 2CO+3HO;
2 5 2 2 2
(2)水样加入肥皂水后产生了较多泡沫、浮渣少的水是软水;
(3)用量筒量取水时俯视读数,则量取水的实际体积偏小,故配得的溶液的质量分数偏大;
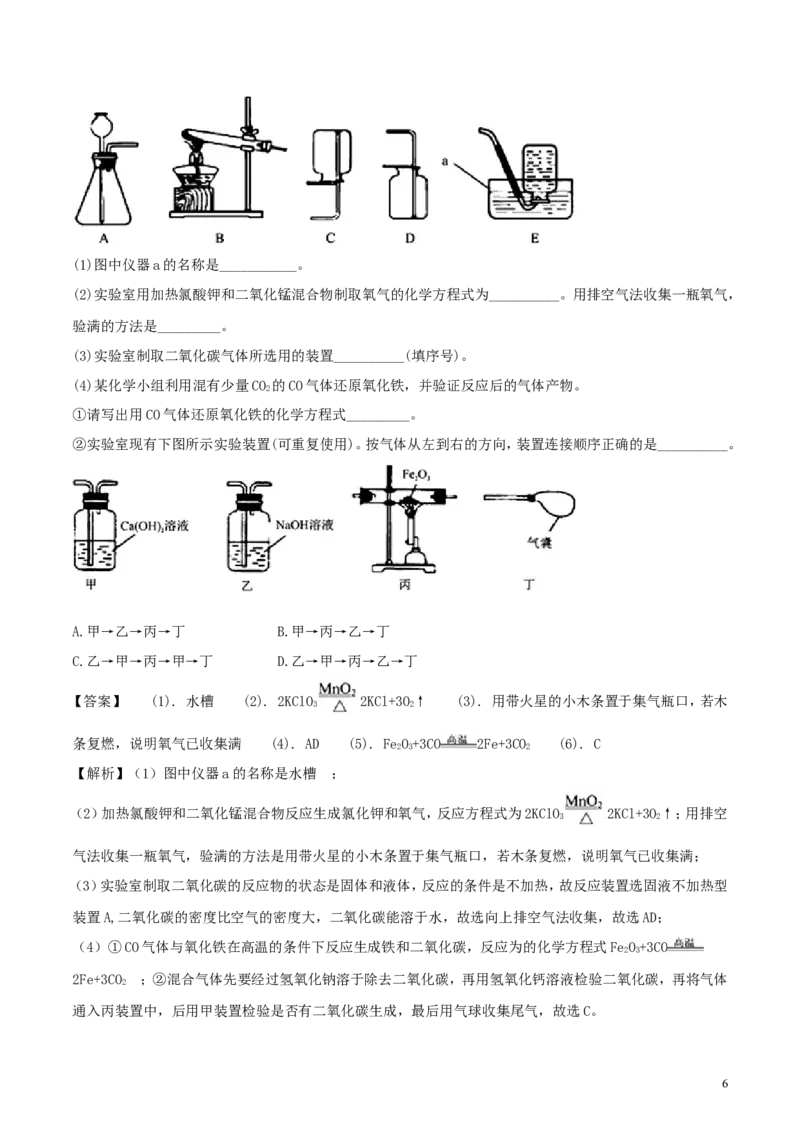
13. 根据下图实验装置,回答问题。
5(1)图中仪器a的名称是___________。
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为__________。用排空气法收集一瓶氧气,
验满的方法是_________。
(3)实验室制取二氧化碳气体所选用的装置__________(填序号)。
(4)某化学小组利用混有少量CO 的CO气体还原氧化铁,并验证反应后的气体产物。
2
①请写出用CO气体还原氧化铁的化学方程式_________。
②实验室现有下图所示实验装置(可重复使用)。按气体从左到右的方向,装置连接顺序正确的是__________。
A.甲→乙→丙→丁 B.甲→丙→乙→丁
C.乙→甲→丙→甲→丁 D.乙→甲→丙→乙→丁
【答案】 (1). 水槽 (2). 2KClO 2KCl+3O↑ (3). 用带火星的小木条置于集气瓶口,若木
3 2
条复燃,说明氧气已收集满 (4). AD (5). FeO+3CO 2Fe+3CO (6). C
2 3 2
【解析】(1)图中仪器a的名称是水槽 ;
(2)加热氯酸钾和二氧化锰混合物反应生成氯化钾和氧气,反应方程式为2KClO 2KCl+3O↑;用排空
3 2
气法收集一瓶氧气,验满的方法是用带火星的小木条置于集气瓶口,若木条复燃,说明氧气已收集满;
(3)实验室制取二氧化碳的反应物的状态是固体和液体,反应的条件是不加热,故反应装置选固液不加热型
装置A,二氧化碳的密度比空气的密度大,二氧化碳能溶于水,故选向上排空气法收集,故选AD;
(4)①CO气体与氧化铁在高温的条件下反应生成铁和二氧化碳,反应为的化学方程式FeO+3CO
2 3
2Fe+3CO ;②混合气体先要经过氢氧化钠溶于除去二氧化碳,再用氢氧化钙溶液检验二氧化碳,再将气体
2
通入丙装置中,后用甲装置检验是否有二氧化碳生成,最后用气球收集尾气,故选C。
614. 某种手机电路板中含有Fe、Cu、Au、Ag、Ni(镍,银白色金属)等金属,如下是某工厂回收部分金属的流程
图。已知:2Cu+O+2HSO 2CuSO+2HO
2 2 4 4 2
(1)操作①的名称是____________________。
(2)写出滤液②中金属阳离子符号____________________。
(3)写出滤液③和铁粉发生反应的一个化学方程式____________________________。
(4)Cu、Ag、Ni在溶液中的活动性由强到弱的顺序依次是____________________。
【答案】 (1). 过滤 (2). Fe2+ (3). Fe+CuSO=FeSO+Cu(或Fe+HSO=FeSO +H↑) (4). Ni
4 4 2 4 4 2
Cu Ag
【解析】(1)操作①将固液分离,故是过滤;
(2)固体中的镍和铁与稀硫酸反应生成硫酸镍和硫酸亚铁,过量的铁粉于硫酸镍反应生成镍和硫酸亚铁,故
滤液2是硫酸亚铁溶液,阳离子是Fe2+ ;
(4)Cu、Ag、Ni在溶液中的活动性由强到弱的顺序依次是Ni Cu Ag;
15. 咸宁市某校2018年实验操作模拟考试的一个考题是:用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水。
【进行实验】
实验步骤 实验现象 实验结论
a中有气泡产生 a中物质是稀盐酸
分别用a、b、c三支试管取样,各加
b中无明显现象 b中物质是食盐水
入一定量碳酸钠溶液
c中__________ c中物质是澄清石灰水
写出a试管中发生反应的化学方程式__________。把c试管反应后的物质进行过滤,得到滤液。
【提出问题】滤液中溶质的成分是什么?
猜想一:NaCO 和NaOH;猜想二:NaOH;猜想三:__________。
2 3
7提示:Ca(OH) 微溶于水。
2
【实验过程】为证明猜想一是否正确,进行了如下实验:
实验步骤 实验现象 实验结论
取一定量滤液于试管中,加入一种盐溶液
有白色沉淀 猜想一正确
(写溶质化学式)__________。
写出上述有白色沉淀生成的化学方程式__________。
同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值
用pH试纸测定a试管反应后废液酸碱性的过程 测定结果
在白瓷板上放一小片pH试纸,用玻璃棒蘸取_________。 pH<7(废液显酸性)
【反思与交流】a试管中的废液显酸性,从环保、经济、操作简便等方面考虑,应向废液加入(写化学
式)_________后再排放
【答案】 (1). 有白色沉淀生成(或溶液变浑浊) (2). NaCO+2HCl=2NaCl+HO+CO↑ (3).
2 3 2 2
Ca(OH) 和NaOH (4). BaCl(或Ba(NO)) (5). NaCO+BaCl=Ba(CO)↓+2NaCl(或
2 2 3 2 2 3 2 3 2
NaCO+Ba(NO)=Ba(CO)↓+2NaNO) (6). a试管中的废液滴到pH试纸上,把试纸显示的颜色与标准比
2 3 3 2 3 2 3
色卡比较(读出溶液的pH值) (7). Ca(OH)(或CaCO,答CaO也算对)
2 3
【解析】碳酸钠与氢氧化钙反应生成碳酸钙沉淀,故c中的现象是变浑浊;a试管中是碳酸钠与稀盐酸反应生
成氯化钠、二氧化碳和水,反应方程式为NaCO+2HCl=2NaCl+HO+CO↑;当氢氧化钙过量时,c中的溶质是氢
2 3 2 2
氧化钠和氢氧化钙的混合物,故猜想3是Ca(OH) 和NaOH ;如结论猜想一正确,则溶液中有碳酸钠,故加入
2
的盐是氯化钡,有碳酸钡沉淀生成;氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠,故方程式为
NaCO+BaCl=Ba(CO)↓+2NaCl;用pH试纸测定a试管反应后废液酸碱性的过程是在白瓷板上放一小片pH
2 3 2 3 2
试纸,用玻璃棒蘸取a试管中的废液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较(读出溶液的pH
值);废液显酸性可以加入氢氧化钙溶液调节酸碱性;
16. 为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的
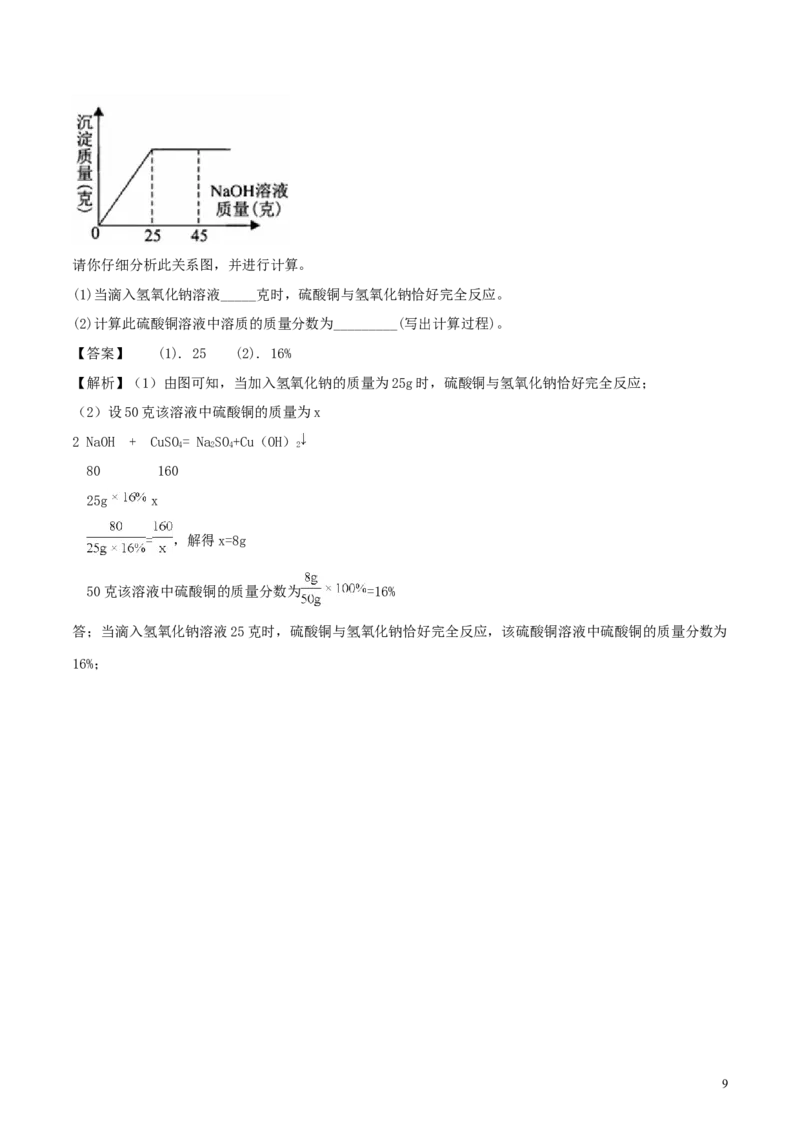
氢氧化钠溶淀液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
8请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
【答案】 (1). 25 (2). 16%
【解析】(1)由图可知,当加入氢氧化钠的质量为25g时,硫酸铜与氢氧化钠恰好完全反应;
(2)设50克该溶液中硫酸铜的质量为x
2 NaOH + CuSO= NaSO+Cu(OH)
4 2 4 2
80 160
25g x
= ,解得x=8g
50克该溶液中硫酸铜的质量分数为 =16%
答;当滴入氢氧化钠溶液25克时,硫酸铜与氢氧化钠恰好完全反应,该硫酸铜溶液中硫酸铜的质量分数为
16%;
9