文档内容
鄂州市2019年初中毕业生学业考试化学试题
学校: 考生姓名: 准考证
号:
注意事项:
1.本试题卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。第Ⅰ卷1至6页,第Ⅱ卷7
至12页。满分130分,其中物理80分,化学50分。考试时间120分钟。
2.答题前,考生务必将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号
条形码粘贴在答题卡上的指定位置。
3.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。答在试题卷上无效。
4.非选择题用0.5毫米黑色墨水签字笔直接答在答题卡上对应的答题区域内。答在试
题卷上无效。
5.考生必须保持答题卡的整洁。考试结束后,请将本试题卷和答题卡一并上交。
6.物理试题中g取10N/kg,ρ =1.0×103kg/m3。
水
7.相对原子质量:H—1 N —14 O—16 Cl—35.5 Na—23
第Ⅰ卷 选择题(共54分)
一、选择题(每小题只有一个选项符合题意,本大题共12小题,每小题2分,共24分)
1.下列事例中,一定发生了化学变化的是( )
A.瓷碗摔碎了B.潮湿的衣服晒干了C.桌子上的苹果腐烂了D.冰箱中的水结冰了
【答案】C
【解析】瓷碗摔碎、潮湿的衣服晒干、冰箱中的水结冰发生变化时都没有新的物质生成;苹果
腐烂变质过程中生成新的物质。故选C。
2.空气中含量较多且化学性质比较活泼的气体是( )
A.氧气 B.氮气 C.二氧化碳 D.稀有气体
【答案】A
1【解析】空气中含量较多且化学性质比较活泼的气体是氧气,占21%;氮气占78%,化学性质较
稳定;二氧化碳占0.03%,稀有气体占0.94%。故选A。
3.下列化学符号能表示2个氢原子的是( )
A.2H B.H C.2H D.2H+
2 2
【答案】A
【解析】2H表示2个氢原子;H 表示一个氢分子或氢气;2H 表示2个氢分子;2H+表示2个氢离
2 2
子。故选A。
4.下列生活用品所含的主要材料,属于有机合成材料的是( )
A.纯棉毛巾 B.塑料垃圾袋 C.玻璃啤酒瓶 D.铝质饮料罐
【答案】B
【解析】纯棉毛巾属于天然有机材料;塑料垃圾袋属于 有机合成材料;玻璃啤酒瓶属于无机
材料;铝质饮料罐属于金属材料。故选B。
5.下列关于水的说法中不正确的是( )
A.农业和园林浇灌改大水漫灌为喷灌、滴灌,可节约用水
B.农业生产中不合理施用农药、化肥会对水体造成污染
C.水是一种常用的溶剂
D.电解水生成了氢气和氧气,因此,水是由氢气和氧气组成的
【答案】D
【解析】农业和园林浇灌改大水漫灌为喷灌、滴灌,可以提高水资源的利用率,可节约用水;
农业生产中不合理施用农药、化肥会对水体造成污染;水是一种常用的溶剂;电解水生成了
氢气和氧气,因此,水是由氢、氧元素组成的。故选D。
6.分类是化学学习的重要方法,下列关于物质分类正确的是( )
A.煤、石油、天然气都属于混合物B.干冰、生石灰、高锰酸钾都属于氧化物
C.熟石灰、烧碱、纯碱都属于碱 D.尿素、硝酸钾、磷酸铵都属于复合肥
【答案】A
【解析】煤、石油、天然气三大化石燃料都属于混合物;干冰和生石灰属于氧化物,高锰酸钾
不属于氧化物;熟石灰和烧碱属于碱,纯碱属于盐;尿素属于氮肥,硝酸钾和磷酸铵都属于复
2合肥。故选A。
7.甲、乙、丙、丁都是含碳的物质,它们有如下关系:①甲与丙在高温的条件下反应生成
乙;②乙与氧气在点燃的条件下反应生成丙;③常温下丁能分解生成丙。则甲、乙、丙、丁分
别是( )
A.C、CO、CO、CaCO B.C、CO、CO、HCO
2 3 2 2 3
C.CO、C、CO、CaCO D.CO、C、CO、HCO
2 3 2 2 3
【答案】B
【解析】甲与丙反应:C+ CO 高温 2CO,乙与氧气反应:2CO + O 点燃 2CO,常温下丁能分解生
2 2 2
成丙:HCO △ CO↑+HO,可以判断甲为C,乙为CO,丙为CO,丁为HCO。故选B。
2 3 2 2 2 2 3
8.下列灭火方法中不正确的是( )
A.炒菜时油锅着火,用锅盖盖灭B.贵重图书资料着火,用液态二氧化碳灭火器扑灭
C.电器短路着火,未切断电源直接用水浇灭D.家中燃气泄漏着火,关闭燃气阀门
【答案】C
【解析】炒菜时油锅着火,用锅盖盖灭,可以隔绝空气,达到灭火的目的;贵重图书资料着火,
用液态二氧化碳灭火器扑灭,液态二氧化碳升华吸收热量,达到降低温度到着火点以下且二
氧化碳不能燃烧,也不支持燃烧,达到灭火和保护图书资料的目的;电器短路着火,先切断电
源再直接用水浇灭;家中燃气泄漏着火,关闭燃气阀门,切断气源,达到灭火的目的。故选C。
9.某火箭在发射过程中,发生反应的微观过程示意图如下:
下列说法不正确的是( )
A.甲中氮、氧原子个数比是1∶2 B.乙的相对分子质量是32
C.反应前后氢元素的质量减小 D.生成的丙和丁的分子个数比是3∶4
3【答案】C
【解析】根据微观示意图判断反应方程式:NO+2 NH 点燃 3N+ 4HO。甲为NO 中氮、氧原子
2 4 2 4 2 2 2 4
个数比=2:4=1∶2;乙为NH 的相对分子质量=14×2+1×4=32;反应前后氢元素的质量不变;
2 4
生成的丙和丁的分子个数比是3∶4。故选C。
10.提纯是化学实验常用的方法。除去下列物质中所含的少量杂质(括号内为杂质),
选用的实验方案不合理的是( )
选项 物质 实验方案
A CO(CO) 通过灼热的氧化铜
2
B CaO(CaCO) 在高温下煅烧
3
C O(HO) 通过盛有浓硫酸的洗气瓶
2 2
D MnO(KCl) 溶解、过滤、洗涤、干燥
2
【答案】A
【解析】CO+CuO高温 CO+Cu,不符合除杂原则;CaCO 高温 CO↑+ CaO,符合除杂原则;浓硫酸
2 3 2
可以除去氧气中的水汽,符合除杂原则;二氧化锰不溶于水,氯化钾溶于水,溶解、过滤、洗
涤、干燥可以除去MnO 中KCl,符合除杂原则。故选A。
2
11.下列各组物质在水中能大量共存且溶液为无色的是( )
A.NHCl、KCO、NaOH、NaSO B.MgSO、NaCl、Ba(NO)、FeCl
4 2 3 2 4 4 3 2 3
C.KOH、NaSO、HCl、NaHCO D.HCl、NaNO、KSO、NHCl
2 4 3 3 2 4 4
【答案】D
【解析】NHCl和NaOH不能共存,产生刺激性气味氨气;MgSO 与Ba(NO) 生成白色沉淀,FeCl
4 4 3 2 3
溶液显黄色;KOH、NaHCO 都与HCl发生,不能共存;HCl、NaNO、KSO、NHCl两两均不能反应
3 3 2 4 4
且溶液为无色。故选D。
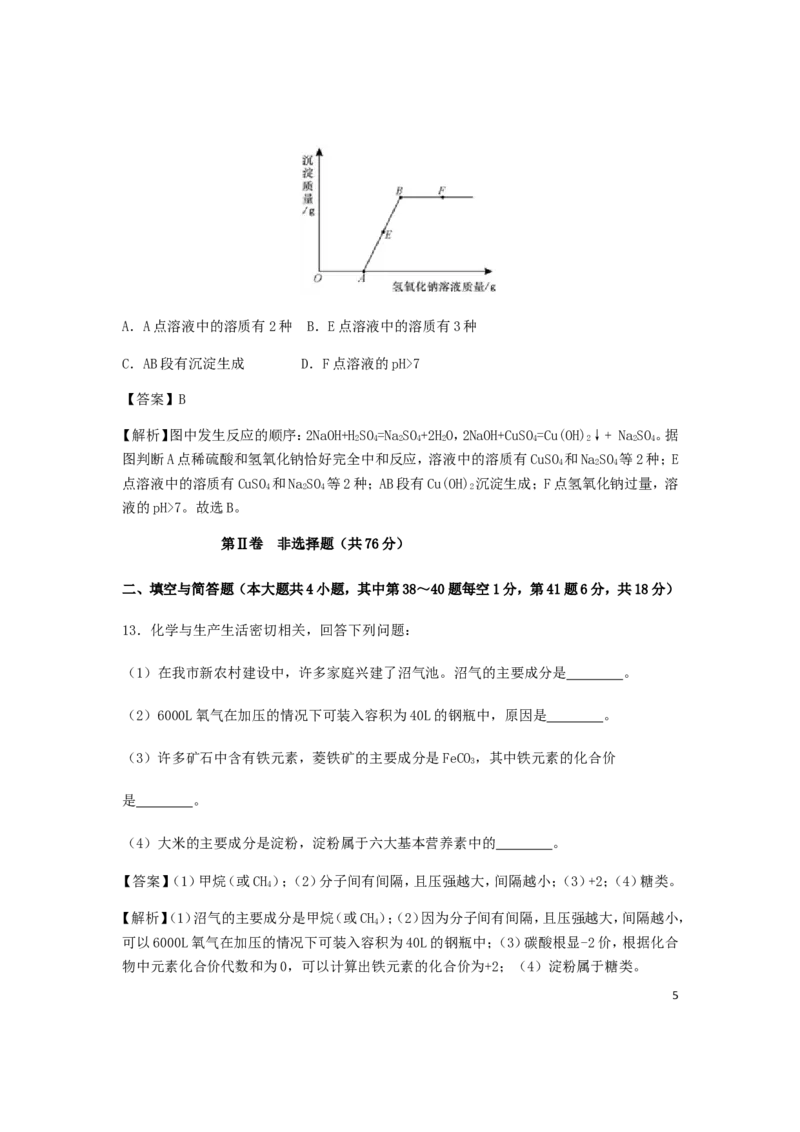
12.向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生的沉淀
质量与加入的氢氧化钠溶液质量关系如下图所示。下列说法不正确的是( )
4A.A点溶液中的溶质有2种 B.E点溶液中的溶质有3种
C.AB段有沉淀生成 D.F点溶液的pH>7
【答案】B
【解析】图中发生反应的顺序:2NaOH+HSO=NaSO+2HO,2NaOH+CuSO=Cu(OH)↓+ NaSO。据
2 4 2 4 2 4 2 2 4
图判断A点稀硫酸和氢氧化钠恰好完全中和反应,溶液中的溶质有CuSO 和NaSO 等2种;E
4 2 4
点溶液中的溶质有CuSO 和NaSO 等2种;AB段有Cu(OH) 沉淀生成;F点氢氧化钠过量,溶
4 2 4 2
液的pH>7。故选B。
第Ⅱ卷 非选择题(共76分)
二、填空与简答题(本大题共4小题,其中第38~40题每空1分,第41题6分,共18分)
13.化学与生产生活密切相关,回答下列问题:
(1)在我市新农村建设中,许多家庭兴建了沼气池。沼气的主要成分是 。
(2)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,原因是 。
(3)许多矿石中含有铁元素,菱铁矿的主要成分是FeCO,其中铁元素的化合价
3
是 。
(4)大米的主要成分是淀粉,淀粉属于六大基本营养素中的 。
【答案】(1)甲烷(或CH);(2)分子间有间隔,且压强越大,间隔越小;(3)+2;(4)糖类。
4
【解析】(1)沼气的主要成分是甲烷(或CH);(2)因为分子间有间隔,且压强越大,间隔越小,
4
可以6000L氧气在加压的情况下可装入容积为40L的钢瓶中;(3)碳酸根显-2价,根据化合
物中元素化合价代数和为0,可以计算出铁元素的化合价为+2;(4)淀粉属于糖类。
514.硝酸钾在不同温度下的溶解度数据如下表所示:
回 温度/℃ 0 20 40 60 80
答
溶解度/g 13.3 31.6 63.9 110 169
下
列问题:
(1)20℃时,将18g硝酸钾加入到50g水中,充分溶解后,所得溶液的质量是 g。
(2)80℃时,将269g硝酸钾饱和溶液降温到60℃,析出晶体的质量是 g。
(3)0℃时,硝酸钾饱和溶液中溶质的质量分数是 。(结果精确到0.1%)
(4)将40℃的硝酸钾饱和溶液变为不饱和溶液,可采取的措施是 。
【答案】(1)65.8;(2)59;(3)11.7%;(4)加水或升温。
【解析】(1)20℃时,硝酸钾的溶解度为31.6g,将18g硝酸钾加入到50g水中,充分溶解后,
所得溶液的质量是65.8g;(2)20℃时,硝酸钾的溶解度为169g,60℃时,硝酸钾的溶解度为
110g,80℃时,将269g硝酸钾饱和溶液降温到60℃,析出晶体的质量是59g;(3)0℃时,硝酸
钾饱和溶液中溶质的质量分数:13.3g/(13.3g+100g)×100%≈11.7%;(4)根据表格判断硝酸
钾的溶解度随着温度的升高而增大,加水或升温将40℃的硝酸钾饱和溶液变为不饱和溶液。
15.小婷和小彤在帮助老师整理药品时,发现有四瓶失去标签的溶液,只知道它们分别是
氢氧化钙溶液、硫酸铜溶液、碳酸钠溶液和稀盐酸。小婷很快就判断出其中一瓶是硫酸铜
溶液。小彤把其他三种溶液分别编号成A、B、C,然后两两混合进行如下实验:
实验 A+B B+C A+C
现象 无明显现象 有白色沉淀产生 有气体产生
据此,小彤很快就分辨出了三种未知溶液。回答下列问题:
(1)小婷判断出硫酸铜溶液的依据是 。(2)C溶液中溶质的化学式是 。
(3)A与B反应的基本类型是 。 (4)B与C反应的化学方程式是 。
【答案】(1)硫酸铜溶液为蓝色,其他三种溶液为无色;(2)NaCO;(3)复分解反应;
2 3
6(4)NaCO + Ca(OH)=2NaOH + CaCO↓。
2 3 2 3
【解析】(1)根据材料判断D为硫酸铜溶液为蓝色,通过颜色可以判断;(2)根据表格反应现
象判断A. 稀盐酸HCl,B. 氢氧化钙溶液Ca(OH),C.碳酸钠溶液NaCO;(3)A与B反应:
2 2 3
2HCl+Ca(OH)=CaCl+2HO,属于复分解反应;(4)B与C反应:NaCO+Ca(OH)=
2 2 2 2 3 2
2NaOH+CaCO↓。
3
16.某同学为定量研究氢氧化钠溶液与盐酸反应,做了如下实验:取40g氢氧化钠溶液,
加入到50g溶质质量分数为7.3%的稀盐酸中,恰好完全反应。计算:
(1)氢氧化钠溶液中溶质的质量分数是 。
(2)反应后所得溶液中溶质的质量分数。(写出计算过程)
【答案】(1)10% ;(2)6.5%。
【解析】(1)10% (2分)
(2)解:设生成的氯化钠的质量为x
NaOH + HCl = NaCl + HO (1分)
2
36.5 58.5
50g×7.3% x (1分)
36.5/58.5=50g×7.3%/x
x=5.85g (1分)
反应后所得溶液中溶质的质量分数为:
5.85g/(40g+50g)×100%=6.5% (1分)
答:反应后所得溶液中溶质的质量分数为6.5%。。
七、实验与探究题(本大题共2小题,每空1分,共8分)
17.如图所示是几种实验室制取气体的发生装置和收集装置:
7回答下列问题:
(1)写出图中标有数字的仪器名称: 。
(2)实验室用石灰石和稀盐酸制取二氧化碳,发生装置可选用图中的 装置(填
字母序号),写出该反应的化学方程式: 。
(3)实验室用氯酸钾与二氧化锰制取氧气,若要使收集到的氧气较为纯净,最好选用图中的
装置进行收集(填字母序号)。
【答案】(1)试管;(2)B,CaCO+2HCl=CaCl+HO+CO↑;(3)E。
3 2 2 2
【解析】(1)①为试管;(2)实验室用石灰石和稀盐酸制取二氧化碳选用固+液常温型,选用B
装置,反应方程式:CaCO+2HCl=CaCl+HO+CO↑;(3)可以用E装置排水法收集较纯净的氧
3 2 2 2
气。
18.小亮学完合金后,知道了不锈钢的主要成分是铁,白铜中含有铜和镍(Ni)。他决定探
究Fe、Cu、Ni的金属活动性顺序。
(1)[查阅资料]镍能与稀硫酸反应生成能溶于水的NiSO,并放出氢气。写出镍与稀硫酸反
4
应的化学方程式: 。
(2)[猜想与假设]根据教材中常见金属的活动性顺序和查阅的资料,对以上三种金属
的活动性作出猜想:
猜想①Fe>Ni>Cu;猜想② 。
(3)[实验探究]把用砂纸打磨过的镍片浸入FeSO 溶液中,过一会儿取出,发现镍片
4
8表面无明显变化。证明 (填“猜想①”或“猜想②”)成立。
(4)[拓展延伸]用铜片、NiSO 溶液和 ,通过实验探究也能判断Fe、Cu、Ni
4
的金属活动性顺序。
【答案】(1)[查阅资料]Ni + HSO=NiSO + H↑;(2)[猜想与假设]Ni>Fe>Cu;(3)[实验
2 4 4 2
探究]猜想①;(4)[拓展延伸]铁片。
【解析】(1)[查阅资料]根据反应物和生成物判断反应方程式:Ni + HSO=NiSO + H↑;
2 4 4 2
(2)[猜想与假设]根据Ni可以与稀硫酸反应,说明Ni比Cu活泼,猜想②Ni>Fe>Cu;(3)
[实验探究]把用砂纸打磨过的镍片浸入FeSO 溶液中,过一会儿取出,发现镍片
4
表面无明显变化说明Fe比Ni活泼,猜想①成立;(4)[拓展延伸]用铜片、NiSO 溶液和铁片,
4
通过实验探究也能判断Fe、Cu、Ni的金属活动性顺序。
910