文档内容
五年(2021-2025)高考化学真题分类汇编
专题22 工艺流程综合题——分离、提纯类
考向 五年考情(2021-2025) 命题趋势
2025·安徽卷、2025·北京卷、2025·甘
肃卷、2025·河南卷、2025·黑吉辽蒙
工艺流程综合题选取的情境紧密联系
卷、2025·湖北卷、2025·山东卷、
与人类密切相关的生产生活实际,试
2025·陕晋青宁卷、2025·云南卷、 题的命制从情境素材开始,以学科素
2024·全国甲卷、2024·新课标卷、 养为目标导向,选取某个学科素养的
2024·安徽卷、2024·甘肃卷、2024·河 一个方面或几个方面,深入考查学生
分离、提纯类工艺流程
北卷、2024·湖南卷、2023·新课标卷、 学科素养的表现层次。利用科研前沿
综合题
2023·湖北卷、2023·辽宁卷、2023·福 和生产实际的真实情境,展现研究过
建卷、2023·广东卷、2023·河北卷、 程或者生成过程的具体实际问题,考
2022·湖南卷、2022·湖北卷、2022·重 查学生的探究与创新能力。主要分为
两大考查方向:一是分离、提纯类;
庆卷、2021·全国乙卷、2021·全国甲
二是原材料转化制备类。
卷、2021·河北卷、2021·湖南卷、
2021·广东卷
1.(2025·安徽卷)某含锶( )废渣主要含有 和 等,一种提取该废渣
中锶的流程如下图所示。
已知 时,
回答下列问题:
(1)锶位于元素周期表第五周期第ⅡA族。基态原子价电子排布式为 。
(2)“浸出液”中主要的金属离子有 、 (填离子符号)。
(3)“盐浸”中 转化反应的离子方程式为 ; 时,向 粉末中加入
溶液,充分反应后,理论上溶液中 (忽略溶
液体积的变化)。
(4)其他条件相同时,盐浸 ,浸出温度对锶浸出率的影响如图1所示。随温度升高锶浸出率增大的
原因是 。
1 / 25
学科网(北京)股份有限公司(5)“浸出渣2”中主要含有 、 (填化学式)。
(6)将窝穴体a(结构如图2所示)与 形成的超分子加入“浸出液”中,能提取其中的 ,原因是
。
(7)由 制备无水 的最优方法是 (填标号)。
a.加热脱水 b.在 气流中加热 c.常温加压 d.加热加压
2.(2025·北京卷)铅酸电池是用途广泛并不断发展的化学电源。
(1)十九世纪,铅酸电池工作原理初步形成并延续至今。
铅酸电池工作原理:
①充电时,阴极发生的电极反应为 。
②放电时,产生a库仑电量,消耗 的物质的量为 。已知:转移 电子所产生的电
量为96500库仑。
③ 作为电解质溶液性质稳定、有较强的导电能力, 参与电极反应并有利于保持
电压稳定。该体系中 不氧化 , 氧化性弱与其结构有关, 的空间结构是 。
④铅酸电池储存过程中,存在化学能的缓慢消耗: 电极在 作用下产生的 可将 电极氧
化。 氧化 发生反应的化学方程式为 。
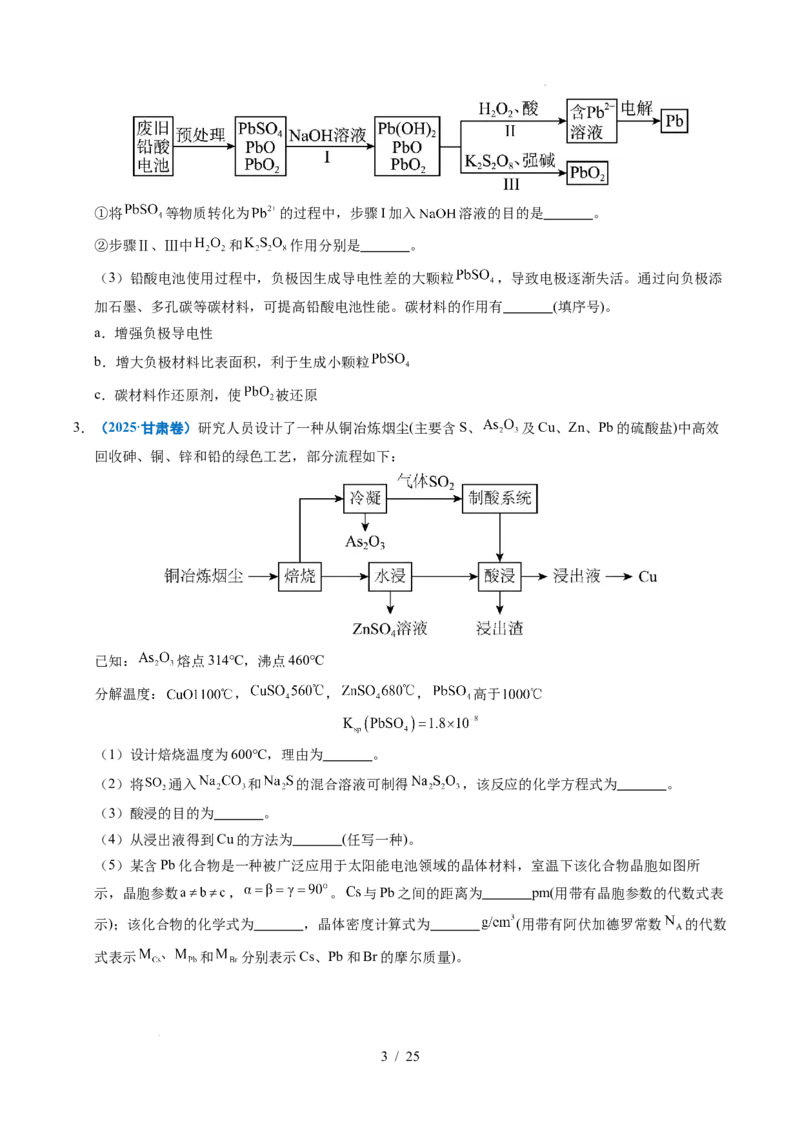
(2)随着铅酸电池广泛应用,需要回收废旧电池材料,实现资源的再利用。回收过程中主要物质的转
化关系示意图如下。
2 / 25
学科网(北京)股份有限公司①将 等物质转化为 的过程中,步骤I加入 溶液的目的是 。
②步骤Ⅱ、Ⅲ中 和 作用分别是 。
(3)铅酸电池使用过程中,负极因生成导电性差的大颗粒 ,导致电极逐渐失活。通过向负极添
加石墨、多孔碳等碳材料,可提高铅酸电池性能。碳材料的作用有 (填序号)。
a.增强负极导电性
b.增大负极材料比表面积,利于生成小颗粒
c.碳材料作还原剂,使 被还原
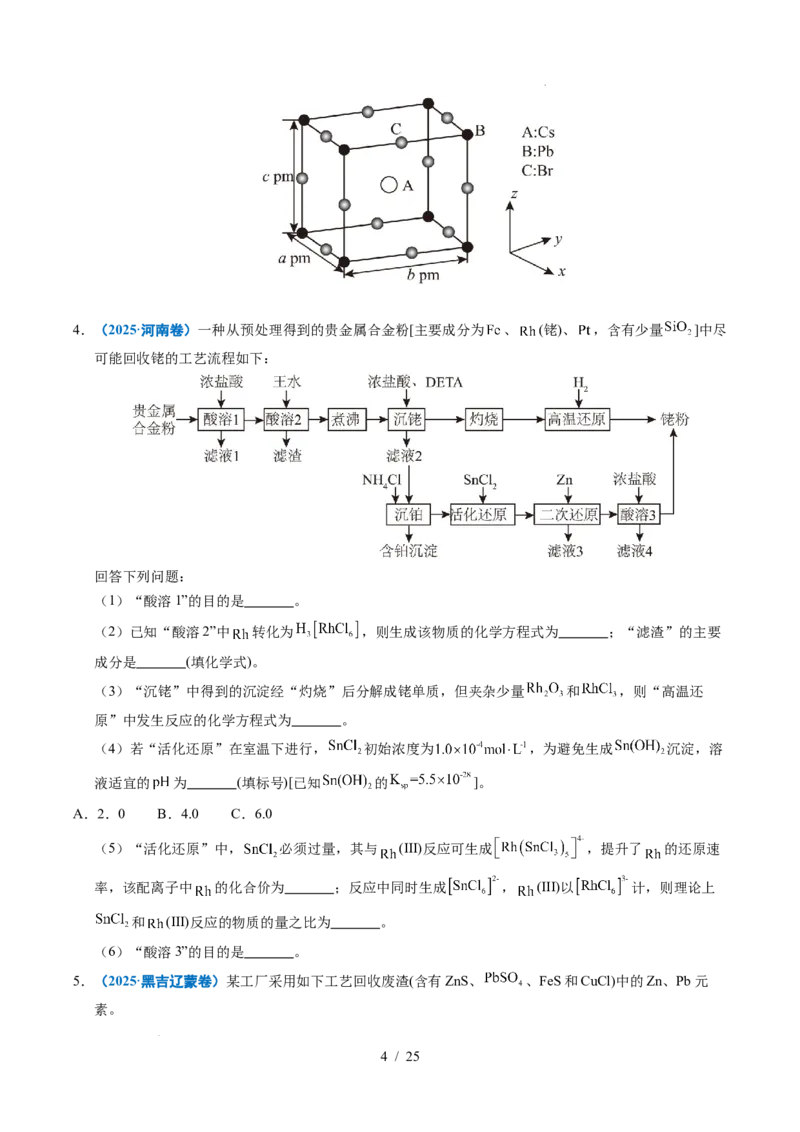
3.(2025·甘肃卷)研究人员设计了一种从铜冶炼烟尘(主要含S、 及Cu、Zn、Pb的硫酸盐)中高效
回收砷、铜、锌和铅的绿色工艺,部分流程如下:
已知: 熔点314℃,沸点460℃
分解温度: , , , 高于
(1)设计焙烧温度为600℃,理由为 。
(2)将 通入 和 的混合溶液可制得 ,该反应的化学方程式为 。
(3)酸浸的目的为 。
(4)从浸出液得到Cu的方法为 (任写一种)。
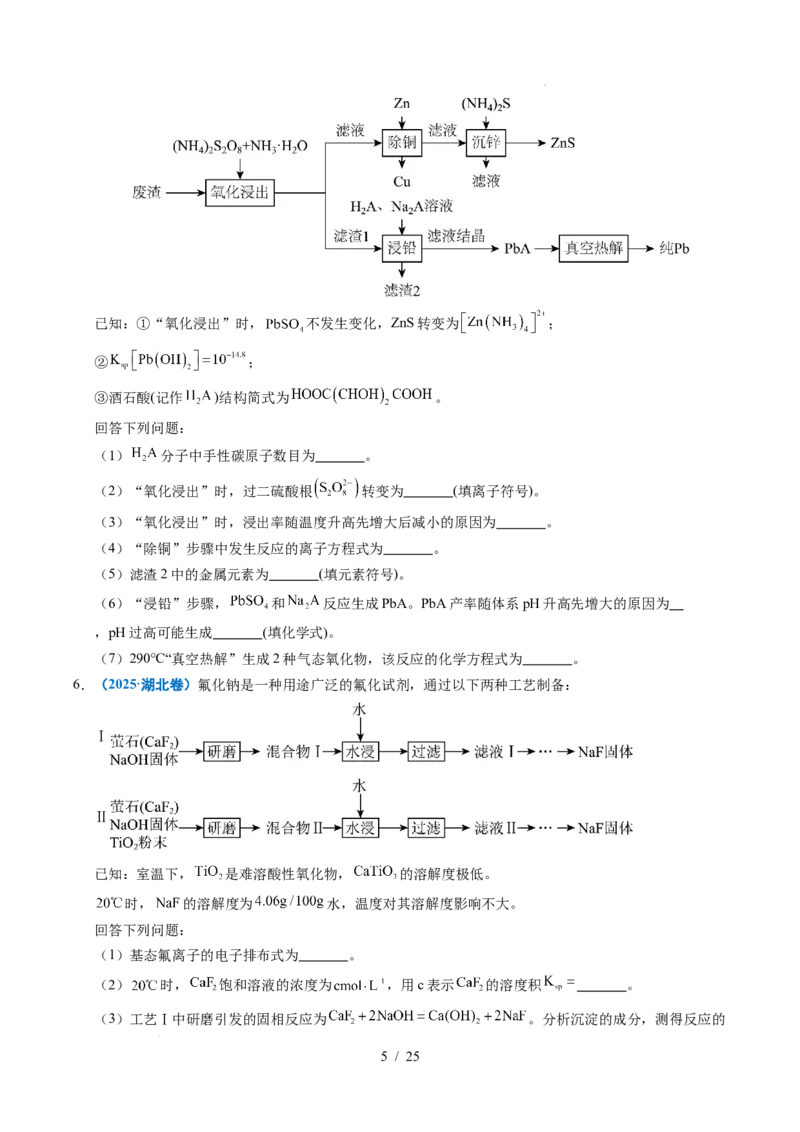
(5)某含Pb化合物是一种被广泛应用于太阳能电池领域的晶体材料,室温下该化合物晶胞如图所
示,晶胞参数 , 。 与Pb之间的距离为 pm(用带有晶胞参数的代数式表
示);该化合物的化学式为 ,晶体密度计算式为 (用带有阿伏加德罗常数 的代数
式表示 和 分别表示Cs、Pb和Br的摩尔质量)。
3 / 25
学科网(北京)股份有限公司4.(2025·河南卷)一种从预处理得到的贵金属合金粉[主要成分为 、 (铑)、 ,含有少量 ]中尽
可能回收铑的工艺流程如下:
回答下列问题:
(1)“酸溶1”的目的是 。
(2)已知“酸溶2”中 转化为 ,则生成该物质的化学方程式为 ;“滤渣”的主要
成分是 (填化学式)。
(3)“沉铑”中得到的沉淀经“灼烧”后分解成铑单质,但夹杂少量 和 ,则“高温还
原”中发生反应的化学方程式为 。
(4)若“活化还原”在室温下进行, 初始浓度为 ,为避免生成 沉淀,溶
液适宜的 为 (填标号)[已知 的 ]。
A.2.0 B.4.0 C.6.0
(5)“活化还原”中, 必须过量,其与 (III)反应可生成 ,提升了 的还原速
率,该配离子中 的化合价为 ;反应中同时生成 , (III)以 计,则理论上
和 (III)反应的物质的量之比为 。
(6)“酸溶3”的目的是 。
5.(2025·黑吉辽蒙卷)某工厂采用如下工艺回收废渣(含有ZnS、 、FeS和CuCl)中的Zn、Pb元
素。
4 / 25
学科网(北京)股份有限公司已知:①“氧化浸出”时, 不发生变化,ZnS转变为 ;
② ;
③酒石酸(记作 )结构简式为 。
回答下列问题:
(1) 分子中手性碳原子数目为 。
(2)“氧化浸出”时,过二硫酸根 转变为 (填离子符号)。
(3)“氧化浸出”时,浸出率随温度升高先增大后减小的原因为 。
(4)“除铜”步骤中发生反应的离子方程式为 。
(5)滤渣2中的金属元素为 (填元素符号)。
(6)“浸铅”步骤, 和 反应生成PbA。PbA产率随体系pH升高先增大的原因为
,pH过高可能生成 (填化学式)。
(7)290℃“真空热解”生成2种气态氧化物,该反应的化学方程式为 。
6.(2025·湖北卷)氟化钠是一种用途广泛的氟化试剂,通过以下两种工艺制备:
Ⅰ
Ⅱ
已知:室温下, 是难溶酸性氧化物, 的溶解度极低。
时, 的溶解度为 水,温度对其溶解度影响不大。
回答下列问题:
(1)基态氟离子的电子排布式为 。
(2) 时, 饱和溶液的浓度为 ,用c表示 的溶度积 。
(3)工艺Ⅰ中研磨引发的固相反应为 。分析沉淀的成分,测得反应的
5 / 25
学科网(北京)股份有限公司转化率为78%。水浸分离, 的产率仅为8%。
①工艺Ⅰ的固相反应 (填“正向”或“逆向”)进行程度大。
②分析以上产率变化,推测溶解度 (填“>”或“<”)
(4)工艺Ⅱ水浸后 的产率可达81%,写出工艺Ⅱ的总化学反应方程式 。
(5)从滤液Ⅱ获取 晶体的操作为 (填标号)。
a.蒸发至大量晶体析出,趁热过滤 b.蒸发至有晶膜出现后冷却结晶,过滤
(6)研磨能够促进固相反应的原因可能有 (填标号)。
a.增大反应物间的接触面积 b.破坏反应物的化学键
c.降低反应的活化能 d.研钵表面跟反应物更好接触
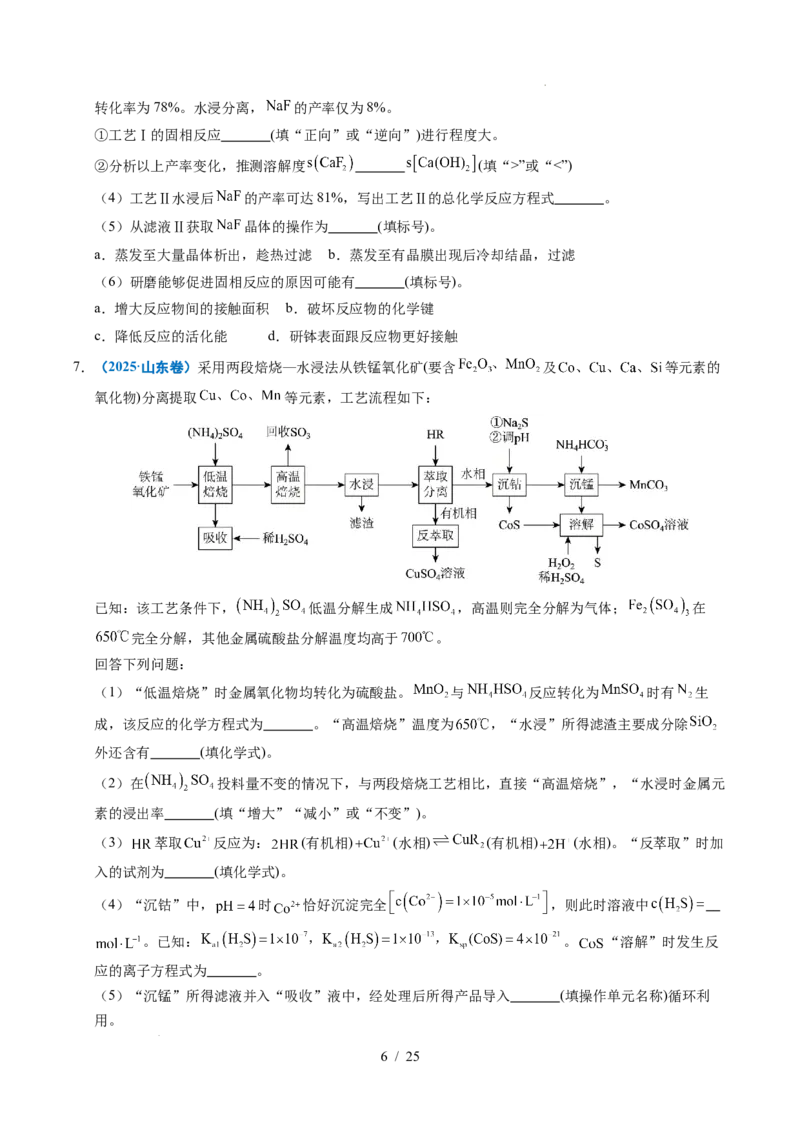
7.(2025·山东卷)采用两段焙烧—水浸法从铁锰氧化矿(要含 及 等元素的
氧化物)分离提取 等元素,工艺流程如下:
已知:该工艺条件下, 低温分解生成 ,高温则完全分解为气体; 在
完全分解,其他金属硫酸盐分解温度均高于 。
回答下列问题:
(1)“低温焙烧”时金属氧化物均转化为硫酸盐。 与 反应转化为 时有 生
成,该反应的化学方程式为 。“高温焙烧”温度为 ,“水浸”所得滤渣主要成分除
外还含有 (填化学式)。
(2)在 投料量不变的情况下,与两段焙烧工艺相比,直接“高温焙烧”,“水浸时金属元
素的浸出率 (填“增大”“减小”或“不变”)。
(3) 萃取 反应为: (有机相) (水相) (有机相) (水相)。“反萃取”时加
入的试剂为 (填化学式)。
(4)“沉钴”中, 时 恰好沉淀完全 ,则此时溶液中
。已知: 。 “溶解”时发生反
应的离子方程式为 。
(5)“沉锰”所得滤液并入“吸收”液中,经处理后所得产品导入 (填操作单元名称)循环利
用。
6 / 25
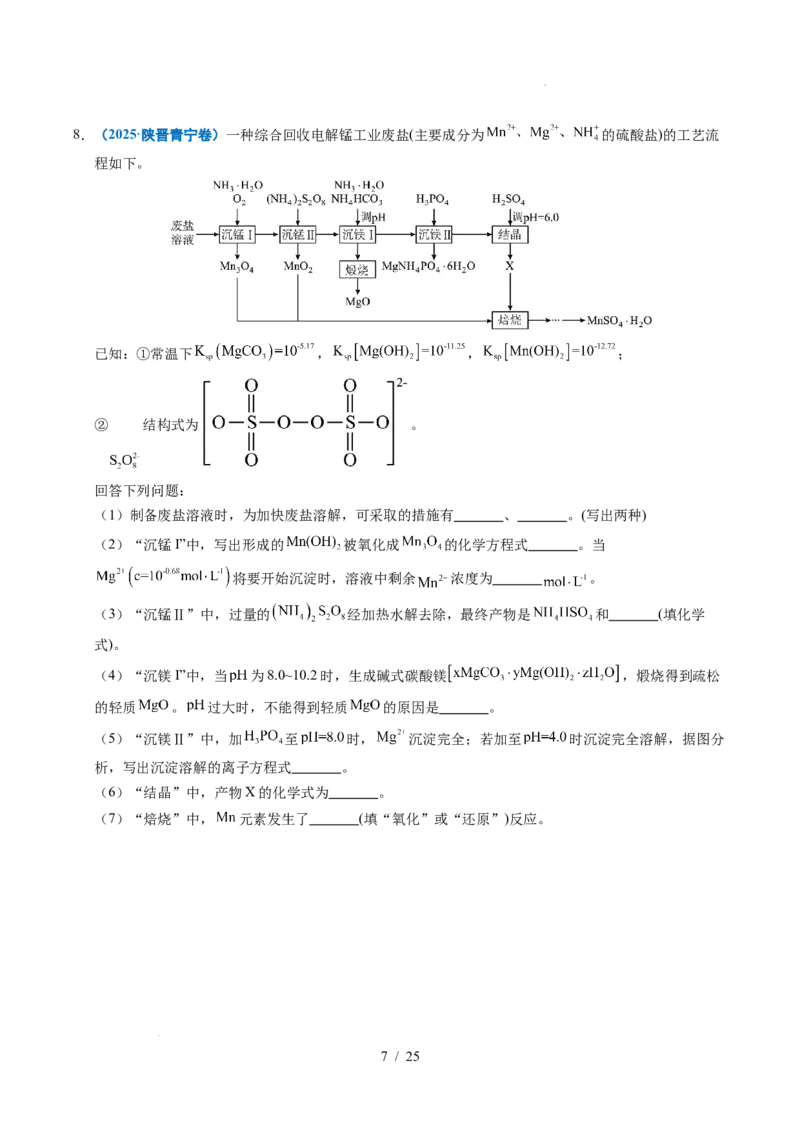
学科网(北京)股份有限公司8.(2025·陕晋青宁卷)一种综合回收电解锰工业废盐(主要成分为 的硫酸盐)的工艺流
程如下。
已知:①常温下 , , ;
② 结构式为 。
回答下列问题:
(1)制备废盐溶液时,为加快废盐溶解,可采取的措施有 、 。(写出两种)
(2)“沉锰I”中,写出形成的 被氧化成 的化学方程式 。当
将要开始沉淀时,溶液中剩余 浓度为 。
(3)“沉锰Ⅱ”中,过量的 经加热水解去除,最终产物是 和 (填化学
式)。
(4)“沉镁I”中,当 为8.0~10.2时,生成碱式碳酸镁 ,煅烧得到疏松
的轻质 。 过大时,不能得到轻质 的原因是 。
(5)“沉镁Ⅱ”中,加 至 时, 沉淀完全;若加至 时沉淀完全溶解,据图分
析,写出沉淀溶解的离子方程式 。
(6)“结晶”中,产物X的化学式为 。
(7)“焙烧”中, 元素发生了 (填“氧化”或“还原”)反应。
7 / 25
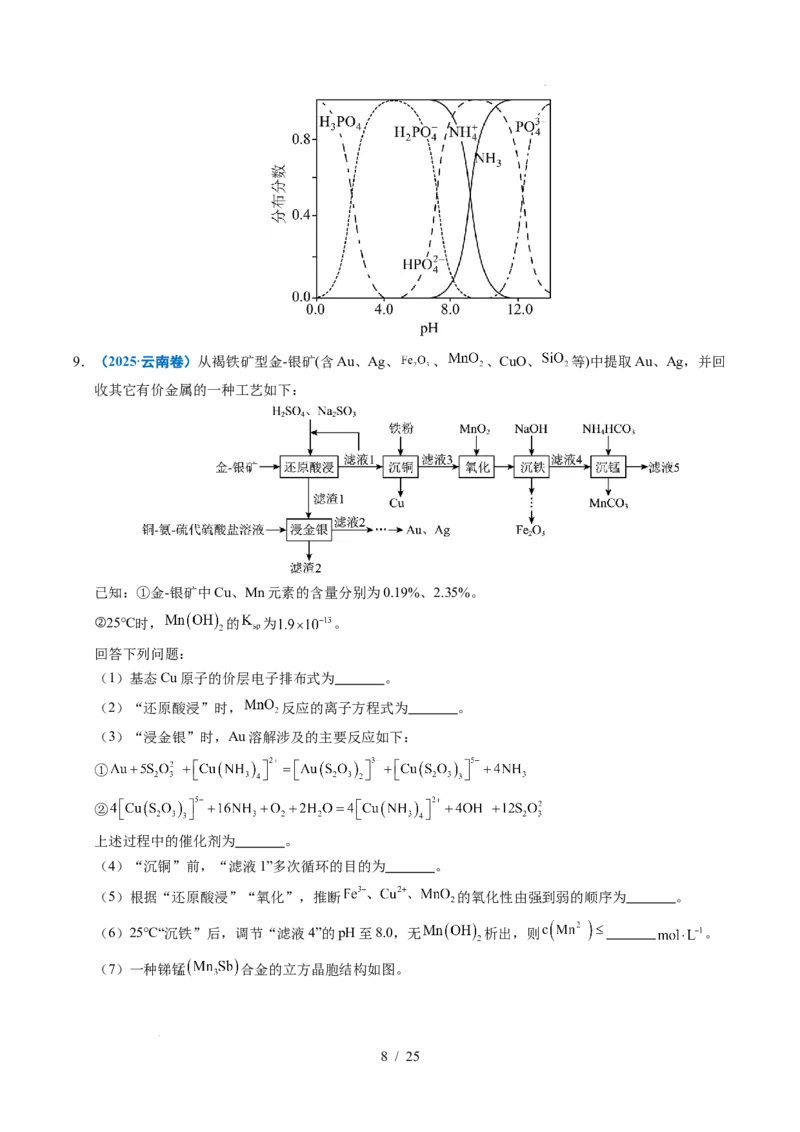
学科网(北京)股份有限公司9.(2025·云南卷)从褐铁矿型金-银矿(含Au、Ag、 、 、CuO、 等)中提取Au、Ag,并回
收其它有价金属的一种工艺如下:
已知:①金-银矿中Cu、Mn元素的含量分别为0.19%、2.35%。
②25℃时, 的 为 。
回答下列问题:
(1)基态Cu原子的价层电子排布式为 。
(2)“还原酸浸”时, 反应的离子方程式为 。
(3)“浸金银”时,Au溶解涉及的主要反应如下:
①
②
上述过程中的催化剂为 。
(4)“沉铜”前,“滤液1”多次循环的目的为 。
(5)根据“还原酸浸”“氧化”,推断 的氧化性由强到弱的顺序为 。
(6)25℃“沉铁”后,调节“滤液4”的pH至8.0,无 析出,则 。
(7)一种锑锰 合金的立方晶胞结构如图。
8 / 25
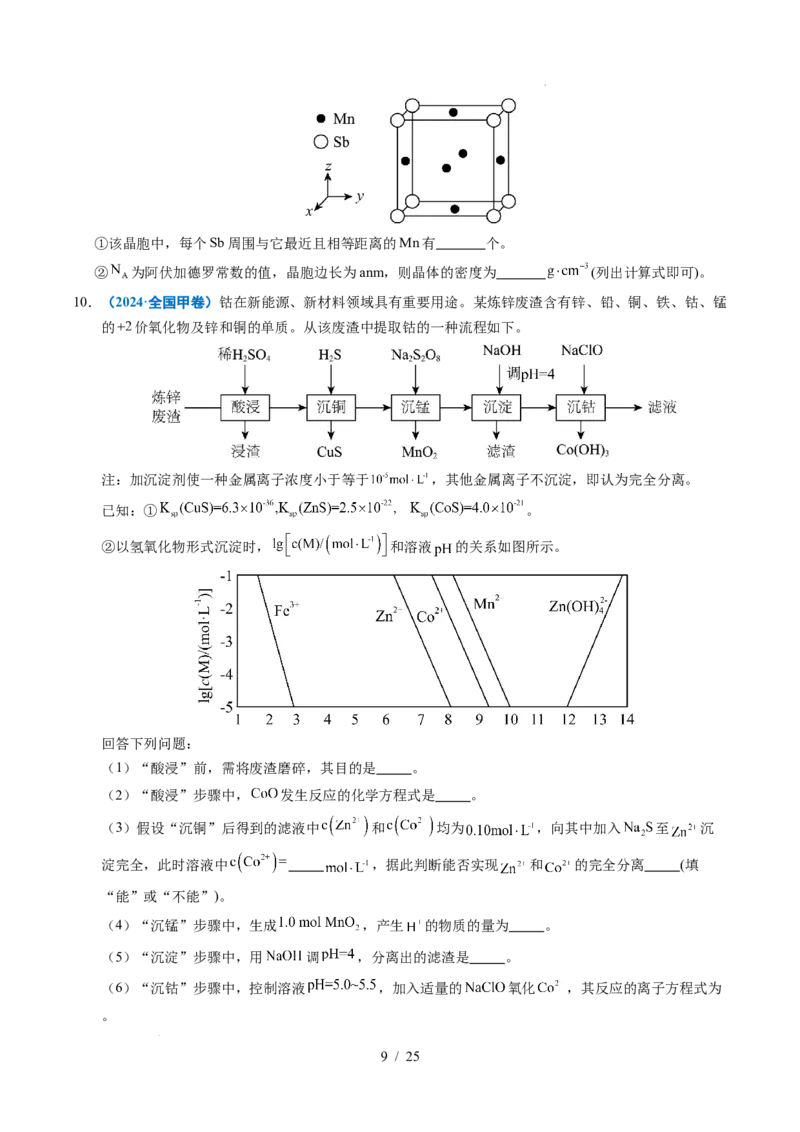
学科网(北京)股份有限公司①该晶胞中,每个Sb周围与它最近且相等距离的Mn有 个。
② 为阿伏加德罗常数的值,晶胞边长为anm,则晶体的密度为 (列出计算式即可)。
10.(2024·全国甲卷)钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰
的 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
注:加沉淀剂使一种金属离子浓度小于等于 ,其他金属离子不沉淀,即认为完全分离。
已知:① 。
②以氢氧化物形式沉淀时, 和溶液 的关系如图所示。
回答下列问题:
(1)“酸浸”前,需将废渣磨碎,其目的是 。
(2)“酸浸”步骤中, 发生反应的化学方程式是 。
(3)假设“沉铜”后得到的滤液中 和 均为 ,向其中加入 至 沉
淀完全,此时溶液中 ,据此判断能否实现 和 的完全分离 (填
“能”或“不能”)。
(4)“沉锰”步骤中,生成 ,产生 的物质的量为 。
(5)“沉淀”步骤中,用 调 ,分离出的滤渣是 。
(6)“沉钴”步骤中,控制溶液 ,加入适量的 氧化 ,其反应的离子方程式为
。
9 / 25
学科网(北京)股份有限公司(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是 。
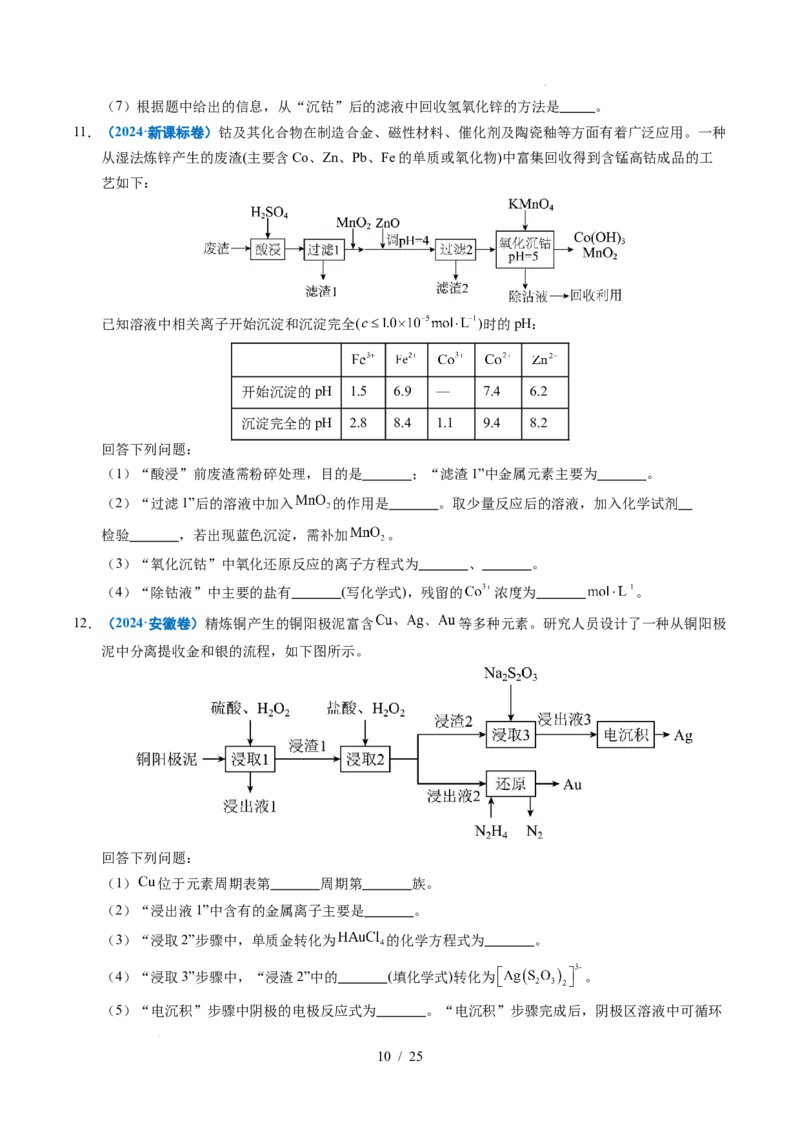
11.(2024·新课标卷)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广泛应用。一种
从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成品的工
艺如下:
已知溶液中相关离子开始沉淀和沉淀完全( )时的pH:
开始沉淀的pH 1.5 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
回答下列问题:
(1)“酸浸”前废渣需粉碎处理,目的是 ;“滤渣1”中金属元素主要为 。
(2)“过滤1”后的溶液中加入 的作用是 。取少量反应后的溶液,加入化学试剂
检验 ,若出现蓝色沉淀,需补加 。
(3)“氧化沉钴”中氧化还原反应的离子方程式为 、 。
(4)“除钴液”中主要的盐有 (写化学式),残留的 浓度为 。
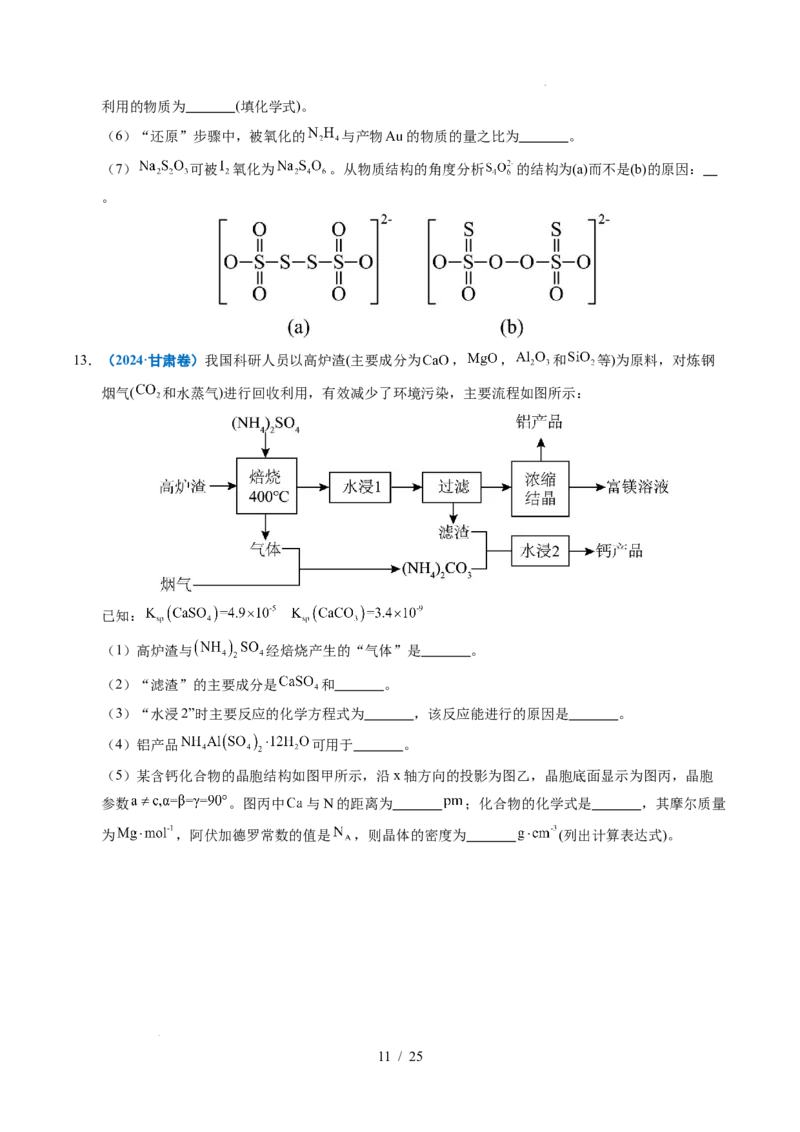
12.(2024·安徽卷)精炼铜产生的铜阳极泥富含 等多种元素。研究人员设计了一种从铜阳极
泥中分离提收金和银的流程,如下图所示。
回答下列问题:
(1) 位于元素周期表第 周期第 族。
(2)“浸出液1”中含有的金属离子主要是 。
(3)“浸取2”步骤中,单质金转化为 的化学方程式为 。
(4)“浸取3”步骤中,“浸渣2”中的 (填化学式)转化为 。
(5)“电沉积”步骤中阴极的电极反应式为 。“电沉积”步骤完成后,阴极区溶液中可循环
10 / 25
学科网(北京)股份有限公司利用的物质为 (填化学式)。
(6)“还原”步骤中,被氧化的 与产物 的物质的量之比为 。
(7) 可被 氧化为 。从物质结构的角度分析 的结构为(a)而不是(b)的原因:
。
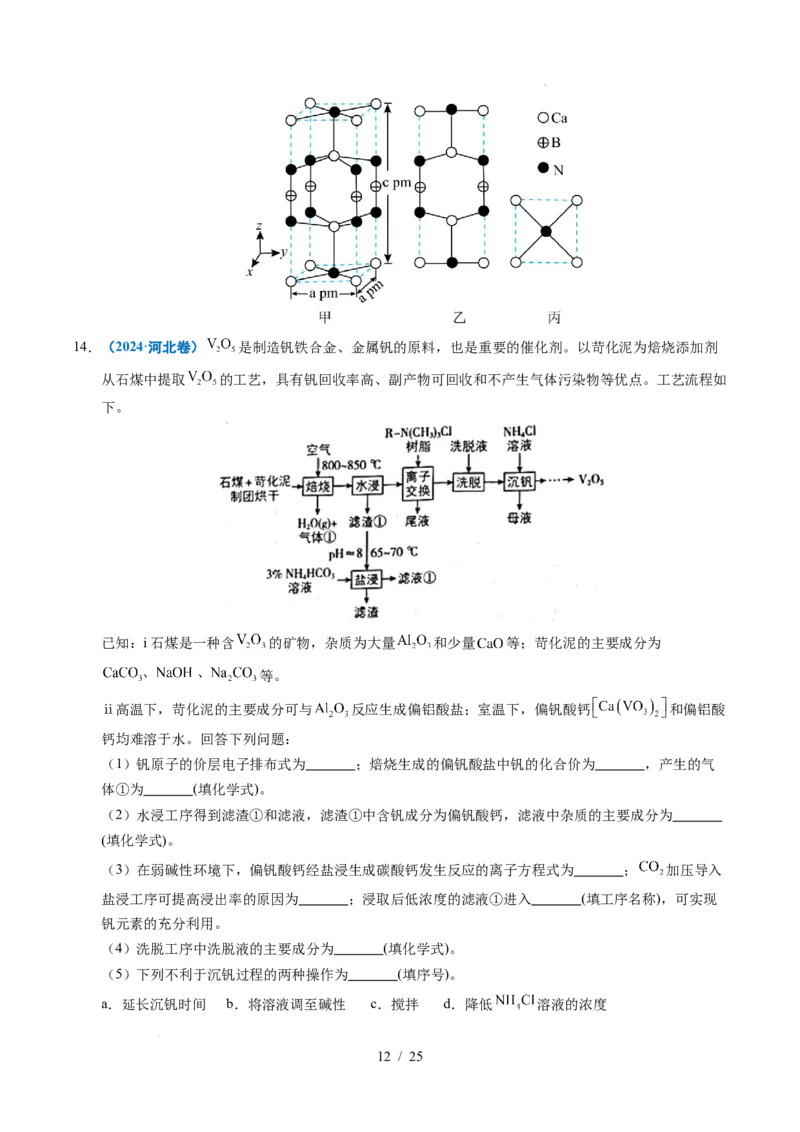
13.(2024·甘肃卷)我国科研人员以高炉渣(主要成分为 , , 和 等)为原料,对炼钢
烟气( 和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:
已知:
(1)高炉渣与 经焙烧产生的“气体”是 。
(2)“滤渣”的主要成分是 和 。
(3)“水浸2”时主要反应的化学方程式为 ,该反应能进行的原因是 。
(4)铝产品 可用于 。
(5)某含钙化合物的晶胞结构如图甲所示,沿x轴方向的投影为图乙,晶胞底面显示为图丙,晶胞
参数 。图丙中 与N的距离为 ;化合物的化学式是 ,其摩尔质量
为 ,阿伏加德罗常数的值是 ,则晶体的密度为 (列出计算表达式)。
11 / 25
学科网(北京)股份有限公司14.(2024·河北卷) 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添加剂
从石煤中提取 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程如
下。
已知:i石煤是一种含 的矿物,杂质为大量 和少量 等;苛化泥的主要成分为
等。
ⅱ高温下,苛化泥的主要成分可与 反应生成偏铝酸盐;室温下,偏钒酸钙 和偏铝酸
钙均难溶于水。回答下列问题:
(1)钒原子的价层电子排布式为 ;焙烧生成的偏钒酸盐中钒的化合价为 ,产生的气
体①为 (填化学式)。
(2)水浸工序得到滤渣①和滤液,滤渣①中含钒成分为偏钒酸钙,滤液中杂质的主要成分为
(填化学式)。
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙发生反应的离子方程式为 ; 加压导入
盐浸工序可提高浸出率的原因为 ;浸取后低浓度的滤液①进入 (填工序名称),可实现
钒元素的充分利用。
(4)洗脱工序中洗脱液的主要成分为 (填化学式)。
(5)下列不利于沉钒过程的两种操作为 (填序号)。
a.延长沉钒时间 b.将溶液调至碱性 c.搅拌 d.降低 溶液的浓度
12 / 25
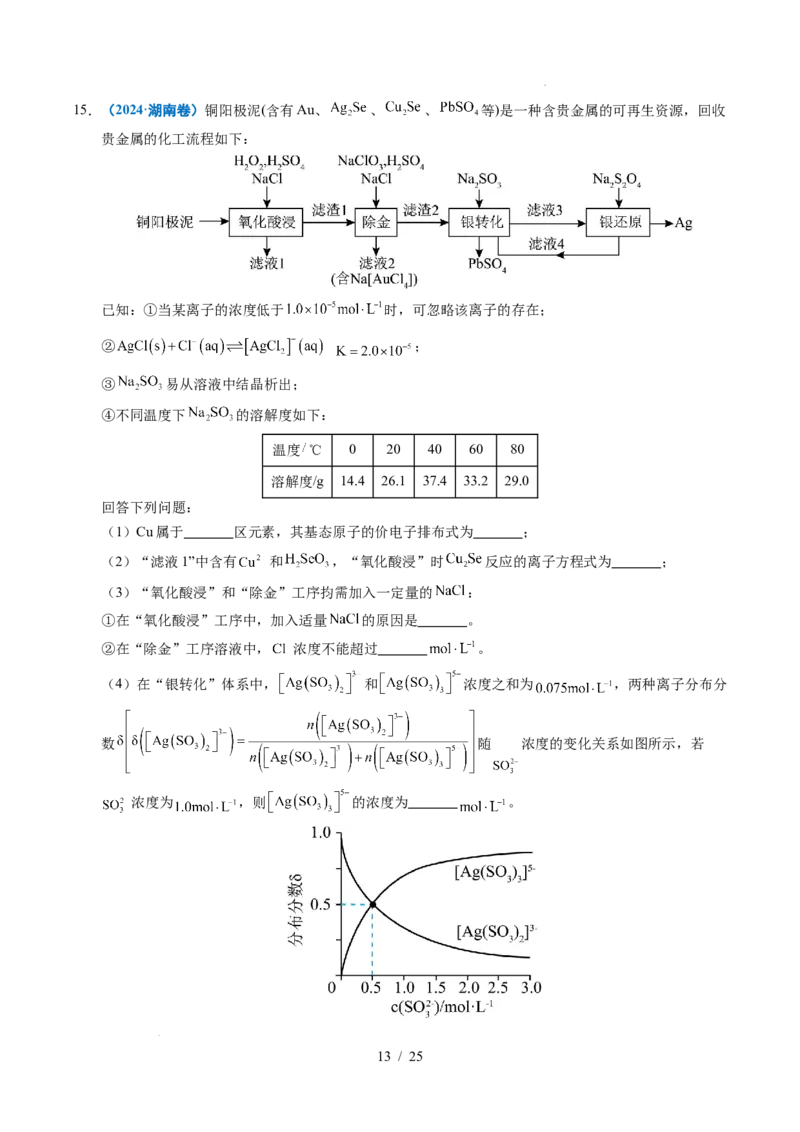
学科网(北京)股份有限公司15.(2024·湖南卷)铜阳极泥(含有Au、 、 、 等)是一种含贵金属的可再生资源,回收
贵金属的化工流程如下:
已知:①当某离子的浓度低于 时,可忽略该离子的存在;
② ;
③ 易从溶液中结晶析出;
④不同温度下 的溶解度如下:
温度 ℃ 0 20 40 60 80
溶解度/g 14.4 26.1 37.4 33.2 29.0
回答下列问题:
(1)Cu属于 区元素,其基态原子的价电子排布式为 ;
(2)“滤液1”中含有 和 ,“氧化酸浸”时 反应的离子方程式为 ;
(3)“氧化酸浸”和“除金”工序抣需加入一定量的 :
①在“氧化酸浸”工序中,加入适量 的原因是 。
②在“除金”工序溶液中, 浓度不能超过 。
(4)在“银转化”体系中, 和 浓度之和为 ,两种离子分布分
数 随 浓度的变化关系如图所示,若
浓度为 ,则 的浓度为 。
13 / 25
学科网(北京)股份有限公司(5)滤液4中溶质主要成分为 (填化学式);在连续生产的模式下,“银转化”和“银还原”
工序需在 ℃左右进行,若反应温度过高,将难以实现连续生产,原因是 。
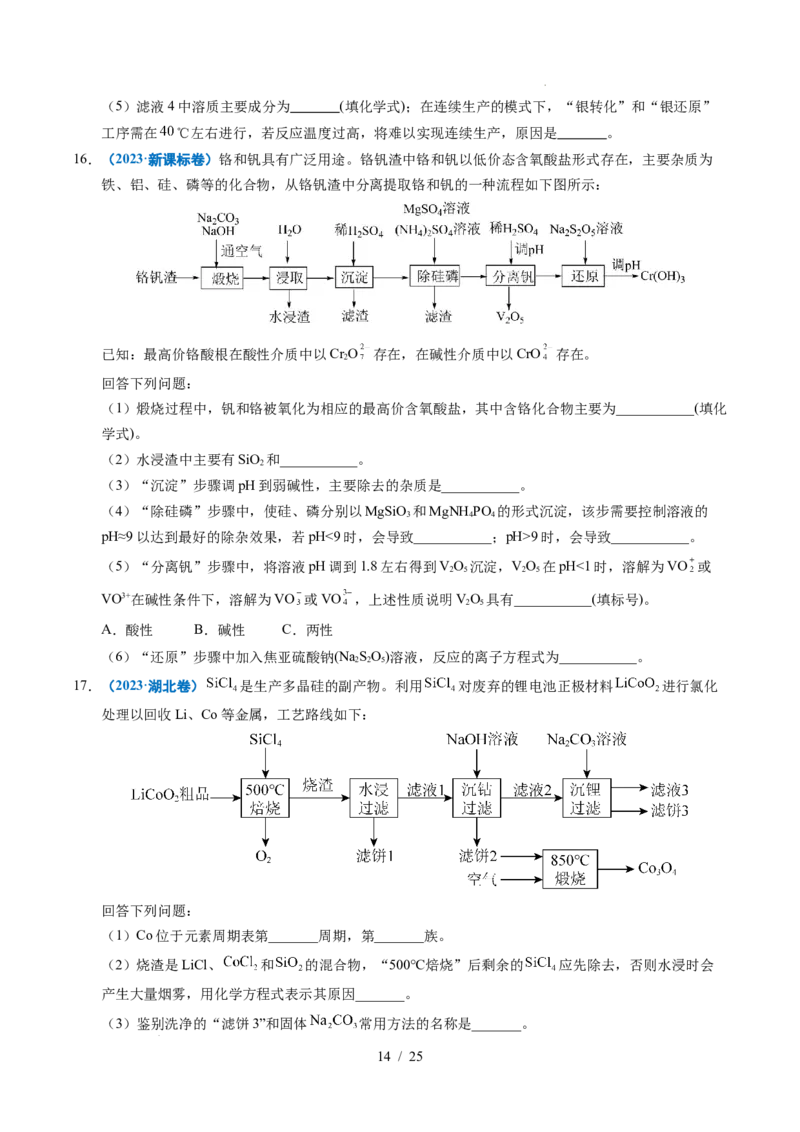
16.(2023·新课标卷)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为
铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________(填化
学式)。
(2)水浸渣中主要有SiO 和___________。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控制溶液的
3 4 4
pH≈9以达到最好的除杂效果,若pH<9时,会导致___________;pH>9时,会导致___________。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解为VO 或
2 5 2 5
VO3+在碱性条件下,溶解为VO 或VO ,上述性质说明VO 具有___________(填标号)。
2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为___________。
2 2 5
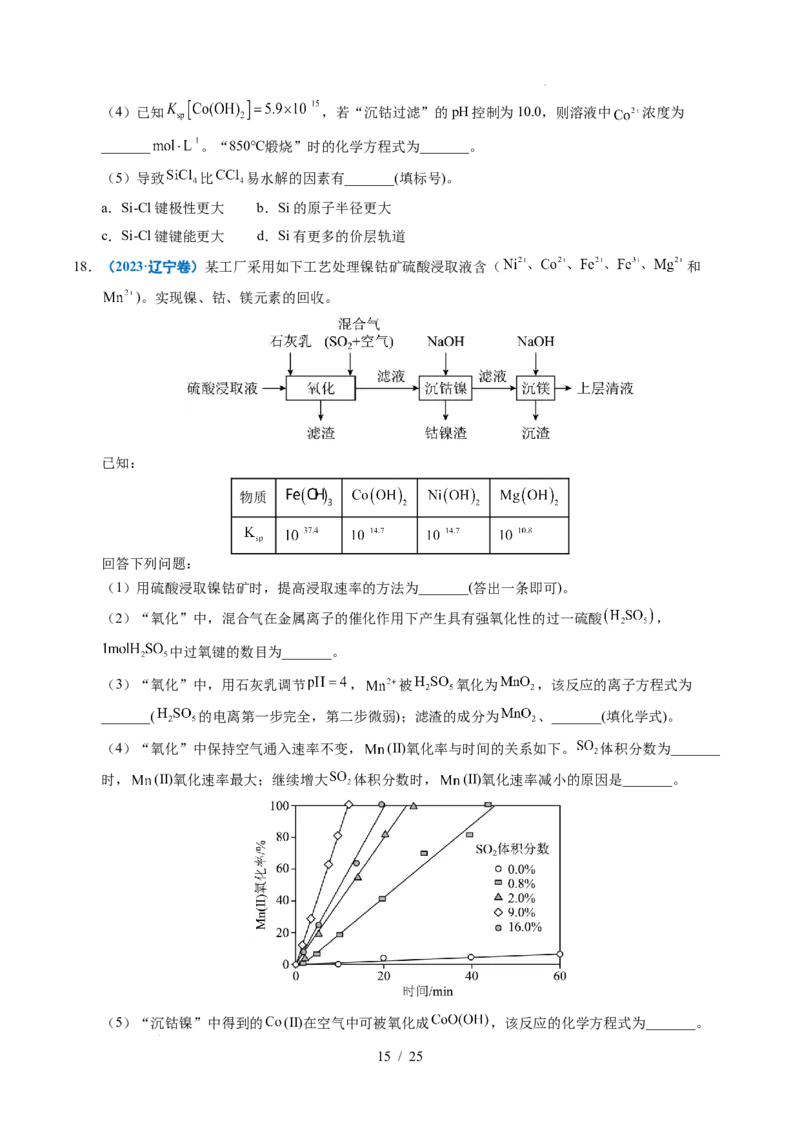
17.(2023·湖北卷) 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料 进行氯化
处理以回收Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第_______周期,第_______族。
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会
产生大量烟雾,用化学方程式表示其原因_______。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是_______。
14 / 25
学科网(北京)股份有限公司(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
_______ 。“850℃煅烧”时的化学方程式为_______。
(5)导致 比 易水解的因素有_______(填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
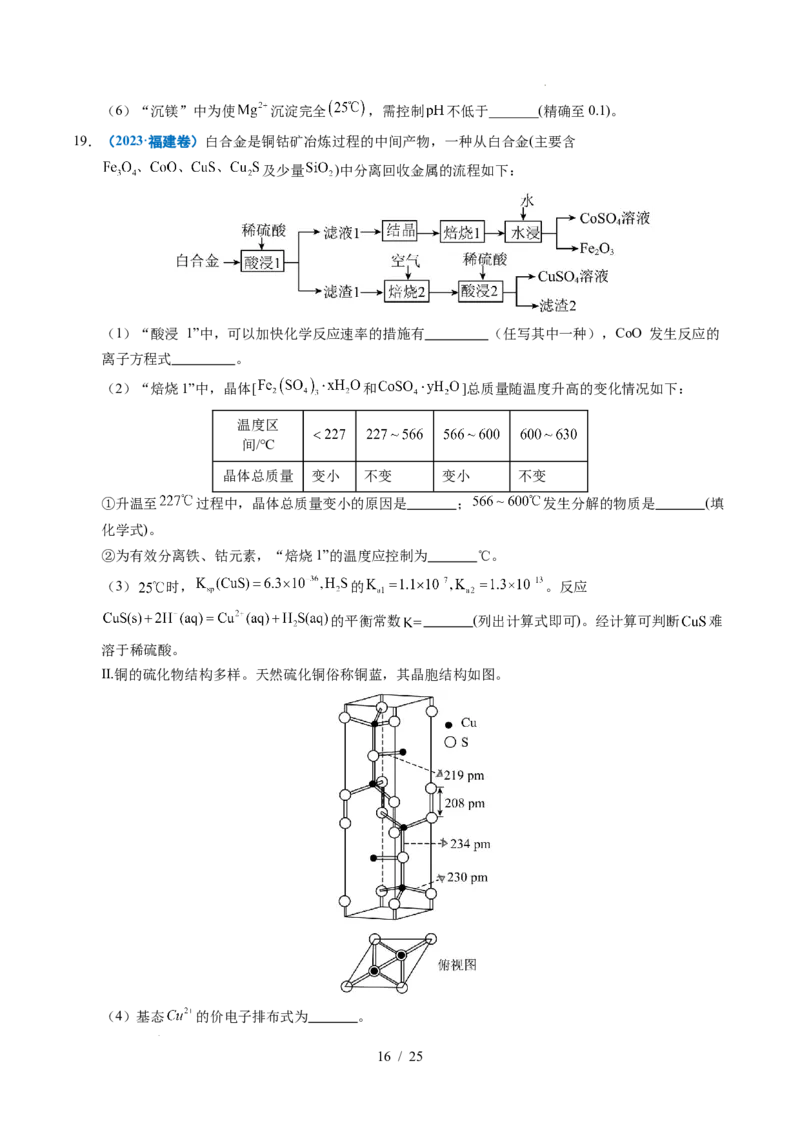
18.(2023·辽宁卷)某工厂采用如下工艺处理镍钴矿硫酸浸取液含( 和
)。实现镍、钴、镁元素的回收。
已知:
物质
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_______(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸 ,
中过氧键的数目为_______。
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为
_______( 的电离第一步完全,第二步微弱);滤渣的成分为 、_______(填化学式)。
(4)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如下。 体积分数为_______
时, (Ⅱ)氧化速率最大;继续增大 体积分数时, (Ⅱ)氧化速率减小的原因是_______。
(5)“沉钴镍”中得到的 (Ⅱ)在空气中可被氧化成 ,该反应的化学方程式为_______。
15 / 25
学科网(北京)股份有限公司(6)“沉镁”中为使 沉淀完全 ,需控制 不低于_______(精确至0.1)。
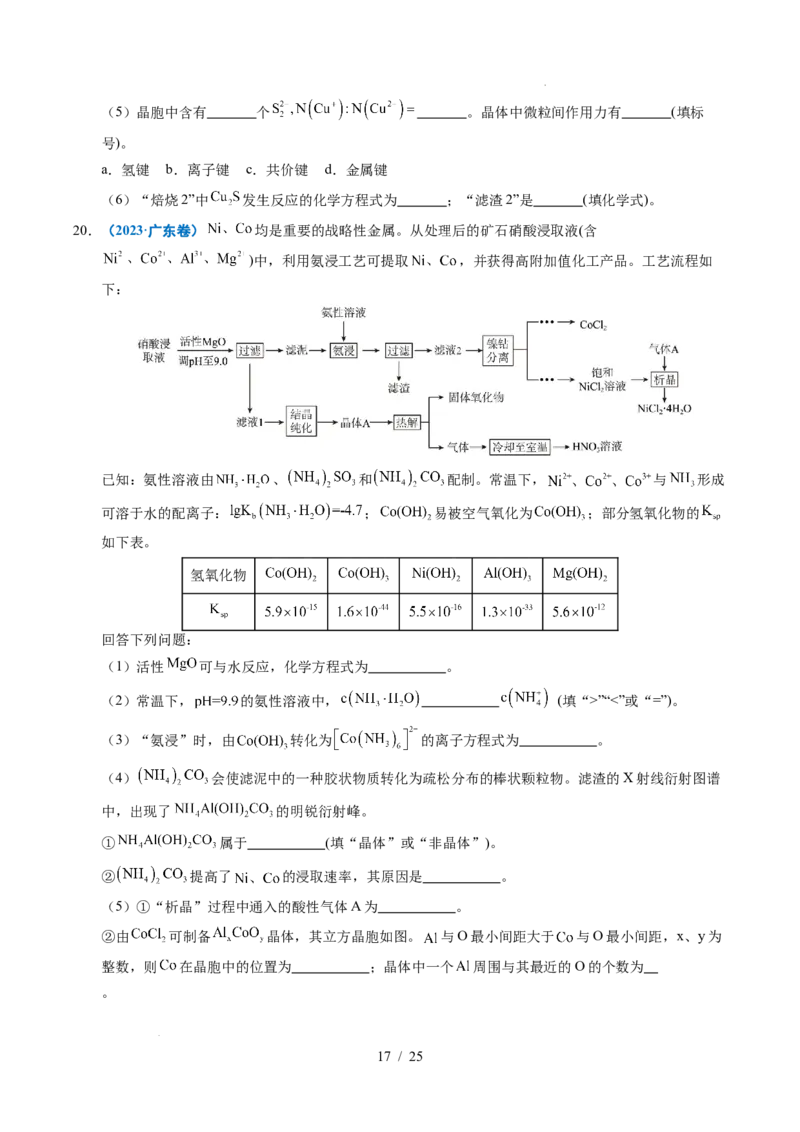
19.(2023·福建卷)白合金是铜钴矿冶炼过程的中间产物,一种从白合金(主要含
及少量 )中分离回收金属的流程如下:
(1)“酸浸 1”中,可以加快化学反应速率的措施有 (任写其中一种),CoO 发生反应的
离子方程式 。
(2)“焙烧1”中,晶体[ 和 ]总质量随温度升高的变化情况如下:
温度区
间/℃
晶体总质量 变小 不变 变小 不变
①升温至 过程中,晶体总质量变小的原因是 ; 发生分解的物质是 (填
化学式)。
②为有效分离铁、钴元素,“焙烧1”的温度应控制为 ℃。
(3) 时, 的 。反应
的平衡常数 (列出计算式即可)。经计算可判断 难
溶于稀硫酸。
II.铜的硫化物结构多样。天然硫化铜俗称铜蓝,其晶胞结构如图。
(4)基态 的价电子排布式为 。
16 / 25
学科网(北京)股份有限公司(5)晶胞中含有 个 。晶体中微粒间作用力有 (填标
号)。
a.氢键 b.离子键 c.共价键 d.金属键
(6)“焙烧2”中 发生反应的化学方程式为 ;“滤渣2”是 (填化学式)。
20.(2023·广东卷) 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含
)中,利用氨浸工艺可提取 ,并获得高附加值化工产品。工艺流程如
下:
已知:氨性溶液由 、 和 配制。常温下, 与 形成
可溶于水的配离子: ; 易被空气氧化为 ;部分氢氧化物的
如下表。
氢氧化物
回答下列问题:
(1)活性 可与水反应,化学方程式为 。
(2)常温下, 的氨性溶液中, (填“>”“<”或“=”)。
(3)“氨浸”时,由 转化为 的离子方程式为 。
(4) 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱
中,出现了 的明锐衍射峰。
① 属于 (填“晶体”或“非晶体”)。
② 提高了 的浸取速率,其原因是 。
(5)①“析晶”过程中通入的酸性气体A为 。
②由 可制备 晶体,其立方晶胞如图。 与O最小间距大于 与O最小间距,x、y为
整数,则 在晶胞中的位置为 ;晶体中一个 周围与其最近的O的个数为
。
17 / 25
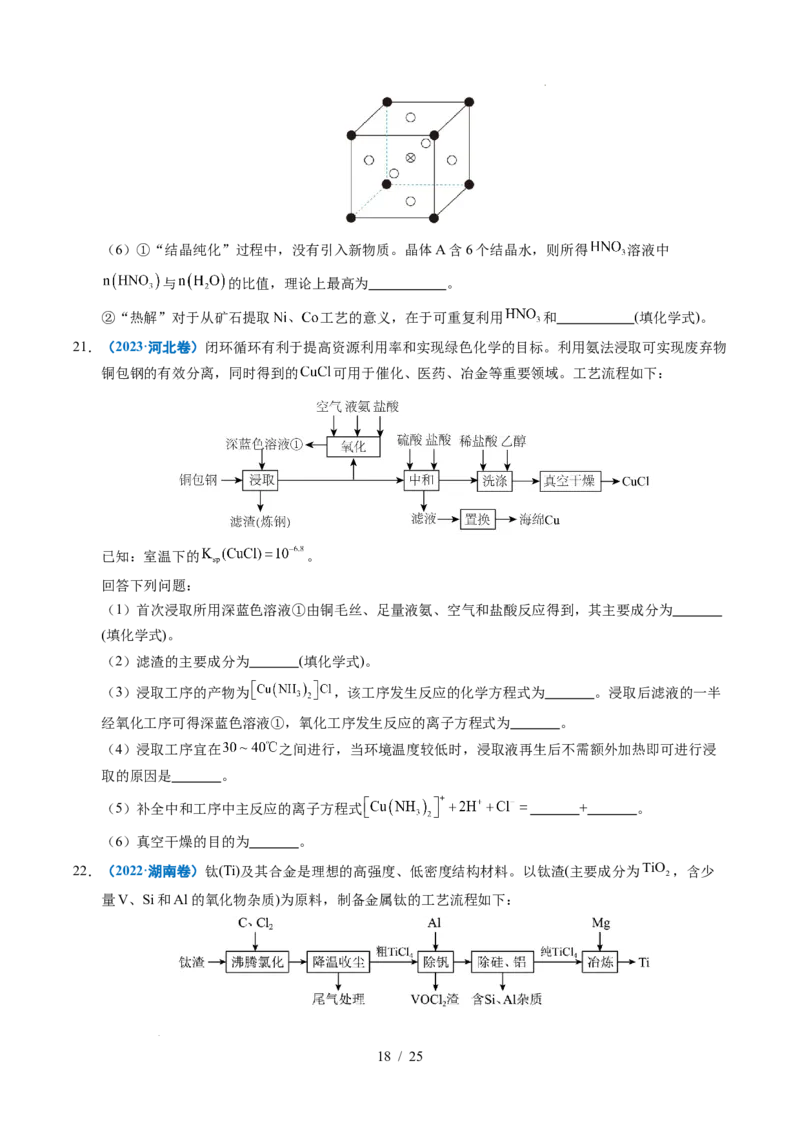
学科网(北京)股份有限公司(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得 溶液中
与 的比值,理论上最高为 。
②“热解”对于从矿石提取 工艺的意义,在于可重复利用 和 (填化学式)。
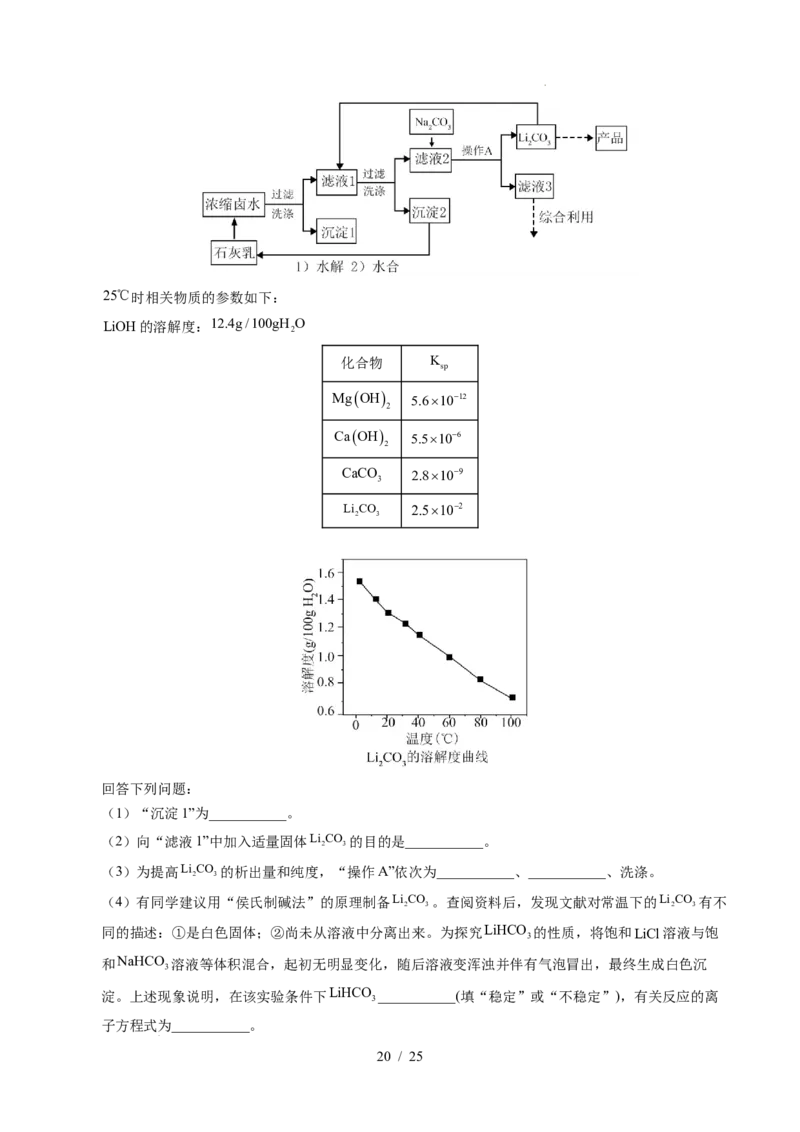
21.(2023·河北卷)闭环循环有利于提高资源利用率和实现绿色化学的目标。利用氨法浸取可实现废弃物
铜包钢的有效分离,同时得到的 可用于催化、医药、冶金等重要领域。工艺流程如下:
已知:室温下的 。
回答下列问题:
(1)首次浸取所用深蓝色溶液①由铜毛丝、足量液氨、空气和盐酸反应得到,其主要成分为
(填化学式)。
(2)滤渣的主要成分为 (填化学式)。
(3)浸取工序的产物为 ,该工序发生反应的化学方程式为 。浸取后滤液的一半
经氧化工序可得深蓝色溶液①,氧化工序发生反应的离子方程式为 。
(4)浸取工序宜在 之间进行,当环境温度较低时,浸取液再生后不需额外加热即可进行浸
取的原因是 。
(5)补全中和工序中主反应的离子方程式 + 。
(6)真空干燥的目的为 。
22.(2022·湖南卷)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为TiO ,含少
2
量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
18 / 25
学科网(北京)股份有限公司已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(1)已知ΔG=ΔH-TΔS,ΔG的值只决定于反应体系的始态和终态,忽略ΔH、ΔS随温度的变化。若
ΔG<0,则该反应可以自发进行。根据下图判断:600℃时,下列反应不能自发进行的是_______。
A.C(s)O (g)CO (g)
2 2
B.2C(s)O (g)2CO(g)
2
C.TiO (s)2Cl (g)TiCl (g)O (g)
2 2 4 2
D.TiO (s)C(s)2Cl (g)TiCl (g)CO (g)
2 2 4 2
(2)TiO 与C、Cl ,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
2 2
物质 TiCl CO CO Cl
4 2 2
分压MPa 4.59102 1.84102 3.70102 5.98109
①该温度下,TiO 与C、Cl 反应的总化学方程式为_______;
2 2
②随着温度升高,尾气中CO的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离TiCl
4
中含Si、Al杂质的
方法是_______。
(4)“除钒”和“除硅、铝”的顺序_______(填“能”或“不能”)交换,理由是_______。
(5)下列金属冶炼方法与本工艺流程中加入Mg冶炼Ti的方法相似的是_______。
A.高炉炼铁 B.电解熔融氯化钠制钠
C.铝热反应制锰D.氧化汞分解制汞
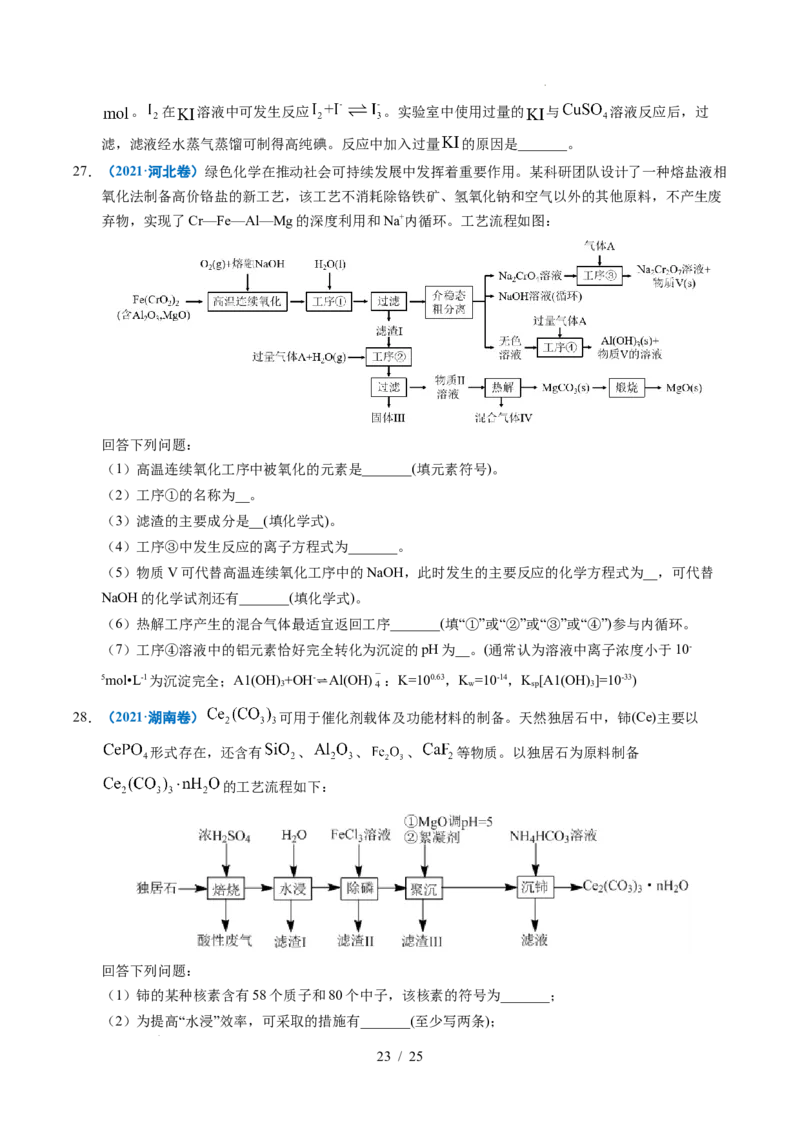
23.(2022·湖北卷)全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重视。某兴趣小组取盐湖水
进行浓缩和初步除杂后,得到浓缩卤水(含有Na+、Li+、Cl-和少量Mg2+、Ca2+),并设计了以下流程通
过制备碳酸锂来提取锂。
19 / 25
学科网(北京)股份有限公司25℃时相关物质的参数如下:
LiOH的溶解度:12.4g/100gH O
2
化合物 K
sp
MgOH 5.61012
2
CaOH 5.5106
2
CaCO 2.8109
3
Li CO 2.5102
2 3
回答下列问题:
(1)“沉淀1”为___________。
(2)向“滤液1”中加入适量固体Li CO 的目的是___________。
2 3
(3)为提高Li CO 的析出量和纯度,“操作A”依次为___________、___________、洗涤。
2 3
(4)有同学建议用“侯氏制碱法”的原理制备Li CO 。查阅资料后,发现文献对常温下的Li CO 有不
2 3 2 3
同的描述:①是白色固体;②尚未从溶液中分离出来。为探究LiHCO 的性质,将饱和LiCl溶液与饱
3
和NaHCO 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉
3
淀。上述现象说明,在该实验条件下LiHCO ___________(填“稳定”或“不稳定”),有关反应的离
3
子方程式为___________。
20 / 25
学科网(北京)股份有限公司(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入Na CO 改为通入CO 。这一改动能
2 3 2
否达到相同的效果,作出你的判断并给出理由___________。
24.(2022·重庆卷)电子印制工业产生的某退锡废液含硝酸、锡化合物及少量Fe3+和Cu2+等,对其处理
的流程如图。
Sn与Si同族,25℃时相关的溶度积见表。
化学式 Sn(OH)(或SnO ·2H O) Fe(OH) Cu(OH)
4 2 2 3 2
溶度积 1.0×10-56 4×10-38 2.5×10-20
(1)NaSnO 的回收
2 3
①产品NaSnO 中Sn的化合价是______。
2 3
②退锡工艺是利用稀HNO 与Sn反应生成Sn2+,且无气体生成,则生成的硝酸盐是_____,废液中的
3
Sn2+易转化成SnO ·xH O。
2 2
③沉淀1的主要成分是SnO ,焙烧时,与NaOH反应的化学方程式为______。
2
(2)滤液1的处理
①滤液1中Fe3+和Cu2+的浓度相近,加入NaOH溶液,先得到的沉淀是______。
②25℃时,为了使Cu2+沉淀完全,需调节溶液H+浓度不大于______mol•L-1。
(3)产品中锡含量的测定
称取产品1.500g,用大量盐酸溶解,在CO 保护下,先用Al片将Sn4+还原为Sn2+,再用
2
0.1000mol•L-1KIO 标准溶液滴定,以淀粉作指示剂滴定过程中IO 被还原为I—,终点时消耗KIO 溶液
3 3
20.00mL。
①终点时的现象为______,产生I 的离子反应方程式为_____。
2
②产品中Sn的质量分数为_____%。
25.(2021·全国乙卷)磁选后的炼铁高钛炉渣,主要成分有 、 、 、 、 以及
少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
21 / 25
学科网(北京)股份有限公司该工艺条件下,有关金属离子开始沉淀和沉淀完全的 见下表
金属离子
开始沉淀的 2.2 3.5 9.5 12.4
沉淀完全 的
3.2 4.7 11.1 13.8
回答下列问题:
(1)“焙烧”中, 、 几乎不发生反应, 、 、 、 转化为相应的硫酸
盐,写出 转化为 的化学方程式_______。
(2)“水浸”后“滤液”的 约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6,依次析出的金属离
子是_______。
(3)“母液①"中 浓度为_______ 。
(4)“水浸渣”在160℃“酸溶”最适合的酸是_______。“酸溶渣”的成分是_______、_______。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出 沉淀,该反应的离子方程式
是_______。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得_______,循环利用。
26.(2021·全国甲卷)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问
题:
(1) 的一种制备方法如下图所示:
①加入 粉进行转化反应的离子方程式为_______,生成的沉淀与硝酸反应,生成_______后可循环使
用。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为_______;若反应物用量比
时,氧化产物为_______;当 ,单质碘的收率会降低,原
因是_______。
(2)以 为原料制备 的方法是:先向 溶液中加入计量的 ,生成碘化物;再
向混合溶液中加入 溶液,反应得到 ,上述制备 的总反应的离子方程式为_______。
(3) 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少为_______
22 / 25
学科网(北京)股份有限公司。 在 溶液中可发生反应 。实验室中使用过量的 与 溶液反应后,过
滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量 的原因是_______。
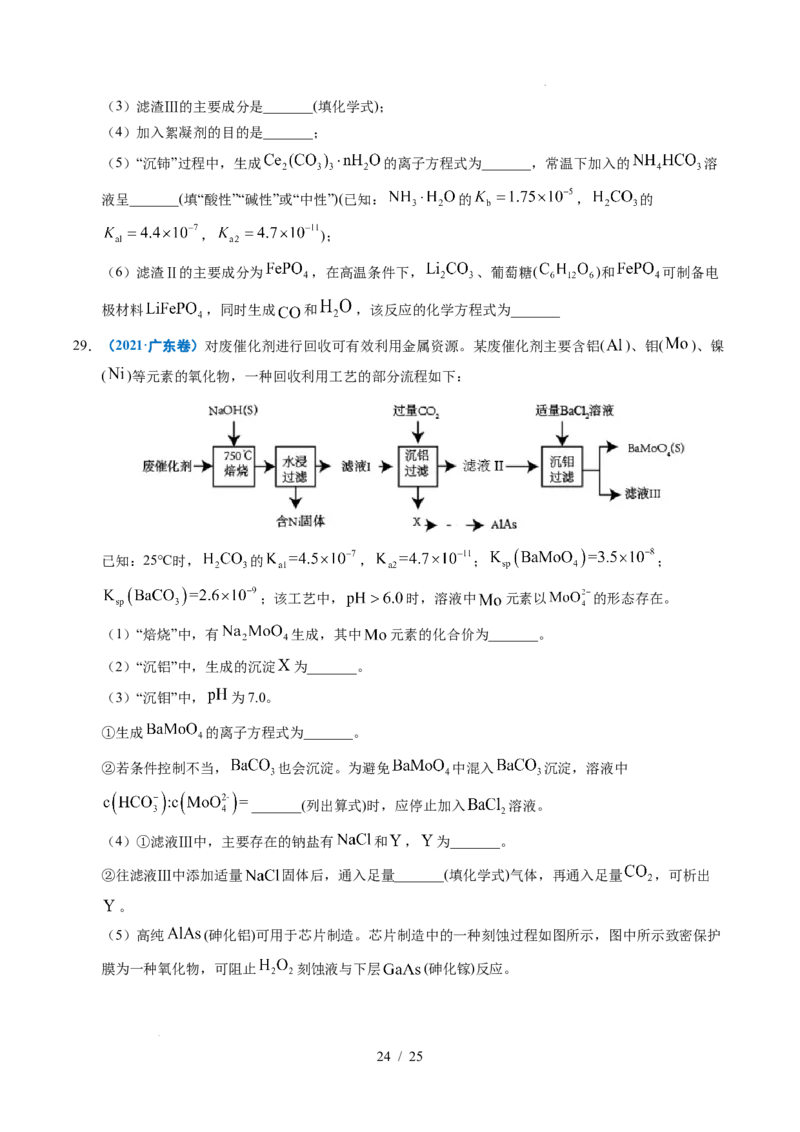
27.(2021·河北卷)绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相
氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废
弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
(1)高温连续氧化工序中被氧化的元素是_______(填元素符号)。
(2)工序①的名称为__。
(3)滤渣的主要成分是__(填化学式)。
(4)工序③中发生反应的离子方程式为_______。
(5)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为__,可代替
NaOH的化学试剂还有_______(填化学式)。
(6)热解工序产生的混合气体最适宜返回工序_______(填“①”或“②”或“③”或“④”)参与内循环。
(7)工序④溶液中的铝元素恰好完全转化为沉淀的pH为__。(通常认为溶液中离子浓度小于10-
5mol•L-1为沉淀完全;A1(OH)
3
+OH- ⇌Al(OH) :K=100.63,K
w
=10-14,K
sp
[A1(OH)
3
]=10-33)
28.(2021·湖南卷) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
形式存在,还含有 、 、 、 等物质。以独居石为原料制备
的工艺流程如下:
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______;
(2)为提高“水浸”效率,可采取的措施有_______(至少写两条);
23 / 25
学科网(北京)股份有限公司(3)滤渣Ⅲ的主要成分是_______(填化学式);
(4)加入絮凝剂的目的是_______;
(5)“沉铈”过程中,生成 的离子方程式为_______,常温下加入的 溶
液呈_______(填“酸性”“碱性”或“中性”)(已知: 的 , 的
, );
(6)滤渣Ⅱ的主要成分为 ,在高温条件下, 、葡萄糖( )和 可制备电
极材料 ,同时生成 和 ,该反应的化学方程式为_______
29.(2021·广东卷)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、镍
( )等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的 , ; ;
;该工艺中, 时,溶液中 元素以 的形态存在。
(1)“焙烧”中,有 生成,其中 元素的化合价为_______。
(2)“沉铝”中,生成的沉淀 为_______。
(3)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
②若条件控制不当, 也会沉淀。为避免 中混入 沉淀,溶液中
_______(列出算式)时,应停止加入 溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有 和 , 为_______。
②往滤液Ⅲ中添加适量 固体后,通入足量_______(填化学式)气体,再通入足量 ,可析出
。
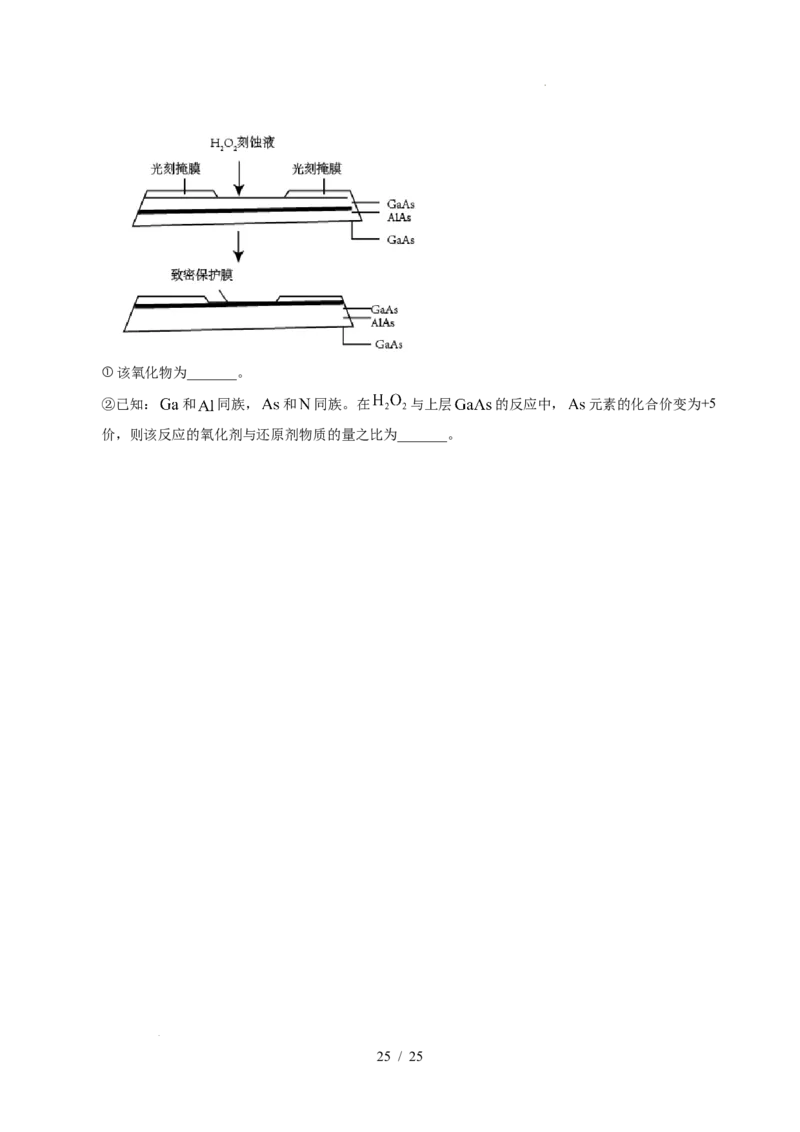
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护
膜为一种氧化物,可阻止 刻蚀液与下层 (砷化镓)反应。
24 / 25
学科网(北京)股份有限公司①该氧化物为_______。
②已知: 和 同族, 和 同族。在 与上层 的反应中, 元素的化合价变为+5
价,则该反应的氧化剂与还原剂物质的量之比为_______。
25 / 25
学科网(北京)股份有限公司