文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
2025 年中考化学一轮复习
专题四 水和溶液
基础练
考点 1 水的净化
某学习小组开展“自制简易净水器”的实践活动,作品如图。完成1—2题。
1.[2024四川成都]任务二:设计并制作净水器。下列说法合理的是( )
A.用聚氯乙烯塑料制作外壳,安全环保
B.小卵石和石英砂主要除去可溶性杂质
C.用活性炭净水是因为其结构疏松多孔
D.蓬松棉的主要作用是提高净水的速率
2.[2024四川成都]任务三:展示并评价作品。下列评价不合理的是( )
A.净化水硬度变得更小 B.制作材料廉价易得
C.制作简单,操作简便 D.作品设计简洁美观
3.[2024北京房山二模]下图为自来水厂的生产流程。下列说法不正确的是(
)
A.过滤池可以除去水中的难溶性杂质
B.活性炭可以吸附水中有色有味的杂质
C.投药消毒可以杀灭水中的细菌和病毒
D.从水泵中出来的水是蒸馏水
考点 2 溶液的形成
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
4.[2024江苏苏州]下列有关溶液的说法正确的是 ( )
A.溶液由溶质和溶剂组成
B.碘酒中,碘是溶剂,酒精是溶质
C.溶液的溶质只能是一种
D.所有溶液均是无色、澄清的液体
5.[2024湖北]把少量下列物质加入水中,充分搅拌,能形成溶液的是( )
A.泥土 B.蜡烛 C.蔗糖 D.汽油
6.[2024山东聊城阳谷二模]溶液用途广泛,与人们的生活息息相关。下列有
关溶液的说法正确的是( )
A.溶质可以是固体,也可以是液体或者气体
B.水是一种重要的溶剂,能溶解所有物质
C.配制好的溶液装入试剂瓶时有少量溅出,导致溶质质量分数减小
D.NaCl的饱和溶液不可以再溶解蔗糖
考点 3 饱和溶液与不饱和溶液
7.[2024山东枣庄二模]某兴趣小组为探究硝酸钾的溶解性,进行了下图所示
实验:
结合硝酸钾在不同温度下的溶解度,判断下列说法不正确的是( )
温度/℃ 10 20 30 40 50 60
KNO 溶解度/g 20.9 31.6 45.8 63.9 85.5 110
3
A.①③中的溶液均为不饱和溶液
B.②③中溶液的质量:③>②
C.④中析出晶体的质量是0.9g
D.②③④中溶液的溶质质量分数:③>②>④
8.[2024广东东莞一模]物质M的溶解度曲线如图所示。下列说法正确的是(
)
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.物质M属于微溶物质
B.A、B、C三点对应的溶液均为饱和溶液
C.从物质M的溶液中获得晶体的方法:冷却热饱和溶液
D.溶质的质量分数:A>B>C
9.[2024山东德州夏津二模改编]硼酸是一种白色固体,为探究硼酸在水中的
溶解情况,进行如下实验:在A∼G七个烧杯中各加入25.0g硼酸,再分别加入
100g水。在不同温度下,搅拌使固体充分溶解后静置,测定溶液中硼酸的含
量。实验结果见下表:
温度/℃ 20 30 40 60
静置后的现象
100g水中溶解的硼酸质量/g 5.0 6.7 8.7 14.8
温度/℃ 80 90 100 —
静置后的现象
100g水中溶解的硼酸质量/g 23.6 25.0 25.0
一定是饱和溶液的是____________(填序号),若F烧杯中为不饱和状态,将
其变为饱和状态可以采取的一种方法是
__________________________________。
考点 4 溶解度
10.[2024四川成都]将某碳酸饮料拧开,倒入装有冰块的杯中,如图。下列分
析合理的是( )
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.拧开瓶盖后,二氧化碳溶解度变大
B.产生气泡的原因是饮料与冰发生化学反应
C.冒泡刚结束时,饮料仍然是二氧化碳的饱和溶液
D.图中现象能说明二氧化碳溶解度与压强、温度的关系
11.[2024河北邯郸三模]KNO 和NaCl溶解度曲线如图1所示,某化学兴趣小
3
组同学用KNO 和NaCl中的一种物质进行了如图2所示实验(忽略水的损失)。
3
下列说法正确的是( )
图1
图2
A.甲是氯化钠
B.溶液③④的溶质质量分数相同
C.50℃时分别用两种固体配制质量相等的饱和溶液,KNO 中加水更多
3
D.④中析出晶体的质量为40g
12.[2024湖南]《天工开物·作咸》记载“候潮一过,明日天晴,半日晒出盐
霜,疾趋扫起煎炼。”
“盐霜”的主要成分是氯化钠固体,结合氯化钠溶解度曲线,回答下列问题:
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1) 20℃时,氯化钠的溶解度是____g。
(2) 氯化钠的溶解度随温度升高而____。
(3) “半日晒出盐霜”中的“晒”说明,从氯化钠溶液中得到晶体的方法是
____结晶。
13.[2024吉林]根据图中两种物质的溶解度曲线回答下列问题。
(1) 当温度为________℃时,NaCl与KNO 的溶解度相同,在此温度下,两
3
种物质饱和溶液的溶质质量分数的大小关系是____;
(2) 海水里含有大量NaCl,海水晒“盐”需要经过____结晶过程。
14.[2024湖北武汉江汉三模]依据物质的溶解度可以进行溶液配制、物质分离
和制备等,下表中数据是四种物质在不同温度下水中的溶解度(g):
10℃ 20℃ 30℃ 40℃ 50℃ 60℃
NaCl 35.8 36.0 36.3 36.6 37.0 37.3
NH Cl 33.3 37.2 41.4 45.8 50.4 55.2
4
NH HCO 15.8 21.0 27.0 — — —
4 3
NaHCO 8.1 9.6 11.1 12.7 14.5 16.4
3
回答下列问题:
(1) 20℃时,NaCl饱和溶液中溶质质量分数为
________________________________________(写出计算式)。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2) 将接近饱和的NH Cl溶液变为饱和溶液,可采用的一种方法是
4
________________________________________________________________。
(3) Na+、Cl−、NH+、HCO−四种离子可以组成四种物质:NaCl、NH HCO
4 3 4 3
、NH Cl、NaHCO 。20℃时在NaCl和NH HCO 均达饱和的混合溶液中,会
4 3 4 3
析出______________(填化学式)晶体。
(4) 下列说法中不正确的是______。
A.20℃时配制等质量的四种物质的饱和溶液,需要水质量最小的是NaHCO
3
B.提纯含少量氯化钠的氯化铵,可先将其配制成60℃氯化铵饱和溶液,再降
温结晶
C.30℃以上无法测得NH HCO 溶解度数据,是因为此时NH HCO 已发生分
4 3 4 3
解
考点 5 溶质的质量分数
15.[2024福建节选]请参加“氯化钠欢乐之旅”的实践活动。利用风吹和日晒
使海水不断蒸发至有晶体析出,此过程溶液中NaCl的质量分数逐渐____
(填“增大”或“减小”)。
16.[2024四川成都节选]配制质量分数为7.08%的硝酸钾溶液200g,需要硝酸钾
____g(精确到0.1g)。
17.[2024山东东营节选]“我行其野,芃芃其麦”。东营某智慧高效农业示范
区万亩小麦长势喜人。小麦是我国重要的粮食作物。要向小麦喷洒溶质质量分
数为0.1%的Ca(NO ) 溶液,现有1.5tCa(NO ) 固体,需水________________t。
3 2 3 2
18.[2024河南]硝酸钾固体的溶解度曲线如图所示。硝酸钾的溶解度随着温度
升高而____(填“增大”或“减小”);20℃时,硝酸钾的饱和溶液中溶质的
质量分数为________________________________________(只写出计算式)。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
提升练
19.[2024山东烟台]下列有关水和溶液的说法错误的是( )
A.通过沉降、过滤可除去水中的不溶性杂质
B.生活中常用煮沸的方法对水进行杀菌消毒
C.溶液具有均一性、稳定性的原因是溶液中各种微观粒子都静止不动
D.将50g溶质质量分数为20%的硝酸钾溶液稀释成5%,需要加水150g
20.[2024山东滨州]下列关于溶液的说法正确的是 ( )
A.饱和溶液升高温度一定变为不饱和溶液
B.均一、稳定的液体一定是溶液
C.硝酸铵溶于水使溶液的温度降低
D.只有固体和液体可以作为溶质
21.[2024云南]实验室中存放有如图所示的氯化钾溶液。下列说法错误的是(
)
A.该溶液中的溶剂是水
B.该溶液的溶质质量分数为6%
C.配制100g该溶液需要6gKCl
D.该溶液取出一半后,溶质质量分数变为3%
22.[2024重庆A]已知KCl的溶解度随温度升高而增大,在40℃时KCl的溶解
度为40g,在该温度下,依据下表所示的数据,进行KCl溶于水的实验探究。下
列说法中正确的是( )
实验编号 ① ② ③
KCl的质量/g 10 20 30
水的质量/g 50 60 70
A.在上述实验所得的溶液中,溶质质量分数①>②
B.实验③所得溶液中,溶质与溶剂的质量比为3:7
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.将实验②、③的溶液分别降温,一定都有晶体析出
D.将实验①、③的溶液按一定比例混合可得到与②浓度相等的溶液
23.[2024河北]下表是KNO 和NaNO 在不同温度时的溶解度,小明用其中一
3 3
种物质(X)进行了如图所示的实验(水蒸发忽略不计)。下列分析错误的是(
)
温度/℃ 20 40 60
溶解度/g KNO 31.6 63.9 110
3
NaNO 88.0 103 125
3
A.X为NaNO
3
B.③中溶液为X的不饱和溶液
C.④中溶液的质量为100g
D.溶液中溶质的质量分数:②=③>④
24.[2024广西节选]《天工开物》记载“凡引水种盐,⋯⋯ 南风大起,则一
宵结成,名曰颗盐”,表明古人已经掌握了制盐工艺。回答问题:
用化学知识能很好地解释古人的制盐工艺。如图为氯化钠的溶解度曲线,20℃
时氯化钠的溶解度为____g。此温度下,将9g氯化钠溶解到25g水中,可配得氯
化钠的____(填“饱和”或“不饱和”)溶液;保持温度不变,蒸发部分溶
剂,该溶液溶质的质量分数____(填“变大”“不变”或“变小”)。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
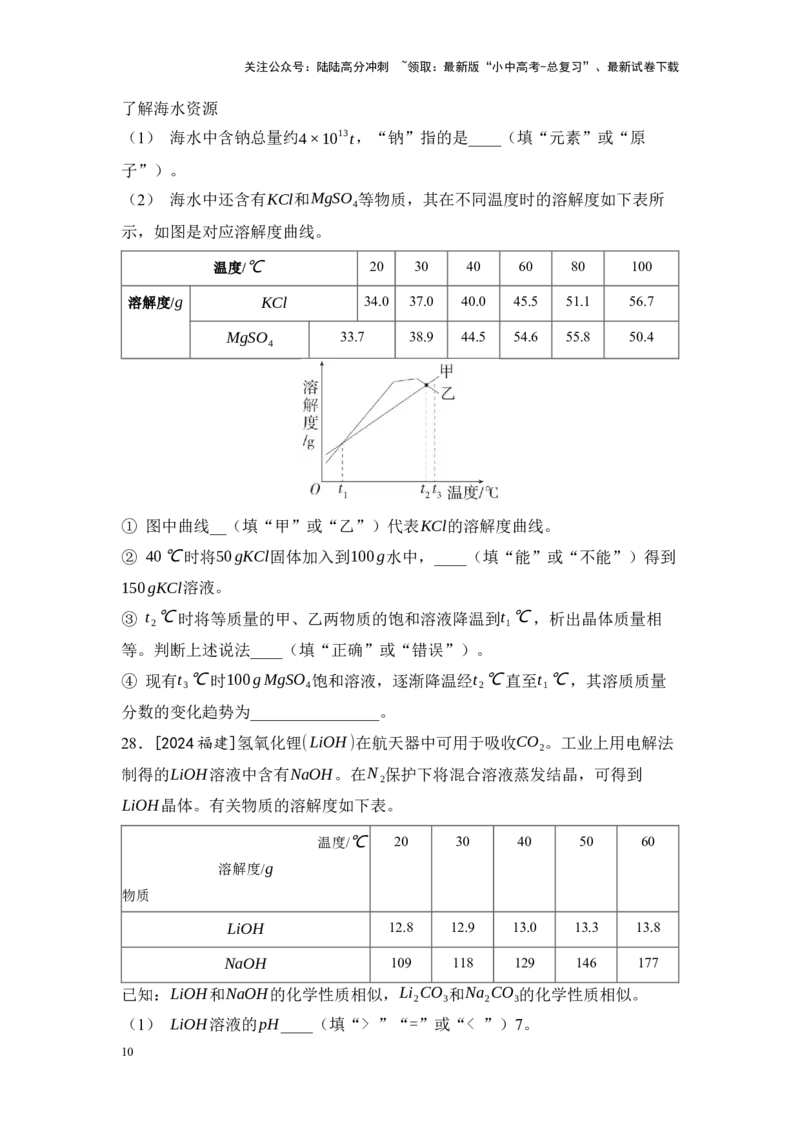
25.[2024山东东营节选]T ℃时,将等质量的硝酸钾和氯化钾分别加入到各盛
1
有100g水的两个烧杯中,充分搅拌后,现象如图1所示。两者的溶解度曲线如
图2所示。
图1 图2
(1) 烧杯__(填“甲”或“乙”)中上层清液为饱和溶液;
(2) 图2中P点的含义是
____________________________________________________;
(3) 将温度由T ℃升高到T ℃,充分搅拌,烧杯乙中固体__
1 2
(填“能”或“不能”)全部溶解。
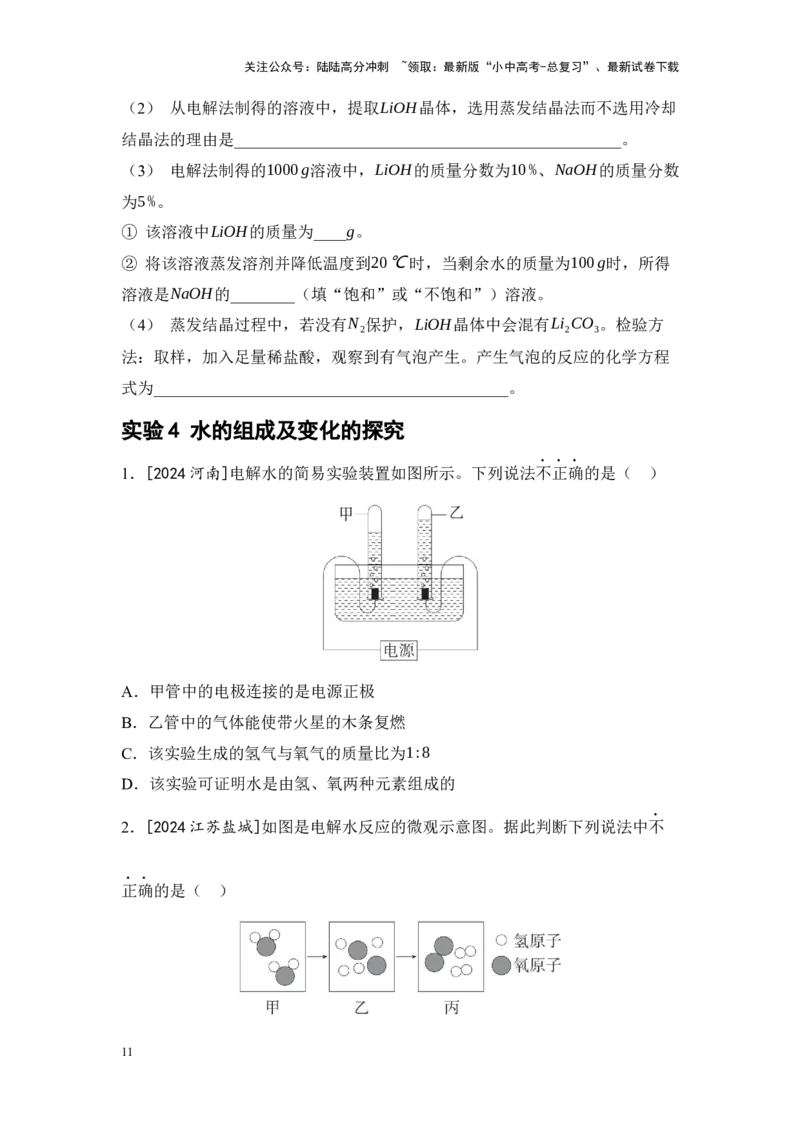
26.[2024陕西]小明同学在测定某氯化钠溶液中溶质的质量分数时,用两只烧
杯各取80g待测溶液分别进行了如下实验。已知20℃时,氯化钠的溶解度为
36g。
(1) 20℃时,100g水中最多溶解氯化钠的质量是__g。
(2) 20℃时,A 、A 中的溶液是氯化钠的________(填“饱和”或“不饱
1 2
和”)溶液。
(3) B 、B 中的溶液溶质与溶剂的质量比____(填“相等”或“不相
1 2
等”)。
(4) x的值等于____。
(5) 由上述实验可得出待测氯化钠溶液中溶质质量分数为__________。
27.[2024江苏盐城节选]海洋蕴藏着丰富的资源,人类应合理开发利用。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
了解海水资源
(1) 海水中含钠总量约4×1013t,“钠”指的是____(填“元素”或“原
子”)。
(2) 海水中还含有KCl和MgSO 等物质,其在不同温度时的溶解度如下表所
4
示,如图是对应溶解度曲线。
温度/℃ 20 30 40 60 80 100
溶解度/g KCl 34.0 37.0 40.0 45.5 51.1 56.7
MgSO 33.7 38.9 44.5 54.6 55.8 50.4
4
① 图中曲线__(填“甲”或“乙”)代表KCl的溶解度曲线。
② 40℃时将50gKCl固体加入到100g水中,____(填“能”或“不能”)得到
150gKCl溶液。
③ t ℃时将等质量的甲、乙两物质的饱和溶液降温到t ℃,析出晶体质量相
2 1
等。判断上述说法____(填“正确”或“错误”)。
④ 现有t ℃时100gMgSO 饱和溶液,逐渐降温经t ℃直至t ℃,其溶质质量
3 4 2 1
分数的变化趋势为________________。
28.[2024福建]氢氧化锂(LiOH)在航天器中可用于吸收CO 。工业上用电解法
2
制得的LiOH溶液中含有NaOH。在N 保护下将混合溶液蒸发结晶,可得到
2
LiOH晶体。有关物质的溶解度如下表。
温度/℃ 20 30 40 50 60
溶解度/g
物质
LiOH 12.8 12.9 13.0 13.3 13.8
NaOH 109 118 129 146 177
已知:LiOH和NaOH的化学性质相似,Li CO 和Na CO 的化学性质相似。
2 3 2 3
(1) LiOH溶液的pH____(填“> ”“=”或“< ”)7。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2) 从电解法制得的溶液中,提取LiOH晶体,选用蒸发结晶法而不选用冷却
结晶法的理由是________________________________________________。
(3) 电解法制得的1000g溶液中,LiOH的质量分数为10%、NaOH的质量分数
为5%。
① 该溶液中LiOH的质量为____g。
② 将该溶液蒸发溶剂并降低温度到20℃时,当剩余水的质量为100g时,所得
溶液是NaOH的________(填“饱和”或“不饱和”)溶液。
(4) 蒸发结晶过程中,若没有N 保护,LiOH晶体中会混有Li CO 。检验方
2 2 3
法:取样,加入足量稀盐酸,观察到有气泡产生。产生气泡的反应的化学方程
式为____________________________________________。
实验 4 水的组成及变化的探究
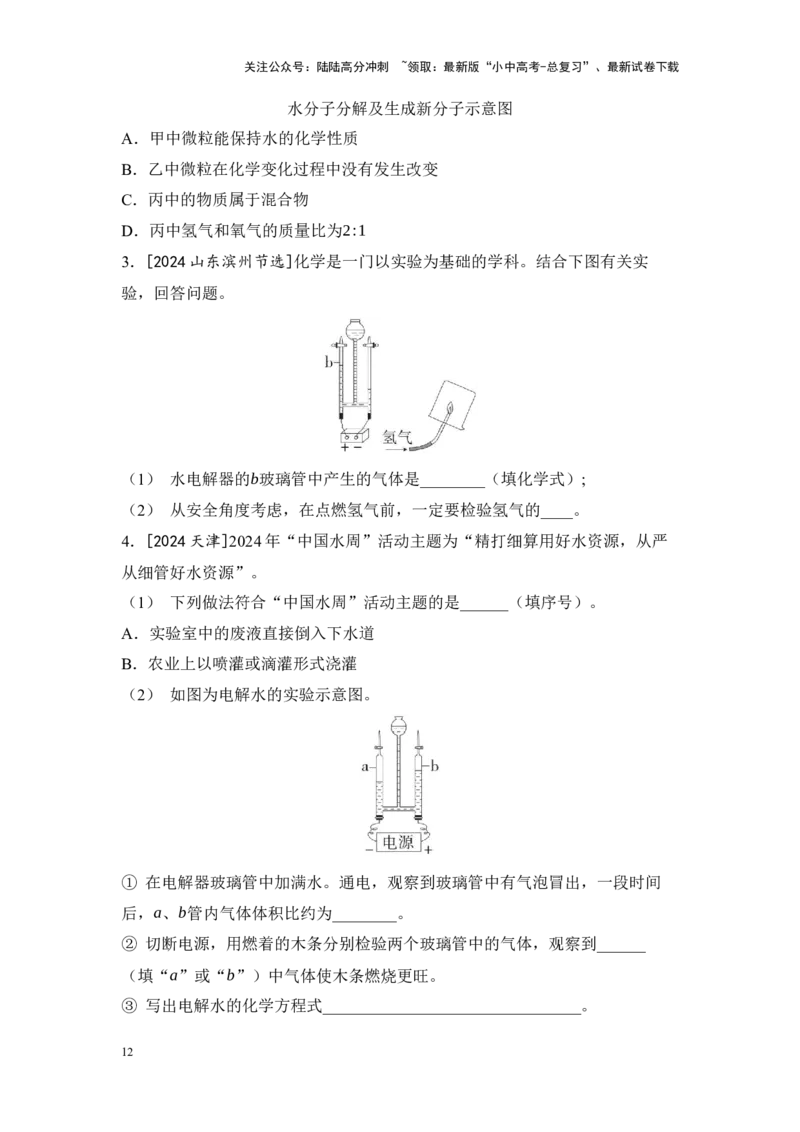
1.[2024河南]电解水的简易实验装置如图所示。下列说法不正确的是( )
A.甲管中的电极连接的是电源正极
B.乙管中的气体能使带火星的木条复燃
C.该实验生成的氢气与氧气的质量比为1:8
D.该实验可证明水是由氢、氧两种元素组成的
2.[2024江苏盐城]如图是电解水反应的微观示意图。据此判断下列说法中不
正确的是( )
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
水分子分解及生成新分子示意图
A.甲中微粒能保持水的化学性质
B.乙中微粒在化学变化过程中没有发生改变
C.丙中的物质属于混合物
D.丙中氢气和氧气的质量比为2:1
3.[2024山东滨州节选]化学是一门以实验为基础的学科。结合下图有关实
验,回答问题。
(1) 水电解器的b玻璃管中产生的气体是________(填化学式);
(2) 从安全角度考虑,在点燃氢气前,一定要检验氢气的____。
4.[2024天津]2024年“中国水周”活动主题为“精打细算用好水资源,从严
从细管好水资源”。
(1) 下列做法符合“中国水周”活动主题的是______(填序号)。
A.实验室中的废液直接倒入下水道
B.农业上以喷灌或滴灌形式浇灌
(2) 如图为电解水的实验示意图。
① 在电解器玻璃管中加满水。通电,观察到玻璃管中有气泡冒出,一段时间
后,a、b管内气体体积比约为________。
② 切断电源,用燃着的木条分别检验两个玻璃管中的气体,观察到______
(填“a”或“b”)中气体使木条燃烧更旺。
③ 写出电解水的化学方程式________________________________。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3) 某新能源汽车以氢气为燃料,使用1kg氢气平均可行驶150km。若通过电
解水产生氢气,54kg水分解产生的氢气理论上可供这辆汽车行驶____km。
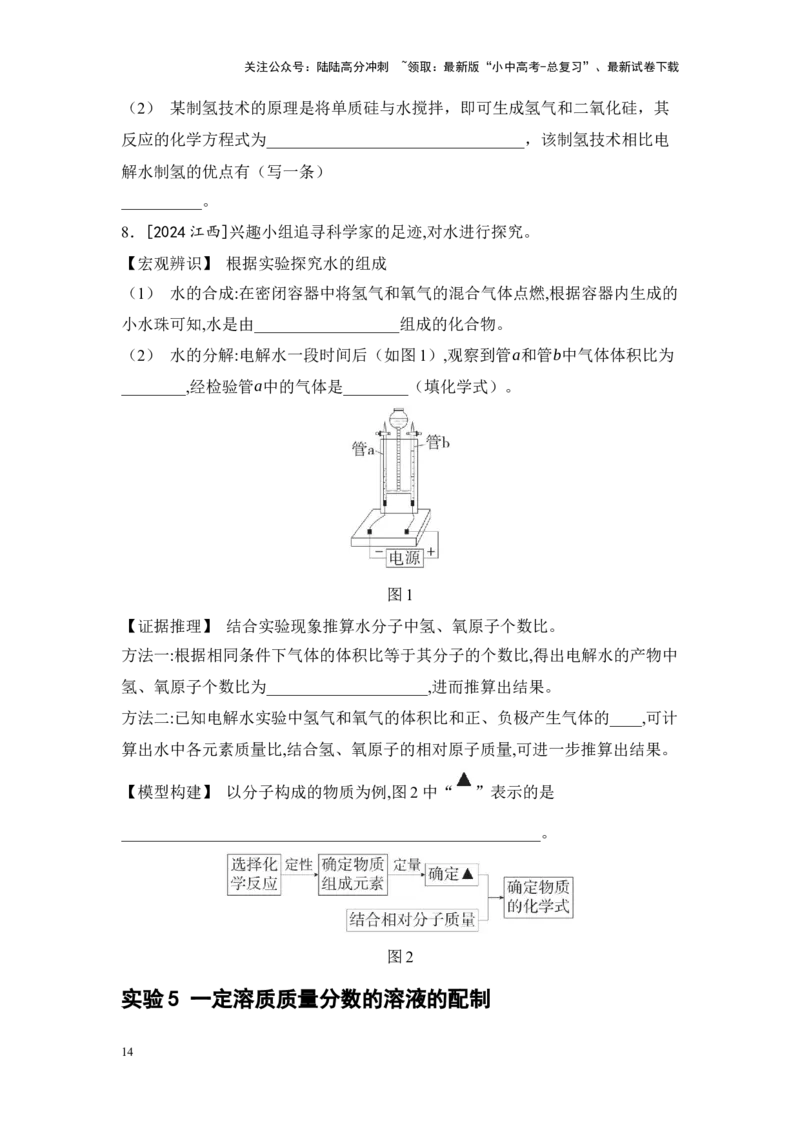
5.[2024陕西]下图是水发生变化的微观示意图,请回答。
(1) 图中共有______种原子。
(2) 水分子本身未发生改变的是变化______(填“①”或“②”)。
(3) 水通电时,参加反应的水与生成的气体的质量比为________。
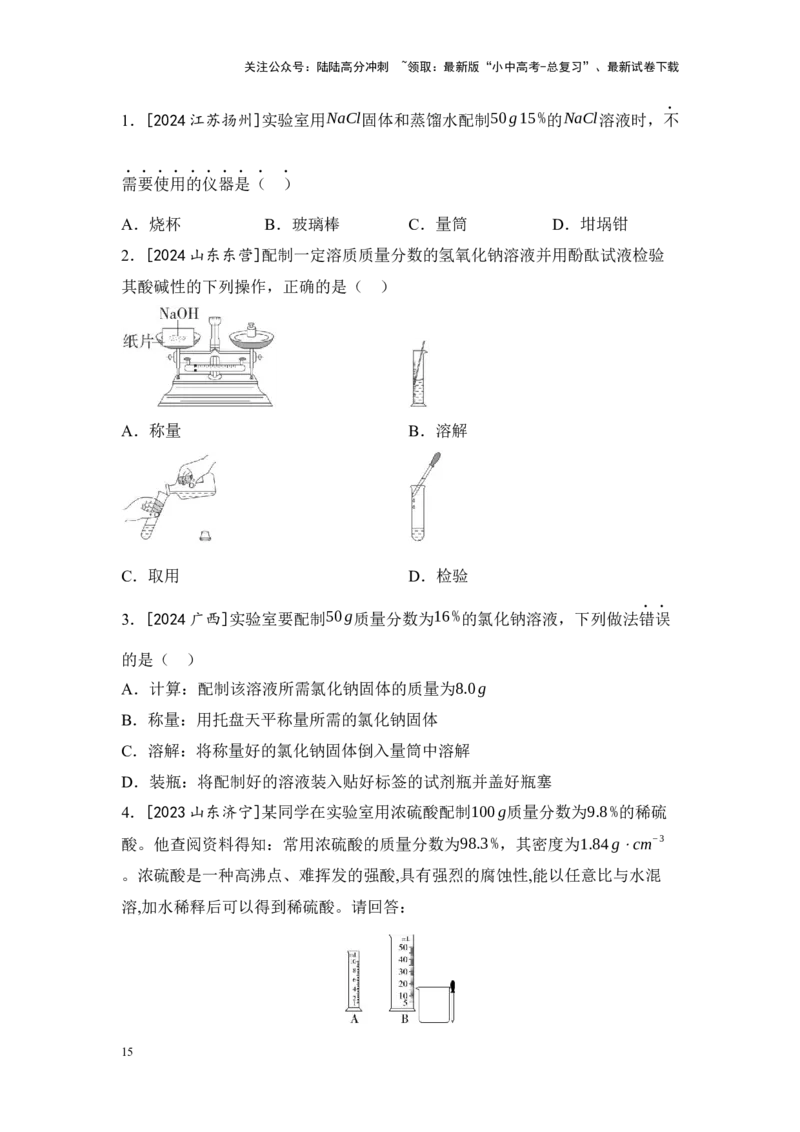
6.[2024湖南]航天员在太空生活需要氧气和水。氧气和水的相互转化,体现
了“合”与“分”的思想。
(1) “合”的思想
液氢和液氧反应产生的能量可为返回舱返回提供动力,该反应的微观示意图如
下:
① 该化学反应的基本类型是____反应。
② 返回舱返回的动力采用液氢作为能源的优点是
____________________________________________________(写一条即可)。
(2) “分”的思想
航天员在空间站生活所需氧气主要通过电解水获得,该反应的化学方程式是
________________________________。
(3) “合”与“分”的思想
通过以上事实,证明了水是由__________________组成的。
7.[2024重庆A节选]发展新质生产力,重庆在行动。重庆企业研发的固态电池
和氢能源汽车全球领先。
(1) 电解水是制氢的一种传统方法。H 在与电源__极相连的一端产生。
2
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2) 某制氢技术的原理是将单质硅与水搅拌,即可生成氢气和二氧化硅,其
反应的化学方程式为________________________________,该制氢技术相比电
解水制氢的优点有(写一条)
__________。
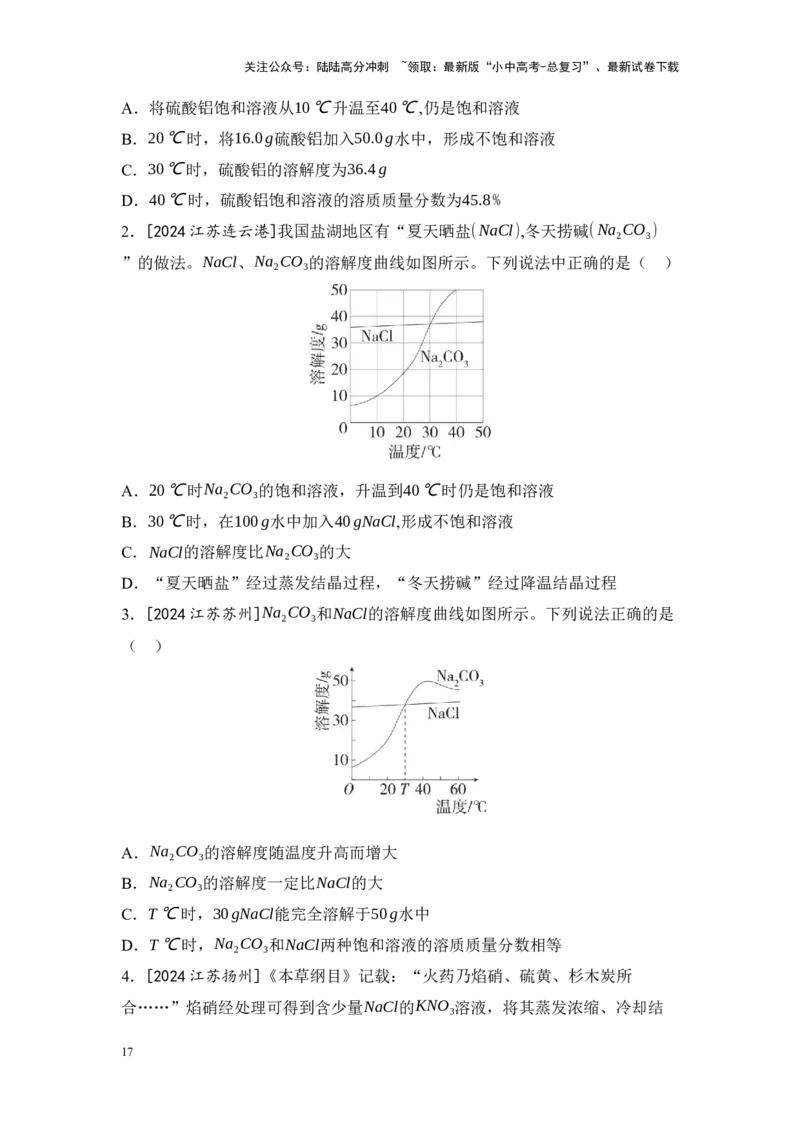
8.[2024江西]兴趣小组追寻科学家的足迹,对水进行探究。
【宏观辨识】 根据实验探究水的组成
(1) 水的合成:在密闭容器中将氢气和氧气的混合气体点燃,根据容器内生成的
小水珠可知,水是由__________________组成的化合物。
(2) 水的分解:电解水一段时间后(如图1),观察到管a和管b中气体体积比为
________,经检验管a中的气体是________(填化学式)。
图1
【证据推理】 结合实验现象推算水分子中氢、氧原子个数比。
方法一:根据相同条件下气体的体积比等于其分子的个数比,得出电解水的产物中
氢、氧原子个数比为____________________,进而推算出结果。
方法二:已知电解水实验中氢气和氧气的体积比和正、负极产生气体的____,可计
算出水中各元素质量比,结合氢、氧原子的相对原子质量,可进一步推算出结果。
【模型构建】 以分子构成的物质为例,图2中“ ”表示的是
____________________________________________________。
图2
实验 5 一定溶质质量分数的溶液的配制
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.[2024江苏扬州]实验室用NaCl固体和蒸馏水配制50g15%的NaCl溶液时,不
需要使用的仪器是( )
A.烧杯 B.玻璃棒 C.量筒 D.坩埚钳
2.[2024山东东营]配制一定溶质质量分数的氢氧化钠溶液并用酚酞试液检验
其酸碱性的下列操作,正确的是( )
A.称量 B.溶解
C.取用 D.检验
3.[2024广西]实验室要配制50g质量分数为16%的氯化钠溶液,下列做法错误
的是( )
A.计算:配制该溶液所需氯化钠固体的质量为8.0g
B.称量:用托盘天平称量所需的氯化钠固体
C.溶解:将称量好的氯化钠固体倒入量筒中溶解
D.装瓶:将配制好的溶液装入贴好标签的试剂瓶并盖好瓶塞
4.[2023山东济宁]某同学在实验室用浓硫酸配制100g质量分数为9.8%的稀硫
酸。他查阅资料得知:常用浓硫酸的质量分数为98.3%,其密度为1.84g⋅cm−3
。浓硫酸是一种高沸点、难挥发的强酸,具有强烈的腐蚀性,能以任意比与水混
溶,加水稀释后可以得到稀硫酸。请回答:
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1) 通过计算,需量取5.4mL浓硫酸,选择量筒______(填“A”或“B”)量取;
(2) 若完成溶液的配制,除如图所提供的仪器外,还需用到的玻璃仪器是
________,浓硫酸稀释时应将______中(填“a”或“b”);
a.水注入浓硫酸 b.浓硫酸注入水
(3) 若用量筒量取浓硫酸时俯视读数,所配溶液溶质质量分数____9.8%
(填“大于”“小于”或“等于”)。
5.[2024重庆A节选]实验能展现化学的魅力,也是重要的学科素养。
实验室用氯化钠固体配制50g质量分数为6%的氯化钠溶液。
(1) 溶解时玻璃棒的作用是________________________,量取水时应选用
______(填序号)mL规格的量筒。
A.25 B.50 C.100
(2) 称量氯化钠时,误将氯化钠放在右盘(未使用游码),若其他操作都正
确,配制所得溶液的溶质质量分数______(填“< ”“> ”或“=”)6%。
6.[2024山西节选]根据情景要求,完成“一定溶质质量分数的碳酸钠溶液的
配制”。
配制如图所示的100g10%的碳酸钠溶液,应该怎样操作?
【温馨提示】①实验要写出具体操作步骤
②语言描述要简练规范
微专题 1 溶解度曲线
1.[2024广东]硫酸铝的溶解度曲线如图所示。下列说法正确的是( )
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.将硫酸铝饱和溶液从10℃升温至40℃,仍是饱和溶液
B.20℃时,将16.0g硫酸铝加入50.0g水中,形成不饱和溶液
C.30℃时,硫酸铝的溶解度为36.4g
D.40℃时,硫酸铝饱和溶液的溶质质量分数为45.8%
2.[2024江苏连云港]我国盐湖地区有“夏天晒盐(NaCl),冬天捞碱(Na CO )
2 3
”的做法。NaCl、Na CO 的溶解度曲线如图所示。下列说法中正确的是( )
2 3
A.20℃时Na CO 的饱和溶液,升温到40℃时仍是饱和溶液
2 3
B.30℃时,在100g水中加入40gNaCl,形成不饱和溶液
C.NaCl的溶解度比Na CO 的大
2 3
D.“夏天晒盐”经过蒸发结晶过程,“冬天捞碱”经过降温结晶过程
3.[2024江苏苏州]Na CO 和NaCl的溶解度曲线如图所示。下列说法正确的是
2 3
( )
A.Na CO 的溶解度随温度升高而增大
2 3
B.Na CO 的溶解度一定比NaCl的大
2 3
C.T℃时,30gNaCl能完全溶解于50g水中
D.T℃时,Na CO 和NaCl两种饱和溶液的溶质质量分数相等
2 3
4.[2024江苏扬州]《本草纲目》记载:“火药乃焰硝、硫黄、杉木炭所
合……”焰硝经处理可得到含少量NaCl的KNO 溶液,将其蒸发浓缩、冷却结
3
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
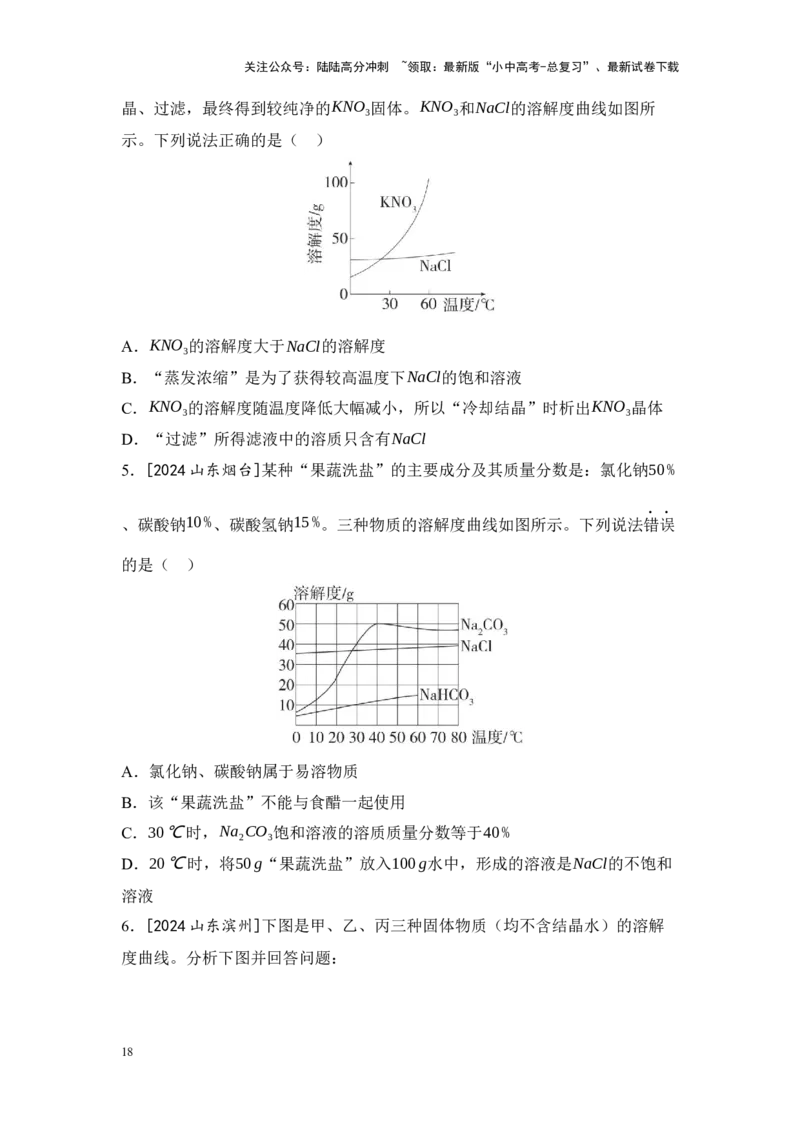
晶、过滤,最终得到较纯净的KNO 固体。KNO 和NaCl的溶解度曲线如图所
3 3
示。下列说法正确的是( )
A.KNO 的溶解度大于NaCl的溶解度
3
B.“蒸发浓缩”是为了获得较高温度下NaCl的饱和溶液
C.KNO 的溶解度随温度降低大幅减小,所以“冷却结晶”时析出KNO 晶体
3 3
D.“过滤”所得滤液中的溶质只含有NaCl
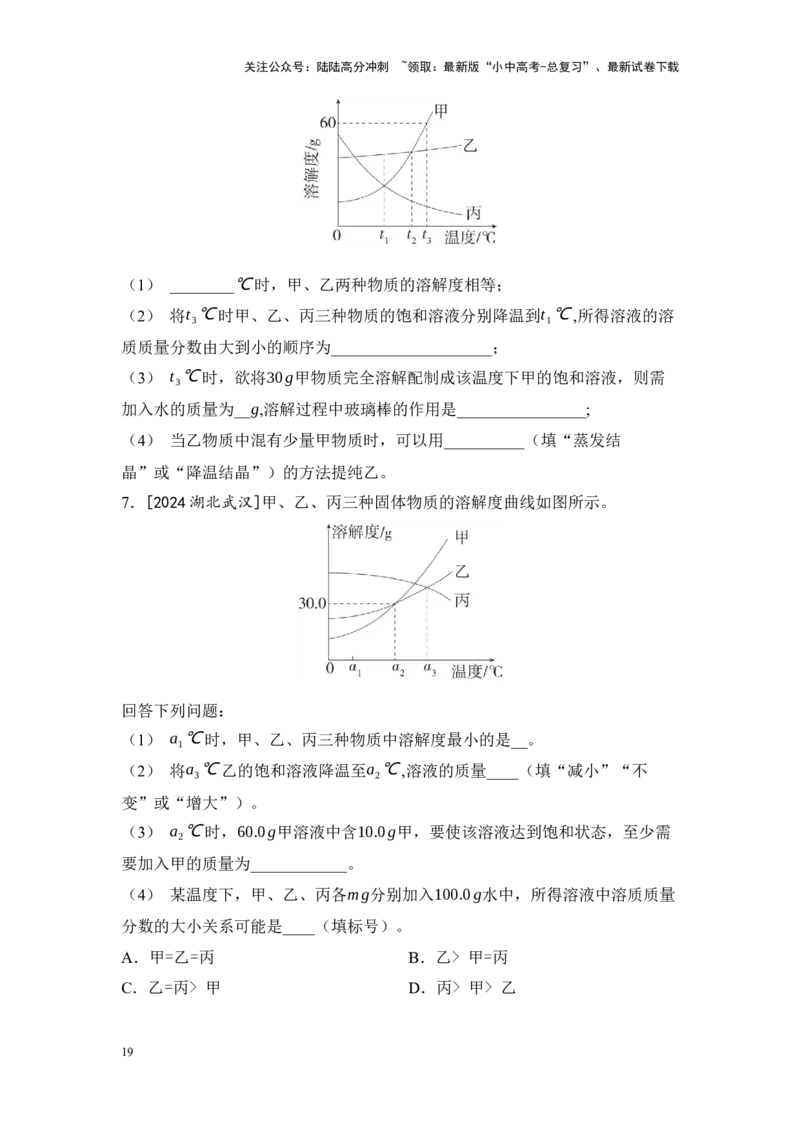
5.[2024山东烟台]某种“果蔬洗盐”的主要成分及其质量分数是:氯化钠50%
、碳酸钠10%、碳酸氢钠15%。三种物质的溶解度曲线如图所示。下列说法错误
的是( )
A.氯化钠、碳酸钠属于易溶物质
B.该“果蔬洗盐”不能与食醋一起使用
C.30℃时,Na CO 饱和溶液的溶质质量分数等于40%
2 3
D.20℃时,将50g“果蔬洗盐”放入100g水中,形成的溶液是NaCl的不饱和
溶液
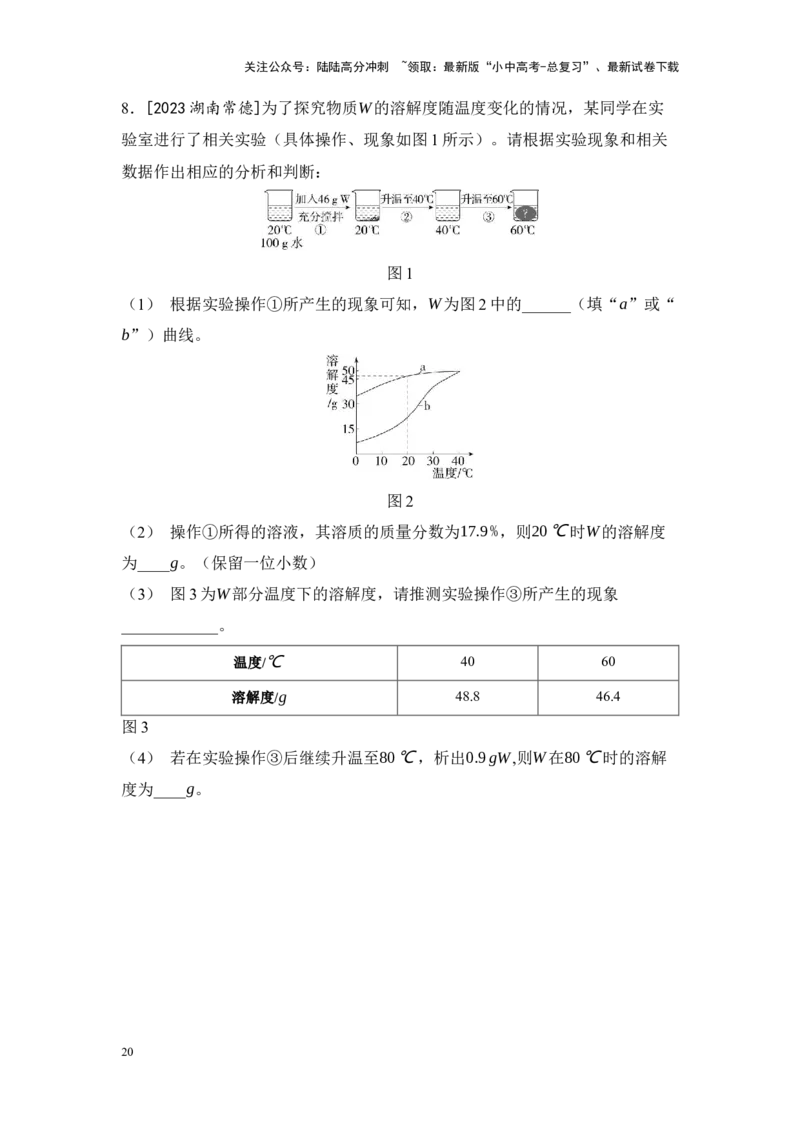
6.[2024山东滨州]下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解
度曲线。分析下图并回答问题:
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1) ________℃时,甲、乙两种物质的溶解度相等;
(2) 将t ℃时甲、乙、丙三种物质的饱和溶液分别降温到t ℃,所得溶液的溶
3 1
质质量分数由大到小的顺序为____________________;
(3) t ℃时,欲将30g甲物质完全溶解配制成该温度下甲的饱和溶液,则需
3
加入水的质量为__g,溶解过程中玻璃棒的作用是________________;
(4) 当乙物质中混有少量甲物质时,可以用__________(填“蒸发结
晶”或“降温结晶”)的方法提纯乙。
7.[2024湖北武汉]甲、乙、丙三种固体物质的溶解度曲线如图所示。
回答下列问题:
(1) a ℃时,甲、乙、丙三种物质中溶解度最小的是__。
1
(2) 将a ℃乙的饱和溶液降温至a ℃,溶液的质量____(填“减小”“不
3 2
变”或“增大”)。
(3) a ℃时,60.0g甲溶液中含10.0g甲,要使该溶液达到饱和状态,至少需
2
要加入甲的质量为____________。
(4) 某温度下,甲、乙、丙各mg分别加入100.0g水中,所得溶液中溶质质量
分数的大小关系可能是____(填标号)。
A.甲=乙=丙 B.乙> 甲=丙
C.乙=丙> 甲 D.丙> 甲> 乙
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
8.[2023湖南常德]为了探究物质W的溶解度随温度变化的情况,某同学在实
验室进行了相关实验(具体操作、现象如图1所示)。请根据实验现象和相关
数据作出相应的分析和判断:
图1
(1) 根据实验操作①所产生的现象可知,W为图2中的______(填“a”或“
b”)曲线。
图2
(2) 操作①所得的溶液,其溶质的质量分数为17.9%,则20℃时W的溶解度
为____g。(保留一位小数)
(3) 图3为W部分温度下的溶解度,请推测实验操作③所产生的现象
____________。
温度/℃ 40 60
溶解度/g 48.8 46.4
图3
(4) 若在实验操作③后继续升温至80℃,析出0.9gW,则W在80℃时的溶解
度为____g。
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题四 水和溶液
基础练
考点 1 水的净化
1.C 2.A
3.D
考点 2 溶液的形成
4.A
5.C
6.A
[解析]A.溶质可以是固体,也可以是液体或者气体,如氯化钠溶于水形成的溶
液中溶质氯化钠是固体,酒精溶于水形成的溶液中溶质酒精是液体,盐酸的溶
质氯化氢是气体,正确;B.水是一种重要的溶剂,但不能溶解所有物质,错误;C.
溶液具有均一性,配制好的溶液装入试剂瓶时有少量溅出,溶质质量分数不
变,错误;D.NaCl的饱和溶液中可以再溶解蔗糖,错误。
考点 3 饱和溶液与不饱和溶液
7.C
[解析]A.由表中数据可知,20℃时,KNO 的溶解度是31.6g,说明在20℃时,
3
100g水中最多能溶解31.6gKNO ,则50g水中最多能溶解15.8gKNO ,而①中
3 3
只加入了10gKNO ,可以完全溶解,所得溶液为不饱和溶液;60℃时,KNO 的
3 3
溶解度是110g,同理可知,50g水中最多能溶解55gKNO ,而③中共加入了
3
20gKNO ,可以完全溶解,所得溶液为不饱和溶液,不符合题意。B.由图中实
3
验可知,②中溶液有未溶解的KNO ,升温后③中KNO 全部溶解,所以溶液质
3 3
量:③>②,不符合题意。C.由表中数据可知,10℃时,KNO 的溶解度为20.9g
3
,则10℃时,50g水中最多溶解KNO 10.45g,④中析出晶体的质量是
3
10g+10g−10.45g=9.55g,符合题意。D.由图中实验可知,②④的溶液中都有
21关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
KNO 剩余,②是20℃时KNO 的饱和溶液、④是10℃时KNO 的饱和溶液;溶解
3 3 3
度越大,饱和溶液的溶质质量分数越大,由于20℃时KNO 的溶解度大于10℃
3
时KNO 的溶解度,所以②中溶液的溶质质量分数大于④;由图中实验可知,
3
②③中溶剂的质量相等,但③中溶解的溶质的质量多,则③中溶液的溶质质量
分数大于②,所以②③④中溶液的溶质质量分数:③>②>④,不符合题意。
8.C
[解析]A.物质的溶解性是根据在20℃时的溶解度来划分的,20℃时溶解度在
0.01g∼1g之间,属于微溶物质,图示无法确定物质M的溶解性,错误;B.A、B
点在溶解度曲线上,对应的溶液均为饱和溶液,C点在溶解度曲线下方,对应
的是不饱和溶液,错误;C.因为物质M的溶解度随温度升高而增大且受温度变化
影响比较大,故从物质M的溶液中获得晶体的方法为冷却热饱和溶液,正确;
D.A、B点分别为物质M在不同温度下的饱和溶液,饱和溶液溶质质量分数为
溶解度
×100%,溶解度越大,溶质质量分数越大,故溶质的质量分数:
100g+溶解度
A>B,C点溶液可看作B点溶液升温至t ℃,溶质质量分数不变,故溶质的质
2
量分数:A>B=C,错误。
9.ABCDE; 蒸发溶剂(或增加硼酸或降温)
考点 4 溶解度
10.C
[解析]拧开瓶盖,气压减小,饮料中气体的溶解度减小,A、B错误;冒泡刚结
束时,饮料是该状态下二氧化碳的饱和溶液,C正确;该实验只能说明二氧化
碳的溶解度与压强有关,不能说明与温度的关系,D错误。
11.B
[解析]A.20℃时,先向100g水中加入20g甲,再加入65.5g甲,然后升温至
50℃,无固体剩余,50℃时,硝酸钾的溶解度为85.5g,而氯化钠的溶解度是
37.0g,所以甲是硝酸钾,错误;B.50℃时,硝酸钾的溶解度为85.5g,则溶液③
为硝酸钾的饱和溶液,溶液④也为此温度下的饱和溶液,则溶液③④的溶质质
量分数相同,正确;C.50℃时,硝酸钾的溶解度大于氯化钠的溶解度,则50℃
时分别用两种固体配制质量相等的饱和溶液,氯化钠加水更多,错误;D.50℃
22关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
时,硝酸钾的溶解度为85.5g,恒温蒸发50g水,则④中析出晶体的质量为
42.75g,错误。
12.(1) 36.0
[解析]根据溶解度曲线可知,20℃时,氯化钠的溶解度是36.0g;
(2) 增大
[解析]根据溶解度曲线可知,氯化钠的溶解度随温度升高而增大;
(3) 蒸发
[解析]“半日晒出盐霜”中的“晒”说明从氯化钠溶液中得到晶体的方法是蒸发
结晶。
13.(1) a ; 相等
1
(2) 蒸发
36.0g
14.(1) ×100%
36.0g+100g
[解析]由表中数据可知,20℃时,NaCl的溶解度为36.0g,即在20℃时,在
100g水中溶解36.0gNaCl,溶液达到饱和状态,则20℃时,NaCl饱和溶液中溶
36.0g
质质量分数为 ×100%。
36.0g+100g
(2) 继续加入溶质NH Cl(或恒温蒸发溶剂或降低温度)
4
[解析]由表中数据可知,NH Cl的溶解度随温度升高而增大,故将接近饱和的
4
NH Cl溶液变为饱和溶液,可采用的方法有继续加入溶质NH Cl、恒温蒸发溶
4 4
剂、降低温度。
(3) NaHCO
3
[解析]20℃时在NaCl和NH HCO 均达饱和的混合溶液中,会形成NaCl、
4 3
NH HCO 、NH Cl、NaHCO 四种物质,其中NaHCO 的溶解度最小,故会析
4 3 4 3 3
出NaHCO 晶体。
3
(4) A
[解析]20℃时,NH Cl的溶解度最大,因此20℃时配制等质量的四种物质的饱
4
和溶液,需水质量最小的是NH Cl,故A符合题意;NH Cl的溶解度随温度升高
4 4
而增大,而NaCl的溶解度受温度影响不大,因此提纯含少量氯化钠的氯化铵,
可先将其配制成60℃氯化铵饱和溶液,再降温结晶,故B不符合题意。
23关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点 5 溶质的质量分数
15.增大
16.14.2
17.1498.5
[解析]设需要水的质量为x,(1.5t+x)×0.1%=1.5t,解得x=1498.5t。
31.6g
18.增大; ×100%
100g+31.6g
提升练
19.C
[解析]溶液具有均一性和稳定性,溶液中各种粒子均是在不断地运动的,C错
误。
20.C
[解析]熟石灰的溶解度随温度升高而减小,饱和的熟石灰溶液升高温度仍然是
饱和溶液,A错误;均一、稳定的液体有可能是纯净物,如酒精等,B错误;
溶质可以是固体,也可以是液体或气体,如盐酸的溶质是氯化氢气体,D错
误。
21.D
[解析]配制100g该溶液需要KCl的质量为100g×6%=6g,C正确;溶液具有均
一性,取出一半溶液后,溶质质量分数不变,D错误。
22.D
[解析]已知40℃时100g水中最多溶解40g氯化钾,所以50g水中最多溶解20g氯
化钾,60g水中最多溶解24g氯化钾,70g水中最多溶解28g氯化钾,①、②形
成的是不饱和溶液,③形成的是饱和溶液。①的溶液的溶质质量分数为
10g 20g
×100%≈16.7%,②的溶液的溶质质量分数为 ×100%=25%,
10g+50g 20g+60g
A错误。③的溶液中溶质质量∶溶剂质量=28g:70g=2:5,B错误。降温时,由
于③形成的是饱和溶液,所以有晶体析出,而②形成的是不饱和溶液,若降温
后②仍为不饱和状态,则不会析出晶体,C错误。实验①所得溶液溶质质量分
数为16.7%,实验②所得溶液溶质质量分数为25%,实验③所得溶液溶质质量分
数为28.6%,将实验①、③所得溶液按一定比例混合能得到与②浓度相等的溶
液,D正确。
24关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
23.C
[解析]40℃时,向100g水中加入100gX全部溶解,说明40℃时X的溶解度大于
或等于100g,结合题表数据可知X为NaNO ,故A正确。③为NaNO 的不饱和
3 3
溶液分成两等份(每份中50g水和50gNaNO )后升温到60℃的溶液,溶解度
3
增大,故③仍然是不饱和溶液,且溶质质量分数与②相等;降温到20℃,
NaNO 的溶解度为88g,故50g水中最多溶解44g溶质,形成94g溶液,溶质质
3
量分数减小,故C错误,B、D正确。
24.36.0; 饱和; 不变
25.(1) 乙
[解析]烧杯乙中有未溶解的固体,一定为饱和溶液;
(2) T ℃时,硝酸钾与氯化钾的溶解度相等
2
[解析]图2中,P点是两条曲线的交点,表示T ℃时,两种物质的溶解度相等;
2
(3) 能
[解析]由图2可知,T ℃时氯化钾的溶解度大于硝酸钾,烧杯甲中是氯化钾溶
1
液,烧杯乙中是硝酸钾溶液,由于两物质在T ℃时溶解度相等,且烧杯中的水
2
量相等,加入的两物质的质量也相等,T ℃时烧杯甲中无剩余固体,烧杯乙中
2
一定也无剩余固体,即烧杯乙中的固体能全部溶解。
26.(1) 36
(2) 不饱和
[解析]20℃时,氯化钠的溶解度为36g,10g水中最多溶解3.6g氯化钠,而B 中
1
只析出2g氯化钠,说明A 中的溶液是氯化钠的不饱和溶液。
1
(3) 相等
[解析]B 、B 中都有未溶解的固体,说明B 、B 中的溶液都是20℃时氯化钠的
1 2 1 2
饱和溶液,溶质与溶剂的质量比相等。
(4) 2.4
[解析]由(2)中解析可知,蒸发出的10g水中还能继续溶解1.6g的氯化钠固
体,故加入4g氯化钠时,会有2.4g氯化钠固体不能溶解,故x=2.4。
(5) 25%
25关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
[解析]20℃,80g待测氯化钠溶液可看成两部分,一部分是10g水和2g氯化钠,
另一部分是80g−10g−2g=68g饱和氯化钠溶液,此部分中氯化钠的质量为
36 18g+2g
68g× =18g,故待测氯化钠溶液的溶质质量分数为 ×100%=25%。
136 80g
27.(1) 元素
(2) ① 甲
② 不能
[解析]40℃时氯化钾溶解度是40.0g,将50gKCl固体加入到100g水中,得到140g
饱和溶液。
③ 正确
④ 先不变后变小
[解析]降温过程中MgSO 的溶解度存在先增大后减小的过程,当溶解度大于
4
t ℃时MgSO 的溶解度时,溶液由饱和溶液变为不饱和溶液,溶质质量分数不
3 4
变;当溶解度小于t ℃时MgSO 的溶解度时,溶液中析出MgSO ,由不饱和溶
3 4 4
液再次变为饱和溶液,但溶质质量分数减小。
28.(1) >
[解析]由题干可知:LiOH和NaOH的化学性质相似,NaOH溶液显碱性,所以
LiOH溶液也显碱性,pH>7。
(2) LiOH的溶解度受温度变化的影响很小
[解析]蒸发结晶的方法适用于溶解度受温度变化影响不大的物质,冷却结晶的
方法适用于溶解度受温度变化影响较大的物质,LiOH的溶解度受温度变化的影
响不大,故可用蒸发结晶的方法提纯。
(3) ① 100
[解析]该溶液中LiOH的质量为1000g×10%=100g。
② 不饱和
[解析]20℃时,NaOH的溶解度为109g,即100g水中最多可溶解109gNaOH;
现该溶液中NaOH的质量为1000g×5%=50g,所以20℃时,当剩余100g水时,
得到的是NaOH的不饱和溶液。
(4) ¿
实验 4 水的组成及变化的探究
26关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.A
[解析]甲管中的气体是氢气,甲管中电极连接的是电源负极,A错误。
2.D
[解析]甲中微粒表示的是水分子,水分子能保持水的化学性质,A正确。乙中微
粒表示的是氢原子和氧原子,原子是化学变化中的最小微粒,在化学变化中不
发生改变,B正确。丙中氢气和氧气的质量比为1:8,D错误。
3.(1) O
2
[解析]水通电时,负极产生氢气,正极产生氧气,体积比约为2:1,b玻璃管与
电源的正极相连,产生的气体是O ;
2
(2) 纯度
[解析]氢气是一种可燃性气体,在点燃氢气前,一定要验纯。
4.(1) B
(2) ① 2:1
② b
③ ¿
(3) 900
[解析]设54kg水分解生成氢气的质量为x。
通电
2H O 2H ↑ + O ↑
2 ¿ 2 2 ¿x¿¿¿
36 ¿4 ¿ ¿
36 54kg
= x=6kg
4 x
使用1kg氢气平均可行驶150km,则使用6kg氢气理论上可供这辆汽车行驶的距离
为150km/kg×6kg=900km。
5.(1) 2
(2) ①
(3) 1:1
6.(1) ① 化合
[解析]由题图可知,氢气和氧气在点燃的条件下生成水,反应的化学方程式为
点燃
2H +O ,该反应符合“多变一”的特点,属于化合反应;
2 2 ¿
② 热值高(或燃烧产物是水,无污染等,合理即可)
27关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
[解析]返回舱返回的动力采用液氢作为能源的优点是热值高,燃烧产物是水,
无污染等。
(2) ¿
[解析]水通电分解生成氢气和氧气,反应的化学方程式为¿ 。
(3) 氢元素和氧元素
[解析]水通电分解生成氢气和氧气,液氧和液氢反应生成水,氢气由氢元素组
成,氧气由氧元素组成,根据质量守恒定律,反应前后元素种类不变,可得出
水是由氢、氧两种元素组成的。
7.(1) 负
(2) ¿; 节约能源
[解析]电解水实验需要消耗电能,所以该方法更加节约能源。
8.【宏观辨识】 (1) 氢元素和氧元素
(2) 2:1; H
2
[解析]电解水实验中,正极产生的气体是氧气,负极产生的气体是氢气,且氢
气与氧气的体积比为2:1。根据图像,管a与电源负极相连,产生的是氢气,管b
与电源正极相连,产生的是氧气,观察到管a和管b中气体体积比为2:1。
【证据推理】 2:1或4:2; 密度
[解析]相同条件下气体的体积比等于其分子的个数比,根据电解水生成氢气和
氧气的体积比为2:1可知,生成氢分子(H )与氧分子(O )的个数比为2:1,得出
2 2
电解水的产物中氢、氧原子个数比为(2×2):(1×2)=2:1。质量=体积×密度,已
知电解水实验中氢气和氧气的体积比,要计算出水中各元素质量比,则需要知
道正、负极产生气体的密度。
【模型构建】 各元素原子个数比(或分子中各原子个数比等)
[解析]化学式是通过元素符号及数字的组合表示物质组成的式子,知道相对分
子质量的情况下,需结合物质中各元素原子个数比来确定物质的化学式。
实验 5 一定溶质质量分数的溶液的配制
1.D
2.C
28关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
[解析]氢氧化钠有腐蚀性,不能放在纸上称量,应该放在小烧杯或表面皿里称
量,A错误;量筒的作用是量取液体,不能用来配制溶液,B错误;用胶头滴
管滴加液体时,不能伸入试管内,也不能触碰试管壁,D错误。
3.C
4.(1) A
(2) 玻璃棒; b
(3) 小于
5.(1) 搅拌,加速氯化钠溶解; B
(2) =
[解析]由于称量3g氯化钠使用的是砝码,未用游码,因此即使砝码和氯化钠的
位置放反了,也不影响称量结果。
6.碳酸钠的质量为100g×10%=10g,水的质量为100g−10g=90g
称取10克碳酸钠,用量筒量取90mL水,分别加入烧杯中,用玻璃棒搅拌溶解/将称
量的碳酸钠和量取的水依次放入烧杯,用玻璃棒搅拌使碳酸钠溶解(合理即可)
微专题 1 溶解度曲线
1.B
[解析]根据题图可知,硫酸铝的溶解度随温度升高而增大,将10℃时的饱和溶
液升温至40℃,会变为不饱和溶液,A错误;20℃时,硫酸铝的溶解度为
50
36.4g,即50.0g水中最多能溶解硫酸铝的质量为36.4g× =18.2g>16.0g,故
100
能形成不饱和溶液,B正确;40℃时,硫酸铝饱和溶液的溶质质量分数为
45.8g
×100%≈31.4%,D错误。
45.8g+100g
2.D
[解析]温度升高,Na CO 的溶解度变大,20℃时Na CO 的饱和溶液升温到40℃
2 3 2 3
时变成不饱和溶液,A错误。30℃时,NaCl的溶解度小于40g,即40gNaCl在
100g水中不能完全溶解,形成饱和溶液,B错误。比较不同物质的溶解度大小时
应指明温度,C错误。NaCl的溶解度受温度的影响不大,因此采用蒸发结晶的
方法;一定温度范围内,Na CO 的溶解度随温度的降低而明显减小,因此采用
2 3
降温结晶的方法,D正确。
29关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3.D
[解析]Na CO 的溶解度随温度升高先增大后减小,A错误;低于T℃时,
2 3
Na CO 的溶解度小于NaCl的溶解度,B错误;T℃时,NaCl的溶解度小于40g
2 3
,达到饱和时,50g水溶解NaCl的质量小于20g,30gNaCl不能完全溶解于50g
水中,C错误;T℃时,Na CO 和NaCl的溶解度相等,两种物质饱和溶液的溶
2 3
质质量分数相等,D正确。
4.C
[解析]“蒸发浓缩”是为了得到较高温度下KNO 的饱和溶液,B错误;“过滤”所
3
得滤液中的溶质除了NaCl还有KNO (滤液是KNO 结晶后过滤所得的,为对应
3 3
温度下KNO 的饱和溶液),D错误。
3
5.C
[解析]根据溶解度曲线,氯化钠、碳酸钠在20℃时的溶解度都大于10g,属于
易溶物质,A正确;该“果蔬洗盐”中含有碳酸钠和碳酸氢钠,会与食醋中的
醋酸反应,不能与食醋一起使用,B正确;碳酸钠在30℃时的溶解度是40g,
40g
则此时碳酸钠的饱和溶液中的溶质质量分数等于 ×100%≈28.6%<40%
40g+100g
,C错误;据题图可知氯化钠在20℃时的溶解度大约是36g,50g“果蔬洗
盐”含有氯化钠的质量是50g×50%=25g,则20℃时25g氯化钠放入100g水
中,形成的是NaCl的不饱和溶液,D正确。
6.(1) t
2
[解析]根据图像,t ℃时,甲、乙物质的溶解度曲线相交于一点,说明此温度
2
下,两种物质的溶解度相等。
(2) 乙> 甲> 丙
[解析]从图中看出,甲、乙的溶解度随温度的升高而增大,丙的溶解度随温度
的升高而减小,t ℃时将甲、乙、丙三种物质的饱和溶液降温到t ℃,甲、乙
3 1
的溶解度减小,有溶质析出,仍然是饱和溶液,溶质质量分数减小;丙的溶解
度增大,变成不饱和溶液,因为溶质和溶剂质量都没变,故溶质质量分数不
变。由于t ℃乙的溶解度大于甲,因此乙的溶液的溶质质量分数大于甲的溶
1
液,由于甲在t ℃时的溶解度大于丙在t ℃时的溶解度,因此甲的溶液的溶质
1 3
30关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
质量分数大于丙的溶液,所得溶液的溶质质量分数由大到小的顺序为乙> 甲>
丙。
(3) 50; 搅拌,加快溶解
[解析]t ℃时,甲的溶解度是60g,即100g水中最多能溶解60g甲,将30g甲物
3
质完全溶解配制成该温度下甲的饱和溶液,则需加入水的质量为50g;溶解过
程中用玻璃棒搅拌,加快溶解。
(4) 蒸发结晶
[解析]乙的溶解度受温度变化影响较小,甲的溶解度受温度变化影响较大,当
乙中混有少量的甲时,可采用蒸发结晶的方法提纯乙。
7.(1) 甲
(2) 减小
[解析]由题图看出,乙的饱和溶液温度降低时,溶解度减小,有晶体析出,溶
质减少,故溶液的质量减小。
(3) 5.0g
[解析]60.0g甲溶液中含10.0g甲,则含水50.0g。由题图看出,a ℃时,甲的溶
2
30g
解度是30.0g,50.0g水中溶解50.0g× =15.0g甲达到饱和,则需要再加入
100g
5.0g甲。
(4) ACD
[解析]若加入的三种固体完全溶解,则溶质质量分数相等,A符合题意;如果溶
解度:乙> 甲,说明温度低于a ℃,此时,丙的溶解度要大于甲和乙,丙的溶
2
质质量分数最大,B不符合题意;当温度低于a ℃时,溶解度:丙> 乙> 甲,
2
则若甲中固体没有完全溶解,乙、丙中固体完全溶解,则溶质质量分数:乙=丙
> 甲,C符合题意;当温度刚大于a ℃时,溶解度:丙> 甲> 乙,则所得溶液的
2
溶质质量分数可能为丙> 甲> 乙,D符合题意。
8.(1) b
[解析]20℃时向100g水中加入46gW,有固体剩余,说明20℃时W的溶解度小
于46g,因此W是题图2中的b曲线。
(2) 21.8
31关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
[解析]操作①所得溶液是饱和溶液,溶解度(S)与溶质质量分数的关系满足:
S
×100%=17.9%,解得S≈21.8g。
S+100g
(3) 无明显现象
[解析]根据表格信息,40℃时W的溶解度为48.8g,100g水中加入46gW,得到
W的不饱和溶液,升温到60℃时,W的溶解度为46.4g,此时溶液仍为W的不
饱和溶液,故经操作③后无明显现象。
(4) 45.1
[解析]操作③后继续升温至80℃,有0.9gW析出,说明80℃时100g水中最多能
溶解W的质量为46g−0.9g=45.1g,即80℃时溶解度为45.1g。
32