文档内容
2016年连云港市中考化学试卷及答案
一、选择题(共12小题,每小题2分,满分24分)
1.今年4月22日是第47个世界地球日,主题是“节约集约利用资源,倡导绿色简约生活”,下列做法不应该提倡
的是
A.少开私家车多步行 B.对废旧金属进行回收利用
C.经常使用一次性筷子,塑料袋等 D.开发太阳能、风能等,减少对化石能源的依赖
2.如图所示变化中,属于化学变化的是
A.冰雪融化 B.燃料燃烧 C.橙汁榨汁 D.品红扩散
3.下列化学用语表示正确的是
A.氧元素:O B.氮气分子:2N C.钠离子: D.高锰酸钾的化学式:KMnO
2 4
4.下列有关物质用途的说法不正确的是
A.可用小苏打治疗胃酸过多症 B.可用甲醛水溶液保存食用海产品
C.可用稀有气体制成多种用途的电光源 D.可用洗涤剂除去衣服、餐具上的油污
5.目前世界上最精确的钟是以锶做钟摆的钟,锶的原子结构示意图及元素周期表中某些信息如图所示,下列说法
正确的是
A.x的值为8
B.锶属于非金属元素
C.锶的相对原子质量为87.62g
D.锶原子在化学反应中易失去电子
6.如图所示实验操作正确的是
A.测溶液的pH B.读出液体体积 C.稀释浓硫酸 D.移走蒸发皿
7.下列说法正确的是
A.金刚石和石墨都是由碳元素组成的单质 B.在化学反应中只有燃烧反应才能放出热量
C.地壳中元素含量由多到少的顺序是:O>Al>Si D.VmL水和VmL酒精混合得VmL溶液:V+V=V
1 2 3 1 2 3
8.金属活动性顺序表在化学学习中有重要作用,下列说法正确的是
A.Zn不能置换出稀硫酸中的氢 B.Ag能将硝酸铜溶液中的铜置换出来
C.在Al、Mg、Fe中金属活动性最强的是Al D.“真金不怕火炼”说明金在高温时也不与氧气反应
9.尿素[CO(NH)]是一种重要的化学肥料,下列说法正确的是
2 2
A.尿素属于复合肥料 B.60g尿素中含有氮元素的质量为28g
C.尿素中含有氢分子 D.尿素中碳、氧两种元素的质量比为1:1
10.下列根据实验目的所设计的实验方案正确的是
选项 实验目的 实验设计
A 除去CO 中的CO 点燃
2
B 测定某地雨水是否为酸雨 加无色酚酞,观察颜色变化
C 鉴别NHCl和(NH)SO 加入熟石灰研磨,闻气味
4 4 2 4
D 探究燃烧的条件之一是需要可燃物 用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻,观察现象
A.A B.B C.C D.D
11.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是
A.a℃时甲的饱和溶液,升温至a℃时仍是饱和溶液
1 2
1B.乙的溶解度随温度的升高而增大
C.相同温度时,甲的溶解度一定大于乙的溶解度
D.分别将甲、乙的饱和溶液从a℃降至a℃时,所得溶液中溶质的质量分数相等
2 1
12.如图所示,甲、乙、丙、丁、戊五种物质分别是铁、盐酸、氢氧化钙、硫酸 铜、碳酸
钠中的一种,连线两端的物质间能发生化学反应,甲与戊反应产生的气体能使澄清石
灰水变浑浊,丙溶液为蓝色,下列能代替图中丁物质的是
A.Ag B.BaCl C.NaOH D.CuO
2
二、解答题(共4小题,满分36分)
13.(6分)化学使人类生活更美好.
(1)豆浆已成为众多家庭的饮品,下表是豆浆中部分营养成分的平均质量分数。请据表回答:
成分 蛋白质 油脂 糖类 钙 铁 维生素
质量分数/% 1.8 0.7 1.1 0.01 0.0005 0.015
① 豆浆中含有人体所需的微量元素是 ,青少年因缺 而导致佝偻病。
② 豆浆所含的营养素中不能供给人体能量,当可以起到调节新陈代谢作用的是 (填字母,下同)
A.蛋白质 B.油脂 C.糖类 D.维生素
(2)材料对我们的生活影响越来越大。
① 用作保险丝的武德合金属于 。
A.金属材料 B.合成材料 C.复合材料
② 下列方法不能防止钢铁腐蚀的是 。
A.表面镀铬 B.表面涂油漆 C.部分浸入食盐水
③ 有一种用“冰蚕丝”面料做的衣服,面料的主要成分是合成纤维,鉴别“冰蚕丝”和天然蚕丝的化学方法是
。
14.(10分)掌握科学的研究方法,探索化学世界的奥秘。
(1)分类是学习化学的重要方法之一.
① 生活中,常会接触到下列物质:
A.铜丝 B.甲烷 C.过氧化氢 D.碘酒
其中属于混合物的是(填字母,下同) ,属于氧化物的是 。
② 根据物质在转化过程中的特点,可将化学反应分为化合反应,分解反应、置换反应和复分解反应四种基本反应
类型,下列转化不属于这四种基本反应类型的是 。
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
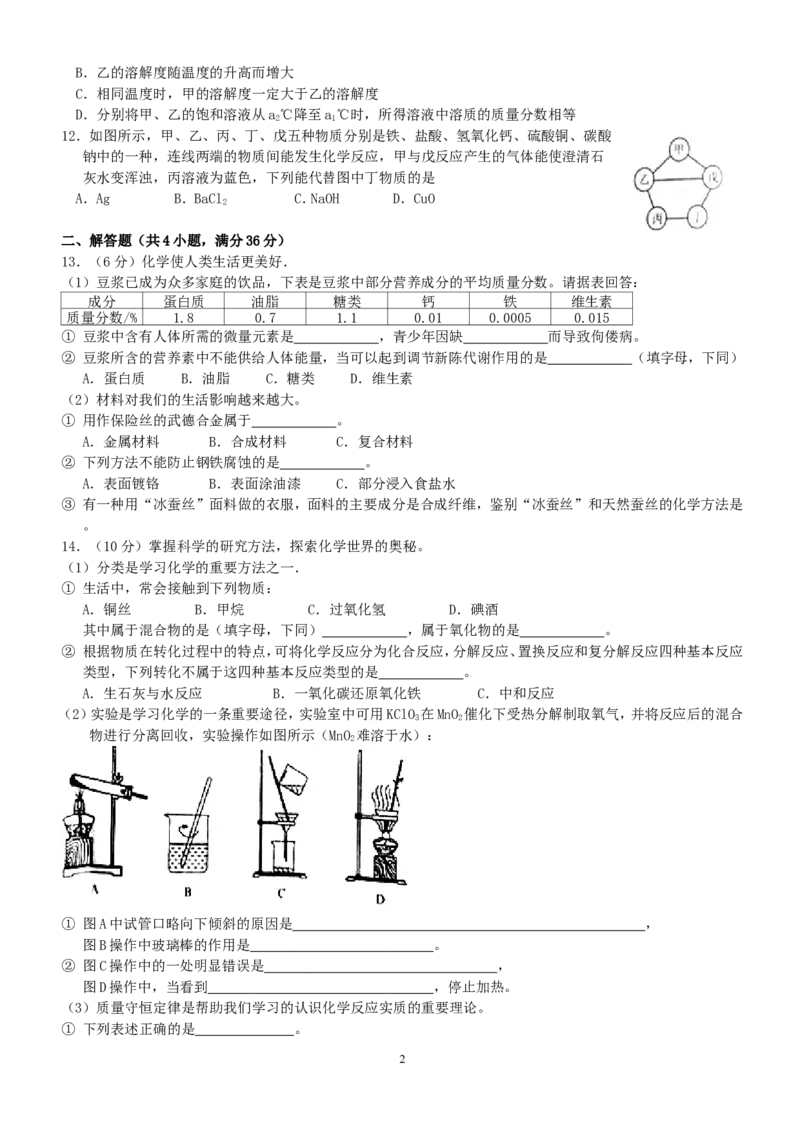
(2)实验是学习化学的一条重要途径,实验室中可用KClO 在MnO 催化下受热分解制取氧气,并将反应后的混合
3 2
物进行分离回收,实验操作如图所示(MnO 难溶于水):
2
① 图A中试管口略向下倾斜的原因是 ,
图B操作中玻璃棒的作用是 。
② 图C操作中的一处明显错误是 ,
图D操作中,当看到 ,停止加热。
(3)质量守恒定律是帮助我们学习的认识化学反应实质的重要理论。
① 下列表述正确的是 。
2A.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
B.每32g S和32g O 完全反应后,生成64g SO
2 2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
② 有机化合物R与足量氧气置于密闭容器中充分反应生成CO 和HO,实验测得反应前后物质的质量如下表:
2 2
R O CO HO
2 2 2
反应前质量/g 46 128 0 0
反应后质量/g 0 32 x 54
则x= ,已知参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是
。
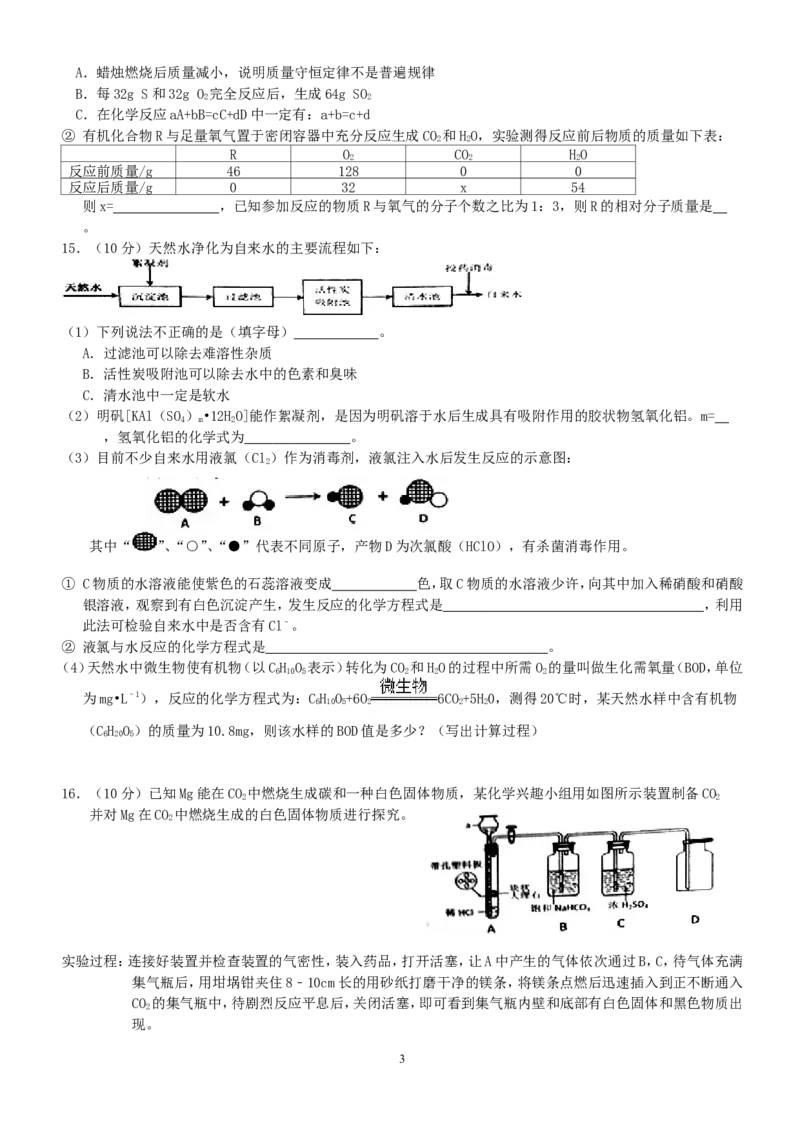
15.(10分)天然水净化为自来水的主要流程如下:
(1)下列说法不正确的是(填字母) 。
A.过滤池可以除去难溶性杂质
B.活性炭吸附池可以除去水中的色素和臭味
C.清水池中一定是软水
(2)明矾[KAl(SO)•12HO]能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。m=
4 m 2
,氢氧化铝的化学式为 。
(3)目前不少自来水用液氯(Cl)作为消毒剂,液氯注入水后发生反应的示意图:
2
其中“ ”、“○”、“●”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用。
① C物质的水溶液能使紫色的石蕊溶液变成 色,取C物质的水溶液少许,向其中加入稀硝酸和硝酸
银溶液,观察到有白色沉淀产生,发生反应的化学方程式是 ,利用
此法可检验自来水中是否含有Cl﹣。
② 液氯与水反应的化学方程式是 。
(4)天然水中微生物使有机物(以CH O 表示)转化为CO 和HO的过程中所需O 的量叫做生化需氧量(BOD,单位
6 10 5 2 2 2
为mg•L﹣1),反应的化学方程式为:CH O+6O 6CO+5H0,测得20℃时,某天然水样中含有机物
6 10 5 2 2 2
(CH O)的质量为10.8mg,则该水样的BOD值是多少?(写出计算过程)
6 20 5
16.(10分)已知Mg能在CO 中燃烧生成碳和一种白色固体物质,某化学兴趣小组用如图所示装置制备CO
2 2
并对Mg在CO 中燃烧生成的白色固体物质进行探究。
2
实验过程:连接好装置并检查装置的气密性,装入药品,打开活塞,让A中产生的气体依次通过B,C,待气体充满
集气瓶后,用坩埚钳夹住8﹣10cm长的用砂纸打磨干净的镁条,将镁条点燃后迅速插入到正不断通入
CO 的集气瓶中,待剧烈反应平息后,关闭活塞,即可看到集气瓶内壁和底部有白色固体和黑色物质出
2
现。
3查阅资料:①饱和NaHCO 溶液可以吸收HCl而不吸收CO;②MgO、Mg(OH)、MgCO 均为白色固体。
3 2 2 3
(1)仪器a的名称是 ;
(2)装置B中发生反应的化学方程式是 ,
装置C的作用是 。
(3)检验D中集气瓶已经充满CO 的方法是 。
2
(4)白色固体物质是什么?甲同学提出了三种猜想:
猜想Ⅰ:白色固体物质是MgO
猜想Ⅱ:白色固体物质是Mg(OH)
2
猜想Ⅲ:白色固体物质是MgCO
3
① 上述猜想中,你认为不合理的猜想是 (填Ⅰ或Ⅱ或Ⅲ),理由是 。
② 乙同学取D中的白色固体于试管中,向其中加入足量的稀硫酸,固体溶解,无气泡产生,据此可知猜想
(填Ⅰ或Ⅱ或Ⅲ)是合理的,则镁在D中发出反应的化学方程式是 。
参考答案
一、选择题(共12小题,每小题2分,满分24分)
1.C 2.B 3.A 4.B 5.D 6.C 7.A 8.D 9.B 10.D 11.D 12.C.
二、解答题13.(1)①铁;钙;②维生素;
(2)①A;②C;③灼烧、闻气味.
14.(1)D,C ②B
(2)①防止水倒流,炸裂试管;搅拌,加速溶解;
②漏斗末端没有仅靠烧杯内壁;当看到有较多固体析出时
(3)①B ②88;46
15. (1)C;(2)2;Al(OH);
3
(3)①红;HCl+AgNO=AgCl↓+HNO.②Cl+HO═HCl+HClO.(4)则该水样的BOD值是12.8mg•L﹣
3 3 2 2
16.(1)长颈漏斗;
(2)NaHCO+HCl=NaCl+HO+CO↑;干燥;
3 2 2
(3)把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满.
(4)
Ⅰ;2Mg+CO 2MgO+C.
2
4连云港市2016年中考化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32
一、选择题(本题包括12小题,每小题2分,共24分,每小题只有一个选项符合题意)
1.今年4月22是第47个世界地球日,主题是“节约集约利用资源,倡导绿色简约生活”。下列做法不应该提倡
的是( )
A.少开私家车多步行 B.对废旧金属进行回收利用
C.经常使用一次性筷子、塑料袋等 D.开发太阳能、风能等,减少对化石能源的依赖
【答案】C
【解析】
试题分析:A、少开私家车多步行,可以减少汽油的燃烧,从而减少汽车尾气的排放,正确,B、对废旧金属进行回收
利用,一可以节约成分,二还可以保护环境,正确,C、一次性筷子需要砍伐树木,破坏环境,使用塑料袋会导
致白色污染,故不宜提倡经常使用一次性筷子、塑料袋等,错误,D、太阳能、风能等,都属于绿色能源,故开发
太阳能、风能等,减少对化石能源的依赖,正确,故选C
考点:化学与环境
2.下图所示变化中,属于化学变化的是( )
【答案】B
考
点:化学变化和物理变化的判别
3.下列化学用语表示正确的是( )
A.氧元素:O B.氮气分子:2N
+1
C.钠离子:Na D.高锰酸钾的化学式:KMnO
2 4
【答案】B
5【解析】
试题分析:A、氧元素:O,正确,B、氮气分子:N,2N表示2个氮原子,错误,C、离子符号表示方法:在元素符号右上
2
角标明电性和电荷数,数字在前,符号在后。若数字为1时,可省略不写,故钠离子:Na+,错误,D、高锰酸钾的
化学式:KMnO,错误,故选B
4
考点:化学用语的书写
4.下列有关物质用途的说法不正确的是( )
A.可用小苏打治疗胃酸过多症 B.可用甲醛水溶液保存食用海产品
C.可用稀有气体制成多种用途的电光源 D.可用洗涤剂除去衣服、餐具上的油污
【答案】B
考
点:物质的性质与用途,甲醛的毒性,乳化作用
5.目前世界上最精准的钟是以锶做钟摆的钟。锶的原子结构示意图及在元素周期表中某些信息如右图所示,下列
说法正确的是( )
A.x的值为8
B.锶属于非金属元素
C.锶的相对原子质量为87.62g
D.锶原子的化学反应中易失去电子
【答案】D
【解析】
试题分析:元素周期表中某方格中的信息:原子序数、元素符号、元素名称、相对原子质量;A、原子中,质子数=核
外电子数,故x的值=38-2-2-8-8=18,错误,B、锶的偏旁部首是“金字旁”,属于金属元素,,错误,C、相对原
子质量是一个比值,单位不是g,错误,D、锶原子的最外层电子数为2<4,故在化学反应中易失去电子,正确,
故选D
考点:元素周期表中信息,核外电子排布的知识
6.下图所示实验操作正确的是( )
6【答案】C
【解析】
试题分析:A、测溶液pH时,不能将pH试纸直接伸入待测液中,而是用玻璃棒蘸取待测液于pH试纸上,显色后与
比色卡对照,错误,B、读数时,视线应与刻度线及凹液面的最低处保持水平,错误,C、稀释浓硫酸时:应把浓
硫酸沿烧杯壁慢慢注入水里,并不断搅动使产生的热量迅速扩散,切不可把水直接倒入浓硫酸中,正确,D、
移走蒸发皿应用坩埚钳,错误,故选C
考点:基本实验操作
7.下列说法正确的是( )
A.金刚石和石墨都是由碳元素组成的单质
B.在化学反应中只有燃烧反应才能放出热量
C.地壳中元素含量由多到少的顺序是:O﹥Al﹥Si
D.VmL水和VmL酒精混合得到VmL溶液:V+ V= V
1 2 3 1 2 3
【答案】A
考点:物质的组成,化学反应中的能量变化,地壳中元素的含量,分子的基本性质
8.金属活动性顺序表在化学学习中有重要作用。下列说法正确的是( )
A.Zn不能置换出稀硫酸中的氢
B.Ag能将硫酸铜溶液中的铜置换出来
C.在Al、Mg、Fe中金属活动性最强的是Al
D.“真金不怕火炼”说明金在高温时也不与氧气反应
【答案】D
【解析】
试题分析:A、在金属活动性顺序表中,锌排在氢前,故Zn能置换出稀硫酸中的氢,错误,B、由于Ag的活动性比Cu
弱,故Ag不能将硫酸铜溶液中的铜置换出来,错误,C、在Al、Mg、Fe中金属活动性最强的是Fe ,错误,D、
7“真金不怕火炼”说明金在高温时也不与氧气反应,正确,故选D
考点:金属的活动性
9.尿素[CO(NH)]是一种重要的化学肥料。下列说法正确的是( )
2 2
A.尿素属于复合肥料 B.60g尿素中含有氮元素的质量为28g
C.尿素中含有氢分子 D.尿素中碳、氧两种元素的质量比为1:1
【答案】B
【解析】
试题分析:A、尿素[CO(NH)]只含营养元素N,属于氮肥,错误,B、根据元素质量=物质质量×元素质量分数,60g
2 2
尿素中含有氮元素的质量=60g×28/60×100%=28g,正确,C、尿素[CO(NH)]是由尿素分子构成,尿素分子中
2 2
含有氢原子,错误,D、尿素中碳、氧两种元素的质量比为12:16,错误,故选B
考点:化学肥料,根据化学式进行的计算,物质的构成
10.下列根据实验目的所设计的实验方案正确的是( )
【答案】D
考点:物质的除杂及鉴别,酸的化学性质,燃烧条件的探究
11.甲、乙两种物质的溶解度曲线如右图所示。下列说法正确的是( )
A.a℃时甲的饱和溶液,升温至a℃时仍是饱和溶液
1 2
B.乙的溶解度随温度的升高而增大
C.相同温度时,甲的溶解度一定大于乙的溶解度
8D.分别将甲、乙的饱和溶液从a℃将至a℃时,所得溶液中溶质的质量分数相等
2 1
【答案】D
考点:溶解度曲线的意义
12.如右图所示,甲、乙、丙、丁、戊五种物质分别是铁、盐酸、氢氧化钙、硫酸铜、碳酸钠中的一种。连线两端的物
质间能发生化学反应,甲与戊反应产生的气体能使澄清石灰水变浑浊,丙溶液为蓝色。下列能替代图中丁物
质的是( )
A.Ag B.BaCl C.NaOH D.CuO
2
【答案】C
【解析】
试题分析:根据丙溶液为蓝色,可判断为硫酸铜;甲与戊反应产生的气体能使澄清石灰水变浑浊,说明两者为盐
酸,碳酸钠;假设甲为盐酸,戊为碳酸钠,那么乙为铁,但是铁不会与碳酸钠反应,故此假设不成立,说明甲应
为碳酸钠,戊为盐酸,那么乙为氢氧化钙,丁则为单质铁,故能代替铁的是NaOH,故选C
考点:酸、碱、盐的化学性质,物质的推断
二、非选择题(本题包括4小题,共36分)
13.(6分)化学使人类生活更美好
(1)豆浆已成为众多家庭的饮品。下表是豆浆中部分营养成分的平均质量分数。
请据表回答:
①豆浆中含有人体所需的微量元素是 ;青少年因缺 而导致佝偻病。
②豆浆所含的营养素中不能供给人体能量,但可以起到调节新陈代谢作用的是(填字母,下同)
9。
A.蛋白质 B.油脂 C.糖类 D.维生素
(2)材料对我们的生活影响越来越大。
①用作保险丝的武德合金属于 。
A.金属材料 B.合成材料 C.复合材料
②下列方法不能防止钢铁腐蚀的是 。
A.表面镀铬 B.表面涂油漆 C.部分浸入食盐水
③有一种“冰蚕丝”面料做的衣服,面料的主要成分是合成纤维。鉴别“冰蚕丝”和天然蚕丝的化学方
法是 。
【答案】(1)①铁 钙 ②D (2)①A ②C ③灼烧闻气味
考
点:化学元素与人体健康,金属材料,铁生锈的条件,合成纤维、天然纤维的鉴别
14.(10分)掌握科学的研究方法,探索化学世界的奥秘。
(1)分类是学习化学的重要方法之一。
①生活中,常会接触到下列物质:A.铜丝 B.甲烷 C.过氧化氢 D.碘酒
其中属于混合物的是(填字母,下同) ,属于氧化物的是 。
②根据物质在转化过程中的特点,可将化学反应分为化合反应、分解反应、置换反应和复分解反应四种
基本反应类型。下列转化不属于这四种基本反应类型的是 。
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
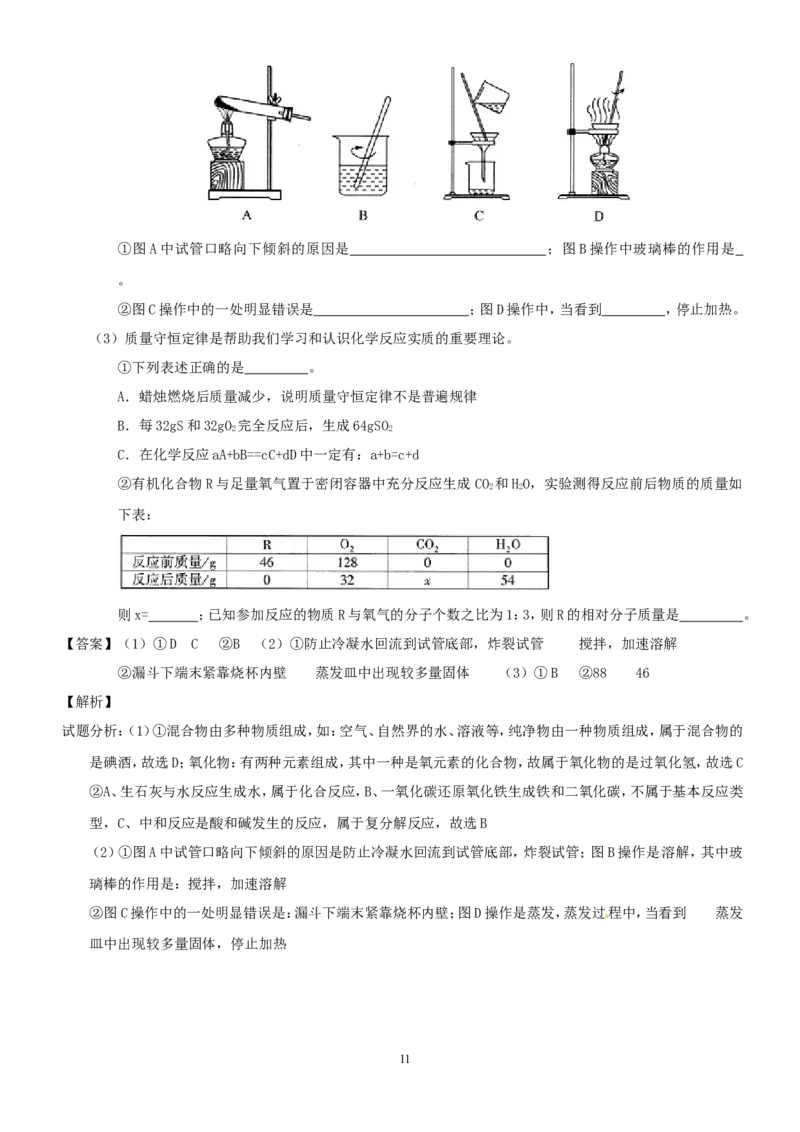
(2)实验是学习化学的一种重要途径。实验室中可用KClO 在MnO 催化下受热分解制取氧气,并将反应后的
3 2
混合物进行分离回收。实验操作如图所示(MnO 难溶于水):
2
10①图A中试管口略向下倾斜的原因是 ;图B操作中玻璃棒的作用是
。
②图C操作中的一处明显错误是 ;图D操作中,当看到 ,停止加热。
(3)质量守恒定律是帮助我们学习和认识化学反应实质的重要理论。
①下列表述正确的是 。
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32gS和32gO 完全反应后,生成64gSO
2 2
C.在化学反应aA+bB==cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO 和HO,实验测得反应前后物质的质量如
2 2
下表:
则x= ;已知参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是 。
【答案】(1)①D C ②B (2)①防止冷凝水回流到试管底部,炸裂试管 搅拌,加速溶解
②漏斗下端末紧靠烧杯内壁 蒸发皿中出现较多量固体 (3)①B ②88 46
【解析】
试题分析:(1)①混合物由多种物质组成,如:空气、自然界的水、溶液等,纯净物由一种物质组成,属于混合物的
是碘酒,故选D;氧化物:有两种元素组成,其中一种是氧元素的化合物,故属于氧化物的是过氧化氢,故选C
②A、生石灰与水反应生成水,属于化合反应,B、一氧化碳还原氧化铁生成铁和二氧化碳,不属于基本反应类
型,C、中和反应是酸和碱发生的反应,属于复分解反应,故选B
(2)①图A中试管口略向下倾斜的原因是防止冷凝水回流到试管底部,炸裂试管;图B操作是溶解,其中玻
璃棒的作用是:搅拌,加速溶解
②图C操作中的一处明显错误是:漏斗下端末紧靠烧杯内壁;图D操作是蒸发,蒸发过程中,当看到 蒸发
皿中出现较多量固体,停止加热
11考点:物质的分类,基本反应类型的判断,基本实验操作,质量守恒定律
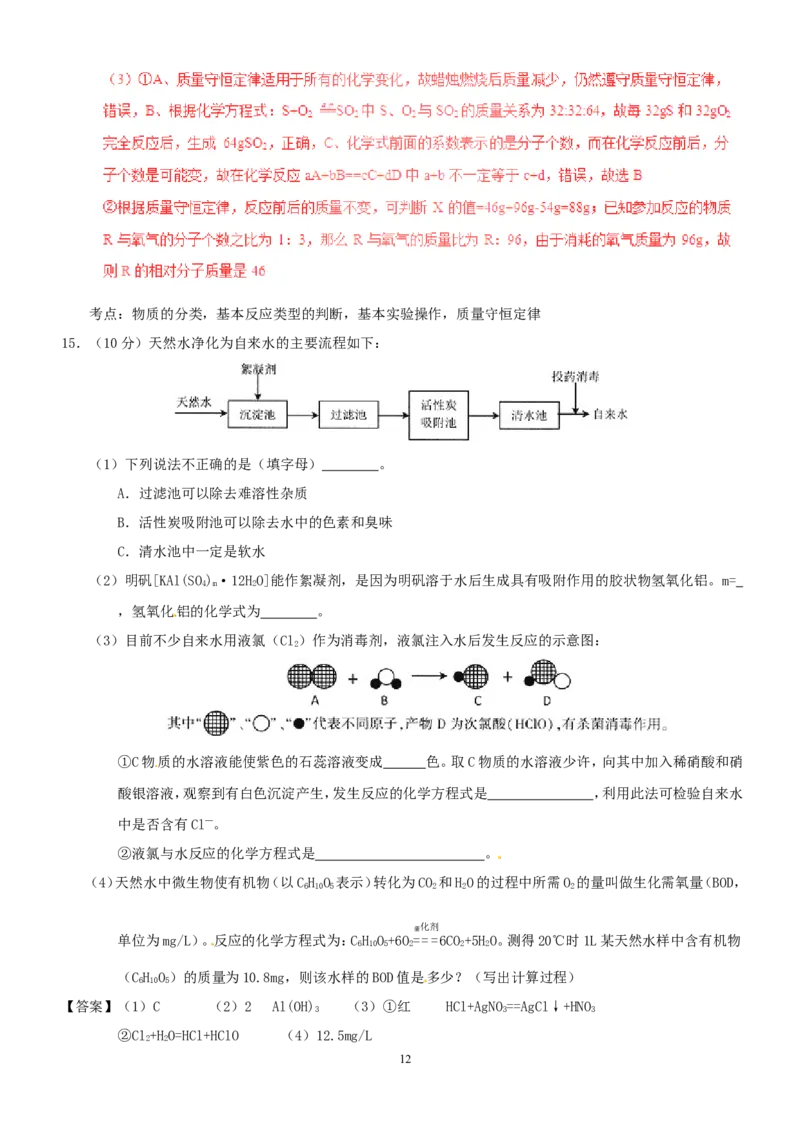
15.(10分)天然水净化为自来水的主要流程如下:
(1)下列说法不正确的是(填字母) 。
A.过滤池可以除去难溶性杂质
B.活性炭吸附池可以除去水中的色素和臭味
C.清水池中一定是软水
(2)明矾[KAl(SO)·12HO]能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。m=
4 m 2
,氢氧化铝的化学式为 。
(3)目前不少自来水用液氯(Cl)作为消毒剂,液氯注入水后发生反应的示意图:
2
①C物质的水溶液能使紫色的石蕊溶液变成 色。取C物质的水溶液少许,向其中加入稀硝酸和硝
酸银溶液,观察到有白色沉淀产生,发生反应的化学方程式是 ,利用此法可检验自来水
中是否含有Cl—。
②液氯与水反应的化学方程式是 。
(4)天然水中微生物使有机物(以CH O 表示)转化为CO 和HO的过程中所需O 的量叫做生化需氧量(BOD,
6 10 5 2 2 2
催化剂
单位为mg/L)。反应的化学方程式为:CH O+6O===6CO+5HO。测得20℃时1L某天然水样中含有机物
6 10 5 2 2 2
(CH O)的质量为10.8mg,则该水样的BOD值是多少?(写出计算过程)
6 10 5
【答案】(1)C (2)2 Al(OH) (3)①红 HCl+AgNO==AgCl↓+HNO
3 3 3
②Cl+HO=HCl+HClO (4)12.5mg/L
2 2
12催化剂
(4)根据化学方程式:CH O+6O===6CO+5HO中CH O 与O 的质量关系,可计算出氧气的质量,进而计算该水样
6 10 5 2 2 2 6 10 5 2
的BOD
解:设氧气的质量为x
催化剂
CH O+6O===6CO+5HO
6 10 5 2 2 2
162 192
10.8mg x
162:192=10.8mg:x
x=12.8mg
该水样的BOD的值=12.8mg÷1L=12.8mg/L
考点:水的净化,元素化合价的一般规律,化学反应微粒示意图,酸的化学性质,根据化学方程式进行的计算
16.(10分)已知Mg能在CO 中中燃烧生成碳和一种白色固体物质。某化学兴趣小组用下图所示装置制备CO 并对
2 2
Mg在CO 中燃烧生成的白色固体物质进行探究。
2
实验过程:连接好装置并检查装置的气密性,装入药品。打开活塞,让A中产生的气体依次通过B、C,待气体充满
13集气瓶后,用坩埚钳夹住8~10cm长的用砂纸打磨干净的镁条,将镁条点燃后迅速插入到正不断通入CO 的
2
集气瓶中,待剧烈反应平息后,关闭活塞,即可看到集气瓶内壁和底部有白色固体和黑色固体物质出现。
查阅资料:①饱和NaHCO 溶液可以吸收HCl而不吸收CO;
3 2
②MgO、Mg(OH)、MgCO 均为白色固体。
2 3
(1)仪器a的名称是 。
(2)装置B中发生反应的化学方程式是 ;装置C的作用是 。
(3)检验D中集气瓶已经充满CO 的方法是 。
2
(4)白色固体物质是什么?甲同学提出了三种猜想:
猜想Ⅰ:白色固体物质是MgO
猜想Ⅱ:白色固体物质是Mg(OH)
2
猜想Ⅲ:白色固体物质是MgCO
3
①上述猜想中,你认为不合理的猜想是 (填Ⅰ或Ⅱ或Ⅲ),理由是 。
②乙同学取D中的白色固体于试管中,向其中加入足量的稀硫酸,固体溶解,无气泡产生。据此可知猜想
( 填 Ⅰ 或 Ⅱ 或 Ⅲ ) 是 合 理 的 , 则 镁 在 D 中 发 生 反 应 的 化 学 方 程 式 是
。
【答案】(1)长颈漏斗 (2)NaHCO+HCl==NaCl+HO+CO↑ 干燥(除去水分)
3 2 2
(3)将燃着的木条放在集气瓶口,熄灭 (4)①Ⅱ 反应物中无氢元素
②Ⅰ 2Mg + CO 点燃 2MgO+C
2
考
点:常见仪器的识记,气体的除杂和干燥,反应后物质成分的探究,质量守恒定律,碳酸盐的化学性质
14