文档内容
2024 年江苏省南通市中考化学试卷
一、选择题
1. 江海大地河网密布,水资源丰富。下列有利于构建人水和谐新南通的是
A. 直接向河流中排放生活废水 B. 及时清理河道垃圾
C. 大量抽取地下水作工业用水 D. 过度繁殖水生植物
2. 诗句“千锤万凿出深山,烈火焚烧若等闲”中涉及的石灰石,其主要成分CaCO 属于
3
A. 酸 B. 碱 C. 盐 D. 氧化物
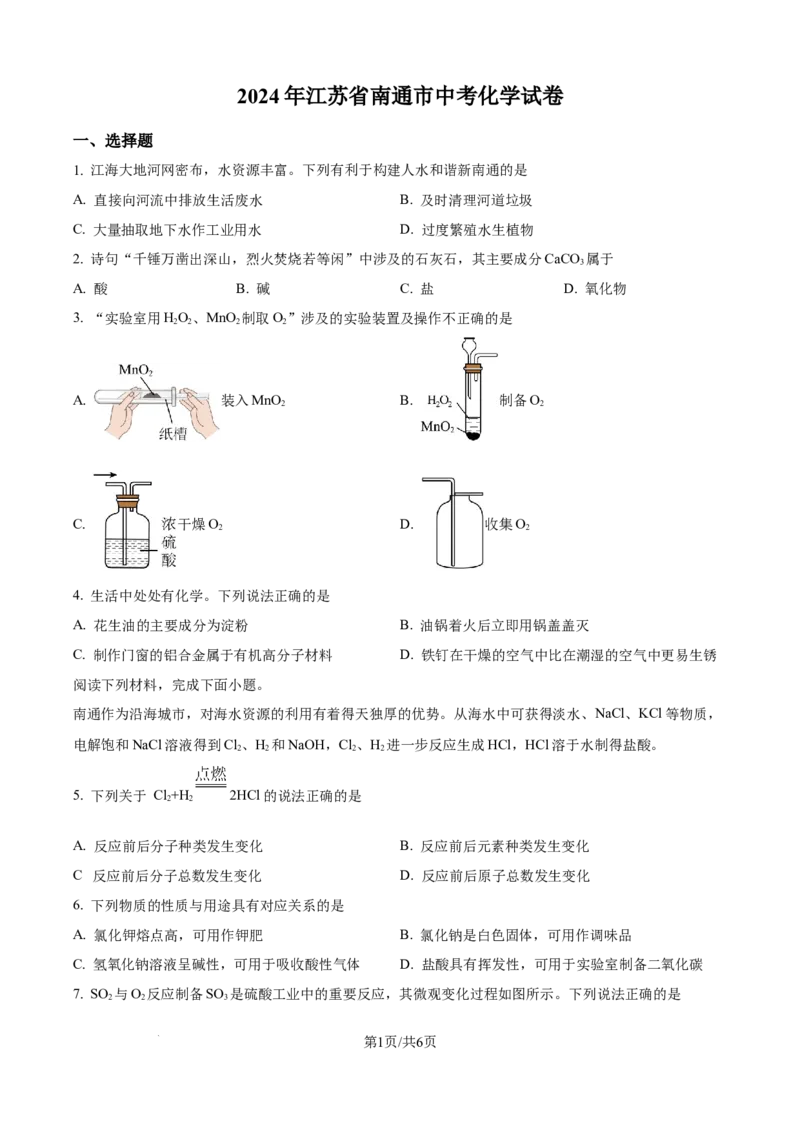
3. “实验室用HO、MnO 制取O”涉及的实验装置及操作不正确的是
2 2 2 2
A. 装入MnO B. 制备O
2 2
C. 干燥O D. 收集O
2 2
4. 生活中处处有化学。下列说法正确的是
A. 花生油的主要成分为淀粉 B. 油锅着火后立即用锅盖盖灭
C. 制作门窗的铝合金属于有机高分子材料 D. 铁钉在干燥的空气中比在潮湿的空气中更易生锈
阅读下列材料,完成下面小题。
南通作为沿海城市,对海水资源的利用有着得天独厚的优势。从海水中可获得淡水、NaCl、KCl等物质,
电解饱和NaCl溶液得到Cl、H 和NaOH,Cl、H 进一步反应生成HCl,HCl溶于水制得盐酸。
2 2 2 2
5. 下列关于 Cl+H 2HCl的说法正确的是
2 2
A. 反应前后分子种类发生变化 B. 反应前后元素种类发生变化
.
C 反应前后分子总数发生变化 D. 反应前后原子总数发生变化
6. 下列物质的性质与用途具有对应关系的是
A. 氯化钾熔点高,可用作钾肥 B. 氯化钠是白色固体,可用作调味品
C. 氢氧化钠溶液呈碱性,可用于吸收酸性气体 D. 盐酸具有挥发性,可用于实验室制备二氧化碳
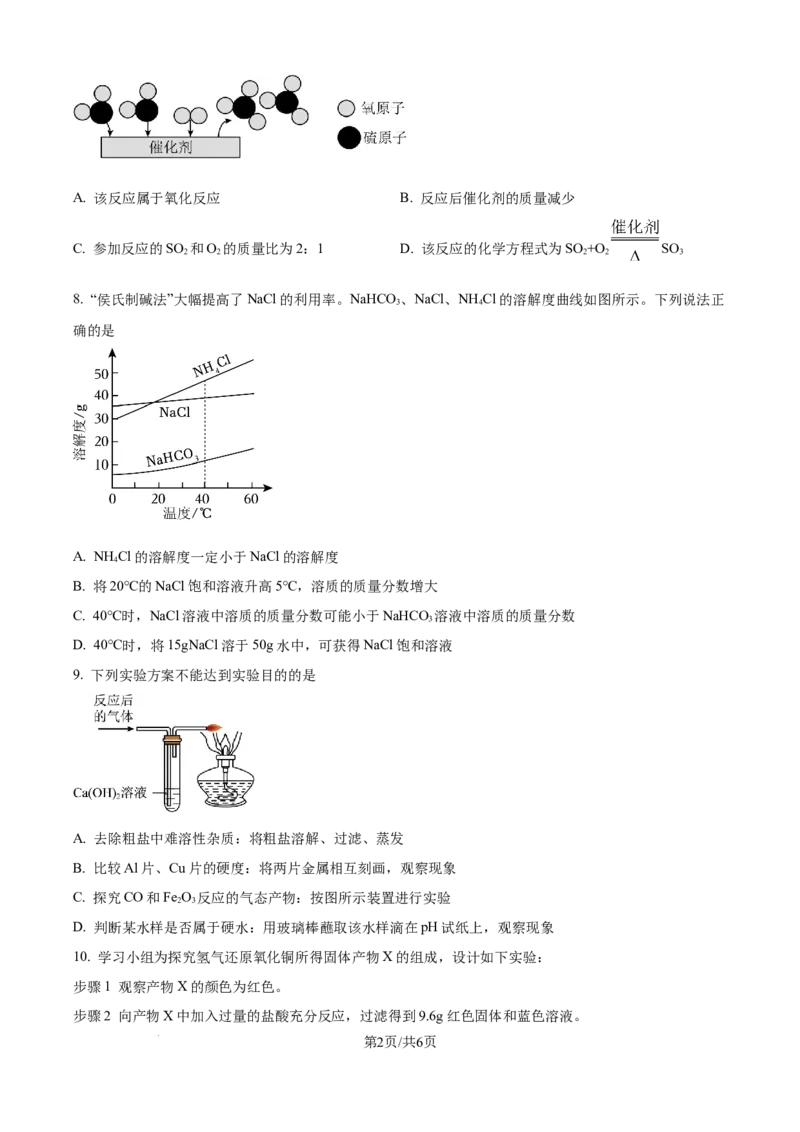
7. SO 与O 反应制备SO 是硫酸工业中的重要反应,其微观变化过程如图所示。下列说法正确的是
2 2 3
第1页/共6页
学科网(北京)股份有限公司A. 该反应属于氧化反应 B. 反应后催化剂的质量减少
C. 参加反应的SO 和O 的质量比为2:1 D. 该反应的化学方程式为SO +O SO
2 2 2 2 3
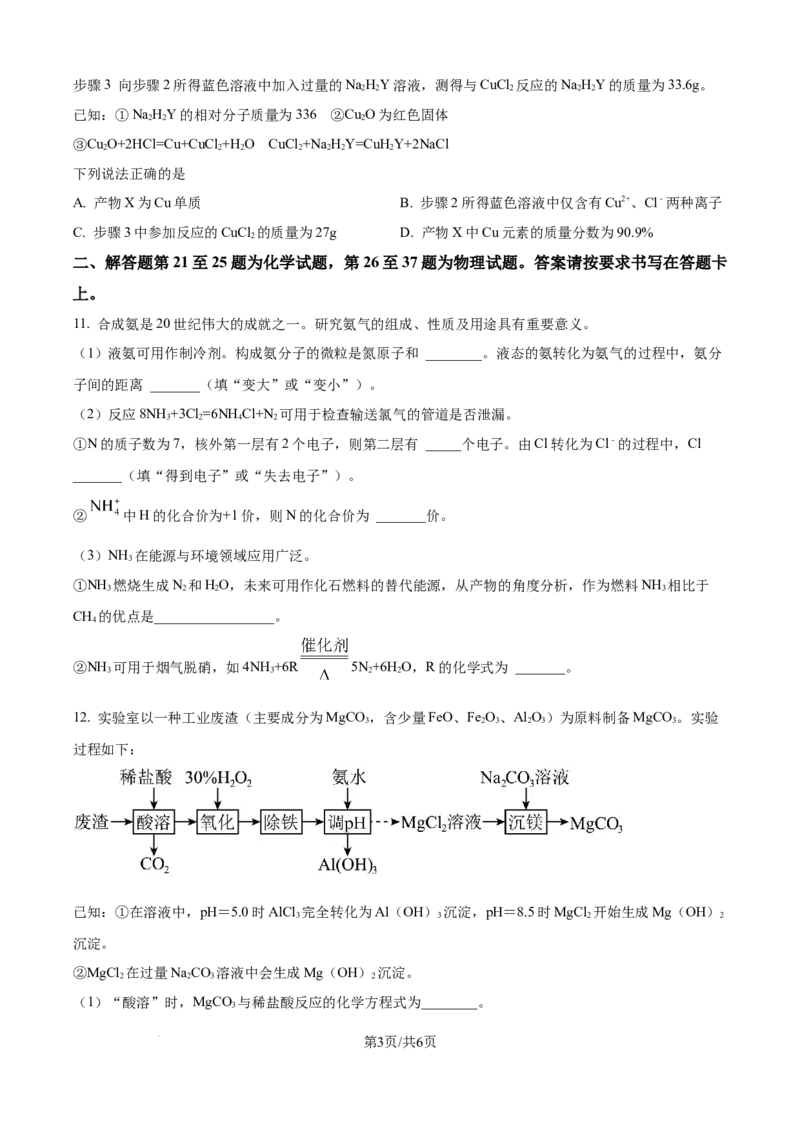
8. “侯氏制碱法”大幅提高了NaCl的利用率。NaHCO 、NaCl、NH Cl的溶解度曲线如图所示。下列说法正
3 4
确的是
A. NH Cl的溶解度一定小于NaCl的溶解度
4
B. 将20℃的NaCl饱和溶液升高5℃,溶质的质量分数增大
C. 40℃时,NaCl溶液中溶质的质量分数可能小于NaHCO 溶液中溶质的质量分数
3
D. 40℃时,将15gNaCl溶于50g水中,可获得NaCl饱和溶液
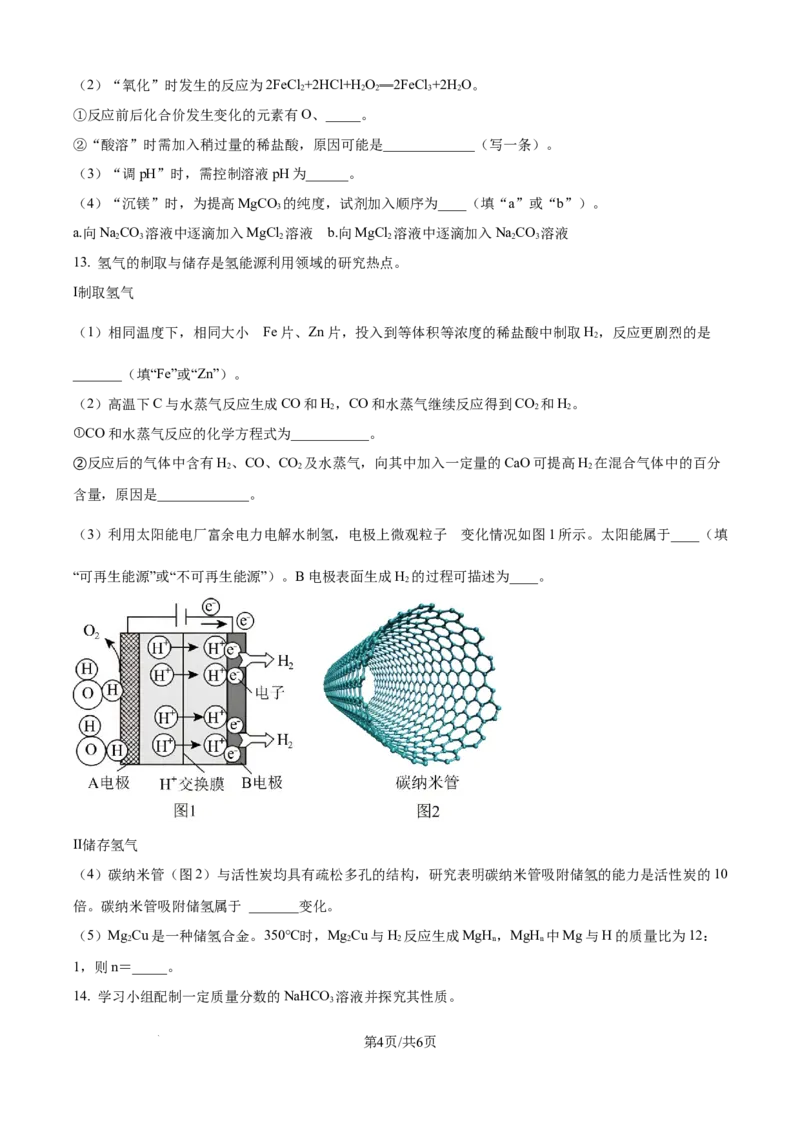
9. 下列实验方案不能达到实验目的的是
A. 去除粗盐中难溶性杂质:将粗盐溶解、过滤、蒸发
B. 比较Al片、Cu片的硬度:将两片金属相互刻画,观察现象
C. 探究CO和Fe O 反应的气态产物:按图所示装置进行实验
2 3
D. 判断某水样是否属于硬水:用玻璃棒蘸取该水样滴在pH试纸上,观察现象
10. 学习小组为探究氢气还原氧化铜所得固体产物X的组成,设计如下实验:
步骤1 观察产物X的颜色为红色。
步骤2 向产物X中加入过量的盐酸充分反应,过滤得到9.6g红色固体和蓝色溶液。
第2页/共6页
学科网(北京)股份有限公司步骤3 向步骤2所得蓝色溶液中加入过量的NaHY溶液,测得与CuCl 反应的NaHY的质量为33.6g。
2 2 2 2 2
已知:①NaHY的相对分子质量为336 ②Cu O为红色固体
2 2 2
③Cu O+2HCl=Cu+CuCl +H O CuCl +Na HY=CuHY+2NaCl
2 2 2 2 2 2 2
下列说法正确的是
A. 产物X为Cu单质 B. 步骤2所得蓝色溶液中仅含有Cu2+、Cl﹣两种离子
C. 步骤3中参加反应的CuCl 的质量为27g D. 产物X中Cu元素的质量分数为90.9%
2
二、解答题第21至25题为化学试题,第26至37题为物理试题。答案请按要求书写在答题卡
上。
11. 合成氨是20世纪伟大的成就之一。研究氨气的组成、性质及用途具有重要意义。
(1)液氨可用作制冷剂。构成氨分子的微粒是氮原子和 ________。液态的氨转化为氨气的过程中,氨分
子间的距离 _______(填“变大”或“变小”)。
(2)反应8NH +3Cl=6NHCl+N 可用于检查输送氯气的管道是否泄漏。
3 2 4 2
①N的质子数为7,核外第一层有2个电子,则第二层有 _____个电子。由Cl转化为Cl﹣的过程中,Cl
_______(填“得到电子”或“失去电子”)。
② 中H的化合价为+1价,则N的化合价为 _______价。
(3)NH 在能源与环境领域应用广泛。
3
①NH 燃烧生成N 和HO,未来可用作化石燃料的替代能源,从产物的角度分析,作为燃料NH 相比于
3 2 2 3
CH 的优点是_________________。
4
②NH 可用于烟气脱硝,如4NH +6R 5N+6H O,R的化学式为 _______。
3 3 2 2
12. 实验室以一种工业废渣(主要成分为MgCO ,含少量FeO、Fe O、Al O)为原料制备MgCO 。实验
3 2 3 2 3 3
过程如下:
已知:①在溶液中,pH=5.0时AlCl 完全转化为Al(OH) 沉淀,pH=8.5时MgCl 开始生成Mg(OH)
3 3 2 2
沉淀。
②MgCl 在过量NaCO 溶液中会生成Mg(OH) 沉淀。
2 2 3 2
(1)“酸溶”时,MgCO 与稀盐酸反应的化学方程式为________。
3
第3页/共6页
学科网(北京)股份有限公司(2)“氧化”时发生的反应为2FeCl +2HCl+H O═2FeCl +2H O。
2 2 2 3 2
①反应前后化合价发生变化的元素有O、_____。
②“酸溶”时需加入稍过量的稀盐酸,原因可能是_____________(写一条)。
(3)“调pH”时,需控制溶液pH为______。
(4)“沉镁”时,为提高MgCO 的纯度,试剂加入顺序为____(填“a”或“b”)。
3
a.向NaCO 溶液中逐滴加入MgCl 溶液 b.向MgCl 溶液中逐滴加入NaCO 溶液
2 3 2 2 2 3
13. 氢气的制取与储存是氢能源利用领域的研究热点。
Ⅰ制取氢气
的
(1)相同温度下,相同大小 Fe片、Zn片,投入到等体积等浓度的稀盐酸中制取H,反应更剧烈的是
2
_______(填“Fe”或“Zn”)。
(2)高温下C与水蒸气反应生成CO和H,CO和水蒸气继续反应得到CO 和H。
2 2 2
①CO和水蒸气反应的化学方程式为___________。
②反应后的气体中含有H、CO、CO 及水蒸气,向其中加入一定量的CaO可提高H 在混合气体中的百分
2 2 2
含量,原因是_____________。
的
(3)利用太阳能电厂富余电力电解水制氢,电极上微观粒子 变化情况如图1所示。太阳能属于____(填
“可再生能源”或“不可再生能源”)。B电极表面生成H 的过程可描述为____。
2
Ⅱ储存氢气
(4)碳纳米管(图2)与活性炭均具有疏松多孔的结构,研究表明碳纳米管吸附储氢的能力是活性炭的10
倍。碳纳米管吸附储氢属于 _______变化。
(5)MgCu是一种储氢合金。350℃时,MgCu与H 反应生成MgH ,MgH 中Mg与H的质量比为12:
2 2 2 n n
1,则n=_____。
14. 学习小组配制一定质量分数的NaHCO 溶液并探究其性质。
3
第4页/共6页
学科网(北京)股份有限公司Ⅰ配制一定质量分数的NaHCO 溶液
3
(1)“称量”时,用_______(填“镊子”或“药匙”)从试剂瓶中取出NaHCO 粉末。
3
(2)“溶解”时,若需量取15.0mL的水,当量筒中已有14.6mL水时,后续加水使用的仪器为_____(填
字母)。
(3)配制过程中玻璃棒的作用是_____(填字母)。
a.搅拌 b.引流 c.蘸取
Ⅱ探究NaHCO 溶液的性质
3
(4)取少量NaHCO 溶液,向其中滴入无色酚酞溶液后显_____色,说明NaHCO 溶液呈碱性。
3 3
(5)取三份NaHCO 溶液,向其中分别滴入CaCl 溶液。试剂用量、浓度及实验现象如下表所示。
3 2
实验编号 实验1 实验2 实验3
NaHCO 溶
3 1mL0.8% 1mL0.8% 1mL0.8%
液
.
CaCl 溶液 1滴01% 1滴11% 6滴11%
2
无明显现 白色沉 白色沉淀、无色气
实验现象
象 淀 体
①“实验3”生成的白色沉淀为CaCO ,无色气体为CO,此外还生成NaCl和HO,“实验3”中反应的
3 2 2
化学方程式为__________。
②“实验2、3”中发生的化学反应相同,从气体溶解度的角度分析“实验2”中没有观察到CO 逸出的原
2
因是________。
③三组实验研究表明:1mL0.8%的NaHCO 溶液与CaCl 溶液混合后,能否观察到明显现象与___________
3 2
相关。
④已知:向1mL0.8%的NaCO 溶液中滴入1滴0.1%的CaCl 溶液,有白色沉淀生成。设计实验鉴别浓度
2 3 2
均为0.8%的NaCO 溶液和NaHCO 溶液。简述实验方案(包括操作、现象和结论)______。(实验中须
2 3 3
使用的试剂:0.1%的CaCl 溶液)
2
15. 利用CO 合成甲醇(CHOH)是捕集CO 的一种方法。
2 3 2
(1)CO 催化加氢合成CHOH 反应为CO+3H CHOH+H O。
2 3 的2 2 3 2
①该反应________(填“属于”或“不属于”)置换反应。
第5页/共6页
学科网(北京)股份有限公司②以17.6吨CO 为原料反应制得3.2吨CHOH,计算CO 的转化率。_____
2 3 2
(CO 的转化率= ×100%CO,请将计算过程写到答题卡上)
2 2
(2)CO和H 在高温、催化剂作用下也能合成CHOH,该反应的化学方程式为_____。
2 3
第6页/共6页
学科网(北京)股份有限公司