文档内容
1.下列物质在生活中应用时,起还原作用的是( )
A.明矾作净水剂
B.甘油作护肤保湿剂
C.漂粉精作消毒剂
D.铁粉作食品袋内的脱氧剂
2.下列有关CuSO 溶液的叙述正确的是( )
4 [来源:Z*xx*k.Com]
A.该溶液中Na+、NH +、NO -、Mg2+可以大量共存
4 3
B.通入CO 气体产生蓝色沉淀
2
C.与H S反应的离子方程式:Cu2++ S2-=CuS↓
2
D.与过量浓氨水反应的离子方程式:Cu2++2NH ·H O=Cu(OH) ↓+2NH +
3 2 2 4
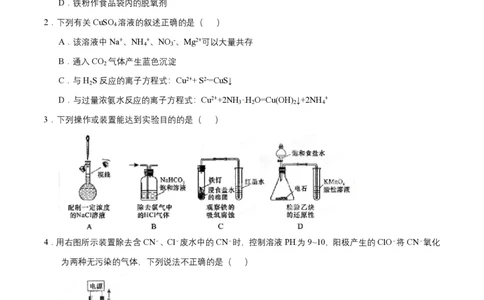
3.下列操作或装置能达到实验目的的是( )
4.用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化
为两种无污染的气体,下列说法不正确的是( )
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H O
2
C.阴极的电极反应式为:2H O + 2e- = H ↑ + 2OH-
2 2
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ = N ↑ + 2CO ↑ + 5Cl-+ H O
2 2 2
5.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
第1页 | 共5页A.2.0gH 18O与D O的混合物中所含中子数为N
2 2 A
B.常温常压下,4.4g乙醛所含σ键数目为0.7N
A
C.标准状况下,5.6LCO 与足量Na O 反应转移的电子数为0.5 N
2 2 2 A
D.50ml 12mol/L盐酸与足量MnO 共热,转移的电子数为0.3N
2 A
6.常温下,将等体积,等物质的量浓度的NHHCO 与NaCl溶液混合,析出部分NaHCO 晶体,过滤,所
4 3 3
得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是( )
Kw
A. <1.0×10-7mol/L
c(H+)
B.c(Na+)= c(HCO -)+ c(CO 2-)+ c(H CO )
3 3 2 3
C.c(H+)+c(NH +)= c(OH-)+ c(HCO -)+2 c(CO 2-)
4 3 3
D.c(Cl-)> c(NH +)> c(HCO -)> c(CO 2-)
4 3 3
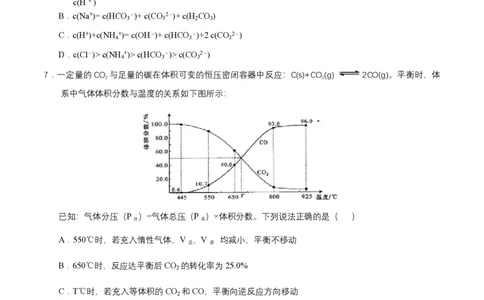
7.一定量的CO 与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO(g) 2CO(g)。平衡时,体
2 2
系中气体体积分数与温度的关系如下图所示:
已知:气体分压(P )=气体总压(P )×体积分数。下列说法正确的是( )
分 总
A.550℃时,若充入惰性气体,V ,V 均减小,平衡不移动
正 逆
B.650℃时,反应达平衡后CO 的转化率为25.0%
2
C.T℃时,若充入等体积的CO 和CO,平衡向逆反应方向移动
2
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数K =24.0P
P 总
8.(13分)X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族元素;Z和U位
于第VIIA族;X和Z可形成化合物XZ;Q基态原子的s轨道和p轨道的电子总数相等;T的一种单质
4
在空气中能够自燃。
请回答下列问题:
(1)R基态原子的电子排布式是_____________________。
第2页 | 共5页(2)利用价层电子对互斥理论判断TU 的立体构型是______。
3
(3)X所在周期元素最高价氧化物对应的水化物中,酸性最强的是______(填化学式);Z和U的氢化物
中沸点较高的是_____(填化学式);Q、R、U的单质形成的晶体,熔点由高到低的排列顺序是_______(填
化学式) 。
(4)CuSO 溶液能用作T 中毒的解毒剂,反应可生成T的最高价含氧酸和铜,该反应的化学方程式是
4 4
_______________________。
9.(13分)(NH)SO 是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
4 2 4
[查阅资料] (NH)SO 在260℃和400℃时分解产物不同。
4 2 4
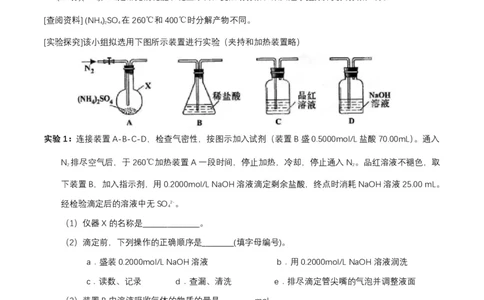
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)
[来源:学§科§网Z§X§X§K]
实验1:连接装置A-B-C-D,检查气密性,按图示加入试剂(装置B盛0.5000mol/L盐酸70.00mL)。通入
N 排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N。品红溶液不褪色,取
2 2
下装置B,加入指示剂,用0.2000mol/L NaOH溶液滴定剩余盐酸,终点时消耗NaOH溶液25.00 mL。
经检验滴定后的溶液中无SO2-。
4
(1)仪器X的名称是________________。
(2)滴定前,下列操作的正确顺序是_________(填字母编号)。
a.盛装0.2000mol/L NaOH溶液 b.用0.2000mol/L NaOH溶液润洗
c.读数、记录 d.查漏、清洗 e.排尽滴定管尖嘴的气泡并调整液面
(3)装置B内溶液吸收气体的物质的量是__________mol
实验2:连接装置A-D-B,检查气密性,按图示重新加入试剂。通入N 排尽空气后,于400℃加热装置A
2
至(NH)SO 完全分解无残留物,停止加热,冷却,停止通入N。观察到装置A、D之间的导气管内有
4 2 4 2
少量白色固体。经检验,该白色固体和装置D内溶液中有SO2-,无SO2-。进一步研究发现,气体产
3 4
物中无氮氧化物。
(4)检验装置D内溶液中有SO2-,无SO2-的实验操作和现象是__________.
3 4
(5)装置B内溶液吸收的气体是____________.
第3页 | 共5页(6)(NH) SO 在400℃分解的化学方程式是______________________.
4 2 4
10.(16分)化合物F(异戊巴比妥)是临床常用的镇静催眠药物,其合成路线如下(部分反应条件和试剂
略);
请回答下列问题:
(1)试剂I的化学名称是 ① ,化合物B的官能团名称是 ② ,第④步的化学反应类型是
③ 。
(2)第①步反应的化学方程式是 。
(3)第⑤步反应的化学方程式是 。
(4)试剂Ⅱ的相对分子质量为60,其结构简式是 。
(5)化合物B的一种同分异构体G与NaOH溶液共热反应,生成乙醇和化合物H。H在一定条件下
发生聚合反应得到高吸水性树脂,该聚合物的结构简式是 。
11.(16分)为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣
(铁主要以FeO 存在)转变成重要的化工原料FeSO(反应条件略)。
2 3 4
活化硫铁矿还原Fe3+的主要反应为:FeS+7Fe(SO)+8HO=15FeSO+8HSO,不考虑其他反应。请回答下
2 2 4 3 2 4 2 4
列问题:
(1)第Ⅰ步HSO 与FeO 反应的离子方程式是 。
2 4 2 3
第4页 | 共5页(2)检验第Ⅱ步中Fe3+是否完全还原,应选择 (填字母编号)。
A.KMnO 溶液 B.K[Fe(CN)]溶液 C.KSCN溶液
4 3 6
(3)第Ⅲ步加FeCO 调溶液pH到5.8左右,然后在第Ⅳ步通入空气使溶液pH降到5.2,此时Fe2+不
3
沉淀,滤液中铝、硅杂质除尽。通入空气引起溶液pH降低的原因是 。
(4)FeSO 可转化为FeCO,FeCO 在空气中加热反应可制得铁系氧化物材料。
4 3 3
已知25℃,101kPa时:4Fe(s) + 3O (g) =2FeO(s) H =-1648kJ/mol
2 2 3 [来源:Zxxk.Com]
C(s)+O(g)=CO(g) H =-393kJ/mol
2 2
2Fe(s)+2C(s)+3O(g)=2FeCO(s) H =-1480kJ/mol
2 3
FeCO 在空气中加热反应生成FeO 的热化学方程式是 。
3 2 3 [来源:学,科,网Z,X,X,K]
(5)FeSO 在一定条件下可制得FeS(二硫化亚铁)纳米材料。该材料可用于制造高容量锂电池,电池
4 2
放电时的总反应为4Li+ FeS= Fe +2LiS,正极反应式是 。
2 2
(6)假如烧渣中的铁全部视为FeO,其含量为50%。将a kg质量分数为b%的硫酸加入到c kg烧渣中
2 3
浸取,铁的浸取率为96%,其他杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的硫酸忽略
不计。按上述流程,第Ⅲ步应加入FeCO kg。
3
第5页 | 共5页