文档内容
2011年普通高等学校招生全国统一考试化学海南卷答案及解析
可能用到的相对原子质量:H1C12N14O16Na23P31S32 Cl35.5 K39Fe56Cu64 I127Au197
第I卷
一、选择题:本题共6小题。每小题2分,共12分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
1. 1下列化合物中,在常温常压下以液态形式存在的是
A.甲醇 B.乙炔 C.丙烯 D.丁烷
2. 2用0.1026mol·L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液
面如下图所示,正确的读数为
A.22.30mL B.22.35mL C.23.65mL D.23.70Ml
3. 3下列固体混合物与过量的稀H SO 反应,能产生气泡并有沉淀生产的是
2 4
A.NaHCO 和Al(OH) B.BaCl 和NaCl
3 3 2
C.HClO 和K SO D.Na SO 和BaCO
3 2 4 2 3 3
4. 4I是常规核裂变产物之一,可以通过测定大气或水中I的含量变化来检测核电站是否发生放射性
物质泄漏。下列有关I的叙述中错误的是
A. I的化学性质与I相同 B. I的原子序数为53
C. I的原子核外电子数为78 D. I的原子核内中子数多于质子数
5. 5已知:2Zn(s)+O (g)=2ZnO(s) △H=-701.0kJ·mol-1
2
2Hg(l)+O (g)=2HgO(s) △H=-181.6kJ·mol-1
2
则反应Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H为
A.+519.4kJ·mol-1 B.+259.7kJ·mol-1 C.-259.7kJ·mol-1 D.-519.4kJ·mol-1
6. 6一种充电电池放电时的电极反应为H +2OH--2e-=2H O; NiO(OH)+H O+e-=Ni(OH) +OH-
2 2 2 2
当为电池充电时,与外电源正极连接的电极上发生的反应是
A.H O的还原 B.NiO(OH)的还原 C.H 的氧化 D.NiO(OH) 的氧化
2 2 2
二、选择题:本题共6小题。每小题4分,共24分。每小题有一个或两个选项符合题意,若正
确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2分,选两个且
都正确得4分,但只要选错一个就得0分。
7. 7下列化合物的分子中,所有原子都处于同一平面的有
A.乙烷 B.甲苯 C.氟苯 D.四氯乙烯
8. 8对于可逆反应H (g)+I (g)≒2HI(g),在温度一定下由H (g)和I (g)开始反应,下列说法正确
2 2 2 2
的是
A.H (g)的消耗速率与HI(g)的生成速率比为2:1
2
B.反应进行的净速率是正、逆反应速率之差
C.正、逆反应速率的比值是恒定的
D.达到平衡时,正、逆反应速率相等
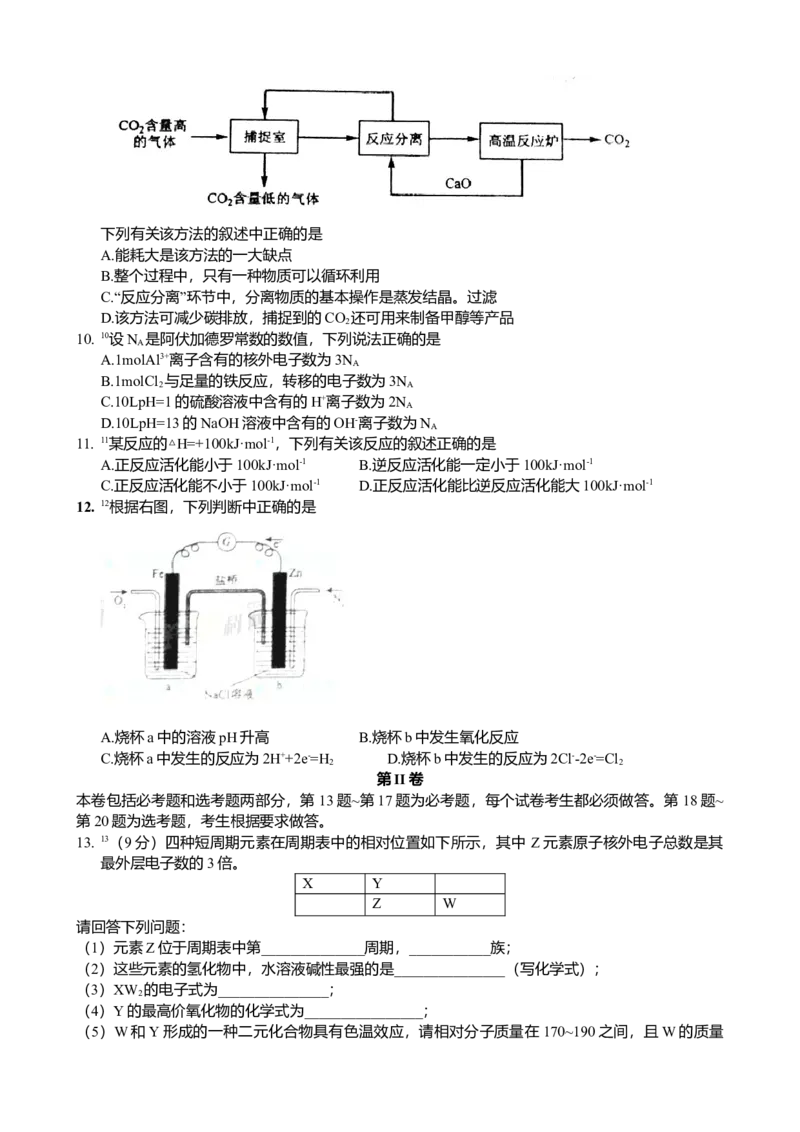
9. 9“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO 分离出来并利用。如可利用NaOH溶
2
液来“捕捉”CO ,其基本过程如下图所示(部分条件及物质未标出)。
2下列有关该方法的叙述中正确的是
A.能耗大是该方法的一大缺点
B.整个过程中,只有一种物质可以循环利用
C.“反应分离”环节中,分离物质的基本操作是蒸发结晶。过滤
D.该方法可减少碳排放,捕捉到的CO 还可用来制备甲醇等产品
2
10. 10设N 是阿伏加德罗常数的数值,下列说法正确的是
A
A.1molAl3+离子含有的核外电子数为3N
A
B.1molCl 与足量的铁反应,转移的电子数为3N
2 A
C.10LpH=1的硫酸溶液中含有的H+离子数为2N
A
D.10LpH=13的NaOH溶液中含有的OH-离子数为N
A
11. 11某反应的△H=+100kJ·mol-1,下列有关该反应的叙述正确的是
A.正反应活化能小于100kJ·mol-1 B.逆反应活化能一定小于100kJ·mol-1
C.正反应活化能不小于100kJ·mol-1 D.正反应活化能比逆反应活化能大100kJ·mol-1
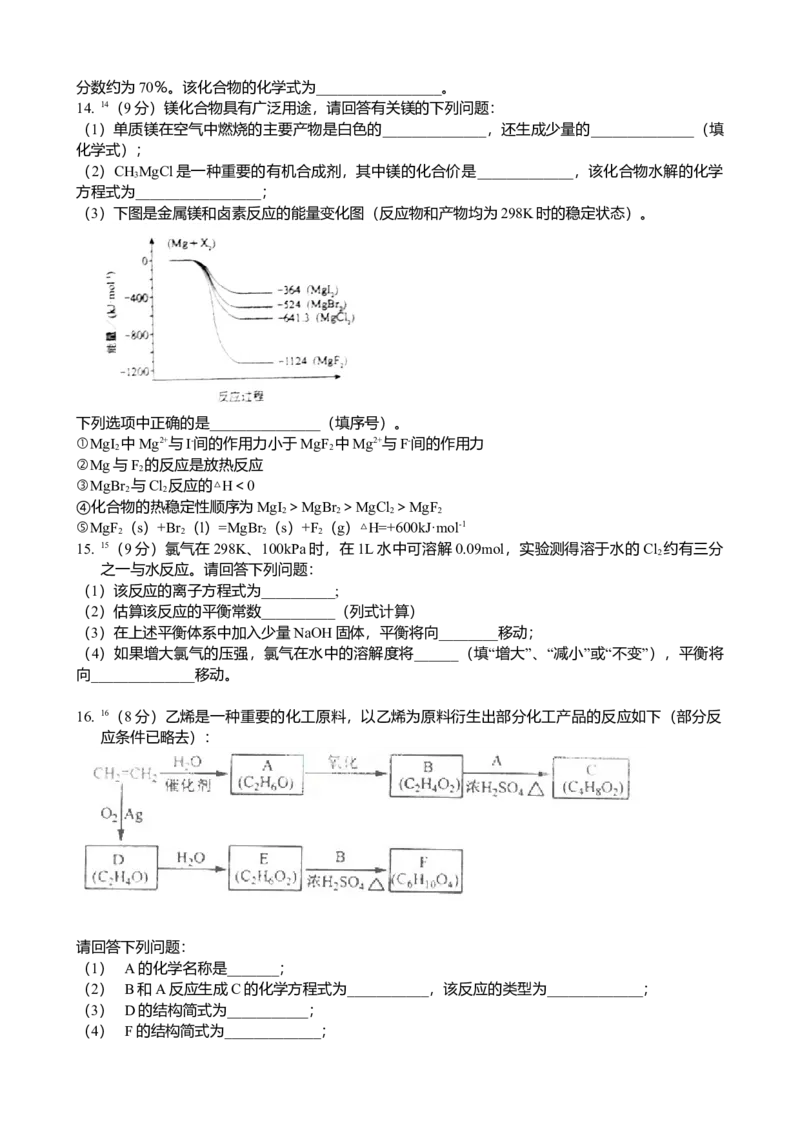
12. 12根据右图,下列判断中正确的是
A.烧杯a中的溶液pH升高 B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-=H D.烧杯b中发生的反应为2Cl--2e-=Cl
2 2
第II卷
本卷包括必考题和选考题两部分,第 13题~第17题为必考题,每个试卷考生都必须做答。第 18题~
第20题为选考题,考生根据要求做答。
13. 13(9分)四种短周期元素在周期表中的相对位置如下所示,其中 Z元素原子核外电子总数是其
最外层电子数的3倍。
X Y
Z W
请回答下列问题:
(1)元素Z位于周期表中第______________周期,___________族;
(2)这些元素的氢化物中,水溶液碱性最强的是_______________(写化学式);
(3)XW 的电子式为_______________;
2
(4)Y的最高价氧化物的化学式为________________;
(5)W和Y形成的一种二元化合物具有色温效应,请相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为_________________。
14. 14(9分)镁化合物具有广泛用途,请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的______________,还生成少量的______________(填
化学式);
(2)CH MgCl是一种重要的有机合成剂,其中镁的化合价是_____________,该化合物水解的化学
3
方程式为_________________;
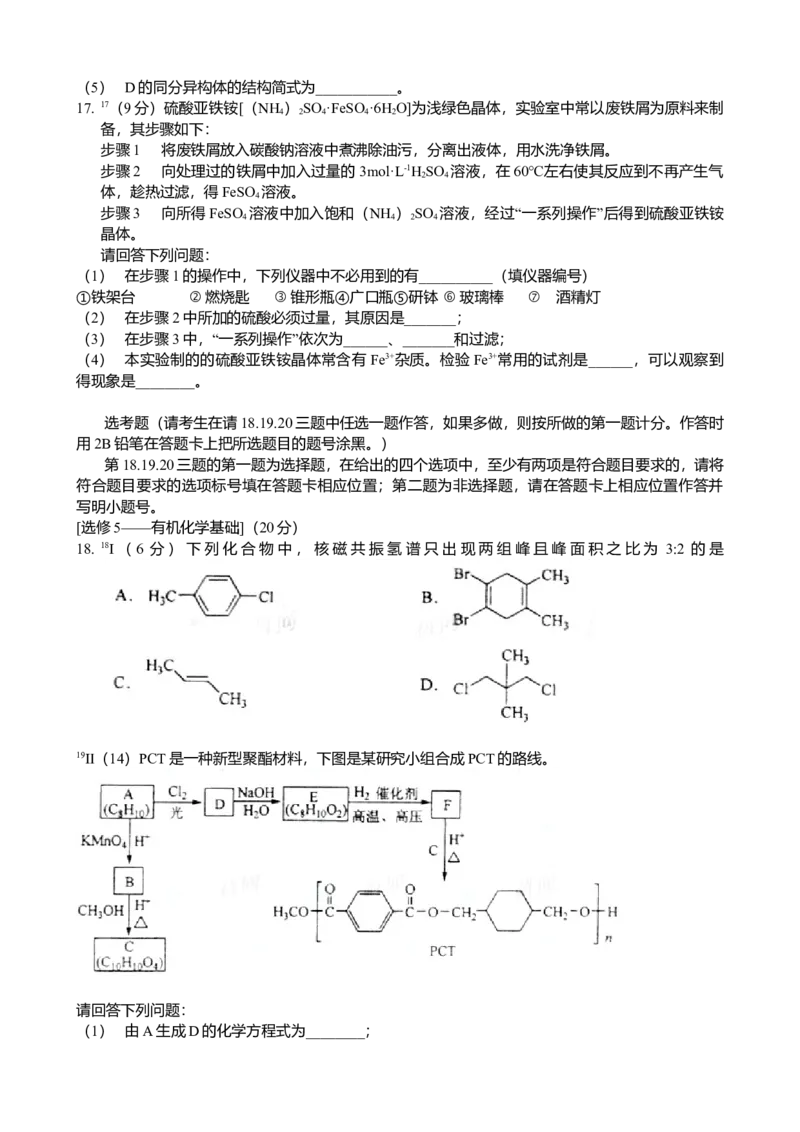
(3)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。
下列选项中正确的是_______________(填序号)。
①MgI 中Mg2+与I-间的作用力小于MgF 中Mg2+与F-间的作用力
2 2
②Mg与F 的反应是放热反应
2
③MgBr 与Cl 反应的△H<0
2 2
④化合物的热稳定性顺序为MgI >MgBr >MgCl >MgF
2 2 2 2
⑤MgF (s)+Br (l)=MgBr (s)+F (g)△H=+600kJ·mol-1
2 2 2 2
15. 15(9分)氯气在298K、100kPa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl 约有三分
2
之一与水反应。请回答下列问题:
(1)该反应的离子方程式为__________;
(2)估算该反应的平衡常数__________(列式计算)
(3)在上述平衡体系中加入少量NaOH固体,平衡将向________移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将______(填“增大”、“减小”或“不变”),平衡将
向______________移动。
16. 16(8分)乙烯是一种重要的化工原料,以乙烯为原料衍生出部分化工产品的反应如下(部分反
应条件已略去):
请回答下列问题:
(1) A的化学名称是_______;
(2) B和A反应生成C的化学方程式为___________,该反应的类型为_____________;
(3) D的结构简式为___________;
(4) F的结构简式为_____________;(5) D的同分异构体的结构简式为___________。
17. 17(9分)硫酸亚铁铵[(NH ) SO ·FeSO ·6H O]为浅绿色晶体,实验室中常以废铁屑为原料来制
4 2 4 4 2
备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2 向处理过的铁屑中加入过量的3mol·L-1H SO 溶液,在60℃左右使其反应到不再产生气
2 4
体,趁热过滤,得FeSO 溶液。
4
步骤3 向所得FeSO 溶液中加入饱和(NH ) SO 溶液,经过“一系列操作”后得到硫酸亚铁铵
4 4 2 4
晶体。
请回答下列问题:
(1) 在步骤1的操作中,下列仪器中不必用到的有__________(填仪器编号)
①铁架台 ②燃烧匙 ③锥形瓶④广口瓶⑤研钵 ⑥玻璃棒 ⑦ 酒精灯
(2) 在步骤2中所加的硫酸必须过量,其原因是_______;
(3) 在步骤3中,“一系列操作”依次为______、_______和过滤;
(4) 本实验制的的硫酸亚铁铵晶体常含有 Fe3+杂质。检验Fe3+常用的试剂是______,可以观察到
得现象是________。
选考题(请考生在请18.19.20三题中任选一题作答,如果多做,则按所做的第一题计分。作答时
用2B铅笔在答题卡上把所选题目的题号涂黑。)
第18.19.20三题的第一题为选择题,在给出的四个选项中,至少有两项是符合题目要求的,请将
符合题目要求的选项标号填在答题卡相应位置;第二题为非选择题,请在答题卡上相应位置作答并
写明小题号。
[选修5——有机化学基础](20分)
18. 18Ⅰ(6 分)下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为 3:2 的是
19Ⅱ(14)PCT是一种新型聚酯材料,下图是某研究小组合成PCT的路线。
请回答下列问题:
(1) 由A生成D的化学方程式为________;(2) 由B生成C的反应类型是________________,C的化学名称为______________;
(3) 由E生成F的化学方程式为____________,该反应的类型为__________________;
(4) D的同分异构体中为单取代芳香化合物的有____________(写结构简式)
(5) B的同分异构体中,能发生水解反应,且苯环上一氯代产物只有一种的是________(写结构
简式)。
19.【选修3——物质结构与性质】(20分)
19. I20(6分)下列分子中,属于非极性的是
A.SO B.BeCl C.BBr D.COCl
2 2 3 2
21II(14分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO 溶液常
4
用作电解液、电镀液等。请回答以下问题:
(1)CuSO 可由金属铜与浓硫酸反应制备,该反应的化学方程式为___________;
4
(2)CuSO 粉末常用来检验一些有机物中的微量水分,其原因是_______;
4
(3)SO 2-的立体构型是________,其中S原子的杂化轨道类型是_______;
4
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一
种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该
合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu
原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF 的结构相似,该晶体储氢后的化学式应
2
为__________。
【选修2——化学与技术】(20分)
20. 22I(6分)下列叙述正确的是
A.“接触法”制H SO 时,催化氧化阶段的反应原理为
2 4
B.海水提镁的主要步骤为
C.普通水泥的主要成分是硅酸钙
D.黏土的主要成分是三氧化二铝
23II(14分)工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)卢布兰芳是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得
纯碱。
①食盐和浓硫酸反应的化学方程式为___________;
②硫酸钠和焦炭、石灰石反应的化学方程式为___________(已知产物之一为CaS);
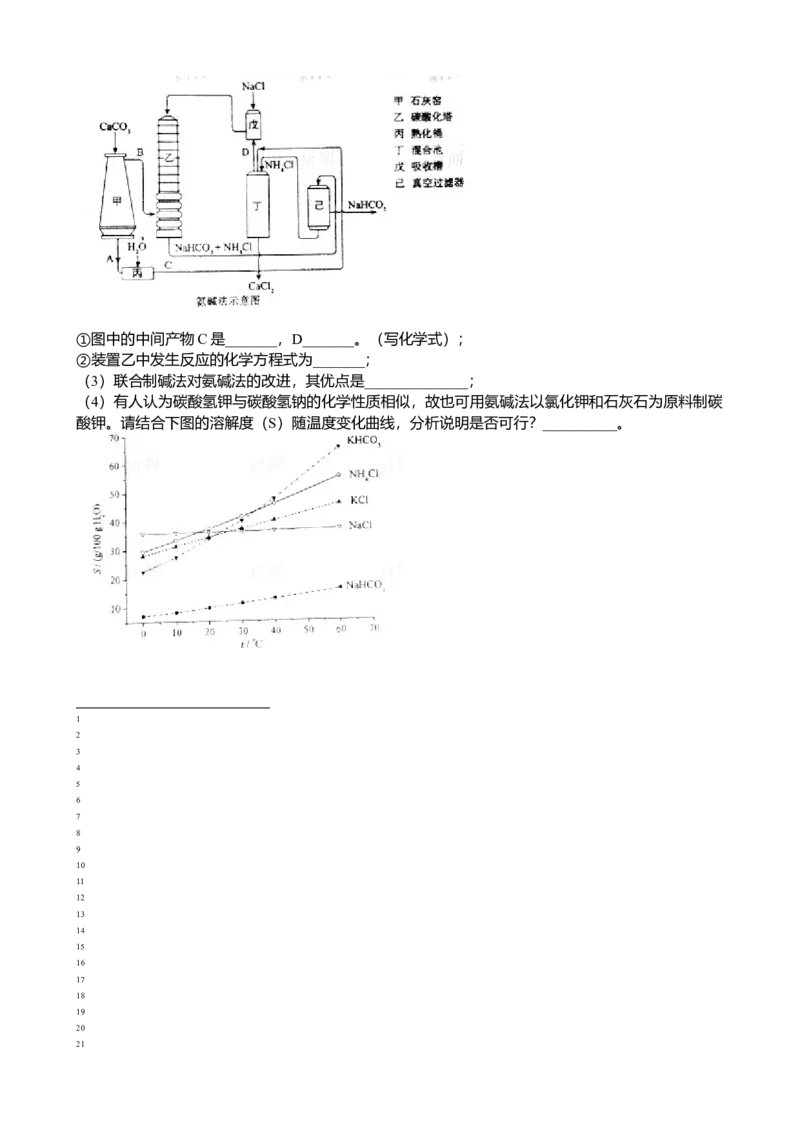
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。①图中的中间产物C是_______,D_______。(写化学式);
②装置乙中发生反应的化学方程式为_______;
(3)联合制碱法对氨碱法的改进,其优点是______________;
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳
酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行?__________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
2122
23