文档内容
2013 年全国统一高考化学试卷(新课标Ⅰ) 10﹣12.某溶液中含有 Cl﹣、Br﹣和 CrO 4 2﹣浓度均为 0.010mol•L﹣1,向该溶液中逐滴加入
0.010mol•L﹣1的AgNO 溶液时,三种阴离子产生沉淀的先后顺序为( )
一、选择题 3
A.Cl﹣、Br﹣、CrO 2﹣ B.CrO 2﹣、Br﹣、Cl﹣
1.(6分)化学无处不在,与化学有关的说法不正确的是( ) 4 4
C.Br﹣、Cl﹣、CrO 2﹣ D.Br﹣、CrO 2﹣、Cl﹣
A.侯氏制碱法的工艺过程中应用了物质溶解度的差异 4 4
6.(6 分)分子式为 C H O 的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些
B.可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 5 10 2
酸和醇重新组合可形成的酯共有( )
C.碘是人体必需微量元素,所以要多吃富含高碘酸的食物
A.28种 B.32 种 C.40种 D.48种
D.黑火药由硫磺、硝石、木炭三种物质按一定比例混合制成
7.(6分)下列实验中,所采取的分离方法与对应原理都正确的是( )
2.(6分)香叶醇是合成玫瑰香油的主要原料,其结构简式如图所示:下列有关香叶醇的叙述正
选项 目的 分离方法 原理
确的是( )
A 分离溶于水中的碘 乙醇萃取 碘在乙醇中的溶解度较大
B 分离乙酸乙酯和乙醇 分液 乙酸乙酯和乙醇的密度不同
C 除去 KNO 固体中混杂的 NaCl 重结晶 NaCl 在水中的溶解度很大
3
D 除去丁醇中的乙醚 蒸馏 丁醇与乙醚的沸点相差较大
A.香叶醇的分子式为C H O
10 18 A.A B.B C.C D.D
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
三、非选择题(包括必考题和选考题两部分.第 22题~第 32题为必考题,每个试题考生都必须
D.能发生加成反应不能发生取代反应
作答.第 33题~第 40 题为选考题,考生根据要求作答)
3.(6分)短周期元素 W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡
8.(13分)醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示.可
的是( )
能用到的有关数据如下:
A.W2﹣、X+ B.X+、Y3+ C.Y3+、Z2﹣ D.X+、Z2﹣
相对分子质量 密度/(g•cm﹣3) 沸点/℃ 溶解性
4.(6 分)银制器皿日久表面会逐渐变黑,这是生成了 Ag S 的缘故.根据电化学原理可进行如
2
环己醇 100 0.9618 161 微溶于水
下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会
环己烯 82 0.8102 83 难溶于水
褪去.下列说法正确的是( )
合成反应:
A.处理过程中银器一直保持恒重
在 a中加入 20g环己醇和 2小片碎瓷片,冷却搅动下慢慢加入 1mL浓硫酸.b中通入冷却水后,
B.银器为正极,Ag S 被还原生成单质银
2
开始缓慢加热a,控制馏出物的温度不超过 90℃.
C.该过程中总反应为2Al+3Ag S═6Ag+Al S
2 2 3
分离提纯:
D.黑色褪去的原因是黑色Ag S 转化为白色AgCl
2
反应粗产物倒入分液漏斗中分别用少量 5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静
5.(6分)已知 K (AgCl)=1.56×10﹣10,K (AgBr)=7.7×10﹣13,K (Ag CrO )=9.0×
sp sp sp 2 4
第1页(共4页)置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是 .
(2)加入碎瓷片的作用是 ;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作
是 (填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为 .
回答下列问题:
(4)分液漏斗在使用前须清洗干净并 ;在本实验分离过程中,产物应该从分液漏斗的
(1)LiCoO 中,Co元素的化合价为 .
(填“上口倒出”或“下口放出”). 2
(2)写出“正极碱浸”中发生反应的离子方程式 .
(5)分离提纯过程中加入无水氯化钙的目的是 .
(3)“酸浸”一般在 80℃下进行,写出该步骤中发生的所有氧化还原反应的化学方程式 ;
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有 (填正确答案标号).
可用盐酸代替H SO 和 H O 的混合液,但缺点是 .
A.蒸馏烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器 2 4 2 2
(4)写出“沉钴”过程中发生反应的化学方程式 .
(7)本实验所得到的环己烯产率是 (填正确答案标号).
(5)充放电过程中,发生 LiCoO 与 Li CoO 之间的转化,写出放电时电池反应方程
A.41% B.50% C.61% D.70% 2 1﹣x 2
式 .
(6)上述工艺中,“放电处理”有利于锂在正极的回收,其原因是 .在整个回收工艺中,
可回收到的金属化合物有 (填化学式).
10.(15分)二甲醚(CH OCH )是无色气体,可作为一种新型能源.由合成气(组成为 H 、
3 3 2
CO 和少量的CO )直接制备二甲醚,其中的主要过程包括以下四个反应:
2
甲醇合成反应:
(Ⅰ)CO(g)+2H (g)═CH OH(g)△H =﹣90.1kJ•mol﹣1
2 3 1
(Ⅱ)CO (g)+3H (g)═CH OH(g)+H O(g)△H =﹣49.0kJ•mol﹣1
2 2 3 2 2
水煤气变换反应:
9.(15 分)锂离子电池的应用很广,其正极材料可再生利用.某锂离子电池正极材料有钴酸锂
(Ⅲ)CO(g)+H O(g)═CO (g)+H (g)△H =﹣41.1kJ•mol﹣1
(LiCoO )、导电剂乙炔黑和铝箔等.充电时,该锂离子电池阴极发生的反应为 6C+xLi++xe﹣ 2 2 2 3
2
二甲醚合成反应:
═Li C .现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出).
x 6
(Ⅳ)2CH OH(g)═CH OCH (g)+H O(g)△H =﹣24.5kJ•mol﹣1
3 3 3 2 4
回答下列问题:
(1)Al O 是合成气直接制备二甲醚反应催化剂的主要成分之一.工业上从铝土矿制备较高纯度
2 3
第2页(共4页)Al O 的主要工艺流程是 (以化学方程式表示). 回答下列问题:
2 3
(2)分析二甲醚合成反应(Ⅳ)对于CO 转化率的影响 . (1)CO 和 NaOH 在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程式分别
(3)由 H 和 CO 直接制备二甲醚(另一产物为水蒸气)的热化学方程式为 .根据化学反 为 、 .
2
应原理,分析增加压强对直接制备二甲醚反应的影响 . (2)该制备工艺中有两次过滤操作,过滤操作①的滤液是 ,滤渣是 ;过滤操作②
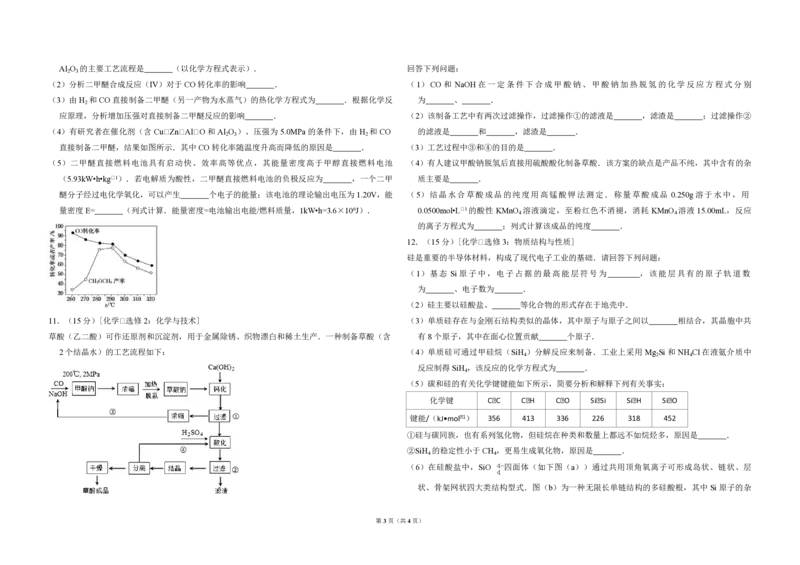
(4)有研究者在催化剂(含 Cu﹣Zn﹣Al﹣O 和 Al O )、压强为 5.0MPa 的条件下,由 H 和 CO 的滤液是 和 ,滤渣是 .
2 3 2
直接制备二甲醚,结果如图所示.其中 CO 转化率随温度升高而降低的原因是 . (3)工艺过程中③和④的目的是 .
(5)二甲醚直接燃料电池具有启动快、效率高等优点,其能量密度高于甲醇直接燃料电池 (4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸.该方案的缺点是产品不纯,其中含有的杂
(5.93kW•h•kg﹣1).若电解质为酸性,二甲醚直接燃料电池的负极反应为 ,一个二甲 质主要是 .
醚分子经过电化学氧化,可以产生 个电子的能量;该电池的理论输出电压为 1.20V,能 (5)结晶水合草酸成品的纯度用高锰酸钾法测定.称量草酸成品 0.250g溶于水中,用
量密度E= (列式计算.能量密度=电池输出电能/燃料质量,1kW•h=3.6×106J). 0.0500mol•L﹣1的酸性 KMnO 溶液滴定,至粉红色不消褪,消耗 KMnO 溶液 15.00mL,反应
4 4
的离子方程式为 ;列式计算该成品的纯度 .
12.(15分)[化学﹣选修3:物质结构与性质]
硅是重要的半导体材料,构成了现代电子工业的基础.请回答下列问题:
(1)基态 Si原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数
为 、电子数为 .
(2)硅主要以硅酸盐、 等化合物的形式存在于地壳中.
11.(15分)[化学﹣选修2:化学与技术] (3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以 相结合,其晶胞中共
草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产.一种制备草酸(含 有8个原子,其中在面心位置贡献 个原子.
2个结晶水)的工艺流程如下: (4)单质硅可通过甲硅烷(SiH )分解反应来制备.工业上采用 Mg Si和 NH Cl在液氨介质中
4 2 4
反应制得SiH ,该反应的化学方程式为 .
4
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
化学键 C﹣C C﹣H C﹣O Si﹣Si Si﹣H Si﹣O
键能/(kJ•mol﹣1) 356 413 336 226 318 452
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是 .
②SiH 的稳定性小于 CH ,更易生成氧化物,原因是 .
4 4
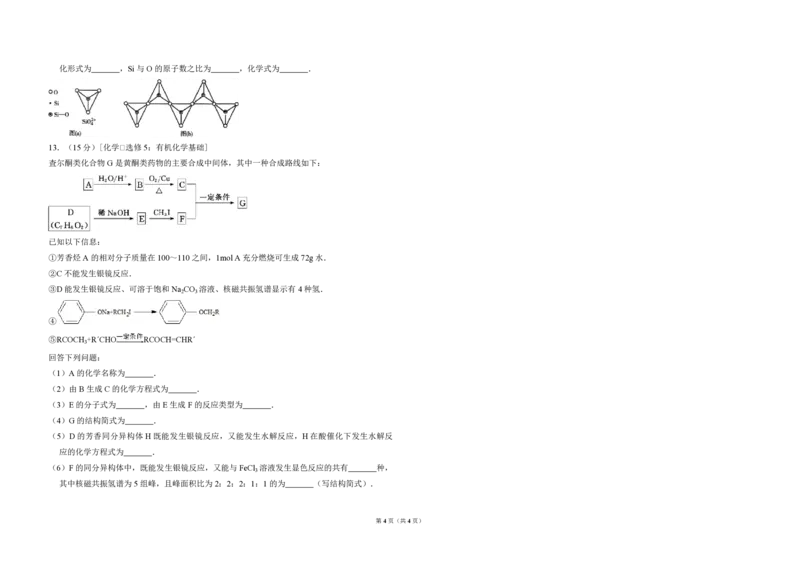
(6)在硅酸盐中,SiO 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层
状、骨架网状四大类结构型式.图(b)为一种无限长单链结构的多硅酸根,其中 Si原子的杂
第3页(共4页)化形式为 ,Si 与O 的原子数之比为 ,化学式为 .
13.(15分)[化学﹣选修5:有机化学基础]
査尔酮类化合物G 是黄酮类药物的主要合成中间体,其中一种合成路线如下:
已知以下信息:
①芳香烃A 的相对分子质量在100~110之间,1mol A 充分燃烧可生成72g水.
②C不能发生银镜反应.
③D 能发生银镜反应、可溶于饱和Na CO 溶液、核磁共振氢谱显示有4种氢.
2 3
④
⑤RCOCH +RˊCHO RCOCH=CHRˊ
3
回答下列问题:
(1)A 的化学名称为 .
(2)由B 生成C 的化学方程式为 .
(3)E的分子式为 ,由E生成F 的反应类型为 .
(4)G 的结构简式为 .
(5)D 的芳香同分异构体 H 既能发生银镜反应,又能发生水解反应,H 在酸催化下发生水解反
应的化学方程式为 .
(6)F 的同分异构体中,既能发生银镜反应,又能与 FeCl 溶液发生显色反应的共有 种,
3
其中核磁共振氢谱为5 组峰,且峰面积比为2:2:2:1:1的为 (写结构简式).
第4页(共4页)