文档内容
2013年海南省高考化学试卷
一、选择题:本题共6小题.每小题2分,共12分.在每小题给出的四个选项中,只有一
项是符合题目要求的.
1.(2分)(2013•海南)下列有机化合物中沸点最高的是( )
A.乙烷B.乙烯 C.乙醇 D.乙酸
2.(2分)(2013•海南)下列化合物的俗称与化学式不对应的是( )
A.绿矾﹣FeSO •7H OB.芒硝﹣Na SO •10H O
4 2 2 4 2
C.明矾﹣Al (SO ) •12H O D.胆矾﹣CuSO •5H O
2 4 3 2 4 2
3.(2分)(2013•海南)重水(D O)是重要的核工业原料,下列说法错误的是( )
2
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H O与D O互称同素异形体
2 2
D.1H 18O与D 16O的相对分子质量相同
2 2
4.(2分)(2013•海南)Mg﹣AgCl电池是一种能被海水激活的一次性贮备电池,电池反
应方程式为:2AgCl+Mg=Mg2++2Ag+2Cl﹣.有关该电池的说法正确的是( )
A.Mg为电池的正极 B.负极反应为AgCl+e﹣=Ag+Cl﹣
C.不能被KCl 溶液激活 D.可用于海上应急照明供电
5.(2分)(2013•海南)已知下列反应的热化学方程式:
6C(s)+5H (g)+3N (g)+9O (g)═2C H (ONO ) (l)△H
2 2 2 3 5 2 3 1
2H (g)+O (g)═2H O(g)△H
2 2 2 2
C(s)+O (g)═CO (g)△H
2 2 3
则反应4C H (ONO ) (l)═12CO (g)+10H O(g)+O (g)+6N (g)的△H为(
3 5 2 3 2 2 2 2
)
A.12△H
3
+5△H
2
﹣2△H
1
B.2△H
1
﹣5△H
2
﹣12△H
3
C.12△H
3
﹣5△H
2
﹣2△H
1
D.△H
1
﹣5△H
2
﹣12△H
3
6.(2分)(2013•海南)如图所示仪器可用于实验室制备少量无水FeCl ,仪器连接顺序
3
正确的是( )
A.a﹣b﹣c﹣d﹣e﹣e﹣f﹣g﹣hB.a﹣e﹣d﹣c﹣b﹣h﹣i﹣g
C.a﹣d﹣e﹣c﹣b﹣h﹣i﹣g D.a﹣c﹣b﹣d﹣e﹣h﹣i﹣f
二、选择题:本题共6小题.每小题4分,共24分.每小题有一个或两个选项符合题意,
若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得
2分,选两个且都正确得4分,但只要选错一个就得0分.7.(4分)(2013•海南)下列鉴别方法不可行的是( )
A.用水鉴别乙醇、甲苯和溴苯
B.用燃烧法鉴别乙醇、苯和四氯化碳
C.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
D.用酸性高锰酸钾溶液鉴别苯、环已烯和环已烷
8.(4分)(2013•海南)0.1mol/LHF溶液的pH=2,则该溶液中有关浓度关系式不正确的
是( )
A.c(H+)>c(F﹣)B.c(H+)>c(HF)C.c(OH﹣)>c(HF) D.c(HF)>c
(F﹣)
9.(4分)(2013•海南)下列烃在光照下与氯气反应,只生成一种一氯代物的有( )
A.2﹣甲基丙烷 B.环戊烷
C.2,2﹣二甲基丁烷 D.2,2﹣二甲基丙烷
10.(4分)(2013•海南)能正确表示下列反应的离子反应方程式为( )
A.NH HCO 溶于过量的浓KOH溶液中:NH ++HCO ﹣+2OH﹣═CO 2﹣+NH ↑+2 H O
4 3 4 3 3 3 2
B.向明矾溶液中滴加Ba(OH) 溶液,恰好使SO 2﹣沉淀完全:2Al3++3SO 2﹣+3Ba2+
2 4 4
+6OH ﹣═2 Al(OH) ↓+3BaSO ↓
3 4
C.向FeBr 溶液中通入足量氯气:2Fe2++4Br﹣+3Cl ═2 Fe3++2Br +6 Cl﹣
2 2 2
D.醋酸除去水垢:2H++CaCO ═Ca2++CO ↑+H O
3 2 2
11.(4分)(2013•海南)下列关于仪器使用的说法正确的是( )
A.滴定管装滴定液时应先用滴定液润洗
B.锥形瓶用作反应容器时一定不能加热
C.蒸馏时温度计水银球可以高于蒸馏瓶支管口
D.振荡分液漏斗时应关闭其玻璃塞和活塞
12.(4分)(2013•海南)如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解
过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的
盐溶液是( )
选项 X Y
A MgSO CuSO
4 4
B AgNO Pb(NO )
3 3 2
C FeSO Al (SO )
4 2 4 3
D CuSO AgNO
4 3
A.A B.B C.C D.D
三、解答题(共11小题,满分146分)
本卷包括必考题和选考题两部分,第13题~第17题为必考题,每个试卷考生都必须做答。
第18题~第20题为选考题,考生根据要求做答。13.(9分)(2013•海南)X、Y和Z均为短周期元素,原子序数依次增大,X的单质为
密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同.
回答下列问题:
(1)X、Y和Z的元素符号分别为 、 、 .
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有 、
.
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的物质的电子式为
此化合物在酸性条件下与高锰酸钾反应的离子方程式为 ;此化合物还可将碱
性工业废水中的CN﹣氧化为碳酸盐和氨,相应的离子方程式为 .
14.(9分)(2013•海南)溴及其化合物广泛应用于医药、农药、纤维、塑料组燃剂等,
回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入 氯气将其中的Br﹣氧化,再用空气吹出溴;
然后用碳酸钠溶液吸收溴,溴歧化为Br﹣和BrO ﹣,其离子方程式为 ;
3
(2)溴与氯能以共价键结合形成BrCl.BrCl分子中, 显正电性.BrCl与水
发生反应的化学方程式为 ;
(3)CuBr 分解的热化学方程式为:2CuBr (s)=2CuBr(s)+Br (g)△H=+105.4kJ/mol
2 2 2
在密闭容器中将过量CuBr 于487K下加热分解,平衡时p(Br )为4.66×103Pa.
2 2
①如反应体系的体积不变,提高反应温度,则p (Br )将会 (填“增大”、
2
“不变”或“减小”).
②如反应温度不变,将反应体系的体积增加一倍,则p(Br )的变化范围为 .
2
15.(9分)(2013•海南)反应A(g)⇌B(g)+C(g)在容积为1.0L的密闭容器中进
行,A的初始浓度为0.050mol/L.温度T 和T 下A的浓度与时间关系如右图所示.回答下
1 2
列问题:
(1)上述反应的温度T T ,平衡常数K(T ) K(T ).(填
1 2 1 2
“大于”、“小于”或“等于”)
(2)若温度T 时,5min后反应达到平衡,A的转化率为70%,则:
2
①平衡时体系总的物质的量为 .
②反应的平衡常数K= .
③反应在0~5min区间的平均反应速率v(A)= .
16.(8分)(2013•海南)2﹣丁烯是石油裂解的产物之一,回答下列问题:
(1)在催化剂作用下,2﹣丁烯与氢气反应的化学方程式为 ,反应类型为
.
(2)烯烃A是2﹣丁烯的一种同分异构体,它在催化剂作用下与氢气反应的产物不是正丁
烷,则A的结构简式为 ;A分子中能够共平面的碳原子个数为 ,
A与溴的四氯化碳溶液反应的化学方程式为 .
17.(9分)(2013•海南)BaCl •xH O中结晶水数目可通过重量法来确定:
2 2
①称取1.222g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到
沉淀完全,静置;②过滤并洗涤沉淀;
③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉淀质量
为1.165g.
回答下列问题:
(1)在操作②中,需要先后用稀硫酸和洗涤沉淀;检验沉淀中氯离子是否洗净的方法是
.
(2)计算BaCl •xH O中的x= ;(要求写出计算过程).
2 2
(3)操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为
BaS,这使x的测定结果 (填“偏低”、“偏高”或“不变”).
选考题(请考生在请18.19.20三题中任选一题作答,如果多做,则按所做的第一题计分.
18.19.20三题的第一题为选择题,在给出的四个选项中,至少有两项是符合题目要求的,
请将符合题目要求的选项标号填在答题卡相应位置;第二题为非选择题
[选修5--有机化学基础
18.(6分)(2013•海南)下列化合物中,同分异构体数目超过7个的有( )
]
A.己烷B.己烯 C.1,2﹣二溴丙烷 D.乙酸乙酯
19.(14分)(2013•海南)肉桂酸异戊酯G( )是一种香料,一种
合成路线如下:
A(C H O) B(C H O) D E G
7 8 7 6
已知以下信息:
① ;
②C为甲醛的同系物,相同条件下其蒸气与氢气的密度比为22.
回答下列问题:
(1)A的化学名称为 .
(2)B和C反应生成D的化学方程式为 .
(3)F中含有官能团的名称为 .
(4)E和F反应生成G的化学方程式为 ,反应类型为 .
(5)F的同分异构体中不能与金属钠反应生成氢气的共有 种(不考虑立体异
构),其中核磁共振氢谱只有两组峰,且峰面积比为3:1的为 (写结构简
式).
[选修3--物质结构与性质
20.(2013•海南)下列化合物中,含有非极性共价键的离子化合物是( )
]
A.CaC B.N H C.Na S D.NH NO
2 2 4 2 2 4 3
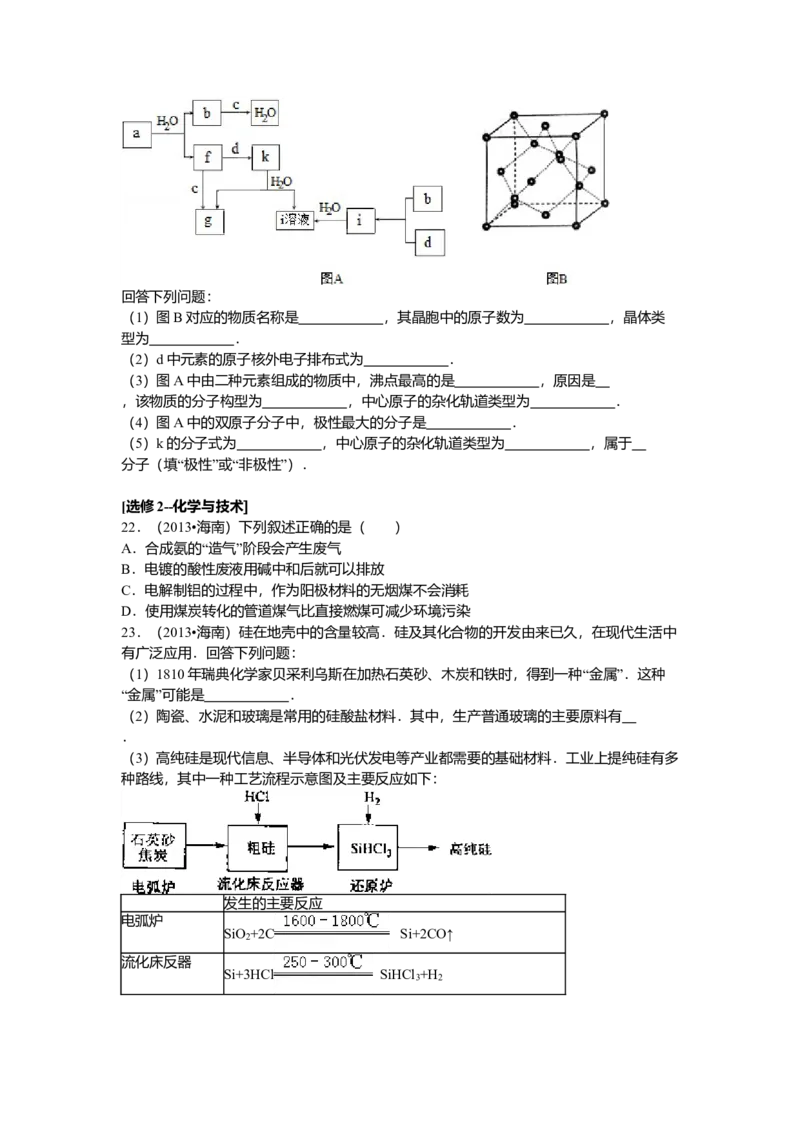
21.(2013•海南)图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种
短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形
体的晶胞如图B所示.回答下列问题:
(1)图B对应的物质名称是 ,其晶胞中的原子数为 ,晶体类
型为 .
(2)d中元素的原子核外电子排布式为 .
(3)图A中由二种元素组成的物质中,沸点最高的是 ,原因是
,该物质的分子构型为 ,中心原子的杂化轨道类型为 .
(4)图A中的双原子分子中,极性最大的分子是 .
(5)k的分子式为 ,中心原子的杂化轨道类型为 ,属于
分子(填“极性”或“非极性”).
[选修2--化学与技术
22.(2013•海南)下列叙述正确的是( )
]
A.合成氨的“造气”阶段会产生废气
B.电镀的酸性废液用碱中和后就可以排放
C.电解制铝的过程中,作为阳极材料的无烟煤不会消耗
D.使用煤炭转化的管道煤气比直接燃煤可减少环境污染
23.(2013•海南)硅在地壳中的含量较高.硅及其化合物的开发由来已久,在现代生活中
有广泛应用.回答下列问题:
(1)1810年瑞典化学家贝采利乌斯在加热石英砂、木炭和铁时,得到一种“金属”.这种
“金属”可能是 .
(2)陶瓷、水泥和玻璃是常用的硅酸盐材料.其中,生产普通玻璃的主要原料有
.
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料.工业上提纯硅有多
种路线,其中一种工艺流程示意图及主要反应如下:
发生的主要反应
电弧炉
SiO +2C Si+2CO↑
2
流化床反器
Si+3HCl SiHCl +H
3 2还原炉
SiHCl +H Si+3HCl
3 2
①用石英砂和焦炭在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为
;碳化硅又称 ,其晶体结构与 相似.
②在流化床反应的产物中,SiHCl 大约占85%,还有SiCl 、SiH Cl 、SiH Cl等,有关物质
3 4 2 2 3
的沸点数据如下表,提纯SiHCl 的主要工艺操作依次是沉降、冷凝和 .
3
物质 Si SiCl SiHCl SiH Cl SiH Cl HCl SiH
4 3 2 2 3 4
沸点/℃ 2355 57.6 31.8 8.2 ﹣30.4 ﹣84.9 ﹣111.9
③SiHCl
3
极易水解,其完全水解的产物为 .
(4)氯碱工业可为上述工艺生产提供部分原料,这些原料是 .