文档内容
2008 年海南高考化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 C1 35.5
第 I 卷
一、选择题:本题共12小题,每小题3分,在每小题给出的四个选项中,只有一项是
符合题目要求的。
1.HBr分子的电子式为:
2.用pH试纸测定溶液pH的正确操作是:
A.将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比
色卡对照
B.将一小块试纸用蒸馏水润湿后放在表面皿上,用玻璃棒蘸取少量待测液点在试纸
上,再与标准比色卡对照
C.将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照
D.将一小条试纸先用蒸馏水润湿后,在待测液中蘸一下,取出后与标准比色卡对照
3.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强
均相同,且甲的密度大于乙的密度,则下列说法正确的是:
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小
D.甲的相对分子质量比乙的相对分子质量小
4.锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成 1 mol硝酸锌时,被还原的硝酸
的物质的量为:
A.2mol B.1 mol C.0.5mol D.0.25mol
5.设N 为阿伏加德罗常数,下列说法正确的是:
A
A.标准状况下,5.6L四氯化碳含有的分子数为0.25N
A
B.标准状况下,14g氮气含有的核外电子数为5N
A
C.标准状况下,22.4L任意比的氢气和氯气的混合气体中含有的分子总数均为N
A
D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为N
A
6.下列离子方程式正确的是:7.关于铅蓄电池的说法正确的是:
A.在放电时,正极发生的反应是 Pb(s) +SO 2—(aq)= PbSO (s) +2e—
4 4
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO (s)+2e—= Pb(s)+ SO 2—(aq)
4 4
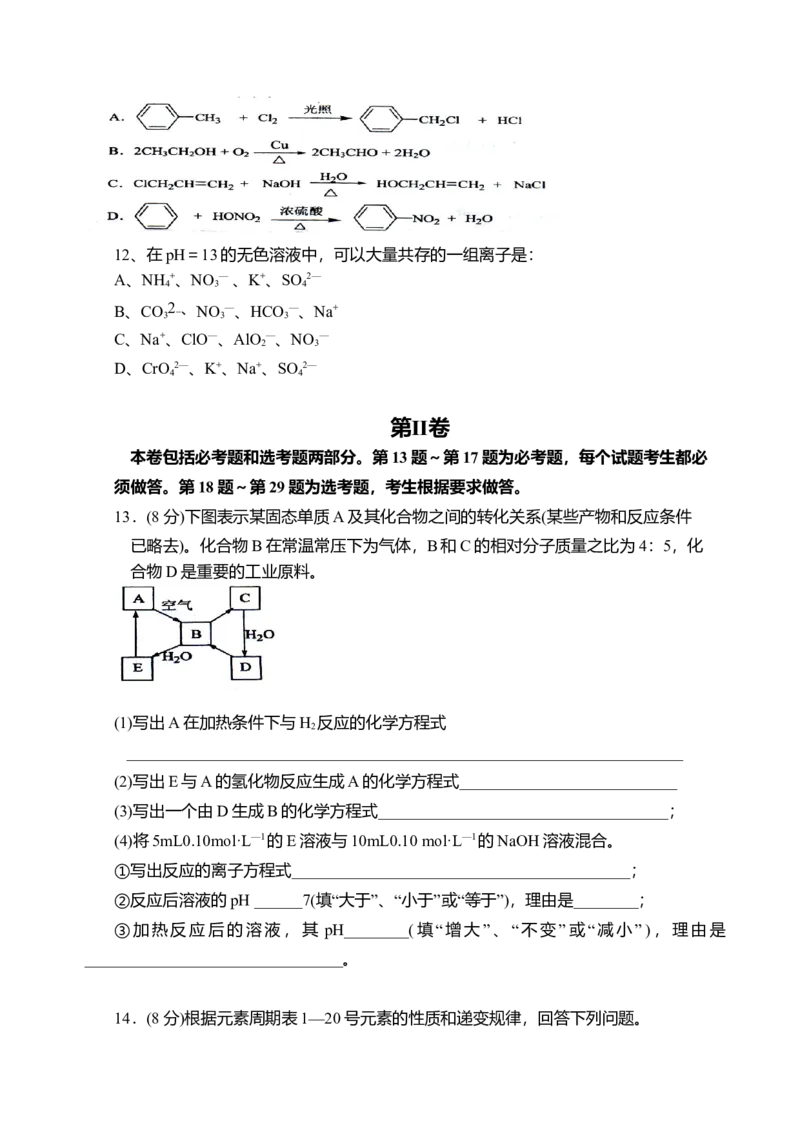
8.白磷与氧可发生如下反应:P +5O =P O 。已知断裂下列化学键需要吸收的能量
4 2 4 10
分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
A、(6a+5d-4c-12b)kJ·mol—1 B(4c+12b-6a-5d)kJ·mol—1
C、(4c+12b-4a-5d)kJ·mol—1 D、(4a+5d-4c-12b)kJ·mol—1
9.下列离子方程式中,属于水解反应的是:
A、HCOOH+H O HCOO— + HO+
2 3
B、CO +H O HCO — + H+
2 2 3
C、CO 2— + H O HCO — + OH—
3 2 3
D、HS— + H O S2— + HO+
2 3
10.X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生
如下反应:X+2Y 2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总
物质的量之比为3:2,则Y的转化率最接近于:
A、33% B、40% C、50% D、65%
11、下列有机反应中,不属于取代反应的是:12、在pH=13的无色溶液中,可以大量共存的一组离子是:
A、NH +、NO — 、K+、SO 2—
4 3 4
B、CO 2_、NO —、HCO —、Na+
3 3 3
C、Na+、ClO—、AlO —、NO —
2 3
D、CrO 2—、K+、Na+、SO 2—
4 4
第Ⅱ卷
本卷包括必考题和选考题两部分。第13题~第17题为必考题,每个试题考生都必
须做答。第18题~第29题为选考题,考生根据要求做答。
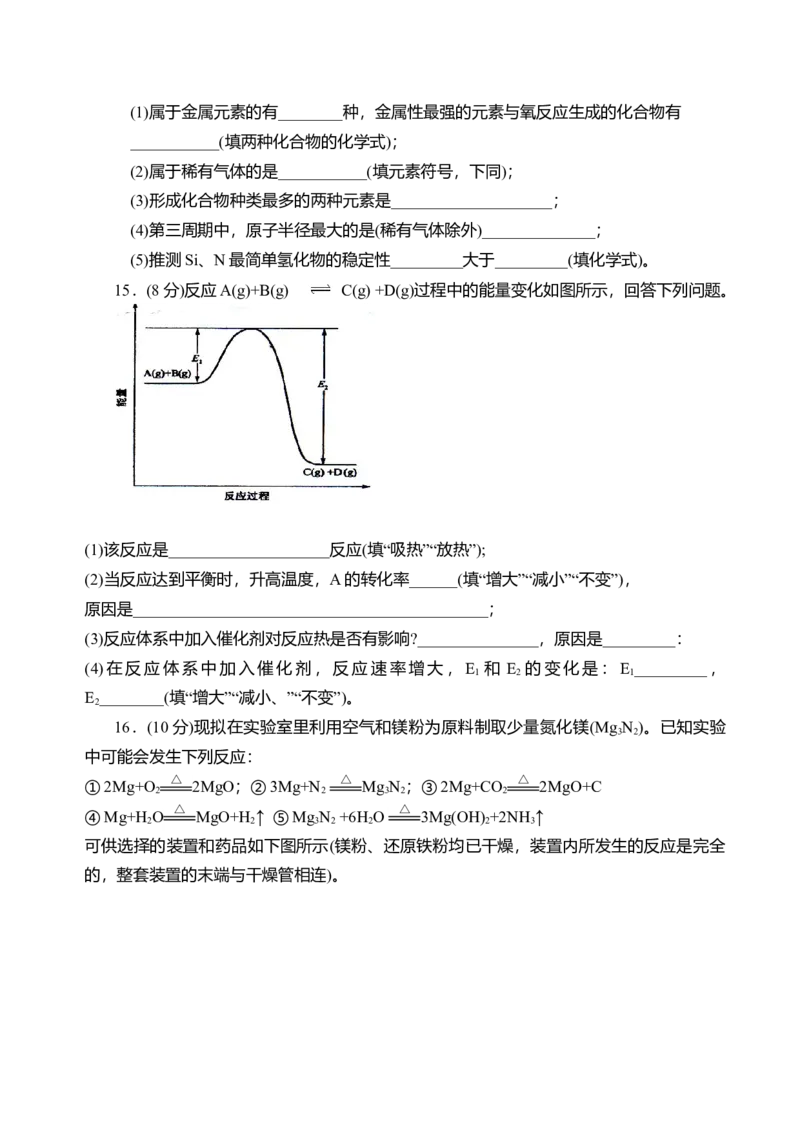
13.(8分)下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件
已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化
合物D是重要的工业原料。
(1)写出A在加热条件下与H 反应的化学方程式
2
_____________________________________________________________________
(2)写出E与A的氢化物反应生成A的化学方程式___________________________
(3)写出一个由D生成B的化学方程式____________________________________;
(4)将5mL0.10mol·L—1的E溶液与10mL0.10 mol·L—1的NaOH溶液混合。
①写出反应的离子方程式__________________________________________;
②反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是________;
③加热反应后的溶液,其 pH________(填“增大”、“不变”或“减小”),理由是
________________________________。
14.(8分)根据元素周期表1—20号元素的性质和递变规律,回答下列问题。(1)属于金属元素的有________种,金属性最强的元素与氧反应生成的化合物有
___________(填两种化合物的化学式);
(2)属于稀有气体的是___________(填元素符号,下同);
(3)形成化合物种类最多的两种元素是____________________;
(4)第三周期中,原子半径最大的是(稀有气体除外)______________;
(5)推测Si、N最简单氢化物的稳定性_________大于_________(填化学式)。
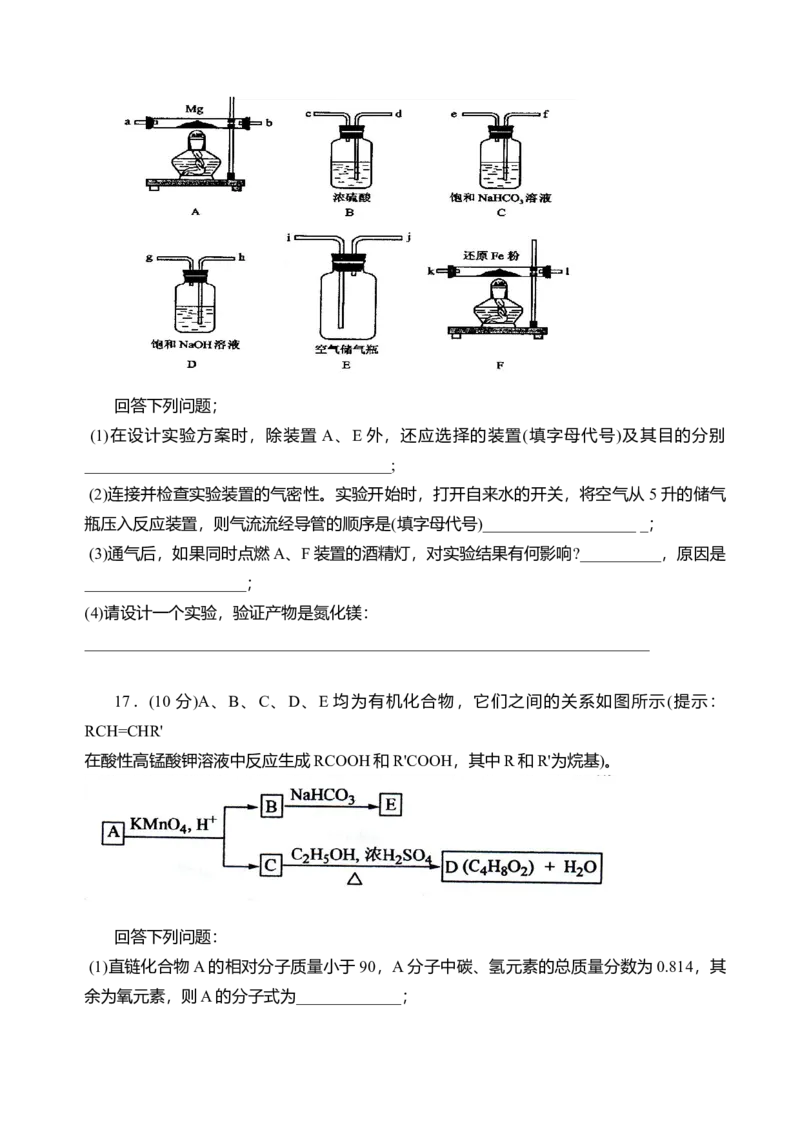
15.(8分)反应A(g)+B(g) C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是____________________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”“减小”“不变”),
原因是____________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?_______________,原因是_________:
(4)在反应体系中加入催化剂,反应速率增大,E 和 E 的变化是:E _________,
1 2 1
E ________(填“增大”“减小、”“不变”)。
2
16.(10分)现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg N )。已知实验
3 2
中可能会发生下列反应:
△ △ △
①2Mg+O 2MgO;②3Mg+N Mg N ;③2Mg+CO 2MgO+C
2 2 3 2 2
④Mg+H O
△
M gO+H ↑ ⑤Mg N +6H O
△
3 M g(OH) +2NH ↑
2 2 3 2 2 2 3
可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全
的,整套装置的末端与干燥管相连)。回答下列问题;
(1)在设计实验方案时,除装置 A、E 外,还应选择的装置(填字母代号)及其目的分别
______________________________________;
(2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从 5升的储气
瓶压入反应装置,则气流流经导管的顺序是(填字母代号)___________________ _;
(3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响?__________,原因是
____________________;
(4)请设计一个实验,验证产物是氮化镁:
______________________________________________________________________
17.(10 分)A、B、C、D、E 均为有机化合物,它们之间的关系如图所示(提示:
RCH=CHR'
在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH,其中R和R'为烷基)。
回答下列问题:
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其
余为氧元素,则A的分子式为_____________;(2)已知B与NaHCO 溶液完全反应,其物质的量之比为 1:2,则在浓硫酸的催化下,B与
3
足量的C H OH发生反应的化学方程式是___________,反应类型为_____:
2 5
(3)A 可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则 A 的结构简式是
__________________
(4)D的同分异构体中,能与NaHCO 溶液反应放出CO 的有__________种,其相应的结构
3 2
简式是__________________。
以下是选考题,其中第 18、19、20、21 题为《有机化学基础》
模块题,第 22、23、24、25 题为(物质结构与性质》模块题,第
26、27、28、29 题为《化学与技术》模块题。考生只能从三个模块
中任选一个作答,不得跨模块答题,否则只能以所答的第一个模块
计分。
《有机化学基础》模块
18-20为选择题,每小题只有一个正确选项,每小题3分
18.在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物是:
19.分子式为C H O并能与金属钠反应放出氢气的有机化合物有:
4 10
A.3种 B.4种 C.5种 D.6种
20.1mo1X能与足量碳酸氢钠溶液反应放出44.8LCO (标准状况),则X的分子式是:
2
A、C H O B.C H O C.C H O D.C H O
5 10 4 4 8 4 3 6 4 2 2 4
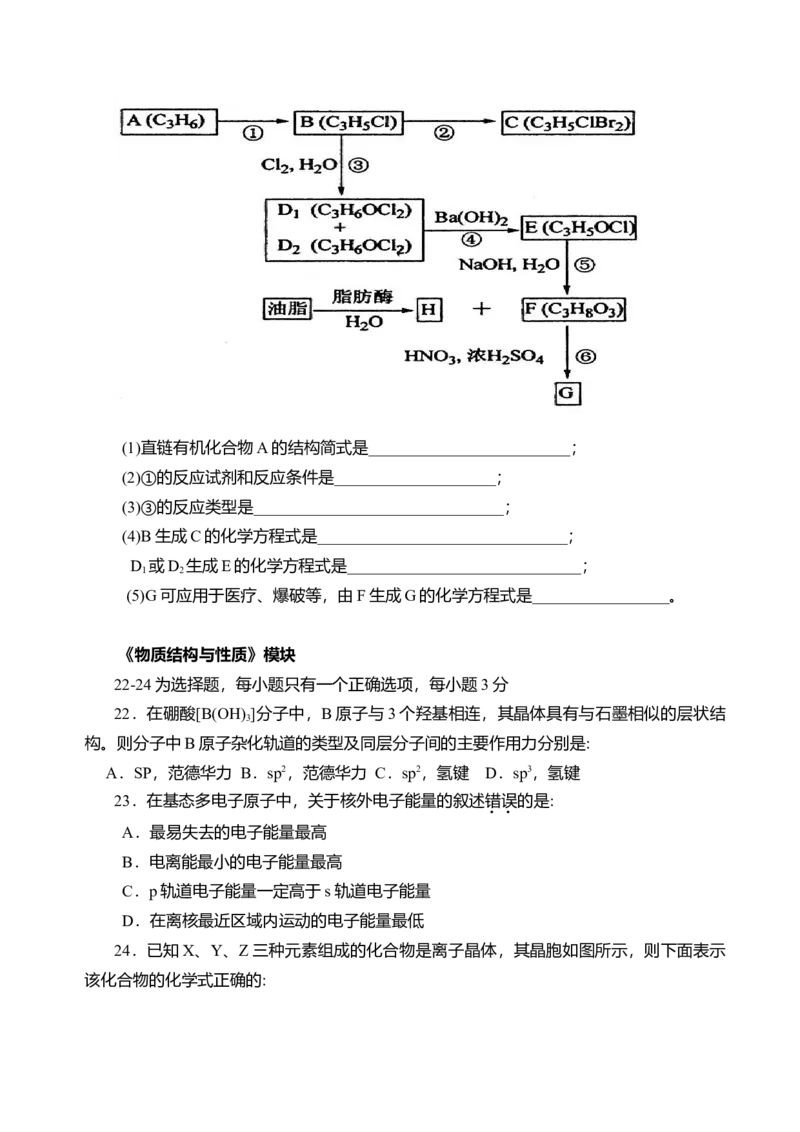
21.(11分)A、B、C、D 、D 、E、F、G、H均为有机化合物,请根据下列图示回答
1 2
问题。(1)直链有机化合物A的结构简式是_________________________;
(2)①的反应试剂和反应条件是____________________;
(3)③的反应类型是_______________________________;
(4)B生成C的化学方程式是_______________________________;
D 或D 生成E的化学方程式是_____________________________;
1 2
(5)G可应用于医疗、爆破等,由F生成G的化学方程式是_________________。
《物质结构与性质》模块
22-24为选择题,每小题只有一个正确选项,每小题3分
22.在硼酸[B(OH) ]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结
3
构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是:
A.SP,范德华力 B.sp2,范德华力 C.sp2,氢键 D.sp3,氢键
23.在基态多电子原子中,关于核外电子能量的叙述错误的是:
A.最易失去的电子能量最高
B.电离能最小的电子能量最高
C.p轨道电子能量一定高于s轨道电子能量
D.在离核最近区域内运动的电子能量最低
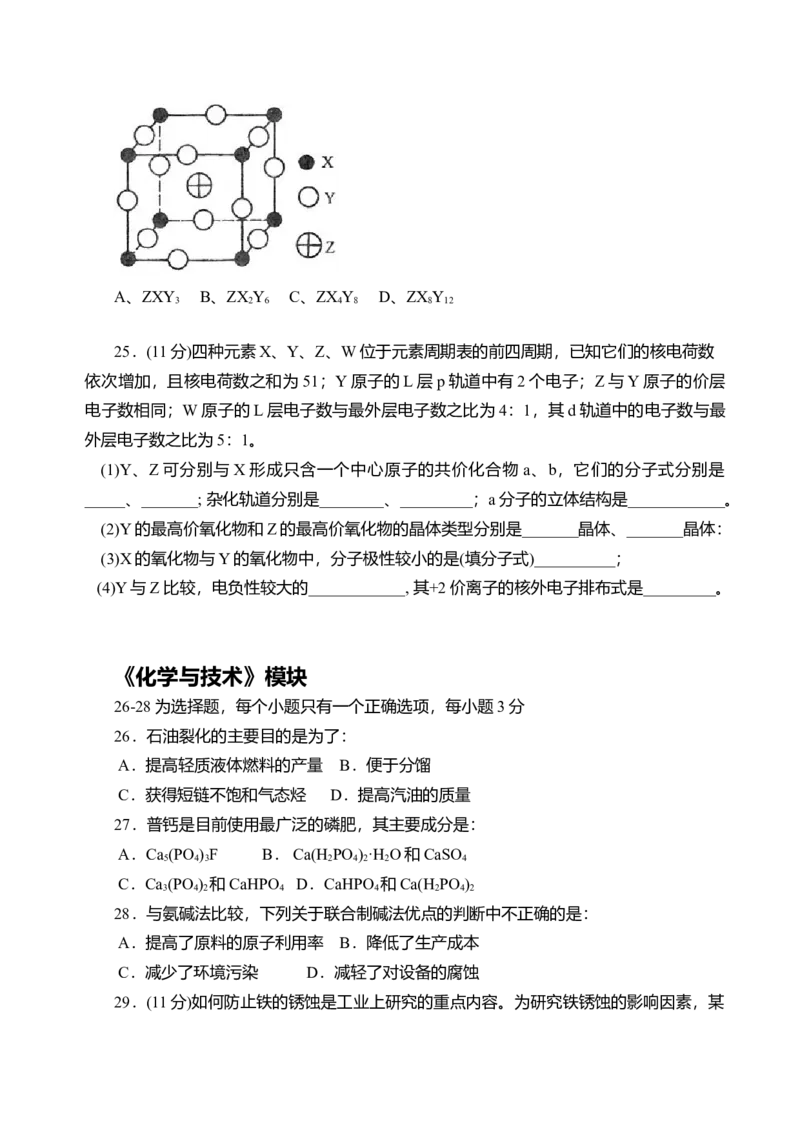
24.已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则下面表示
该化合物的化学式正确的:A、ZXY B、ZX Y C、ZX Y D、ZX Y
3 2 6 4 8 8 12
25.(11分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数
依次增加,且核电荷数之和为 51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层
电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最
外层电子数之比为5:1。
(1)Y、Z可分别与 X形成只含一个中心原子的共价化合物 a、b,它们的分子式分别是
_____、_______; 杂化轨道分别是________、_________;a分子的立体结构是____________。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体:
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)__________;
(4)Y与Z比较,电负性较大的____________, 其+2价离子的核外电子排布式是_________。
《化学与技术》模块
26-28为选择题,每个小题只有一个正确选项,每小题3分
26.石油裂化的主要目的是为了:
A.提高轻质液体燃料的产量 B.便于分馏
C.获得短链不饱和气态烃 D.提高汽油的质量
27.普钙是目前使用最广泛的磷肥,其主要成分是:
A.Ca (PO ) F B. Ca(H PO ) ·H O和CaSO
5 4 3 2 4 2 2 4
C.Ca (PO ) 和CaHPO D.CaHPO 和Ca(H PO )
3 4 2 4 4 2 4 2
28.与氨碱法比较,下列关于联合制碱法优点的判断中不正确的是:
A.提高了原料的原子利用率 B.降低了生产成本
C.减少了环境污染 D.减轻了对设备的腐蚀
29.(11分)如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
序号 内容 实验现象
1 常温下将铁丝放在干燥空气中一个月 干燥的铁丝表面依然光亮
2 常温下将铁丝放在潮湿空气中一小时 铁丝表面依然光亮
3 常温下将铁丝放在潮湿的空气中一个月 铁丝表面已变得灰暗
4 将潮湿的铁丝放在常温的氧气流中一小时 铁丝表面略显灰暗
5 将潮湿的铁丝放在高于常温的氧气流中一小时 铁丝表面已变得灰暗
将浸过氯化钠溶液的铁丝放在高于常温的氧气流 铁丝表面灰暗程度比实验5严
6
中一小时 重
回答以下问题:
(1) 上 述 实 验 中 发 生 了 电 化 学 腐 蚀 的 是 ( 填 实 验 序 号 ) __________; 在 电 化 学 腐
蚀中,负极反应是________________; 正极反应是_______________________;
(2)由该实验可知,可以影响铁锈蚀速率的因素是___________________________;
(3)为防止铁的锈蚀,工业上普遍采用的方法是______________(答两种方法)