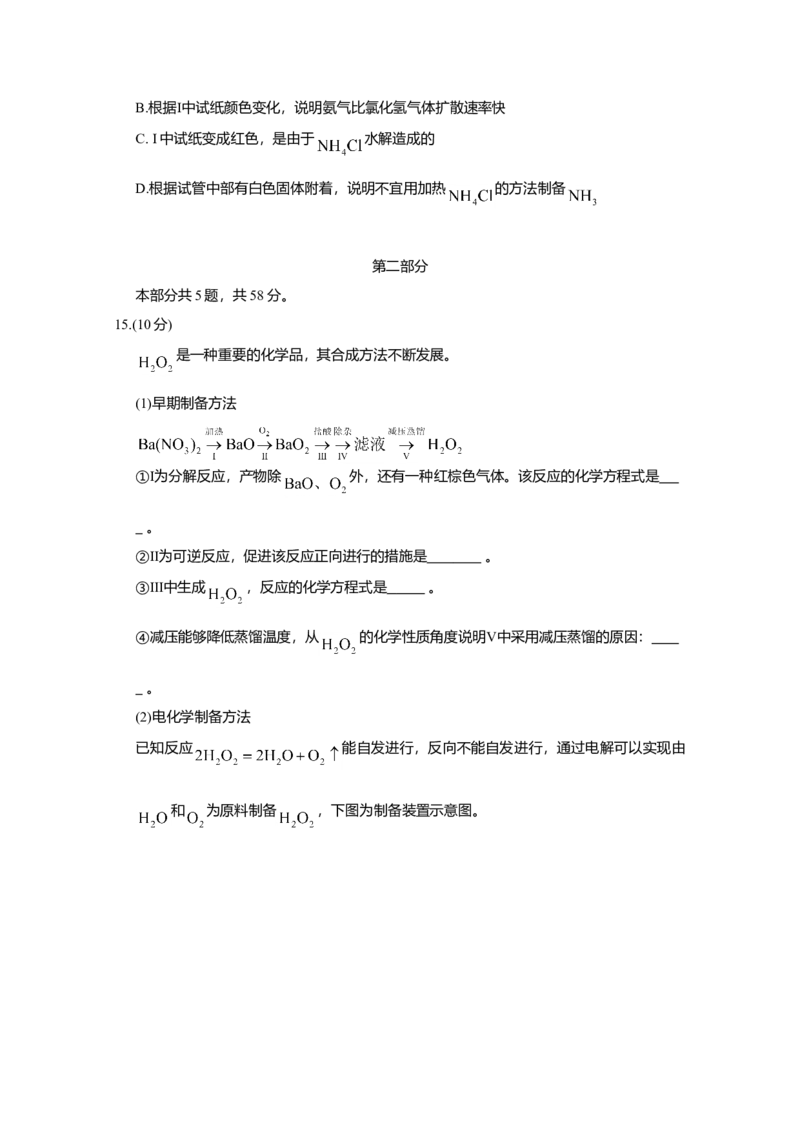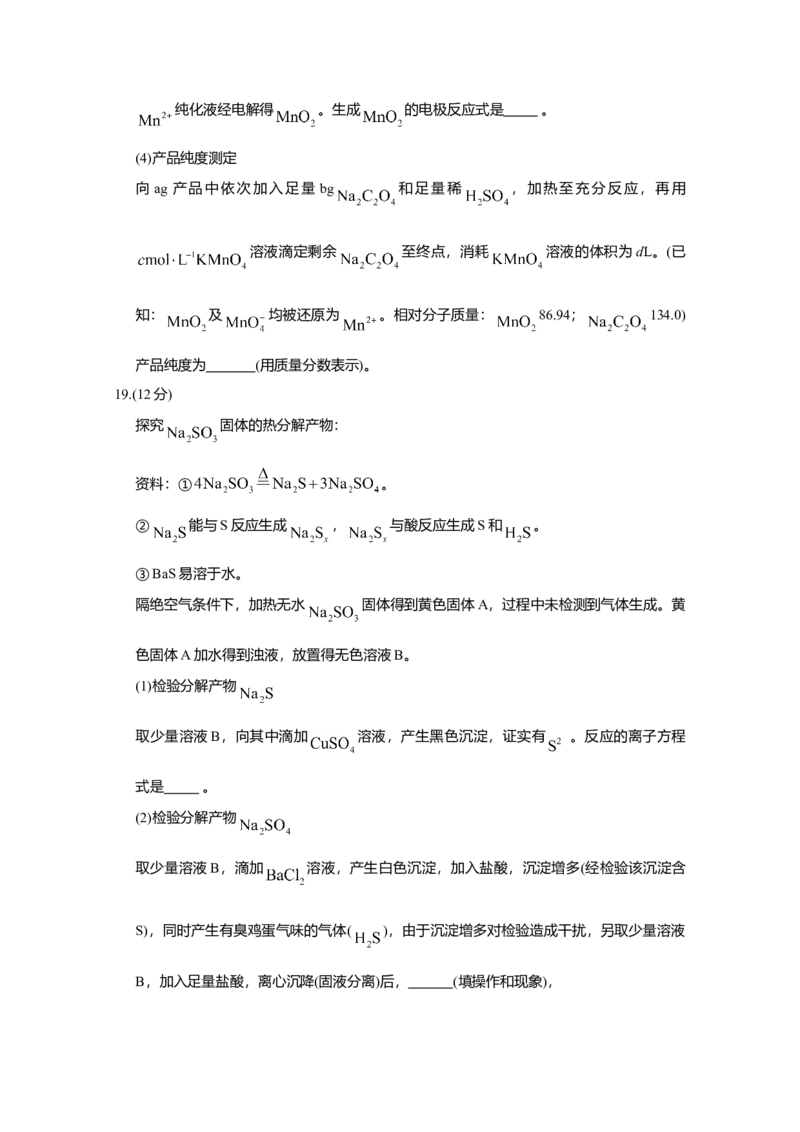文档内容
绝密★启用前
2020年北京市普通高中学业水平等级性考试
化 学
本试卷共9页,100分。考试时长90分钟。考生务必将答案答在答题卡上,在试卷上作
答无效。考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 N14O16
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求
的一项。
1. 近年来,我国航空航天事业成果显著。下列成果所涉及的材料为金属材料的是
A. “天宫二号”航天器使用的质量轻强度高的材料——钛合金
B. “北斗三号”导航卫星使用的太阳能电池材料——砷化镓
C. “长征五号”运载火箭使用的高效燃料——液氢
D. “C919”飞机身使用的复合材料——碳纤维和环氧树脂
2. 下列物质的应用中,利用了氧化还原反应的是
A. 用石灰乳脱除烟气中的
B. 用明矾 处理污水
C. 用盐酸去除铁锈(主要成分 )
D. 用84消毒液(有效成分 )杀灭细菌
3.水与下列物质反应时,水表现出氧化性的是
A. B. C. D.
4.已知: (砷)与P为同族元素。下列说法不正确的是
A. 原子核外最外层有5个电子 B. 的电子式是
C. 热稳定性: D. 非金属性:5.下列说法正确的是
A. 同温同压下, 和 的密度相同
B. 质量相同的 和 (重水)所含的原子数相同
C. 物质的量相同的 和 所含共价键数相同
D.室温下,pH相同的盐酸和硫酸中,溶质的物质的量浓度相同
6.下列说法正确的是
A. 用碳酸钠溶液处理锅炉水垢:
B. 湿润的淀粉碘化钾试纸遇氯气变蓝:
C. 铝粉和氧化铁组成的铝热剂用于焊接钢轨:
D. 淡黄色的过氧化钠敞口放置变成白色:
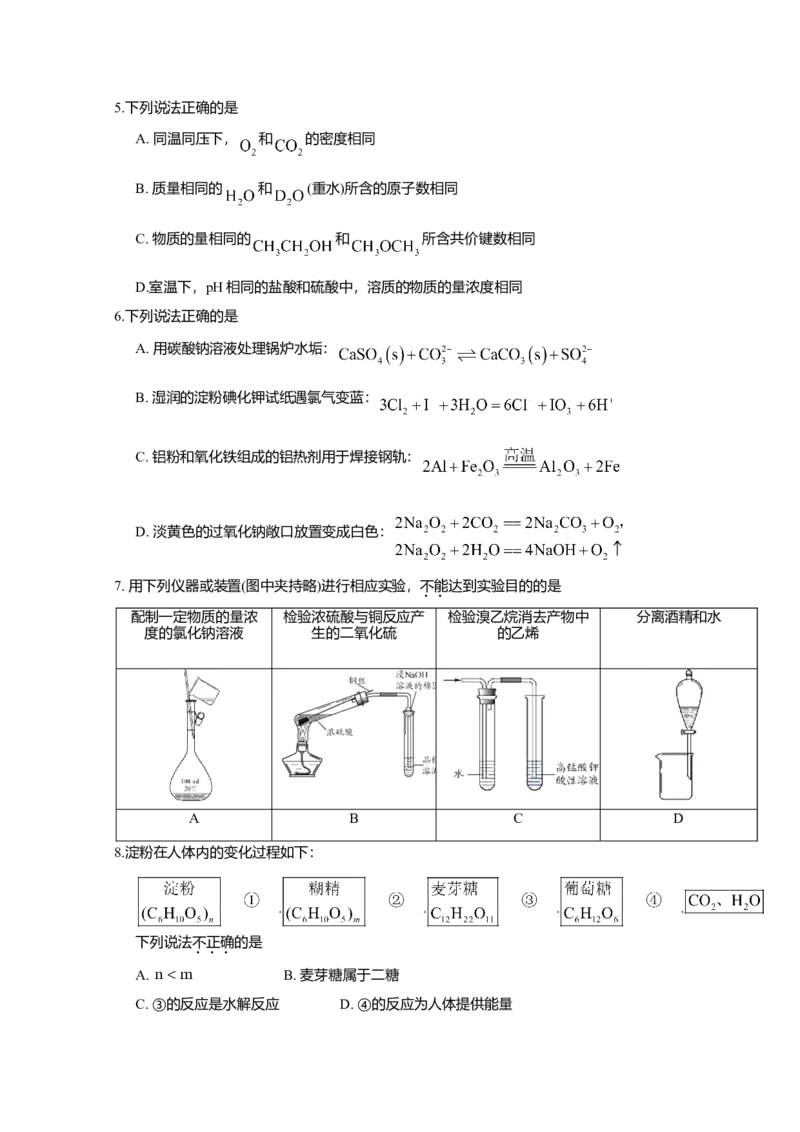
7. 用下列仪器或装置(图中夹持略)进行相应实验,不能达到实验目的的是
配制一定物质的量浓 检验浓硫酸与铜反应产 检验溴乙烷消去产物中 分离酒精和水
度的氯化钠溶液 生的二氧化硫 的乙烯
A B C D
8.淀粉在人体内的变化过程如下:
下列说法不正确的是
A. B. 麦芽糖属于二糖
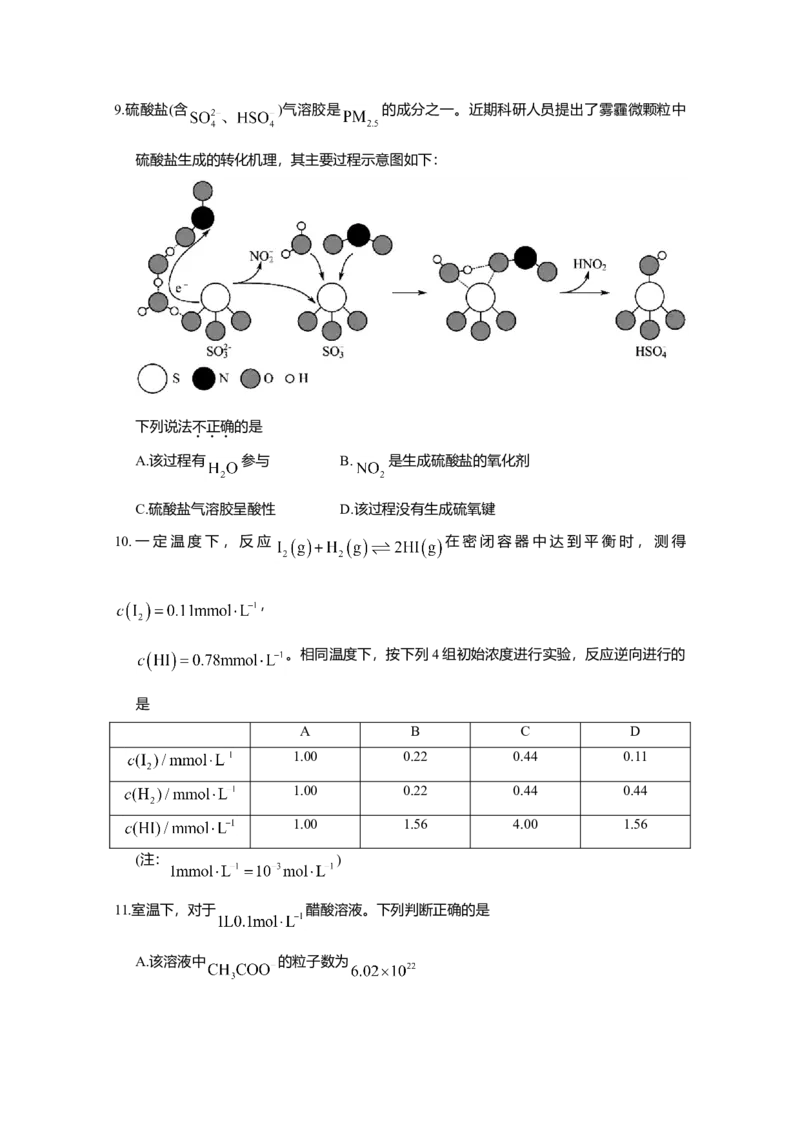
C. ③的反应是水解反应 D. ④的反应为人体提供能量9.硫酸盐(含 )气溶胶是 的成分之一。近期科研人员提出了雾霾微颗粒中
硫酸盐生成的转化机理,其主要过程示意图如下:
下列说法不正确的是
A.该过程有 参与 B. 是生成硫酸盐的氧化剂
C.硫酸盐气溶胶呈酸性 D.该过程没有生成硫氧键
10.一定温度下,反应 在密闭容器中达到平衡时,测得
,
。相同温度下,按下列4组初始浓度进行实验,反应逆向进行的
是
A B C D
1.00 0.22 0.44 0.11
1.00 0.22 0.44 0.44
1.00 1.56 4.00 1.56
(注: )
11.室温下,对于 醋酸溶液。下列判断正确的是
A.该溶液中 的粒子数为B.加入少量 固体后,溶液的pH降低
C.滴加 溶液过程中, 与 之和始终为
D.与 溶液反应的离子方程式为
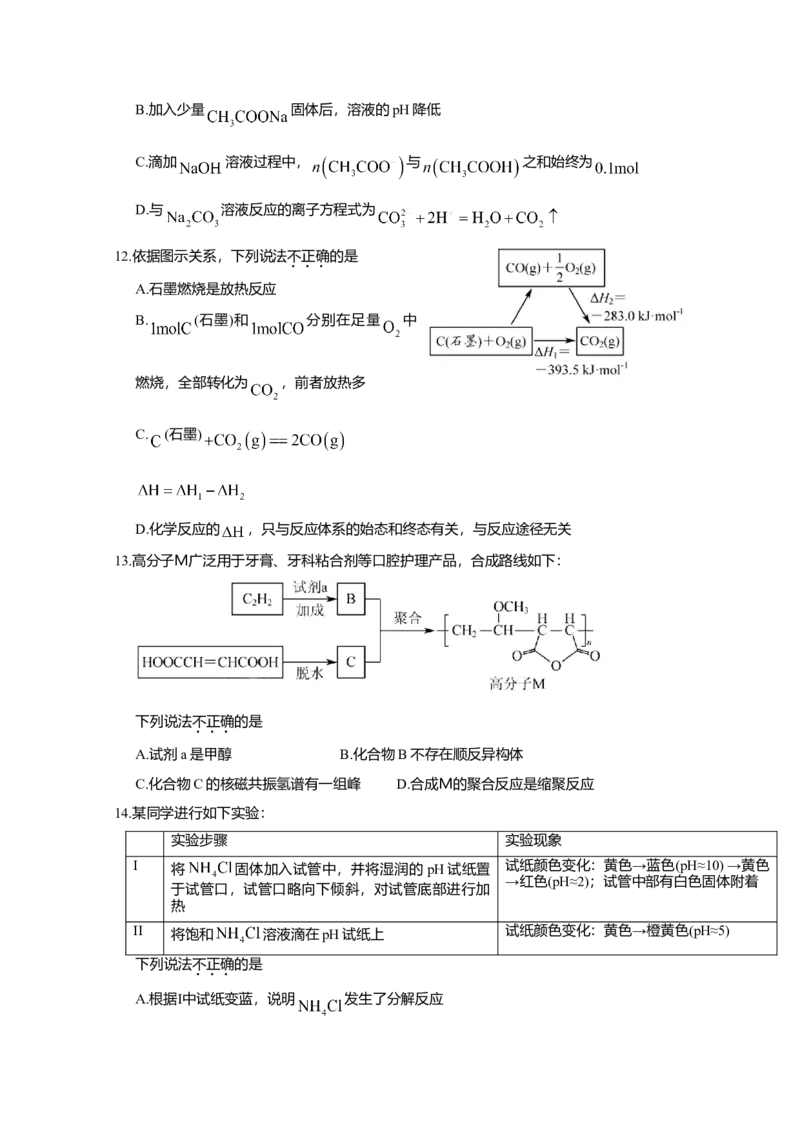
12.依据图示关系,下列说法不正确的是
A.石墨燃烧是放热反应
B. (石墨)和 分别在足量 中
燃烧,全部转化为 ,前者放热多
C. (石墨)
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关
13.高分子M广泛用于牙膏、牙科粘合剂等口腔护理产品,合成路线如下:
下列说法不正确的是
A.试剂a是甲醇 B.化合物B不存在顺反异构体
C.化合物C的核磁共振氢谱有一组峰 D.合成M的聚合反应是缩聚反应
14.某同学进行如下实验:
实验步骤 实验现象
I 将 固体加入试管中,并将湿润的pH试纸置 试纸颜色变化:黄色→蓝色(pH≈10) →黄色
→红色(pH≈2);试管中部有白色固体附着
于试管口,试管口略向下倾斜,对试管底部进行加
热
II 将饱和 溶液滴在pH试纸上 试纸颜色变化:黄色→橙黄色(pH≈5)
下列说法不正确的是
A.根据Ⅰ中试纸变蓝,说明 发生了分解反应B.根据Ⅰ中试纸颜色变化,说明氨气比氯化氢气体扩散速率快
C. Ⅰ中试纸变成红色,是由于 水解造成的
D.根据试管中部有白色固体附着,说明不宜用加热 的方法制备
第二部分
本部分共5题,共58分。
15.(10分)
是一种重要的化学品,其合成方法不断发展。
(1)早期制备方法
①Ⅰ为分解反应,产物除 外,还有一种红棕色气体。该反应的化学方程式是
。
②Ⅱ为可逆反应,促进该反应正向进行的措施是 。
③Ⅲ中生成 ,反应的化学方程式是 。
④减压能够降低蒸馏温度,从 的化学性质角度说明Ⅴ中采用减压蒸馏的原因:
。
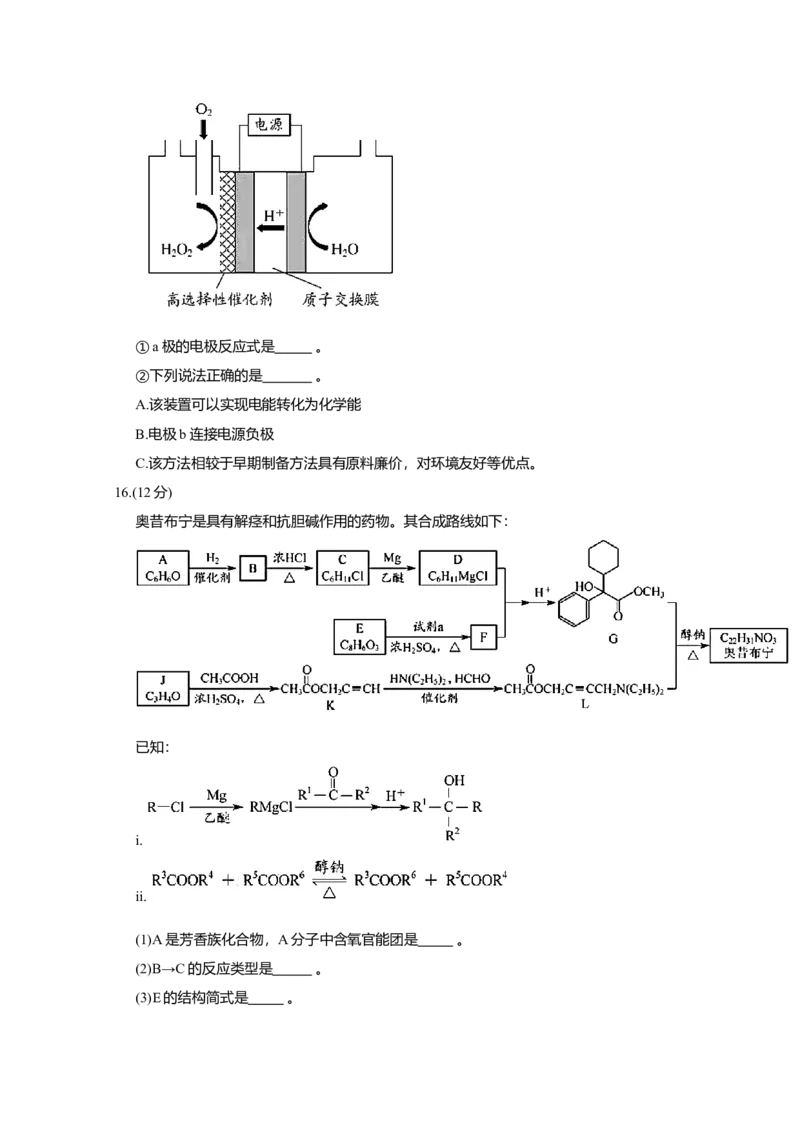
(2)电化学制备方法
已知反应 能自发进行,反向不能自发进行,通过电解可以实现由
和 为原料制备 ,下图为制备装置示意图。①a极的电极反应式是 。
②下列说法正确的是 。
A.该装置可以实现电能转化为化学能
B.电极b连接电源负极
C.该方法相较于早期制备方法具有原料廉价,对环境友好等优点。
16.(12分)
奥昔布宁是具有解痉和抗胆碱作用的药物。其合成路线如下:
已知:
i.
ii.
(1)A是芳香族化合物,A分子中含氧官能团是 。
(2)B→C的反应类型是 。
(3)E的结构简式是 。(4)J→K的化学方程式是 。
(5)已知:G、L和奥昔布宁的沸点均高于200℃,G和L发生反应合成奥昔布宁时,通过
在70℃左右蒸出 (填物质名称)来促进反应。
(6)奥昔布宁的结构简式是 。
17.(12分)
用如下方法回收废旧CPU中的单质Au(金),Ag和Cu。
已知:①浓硝酸不能单独将Au溶解。
②
(1)酸溶后经 操作,将混合物分离。
(2)浓、稀 均可作酸溶试剂。溶解等量的Cu消耗 的物质的量不同,写出消
耗 物质的量少的反应的化学方程式: 。
(3) 与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。
①将溶金反应的化学方程式补充完整:
②关于溶金的下列说法正确的是 。
A.用到了 的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与 也可使Au溶解
(4)若用Zn粉将溶液中的 完全还原,则参加反应的Zn的物质的量是
mol。
(5)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如下方法从酸溶后的溶液中回收
Cu和Ag(图中标注的试剂和物质均不同)。试剂1是 ,试剂2是 。
18.(12分)
是重要化工原料,由软锰矿制备 的一种工艺流程如下:
资料:①软锰矿的主要成分为 ,主要杂质有 和
②金属离子沉淀的pH
开始沉淀时 1.5 3.4 5.8 6.3
完全沉淀时 2.8 4.7 7.8 8.3
③该工艺条件下, 与 不反应。
(1)溶出
①溶出前,软锰矿需研磨。目的是 。
②溶出时,Fe的氧化过程及得到 的主要途径如图所示。
i. Ⅱ是从软锰矿中溶出 的主要反应,反应的离子方程式是 。
ii.若 全部来自于反应 ,完全溶出 所需Fe与 的
物质的量比值为2。而实际比值(0.9)小于2,原因是 。
(2)纯化
已知: 的氧化性与溶液pH有关。纯化时先加入 ,后加入 ,调
溶液pH≈5,说明试剂加入顺序及调节pH的原因: 。
(3)电解纯化液经电解得 。生成 的电极反应式是 。
(4)产品纯度测定
向 ag 产品中依次加入足量 bg 和足量稀 ,加热至充分反应,再用
溶液滴定剩余 至终点,消耗 溶液的体积为dL。(已
知: 及 均被还原为 。相对分子质量: 86.94; 134.0)
产品纯度为 (用质量分数表示)。
19.(12分)
探究 固体的热分解产物:
资料:① 。
② 能与S反应生成 , 与酸反应生成S和 。
③BaS易溶于水。
隔绝空气条件下,加热无水 固体得到黄色固体A,过程中未检测到气体生成。黄
色固体A加水得到浊液,放置得无色溶液B。
(1)检验分解产物
取少量溶液B,向其中滴加 溶液,产生黑色沉淀,证实有 。反应的离子方程
式是 。
(2)检验分解产物
取少量溶液B,滴加 溶液,产生白色沉淀,加入盐酸,沉淀增多(经检验该沉淀含
S),同时产生有臭鸡蛋气味的气体( ),由于沉淀增多对检验造成干扰,另取少量溶液
B,加入足量盐酸,离心沉降(固液分离)后, (填操作和现象),可证实分解产物中含有 。
(3)探究(2)中S的来源
来源1:固体A中有未分解的 ,在酸性条件下与 反应生成S。
来源2:溶液B中有 ,加酸反应生成S。
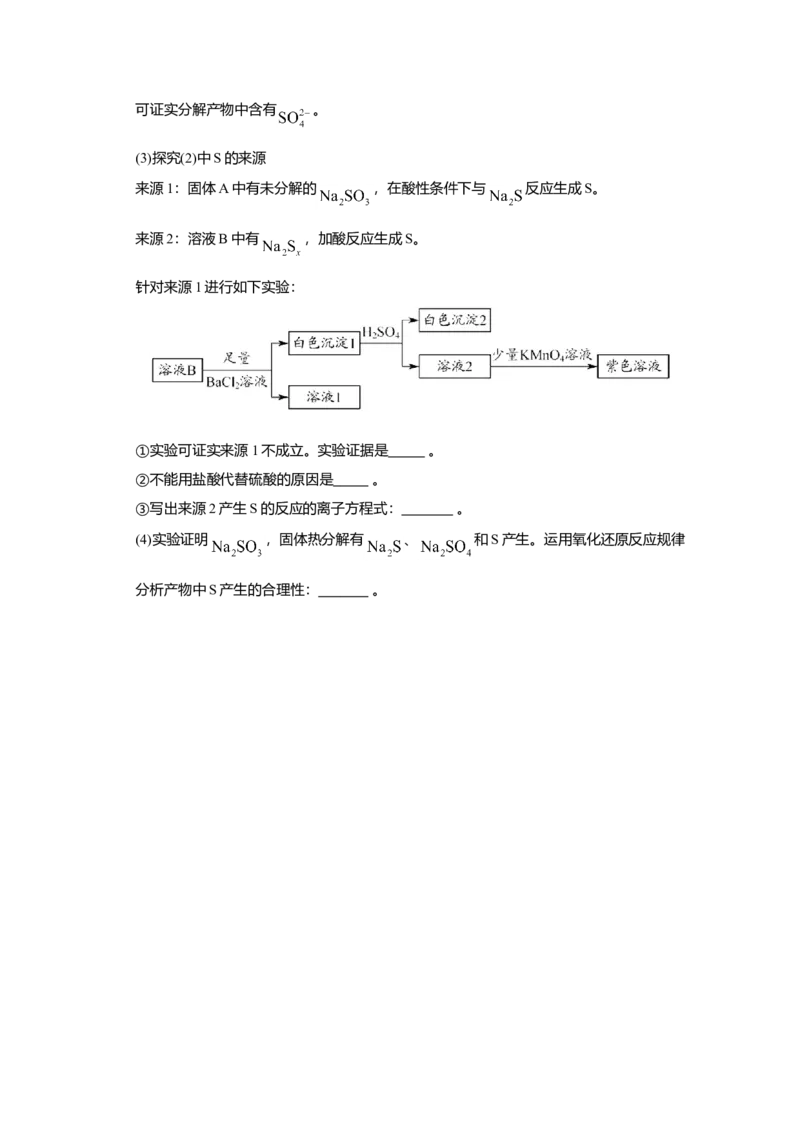
针对来源1进行如下实验:
①实验可证实来源1不成立。实验证据是 。
②不能用盐酸代替硫酸的原因是 。
③写出来源2产生S的反应的离子方程式: 。
(4)实验证明 ,固体热分解有 、 和S产生。运用氧化还原反应规律
分析产物中S产生的合理性: 。