文档内容
2014 年海南省高考化学试题及答案
第Ⅰ卷
一、选择题:本题共6小题,每小题2分,共12分。在每小题给出的四个选项中,只有一
个是正确的
1、化学与日常生活密切相关,下列说法错误的是( )
A、碘酒是指单质碘的乙醇溶液 B、84消毒液的有效成分是NaClO
C、浓硫酸可刻蚀石英制艺术品 D、装饰材料释放的甲醛会造成污染
2、下列有关物质性质的说法错误的是( )
A、热稳定性:HCl>HI B、原子半径:Na>Mg
C、酸性:H SO >H SO D、结合质子能力:S2—>Cl—
2 3 2 4
3、以石墨为电极,电解KI溶液(含有少量的酚酞和淀粉),下列说法错误的是
A、阴极附近溶液呈红色 B、阴极逸出气体
C、阳极附近溶液呈蓝色 D、溶液的PH变小
4、标准状况下,气态分子断开 1mol化学键的焓变称为键焓。已知 H—H,H—O,和
O==O键的键焓△H分别为436KJ/mol,463KJ/mol,495KJ/mol,下列热化学方程式正确的
是( )
A、H O(g)==H (g)+1/2O (g) △H =—485KJ/mol
2 2 2
B、H O(g)==H (g)+1/2O (g) △H = + 485KJ/mol
2 2 2
C、2 H (g) + O (g)==2 H O(g) △H = + 485KJ/mol
2 2 2
D、2 H (g) + O (g)==2 H O(g) △H =—485KJ/mol
2 2 2
5、下列除杂操作可行的是( )
A、通过浓硫酸除去HCl中的H O B、通过灼热的CuO除去H 中的CO
2 2
C、通过灼热的镁粉除去N2中的O D、通过水除去CO中的CO
2 2
6、NaOH溶液滴定盐酸的实验中,不必用到的是( )
A、酚酞 B、圆底烧瓶 C、锥形瓶 D、碱式滴定管
二、选择题:本题共6小题,每小题4分,每小题有1~2个选项符合题意。若正确答案只
包括一个选项,多选的0分,若正确答案包括两个选项,只选一个且正确得2分,选两个
且正确得4分,但只要选错一个就得0分。
7、下列有关物质水解的说法正确的是( )
A、蛋白质水解的最终产物是多肽 B、淀粉水解的最终产物是葡萄糖
C、纤维素不能水解成葡萄糖 D、油脂水解产物之一是甘油
8、某反应工程能量变化如图所示,下列说法正确的是
A、反应过程a有催化剂参与
B、该反应为放热反应,热效应等于△H
C、改变催化剂,可改变该反应的活化能
D、有催化剂的条件下,反应的活化能等于E +E
1 2
9、下列有关物质应用的说法错误的是( )
A、玻璃容器可长期盛放各种酸 B、纯碱可用于清洗油污
1B、浓氨水可检验氯气管道泄漏 D、Na S可除去污水中的Cu2+
2
10、下列关于物质应用和组成的说法正确的是( )
A、P O 可用于干燥Cl 和NH B、“可燃冰”的主要成分是甲烷和水
2 5 2 3
C、CCl 可用于鉴别溴水和碘水 D、Si和SiO 都用于制造光导纤维
4 2
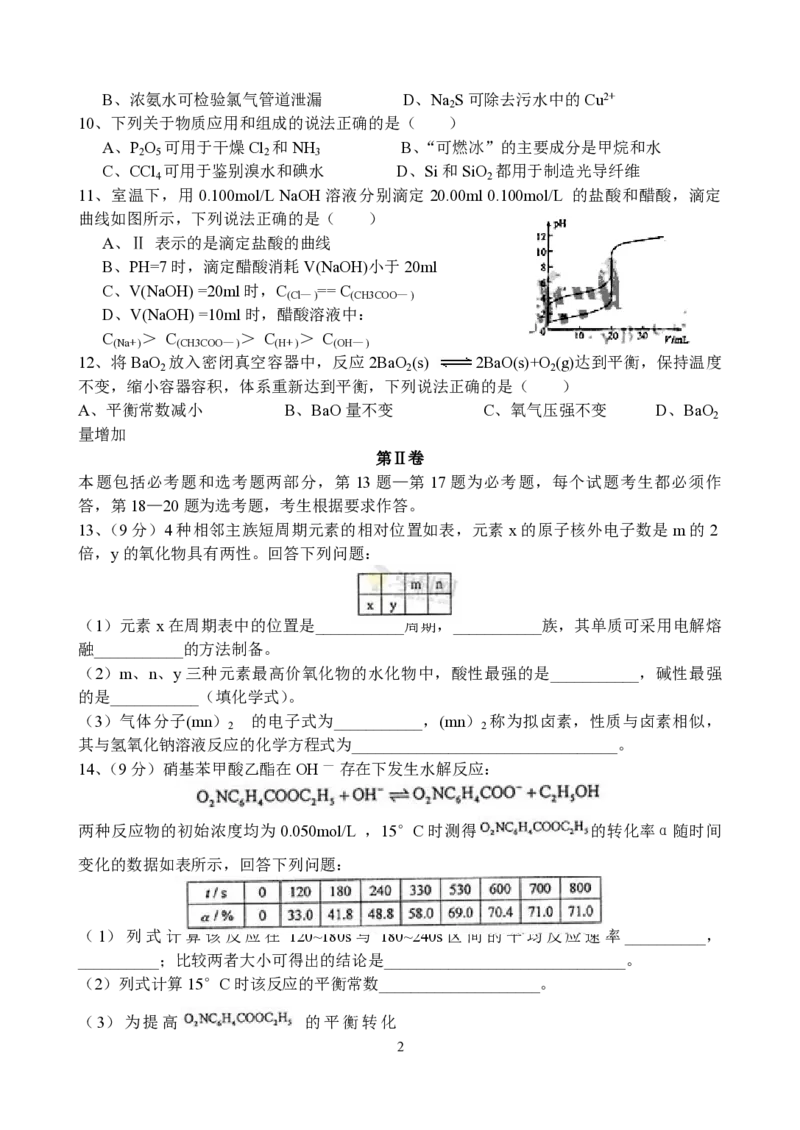
11、室温下,用 0.100mol/L NaOH溶液分别滴定 20.00ml 0.100mol/L 的盐酸和醋酸,滴定
曲线如图所示,下列说法正确的是( )
A、Ⅱ 表示的是滴定盐酸的曲线
B、PH=7时,滴定醋酸消耗V(NaOH)小于20ml
C、V(NaOH) =20ml时,C == C
(Cl— ) (CH3COO— )
D、V(NaOH) =10ml时,醋酸溶液中:
C > C > C > C
(Na+ ) (CH3COO— ) (H+ ) (OH— )
12、将BaO 放入密闭真空容器中,反应2BaO (s) 2BaO(s)+O (g)达到平衡,保持温度
2 2 2
不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )
A、平衡常数减小 B、BaO量不变 C、氧气压强不变 D、BaO
2
量增加
第Ⅱ卷
本题包括必考题和选考题两部分,第 13题—第 17题为必考题,每个试题考生都必须作
答,第18—20题为选考题,考生根据要求作答。
13、(9分)4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2
倍,y的氧化物具有两性。回答下列问题:
(1)元素x在周期表中的位置是___________周期,___________族,其单质可采用电解熔
融___________的方法制备。
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是___________,碱性最强
的是___________(填化学式)。
(3)气体分子(mn) 的电子式为___________,(mn) 称为拟卤素,性质与卤素相似,
2 2
其与氢氧化钠溶液反应的化学方程式为_________________________________。
14、(9分)硝基苯甲酸乙酯在OH — 存在下发生水解反应:
两种反应物的初始浓度均为0.050mol/L ,15°C时测得 的转化率α随时间
变化的数据如表所示,回答下列问题:
(1)列式计算该反应在 120~180s与 180~240s区间的平均反应速率__________,
__________;比较两者大小可得出的结论是______________________________。
(2)列式计算15°C时该反应的平衡常数____________________。
(3)为提高 的平衡转化
2率,除可适当控制反应温度外,还可以采取的措施有______________________________
(要求写出两条)。
15、(8分)卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多氯代甲烷常为有机溶剂,其分子结构为政四面体的是__________,工业上分离这些
多氯代物的方法是____________________。
(2)三氟氯溴乙烯(CF CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式
3
__________(不考虑立体异构)。
(3)聚氯乙烯是生活中常用的塑料,工业生产聚氯乙烯的一种工艺路线如下:
反应①的化学方程式为________________________________________,反应类型为
__________,反应②的反应类型为__________。
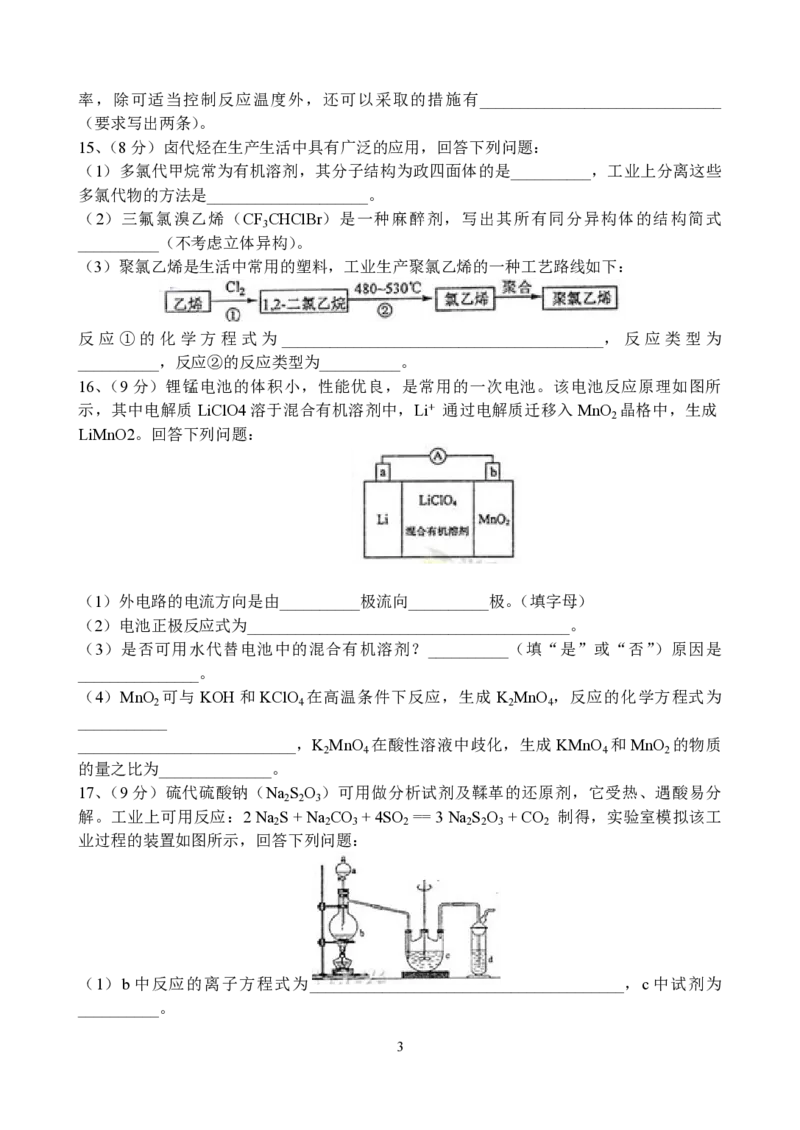
16、(9分)锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图所
示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO 晶格中,生成
2
LiMnO2。回答下列问题:
(1)外电路的电流方向是由__________极流向__________极。(填字母)
(2)电池正极反应式为________________________________________。
(3)是否可用水代替电池中的混合有机溶剂?__________(填“是”或“否”)原因是
_______________。
(4)MnO 可与 KOH和 KClO 在高温条件下反应,生成 K MnO ,反应的化学方程式为
2 4 2 4
___________
___________________________,K MnO 在酸性溶液中歧化,生成KMnO 和MnO 的物质
2 4 4 2
的量之比为______________。
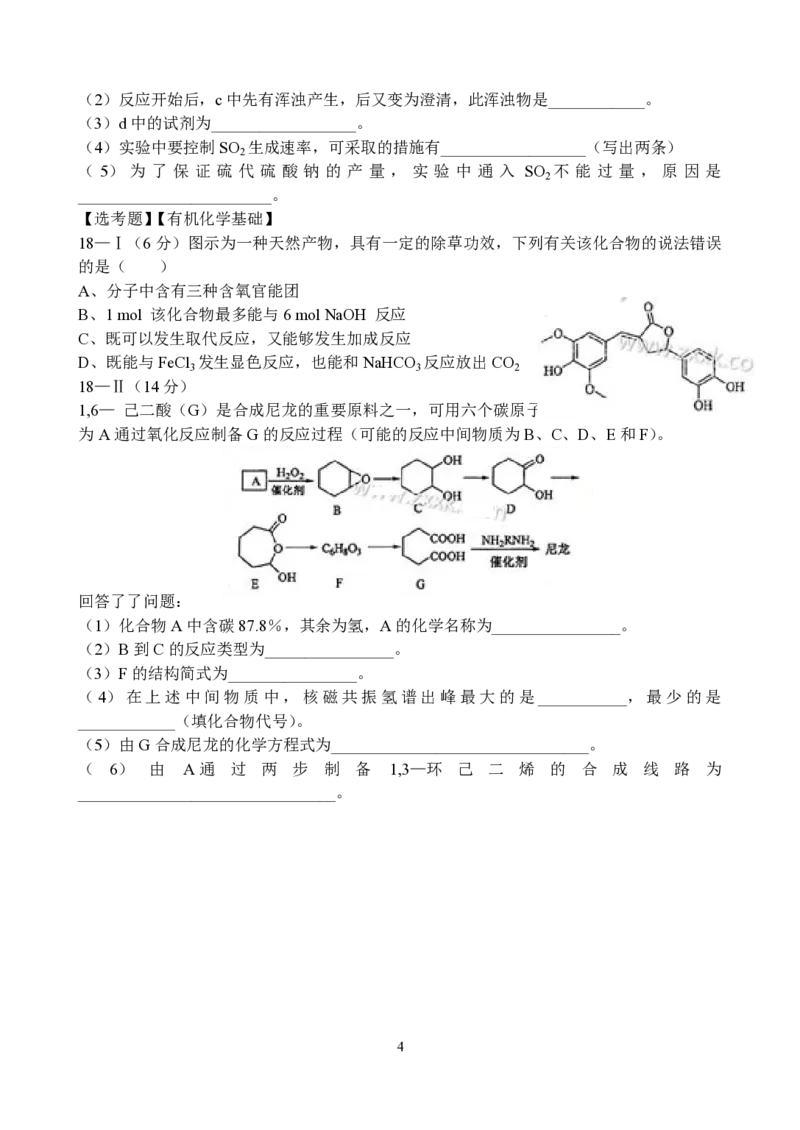
17、(9分)硫代硫酸钠(Na S O )可用做分析试剂及鞣革的还原剂,它受热、遇酸易分
2 2 3
解。工业上可用反应:2 Na S + Na CO + 4SO == 3 Na S O + CO 制得,实验室模拟该工
2 2 3 2 2 2 3 2
业过程的装置如图所示,回答下列问题:
(1)b中反应的离子方程式为_______________________________________,c中试剂为
__________。
3(2)反应开始后,c中先有浑浊产生,后又变为澄清,此浑浊物是____________。
(3)d中的试剂为__________________。
(4)实验中要控制SO 生成速率,可采取的措施有__________________(写出两条)
2
( 5) 为 了 保 证 硫 代 硫 酸 钠 的 产 量 , 实 验 中 通 入 SO 不 能 过 量 , 原 因 是
2
________________________。
【选考题】【有机化学基础】
18—Ⅰ(6分)图示为一种天然产物,具有一定的除草功效,下列有关该化合物的说法错误
的是( )
A、分子中含有三种含氧官能团
B、1 mol 该化合物最多能与6 mol NaOH 反应
C、既可以发生取代反应,又能够发生加成反应
D、既能与FeCl 发生显色反应,也能和NaHCO 反应放出CO
3 3 2
18—Ⅱ(14分)
1,6— 己二酸(G)是合成尼龙的重要原料之一,可用六个碳原子的化合物氧化制备。下图
为A通过氧化反应制备G的反应过程(可能的反应中间物质为B、C、D、E和F)。
回答了了问题:
(1)化合物A中含碳87.8%,其余为氢,A的化学名称为________________。
(2)B到C的反应类型为________________。
(3)F的结构简式为________________。
(4)在上述中间物质中,核磁共振氢谱出峰最大的是___________,最少的是
____________(填化合物代号)。
(5)由G合成尼龙的化学方程式为________________________________。
( 6) 由 A通 过 两 步 制 备 1,3—环 己 二 烯 的 合 成 线 路 为
________________________________。
4