文档内容
2014 年全国统一高考化学试卷(大纲版)
一、选择题:本大题共 8小题,每小题 6分.在每小题给出的四个选项总,只
有一项是符合题目要求的.
1.(6分)下列叙述正确的是( )
A.锥形瓶可用作加热的反应器
B.室温下,不能将浓硫酸盛放在铁桶中
C.配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高
D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低
2.(6分)N 表示阿伏伽德罗常数,下列叙述正确的是( )
A
A.1mol FeI 与足量氯气反应时转移的电子数为2N
2 A
B.2L 0.5mol•L﹣1硫酸钾溶液中阴离子所带电荷数为 N
A
C.1mol Na O 固体中含离子总数为4N
2 2 A
D.丙烯和环丙烷组成的42g混合气体中氢原子的个数为6N
A
3.(6分)下列叙述错误的是( )
A.SO 使溴水褪色与乙烯使KMnO 溶液褪色的原理相同
2 4
B.制备乙酸乙酯时可用热的NaOH 溶液收集产物以除去其中的乙酸
C.用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率
D.用AgNO 溶液可以鉴别KCl和KI
3
4.(6 分)如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍
电池(MH﹣Ni 电池),下列有关说法中不正确的是( )
A.放电时正极反应为:NiOOH+H O+e﹣→Ni(OH) +OH﹣
2 2
B.电池的电解液可为KOH 溶液
C.充电时负极反应为:MH+OH﹣→H O+M+e﹣
2
D.MH 是一类储氢材料,其氢密度越大,电池的能量密度越高
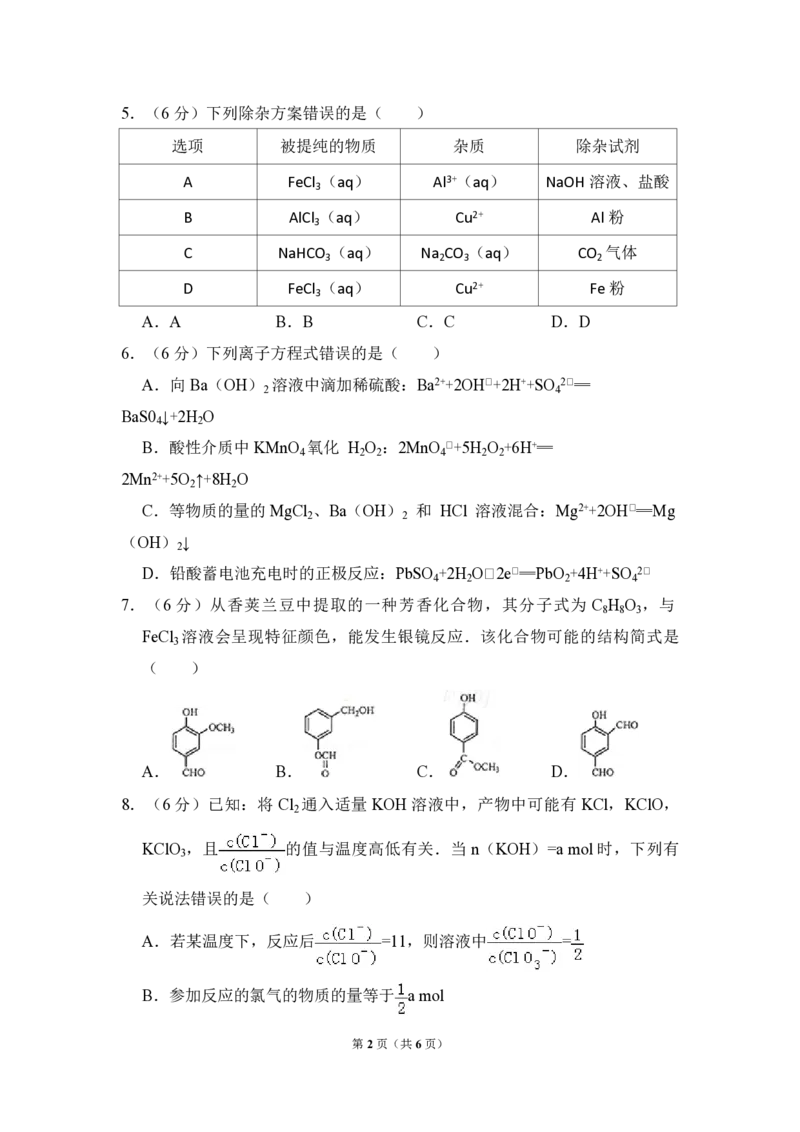
第1页(共6页)5.(6分)下列除杂方案错误的是( )
选项 被提纯的物质 杂质 除杂试剂
A FeCl (aq) Al3+(aq) NaOH溶液、盐酸
3
B AlCl (aq) Cu2+ Al 粉
3
C NaHCO (aq) Na CO (aq) CO 气体
3 2 3 2
D FeCl (aq) Cu2+ Fe粉
3
A.A B.B C.C D.D
6.(6分)下列离子方程式错误的是( )
A.向Ba(OH) 溶液中滴加稀硫酸:Ba2++2OH﹣+2H++SO 2﹣═
2 4
BaS0 ↓+2H O
4 2
B.酸性介质中KMnO 氧化 H O :2MnO ﹣+5H O +6H+═
4 2 2 4 2 2
2Mn2++5O ↑+8H O
2 2
C.等物质的量的MgCl 、Ba(OH) 和 HCl 溶液混合:Mg2++2OH﹣═Mg
2 2
(OH) ↓
2
D.铅酸蓄电池充电时的正极反应:PbSO +2H O﹣2e﹣═PbO +4H++SO 2﹣
4 2 2 4
7.(6分)从香荚兰豆中提取的一种芳香化合物,其分子式为 C H O ,与
8 8 3
FeCl 溶液会呈现特征颜色,能发生银镜反应.该化合物可能的结构简式是
3
( )
A. B. C. D.
8.(6 分)已知:将 Cl 通入适量 KOH 溶液中,产物中可能有 KCl,KClO,
2
KClO ,且 的值与温度高低有关.当 n(KOH)=a mol时,下列有
3
关说法错误的是( )
A.若某温度下,反应后 =11,则溶液中 =
B.参加反应的氯气的物质的量等于 a mol
第2页(共6页)C.改变温度,反应中转移电子的物质的量n 的范围: a mol≤n ≤ a mol
e e
D.改变温度,产物中KClO 的最大理论产量为 amol
3
二、非选择题
9.(15 分)A,B,D,E,F 为短周期元素,非金属元素 A 最外层电子数与其
周期数相同,B的最外层电子数是其所在周期数的 2倍.B在 D 中充分燃烧
能生成其最高价化合物 BD ,E+与 D2﹣具有相同的电子数.A 在 F 中燃烧,
2
产物溶于水得到一种强酸,回答下列问题;
(1)A 在周期表中的位置是 ,写出一种工业制备单质F 的离子方程式
(2)B,D,E组成的一种盐中,E的质量分数为 43%,其俗名为 ,其
水溶液与 F 单质反应的化学方程为 ,在产物总加入少量 KI,反应后
加入CCl 并震荡,有机层显 色.
4
(3)由这些元素组成的物质,其组成和结构信息如表:
物质 组成和结构信息
a 含有 A的二元离子化合物
b 含有非极性共价键的二元离子化合物,且原子数之比为 1:1
c 化学组成为BDF
2
d 只存在一种类型作用力且可导电的单质晶体
a的化学式 ;b的化学式为 ;c的电子式为 ;d的晶体类
型是
(4)有 A 和 B、D 元素组成的两种二元化合物形成一类新能源物质.一种化
合物分子通过 键构成具有空腔的固体;另一种化合物(沼气的主要
成分)分子进入该空腔,其分子的空间结构为 .
10.(15分)化合物 AX 和单质 X 在一定条件下反应可生成化合物 AX .回
3 2 5
答下列问题;
(1)已知 AX 的熔点和沸点分别为﹣93.6℃和 76℃,AX 的熔点为 167℃,室
3 5
温时,AX 与气体 X 反应生成 1mol AX ,放出热量 123.8kJ.该反应的热化
3 2 5
第3页(共6页)学方程是为 .
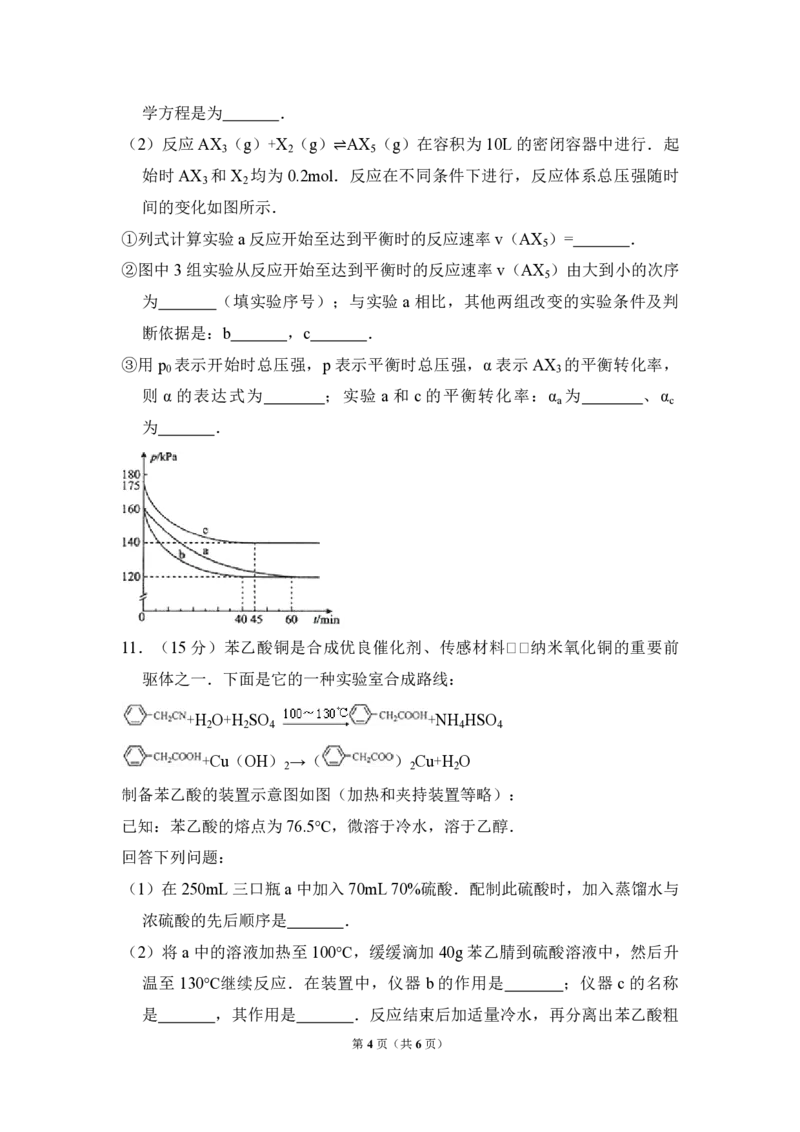
(2)反应 AX (g)+X (g)⇌AX (g)在容积为 10L的密闭容器中进行.起
3 2 5
始时 AX 和 X 均为 0.2mol.反应在不同条件下进行,反应体系总压强随时
3 2
间的变化如图所示.
①列式计算实验a反应开始至达到平衡时的反应速率v(AX )= .
5
②图中 3组实验从反应开始至达到平衡时的反应速率 v(AX )由大到小的次序
5
为 (填实验序号);与实验 a相比,其他两组改变的实验条件及判
断依据是:b ,c .
③用 p 表示开始时总压强,p表示平衡时总压强,α表示 AX 的平衡转化率,
0 3
则 α的表达式为 ;实验 a和 c的平衡转化率:α 为 、α
a c
为 .
11.(15分)苯乙酸铜是合成优良催化剂、传感材料﹣﹣纳米氧化铜的重要前
驱体之一.下面是它的一种实验室合成路线:
+H O+H SO +NH HSO
2 2 4 4 4
+Cu(OH) →( ) Cu+H O
2 2 2
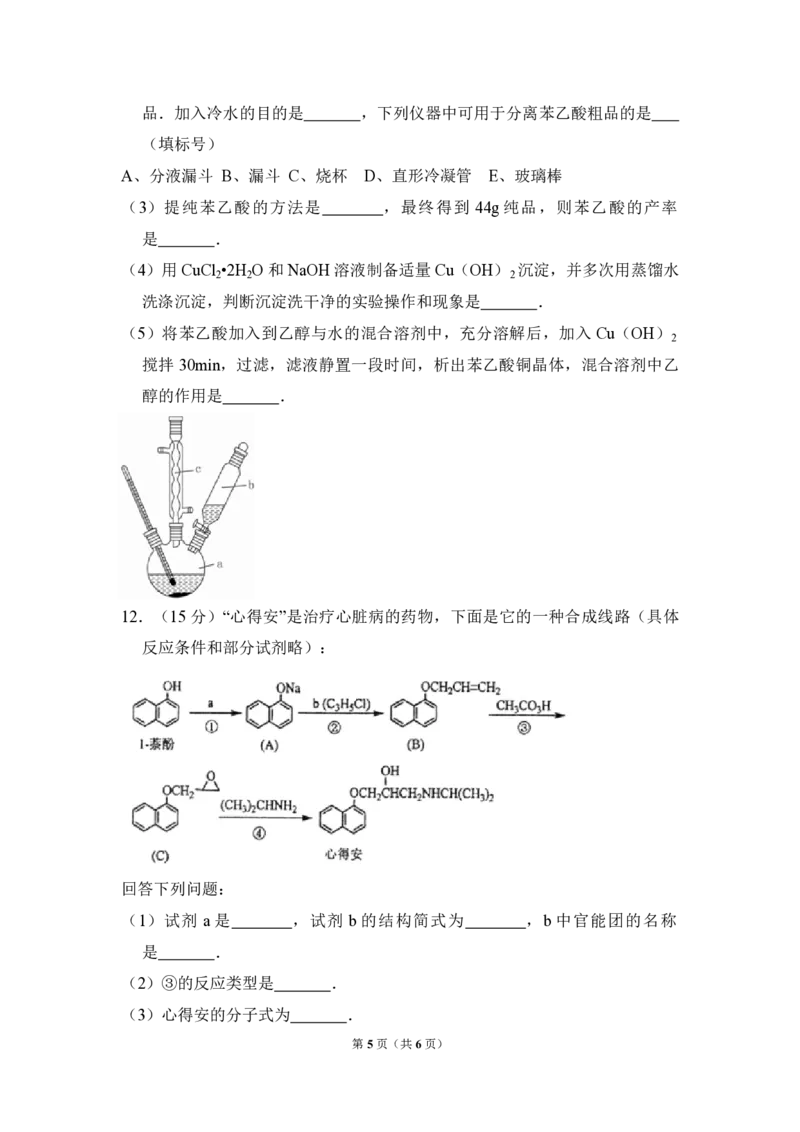
制备苯乙酸的装置示意图如图(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇.
回答下列问题:
(1)在 250mL三口瓶 a中加入 70mL 70%硫酸.配制此硫酸时,加入蒸馏水与
浓硫酸的先后顺序是 .
(2)将 a中的溶液加热至 100℃,缓缓滴加 40g 苯乙腈到硫酸溶液中,然后升
温至 130℃继续反应.在装置中,仪器 b的作用是 ;仪器 c的名称
是 ,其作用是 .反应结束后加适量冷水,再分离出苯乙酸粗
第4页(共6页)品.加入冷水的目的是 ,下列仪器中可用于分离苯乙酸粗品的是
(填标号)
A、分液漏斗 B、漏斗 C、烧杯 D、直形冷凝管 E、玻璃棒
(3)提纯苯乙酸的方法是 ,最终得到 44g纯品,则苯乙酸的产率
是 .
(4)用 CuCl •2H O 和 NaOH 溶液制备适量 Cu(OH) 沉淀,并多次用蒸馏水
2 2 2
洗涤沉淀,判断沉淀洗干净的实验操作和现象是 .
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入 Cu(OH)
2
搅拌 30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙
醇的作用是 .
12.(15分)“心得安”是治疗心脏病的药物,下面是它的一种合成线路(具体
反应条件和部分试剂略):
回答下列问题:
(1)试剂 a是 ,试剂 b的结构简式为 ,b中官能团的名称
是 .
(2)③的反应类型是 .
(3)心得安的分子式为 .
第5页(共6页)(4)试剂b可由丙烷经三步反应合成:
C H X Y 试剂b
3 8
反应1的试剂与条件为 .
反应2的化学反应方程为 .
反应3的反应类型是 .
(5)芳香化合物 D 是 1﹣萘酚的同分异构体,其分子中有两个官能团,能发生
银镜反应,D 能被 KMnO 酸性溶液氧化成 E(C H O )和芳香化合物 F
4 2 4 2
(C H O ),E和 F 与碳酸氢钠溶液反应均能放出 CO 气体,F 芳环上的一
8 6 4 2
硝化产物只有一种,D 的结构简式为 ;由 F 生成的一硝化产物的化
学方程式为 该产物的名称是 .
第6页(共6页)