文档内容
2016年天津市高考化学试卷
一、选择题(共6小题,每小题6分,满分36分)
1.(6分)根据所给信息和标志,判断下列说法错误的是( )
A B C D
《神农本草经》记 碳酸氢钠药片
载,麻黄能“止咳逆
上气”
古代中国人已用麻黄 该药是抗酸药,服用 看到有该标志的丢弃 贴有该标志的物品是
治疗咳嗽 时喝些醋能提高药效 物,应远离并报警 可回收物
A.A B.B C.C D.D
2.(6分)下列对氨基酸和蛋白质的描述正确的是( )
A.蛋白质水解的最终产物是氨基酸
B.氨基酸和蛋白质遇重金属离子均会变性
C. ﹣氨基丙酸与 ﹣氨基苯丙酸混合物脱水成肽,只生成2种二肽
D.α氨基酸溶于过量α氢氧化钠溶液中生成的离子,在电场作用下向负极移动
3.(6分)下列叙述正确的是( )
A.使用催化剂能够降低化学反应的反应热(△H)
B.金属发生吸氧腐蚀时,被腐蚀的速率与氧气浓度无关
C.原电池中发生的反应达平衡时,该电池仍有电流产生
D.在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小
4.(6分)下列实验的反应原理用离子方程式表示正确的是( )
A.室温下,测得氯化铵溶液pH<7,证明一水合氨是碱:NH +
4
+2H O═NH •H O+H O+
2 3 2 3
B.用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH﹣+2H O═2AlO ﹣+3H ↑
2 2 2
C.用碳酸氢钠溶液检验水杨酸中的羧基: +2HCO ﹣→
3
+2H O+2CO ↑
2 2
D.用高锰酸钾标准溶液滴定草酸:2MnO ﹣+16H++5C O 2﹣═2Mn2++10CO ↑+8H O
4 2 4 2 2
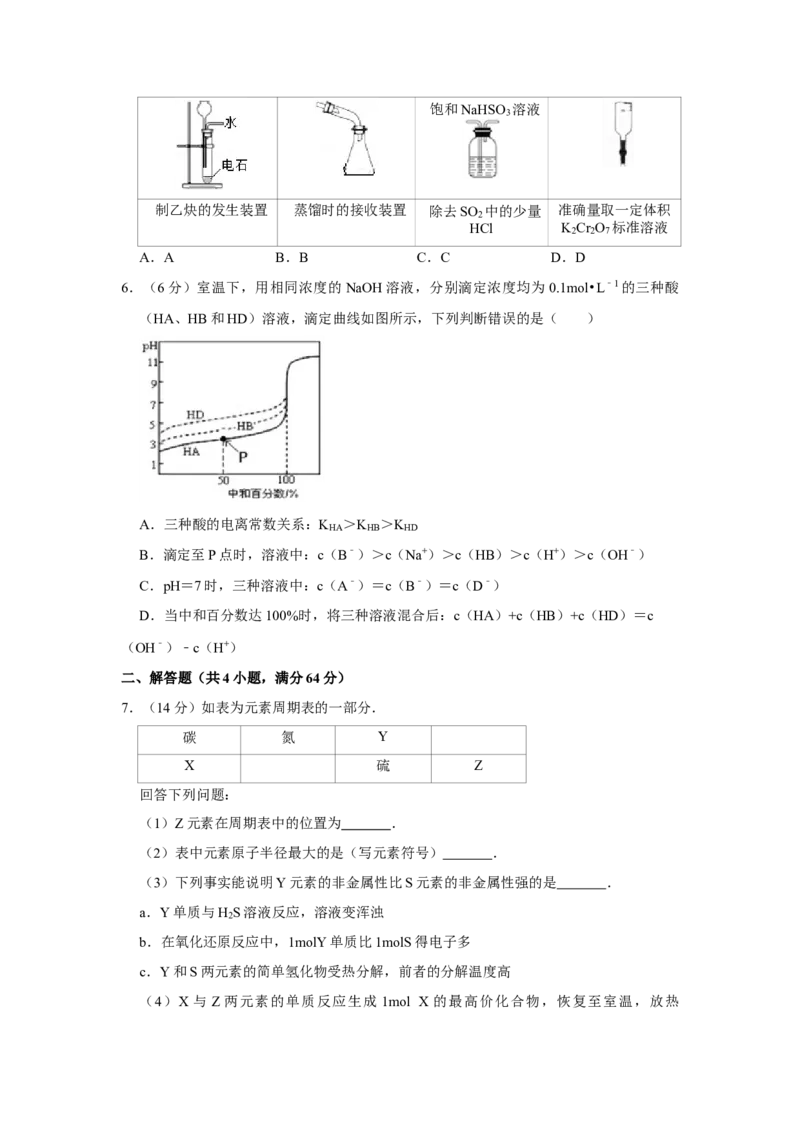
5.(6分)下列选用的仪器和药品能达到实验目的是( )
A B C D饱和NaHSO 溶液
3
制乙炔的发生装置 蒸馏时的接收装置 除去SO 中的少量 准确量取一定体积
2
HCl K Cr O 标准溶液
2 2 7
A.A B.B C.C D.D
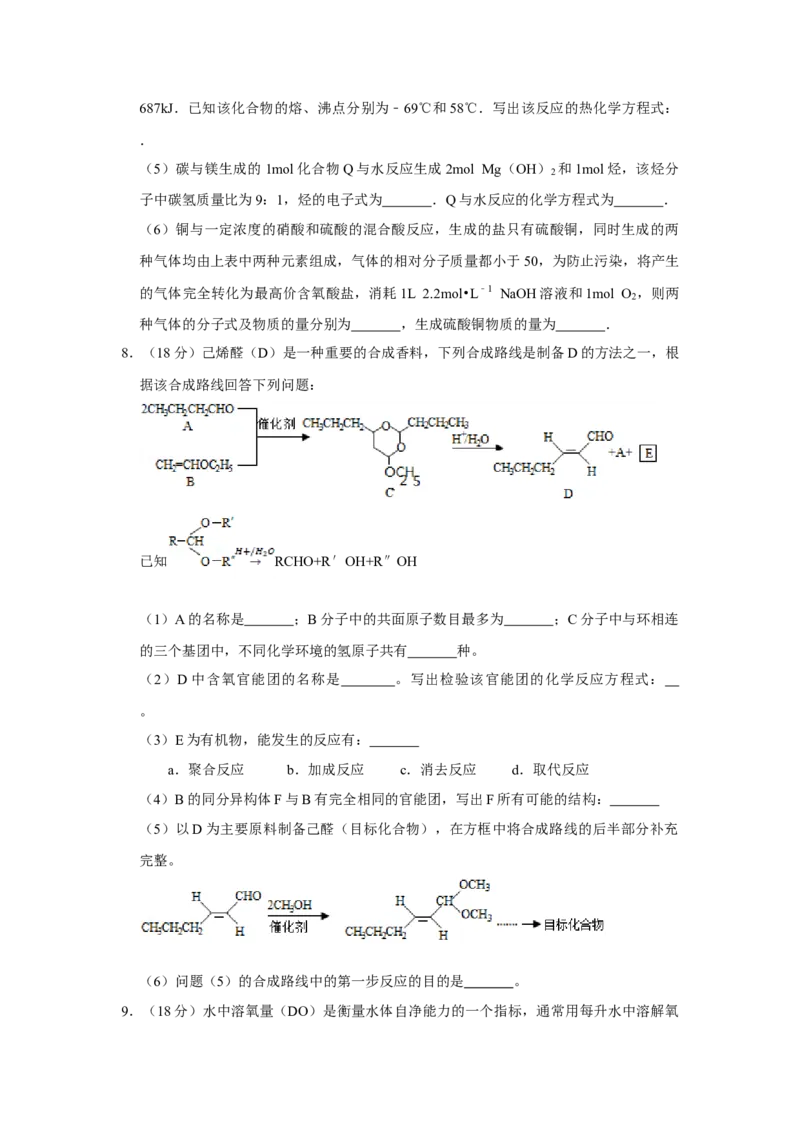
6.(6分)室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L﹣1的三种酸
(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( )
A.三种酸的电离常数关系:K >K >K
HA HB HD
B.滴定至P点时,溶液中:c(B﹣)>c(Na+)>c(HB)>c(H+)>c(OH﹣)
C.pH=7时,三种溶液中:c(A﹣)=c(B﹣)=c(D﹣)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c
(OH﹣)﹣c(H+)
二、解答题(共4小题,满分64分)
7.(14分)如表为元素周期表的一部分.
碳 氮 Y
X 硫 Z
回答下列问题:
(1)Z元素在周期表中的位置为 .
(2)表中元素原子半径最大的是(写元素符号) .
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是 .
a.Y单质与H S溶液反应,溶液变浑浊
2
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X 与 Z 两元素的单质反应生成 1mol X 的最高价化合物,恢复至室温,放热687kJ.已知该化合物的熔、沸点分别为﹣69℃和58℃.写出该反应的热化学方程式:
.
(5)碳与镁生成的1mol化合物Q与水反应生成2mol Mg(OH) 和1mol烃,该烃分
2
子中碳氢质量比为9:1,烃的电子式为 .Q与水反应的化学方程式为 .
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两
种气体均由上表中两种元素组成,气体的相对分子质量都小于50,为防止污染,将产生
的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol•L﹣1 NaOH溶液和1mol O ,则两
2
种气体的分子式及物质的量分别为 ,生成硫酸铜物质的量为 .
8.(18分)己烯醛(D)是一种重要的合成香料,下列合成路线是制备D的方法之一,根
据该合成路线回答下列问题:
已知 RCHO+R′OH+R″OH
(1)A的名称是 ;B分子中的共面原子数目最多为 ;C分子中与环相连
的三个基团中,不同化学环境的氢原子共有 种。
(2)D中含氧官能团的名称是 。写出检验该官能团的化学反应方程式:
。
(3)E为有机物,能发生的反应有:
a.聚合反应 b.加成反应 c.消去反应 d.取代反应
(4)B的同分异构体F与B有完全相同的官能团,写出F所有可能的结构:
(5)以D为主要原料制备己醛(目标化合物),在方框中将合成路线的后半部分补充
完整。
(6)问题(5)的合成路线中的第一步反应的目的是 。
9.(18分)水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg•L﹣1.我国《地表水环境质量标准》规定,生活饮用水源的
DO不能低于5mg•L﹣1.某化学小组同学设计了下列装置(夹持装置略),测定某河水
的DO.
Ⅰ.测定原理:
碱性条件下,O 将Mn2+氧化为MnO(OH) : 2Mn2++O +4OH﹣═2MnO(OH) ↓
2 2 2 2
酸性条件下,MnO(OH) 将I﹣氧化为I : M①nO(OH) +I﹣+H+→Mn2++I +H O(未
2 2 2 2 2
配平) ②
用Na S O 标准溶液滴定生成的I ; 2S O 2﹣+I ═S O 2﹣+2I﹣
2 2 3 2 2 3 2 4 6
Ⅱ.测定步骤: ③
a.安装装置,检验气密性,充N 排尽空气后,停止充N .
2 2
b.向烧瓶中加入200mL水样.
c.向烧瓶中依次迅速加入1mL MnSO 无氧溶液(过量)、2mL碱性KI无氧溶液(过
4
量)开启搅拌器,至反应 完全.
d.搅拌并向烧瓶中加入2①mL H
2
SO
4
无氧溶液,至反应 完全,溶液为中性或弱酸性.
e.从烧瓶中取出40.00mL溶液,以淀粉作指示剂,用②0.01000mol•L﹣1 Na S O 溶液进
2 2 3
行滴定,记录数据.f…
g.处理数据(忽略氧气从水样中的逸出量和加入试剂后水样体积的变化).
回答下列问题:
(1)配制以上无氧溶液时,除去所用溶剂水中氧的简单操作为 .
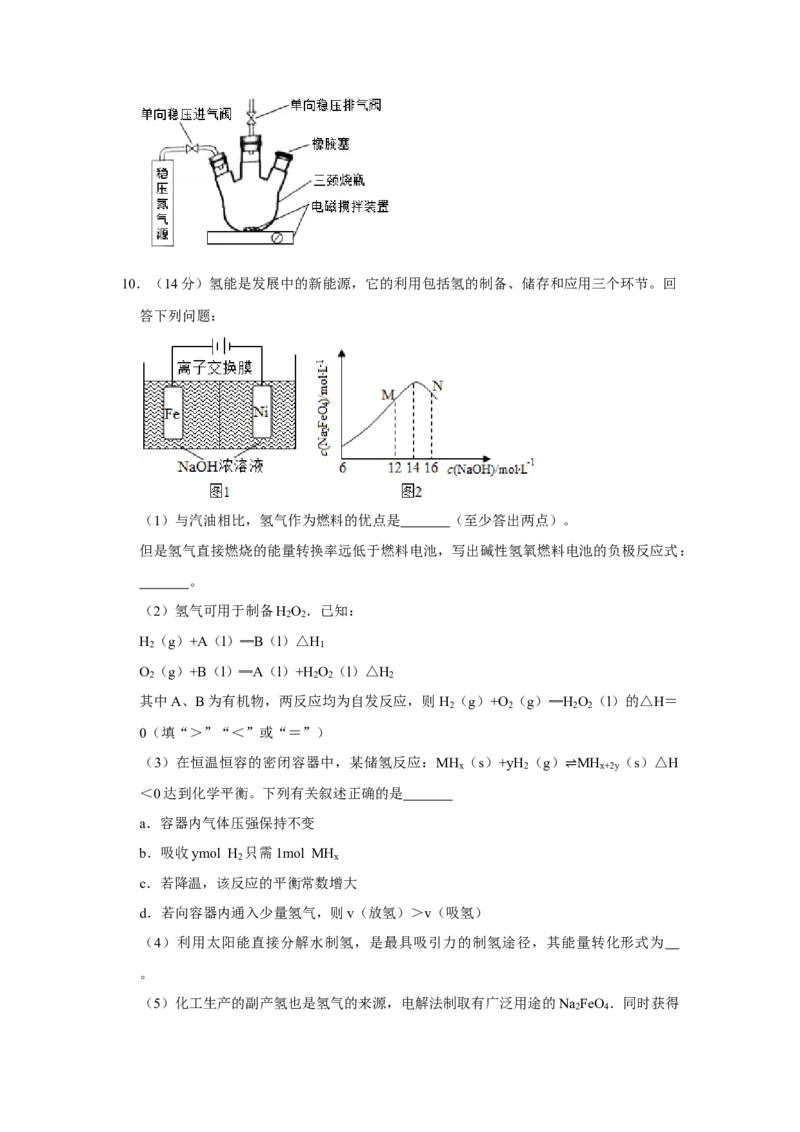
(2)在橡胶塞处加入水样及有关试剂应选择的仪器是 .
滴定管 注射器 量筒
①(3)搅拌的作用②是 .③
(4)配平反应 的方程式,其化学计量数依次为 .
(5)步骤f为 ② .
(6)步骤e中达到滴定终点的标志为 .若某次滴定消耗Na S O 溶液4.50mL,
2 2 3
水样的DO= mg•L﹣1(保留一位小数).作为饮用水源,此次测得DO是否达
标: (填“是”或“否”)
(7)步骤d中加入H SO 溶液反应后,若溶液pH过低,滴定时会产生明显的误差,写
2 4
出产生此误差的原因(用离子方程式表示,至少写出2个) .10.(14分)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回
答下列问题:
(1)与汽油相比,氢气作为燃料的优点是 (至少答出两点)。
但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:
。
(2)氢气可用于制备H O .已知:
2 2
H (g)+A(l)═B(l)△H
2 1
O (g)+B(l)═A(l)+H O (l)△H
2 2 2 2
其中A、B为有机物,两反应均为自发反应,则H (g)+O (g)═H O (l)的△H=
2 2 2 2
0(填“>”“<”或“=”)
(3)在恒温恒容的密闭容器中,某储氢反应:MH (s)+yH (g) MH (s)△H
x 2 x+2y
<0达到化学平衡。下列有关叙述正确的是 ⇌
a.容器内气体压强保持不变
b.吸收ymol H 只需1mol MH
2 x
c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
。
(5)化工生产的副产氢也是氢气的来源,电解法制取有广泛用途的Na FeO .同时获得
2 4氢气:Fe+2H O+2OH﹣→FeO 2﹣+3H ↑,装置如图所示,装置通电后,铁电极附近生成
2 4 2
紫红色FeO 2﹣,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色
4
物质。已知:Na FeO 只在强碱性条件下稳定,易被H 还原。
2 4 2
电解一段时间后,c(OH﹣)降低的区域在 (填“阴极室”或“阳极室”)。
①电解过程中,须将阴极产生的气体及时排出,其原因为 。
②c(Na
2
FeO
4
)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c
③(Na FeO )低于最高值的原因 。
2 4