文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 10 化学式与化学用语
(试题分值:50分 测试时间:30分钟)
一、选择题(本题包括15小题,每小题2分,共30分.每小题只有一个正确答案)
1、【原创题】下列粒子结构示意图中,属于稀有气体的原子的是
A. +B. C. D.
【答案】A
【解析】A、质子数=核外电子数,表示原子,质子数=原子序数,10号元素是氖元素,属于稀有气体元素,
符合题意;
B、质子数=核外电子数,表示原子,质子数=原子序数,8号元素是氧元素,不属于稀有气体元素,不符
合题意;
C、质子数大于核外电子数,表示阳离子,不符合题意;
D、质子数=核外电子数,表示原子,质子数=原子序数,12号元素是镁元素,属于金属元素,不符合题意。
故选A。
2、【原创题】下列粒子结构示意图中,表示阴离子的是
A. B. C. D.
【答案】C
【解析】质子数=核外电子数,为原子;质子数>核外电子数,为阳离子;质子数<核外电子数,为阴离子。
A、质子数=4,核外电子数=4,质子数=核外电子数,为原子,故不符合题意;
B、质子数=11,核外电子数=11,质子数=核外电子数,为原子,故不符合题意;
C、质子数=16,核外电子数=18,质子数<核外电子数,为阴离子,故符合题意;
D、质子数=18,核外电子数=18,质子数=核外电子数,为原子,故不符合题意。故选:C。
【新考法】与科研成果相结合
3、2007年,中国计量科学院研制成功“铯原子钟”,其理论精度为600万年误差小于1秒。如图所示,
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
为铯在元素周期表中的信息。下列叙述中正确的是
A.一个铯原子内含有55个质子 B.一个铯原子内含有55个中子
C.一个铯原子带55个单位的正电荷 D.一个铯原子的质量为132.9千克
【答案】A
【解析】元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的
汉字表示元素名称,下边是元素的相对原子质量。
A、原子中质子数=原子序数;一个铯原子内含有55个质子,正确;
B、没有信息体现一个铯原子内中子数目,错误;
C、原子中质子数=核外电子数,原子核带的正电荷与电子所带的负电荷电性相反、电量相等,相互抵消,
不显电性,错误;
D一个铯原子的相对质量为132.9,错误。故选A。
【新考法】与催化原理相结合
4、NH 的合成开启了工业催化新纪元,为世界粮食增产做出了巨大贡献。以N 和H 为反应物合成NH 的
3 2 2 3
微观过程如下:
下列说法正确的是
A. 表示氢气分子 B.过程中有“NH”“NH ”原子团生成
2
C.参加反应的H 与生成的NH 个数比为2:3 D.反应结束后催化剂的质量增加
2 3
【答案】B
【解析】A、氮气和氢气生成氨气,由微观示意图图可知 表示氮气,错误;
B、由微观示意图可知,过程中有“ ”、“ ”生成即有“NH”、 “NH ”原子团生成,正确;
2
C、由微观示意图可知,参加反应的H 与生成的NH 个数比为3:2,C错误;
2 3
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、根据催化剂概念可知,催化剂反应前后质量不变,D错误。故选:B。
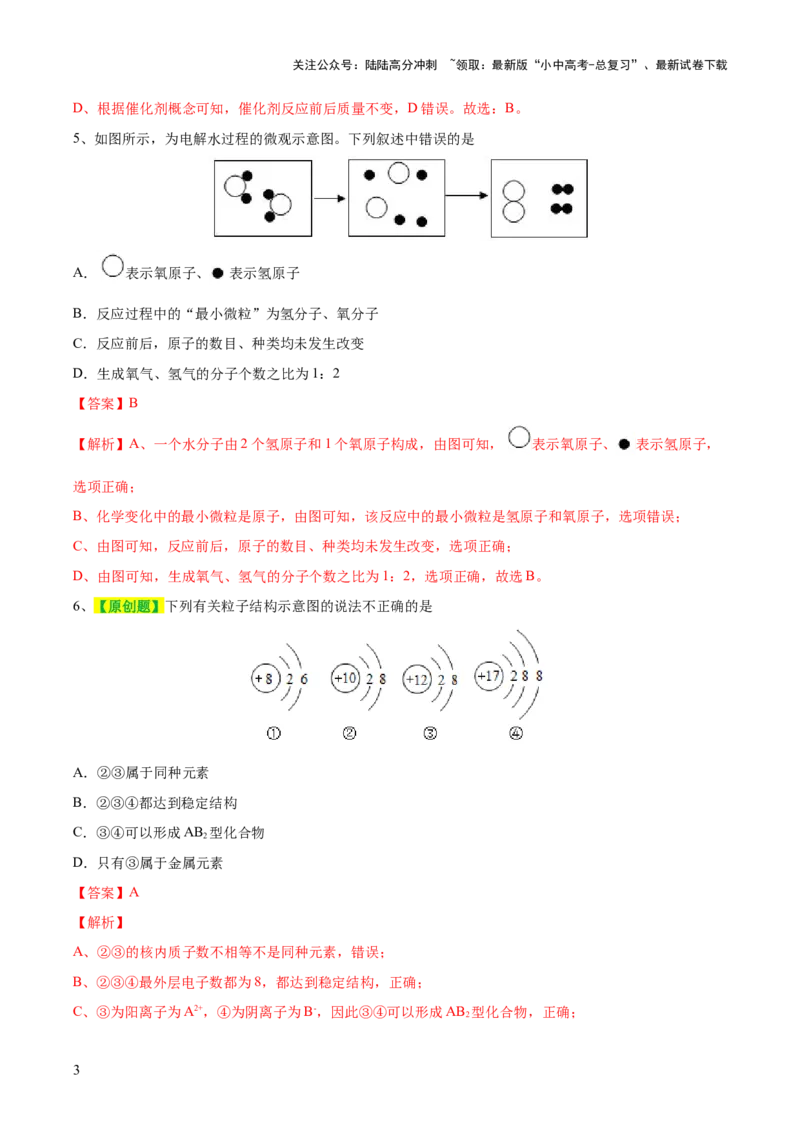
5、如图所示,为电解水过程的微观示意图。下列叙述中错误的是
A. 表示氧原子、 表示氢原子
B.反应过程中的“最小微粒”为氢分子、氧分子
C.反应前后,原子的数目、种类均未发生改变
D.生成氧气、氢气的分子个数之比为1:2
【答案】B
【解析】A、一个水分子由2个氢原子和1个氧原子构成,由图可知, 表示氧原子、 表示氢原子,
选项正确;
B、化学变化中的最小微粒是原子,由图可知,该反应中的最小微粒是氢原子和氧原子,选项错误;
C、由图可知,反应前后,原子的数目、种类均未发生改变,选项正确;
D、由图可知,生成氧气、氢气的分子个数之比为1:2,选项正确,故选B。
6、【原创题】下列有关粒子结构示意图的说法不正确的是
A.②③属于同种元素
B.②③④都达到稳定结构
C.③④可以形成AB 型化合物
2
D.只有③属于金属元素
【答案】A
【解析】
A、②③的核内质子数不相等不是同种元素,错误;
B、②③④最外层电子数都为8,都达到稳定结构,正确;
C、③为阳离子为A2+,④为阴离子为B-,因此③④可以形成AB 型化合物,正确;
2
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、①质子数为8为氧元素;②质子数为10为氖元素;③质子数为12为镁元素;④质子数为17为氯元素,
只有③属于金属元素,正确;故选A。
【新考法】与守恒思想相结合
7、某工业盐酸中因含有少量FeCl (不含其它杂质)而显黄色,测知该盐酸中H+和Cl-的个数比为88:97,则
3
其中Fe3+和Cl-的个数比为
A.1:9 B.1:3 C.3:1 D.3:97
【答案】D
【解析】
溶液呈电中性,即阳离子所带的的正电荷总数等于银离子所带的负电荷总数。氢离子和氯离子个数比为
88∶97,假设氢离子个数为88,则氯离子个数为97,铁离子个数=(97-88)÷3=3,则其中Fe3+和Cl-的个
数比为3∶97,故选D。
8、丙氨酸(C HON)是一种常见的氨基酸。下列叙述正确的是
3 7 2
A.丙氨酸属于有机小分子化合物
B.丙氨酸是一种蛋白质
C.每个丙氨酸分子中含有1个氧分子
D.丙氨酸中碳、氮元素的质量比为3:1
【答案】A
【解析】
A、丙氨酸(C HON)是一种含碳元素的化合物,属于有机小分子化合物,选项A正确;
3 7 2
B、丙氨酸是一种常见的氨基酸,氨基酸是蛋白质的基本组成单位,不是蛋白质,选项B错误;
C、分子是由原子构成的,每个丙氨酸分子中含有2个氧原子,不含氧分子,选项C错误;
D、丙氨酸中碳、氮元素的质量比为(12×3):(1×14)=18:7,选项D错误;故选:A。
9、【原创题】以二氧化碳和氨气合成尿素是固定和利用二氧化碳的成功范例,反应的化学方程式是
CO+2NH CO(NH)+X,下列说法正确的是
2 3 2 2
A.氧是空气中含量最多的元素
B.物质X的化学式为H
2
C.NH 中氮元素的化合价是-3
3
D.尿素属于无机化合物
【答案】C
【解析】
A、氮是空气中含量最多的元素,故A不正确;
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B、根据化学方程式可知,反应前有1个碳原子,2个氧原子,2个氮原子,6个氢原子,反应后有1个碳
原子,1个氧原子,2个氮原子,4个氢原子,则X是HO,故B不正确;
2
C、NH 中氢元素的化合价为+1价,设氮元素的化合价是x,化合物中各元素的正负化合价代数和为零,
3
则x+(+1)×3=0,x=-3,则氮元素的化合价是-3,故C正确;
D、尿素是含碳元素的化合物,属于有机化合物,故D不正确。故选C。
10、对下列化学用语中数字“2”含义的说法正确的是
①2H ②2NH 3 ③SO 2 ④C + u 2 O ⑤Mg2+ ⑥2OH- ⑦H 2 O
A.表示离子个数的是⑤⑥ B.表示分子中原子个数的是③⑦
C.表示离子所带电荷数的是④⑤ D.表示分子个数的是①②
【答案】B
【解析】
①2H:2个氢原子。
②2NH :2个氨气分子。
3
③SO :每个二氧化硫分子中含有两个氧原子。
2
+ 2
④CuO:氧化铜中铜元素显+2价。
⑤Mg2+ :每个镁离子带两个单位正电荷。
⑥2OH-:2个氢氧根离子。
⑦HO:每个水分子中含有两个氢原子。
2
A.表示离子个数的是⑤,选项说法错误。
B.表示分子中原子个数的是③⑦,选项说法正确
C.表示离子所带电荷数的是⑤,选项说法错误。
D.表示分子个数的是②,选项说法错误。故选:B
11.化学用语是学习化学的重要工具。下列用语使用或书写正确的是
A.两个亚铁离子:2Fe3+ B.乙醇:C HO
2 6
C.H:2个氢原子 D.氨气NH 中氮元素化合价是+3
2 3
【答案】B
【解析】
A、两个亚铁离子:2Fe2+,A错误。
B、乙醇:C HO,B正确。
2 6
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C、H:1个氢分子,2个氢原子:2H,C错误。
2
D、氢元素+1价,根据化合价代数和为零,氨气NH 中氮元素化合价是-3价,D错误。故选:B。
3
12.下列化学用语书写正确的是
A.4个N原子—2N B.铁离子—Fe2+
2
C.硫酸铝—AlSO D.钠离子的结构示意图—
4
【答案】D
【解析】
A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数
字,故4个N原子可表示为4N,故选项说法不正确;
B、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正
负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,故铁离
子可表示为Fe3+,故选项说法不正确;
C、硫酸铝中铝元素化合价为+3价,硫酸根的化合价为-2价,所以硫酸铝的化学式为Al (SO ),故选项说
2 4 3
法不正确;
D、钠离子是钠原子失去1个电子形成的的,钠离子的质子数为11,核外电子数为10,核外电子排布为
2、8,所以钠离子的结构示意图为 ,故选项说法正确。故选D。
13、【原创题】学习化学要熟练掌握化学用语。下列叙述正确的是
A.保持一氧化碳化学性质的最小微粒是C、O
B.二氧化硫和水反应生成的酸是HSO
2 4
C.过氧化氢中氧元素的化合价为2价
D.化肥氯化铵是由NH +和C1-构成的盐
4
【答案】D
【解析】
A、分子是保持物质化学性质的最小微粒,故保持一氧化碳化学性质的最小微粒是CO,故选项错误;
B、二氧化硫和水反应生成的酸是HSO ,不是HSO ,故选项错误;
2 3 2 4
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C、过氧化氢中氢元素的化合价为+1,根据化合物中化合价的代数和为零,则氧元素的化合价为-1,故
选项错误;
D、化肥氯化铵是由NH+和C1-构成的盐,故选项正确。故选:D。
14、有机物A含有C、 H、O三种元素,取该有机物14.8g和16.2gO 在密闭容器中燃烧,产物为CO,
2
CO 和水蒸气,把产物依次通过浓硫酸,灼热的氧化铜和碱石灰(主要成分是氢氧化钠和氧化钙的固体混
2
合物),结果浓硫酸增重18g,CuO的质量减轻9.6g,碱石灰的质量增重35.2g,试通过计算该有机物的化
学式是
A. C HO B. C H O C. C H O D. C H O
2 6 12 22 11 4 10 6 12 6
【答案】C
【解析】浓硫酸增重的质量即为生成的水的质量为 18g,故 14.8g 该有机物中含有氢元素的质量为
18g××100%=2g。碱石灰增加的质量35.2g为两部分二氧化碳的质量,一部分是一氧化碳还原氧化铜生成
的二氧化碳,另一部分是有机物燃烧时生成的二氧化碳。但根据质量守恒定律可知,其中的碳元素均来自
于有机物,故14.8g该有机物中含有的碳元素的质量为35.2g××100%=9.6g。故14.8g该有机物中含有的氧
元素的质量为14.8g−9.6g−2g=3.2g。故该有机物中碳、氢、氧原子的个数比为:::=4:10:1,故该有机物的化
学式为C H O,即选C。
4 10
15、将0.72g草酸亚铁(FeC O)放在一个可称量的敞口容器中高温焙烧,500~600℃时,容器中的固体
2 4
质量保持0.4g不变。所得物质的化学式为
A.Fe B.FeO C.Fe O D.Fe O
2 3 3 4
【答案】C
【解析】0.72g草酸亚铁中含铁元素的质量为0.72g××100%=0.28g,而反应后固体质量为0.4g,不可能是
铁单质,结合选项可知,应为铁的氧化物,铁元素和氧元素的质量比为0.28g:(0.4g﹣0.28g)=7:3,
设铁的氧化物的化学式为Fe O ,56x:16y=7:3,则x:y=2:3,故所得物质的化学式为Fe O 故选
x y 2 3,
C。
二、填空题(本题3小题,每空1分,共20分)
16、(4分)用化学符号表示:
(1)水银______________ (2)2个钠离子_____________
(3)人体缺少___________元素会导致甲状腺疾病。 (4)最常用的溶剂_____________
【答案】(1)Hg (2)2Na+ (3)I (4)HO
2
【解析】
(1)水银是金属,可用元素符号表示其化学式,水银化学式为Hg;
(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正
负符号在后,带1个电荷时,1要省略。表示多个该离子,就在其元素符号前加上相应的数字,故2个钠
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
离子可表示为:2Na+;
(3)人体缺少碘元素会导致甲状腺疾病,碘元素的元素符号为:I;
(4)最常用的溶剂是水,水的化学式为HO。
2
17、【新考法】与离子反应相结合
(7分)宏观辨识与微观探析是化学学科的核心素养之一、
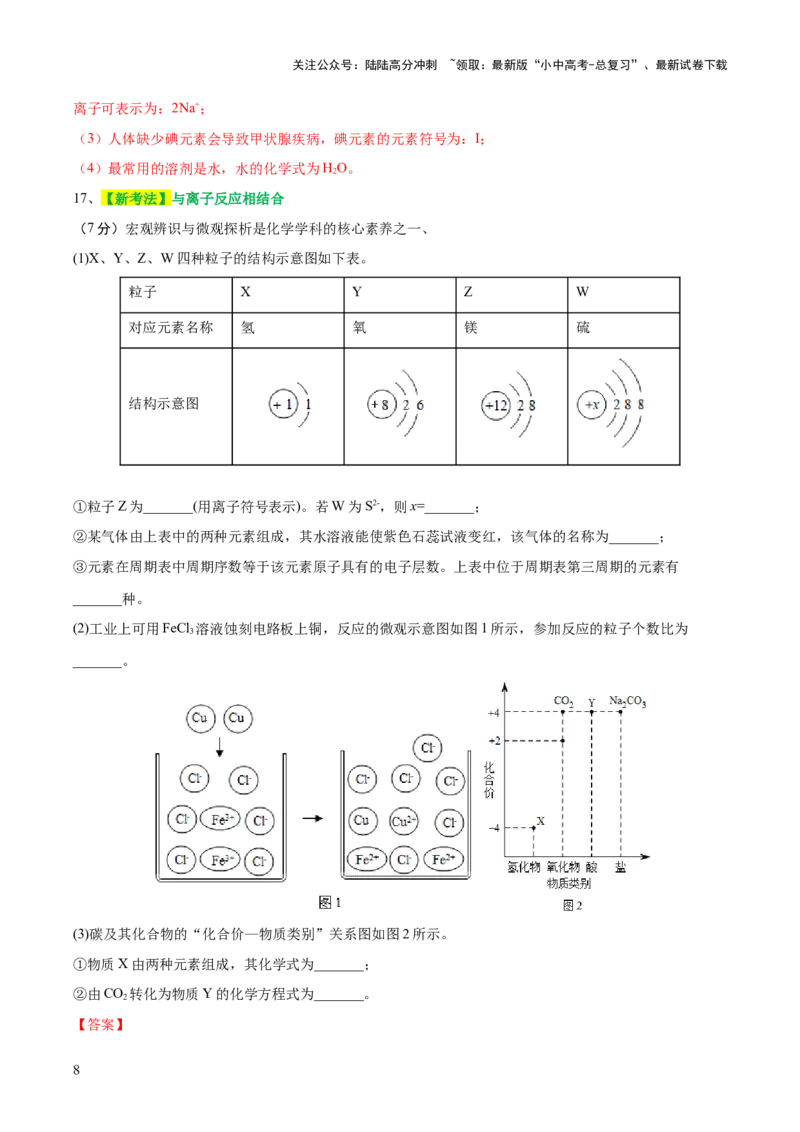
(1)X、Y、Z、W四种粒子的结构示意图如下表。
粒子 X Y Z W
对应元素名称 氢 氧 镁 硫
结构示意图
①粒子Z为_______(用离子符号表示)。若W为S2-,则x=_______;
②某气体由上表中的两种元素组成,其水溶液能使紫色石蕊试液变红,该气体的名称为_______;
③元素在周期表中周期序数等于该元素原子具有的电子层数。上表中位于周期表第三周期的元素有
_______种。
(2)工业上可用FeCl 溶液蚀刻电路板上铜,反应的微观示意图如图1所示,参加反应的粒子个数比为
3
_______。
(3)碳及其化合物的“化合价—物质类别”关系图如图2所示。
①物质X由两种元素组成,其化学式为_______;
②由CO 转化为物质Y的化学方程式为_______。
2
【答案】
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
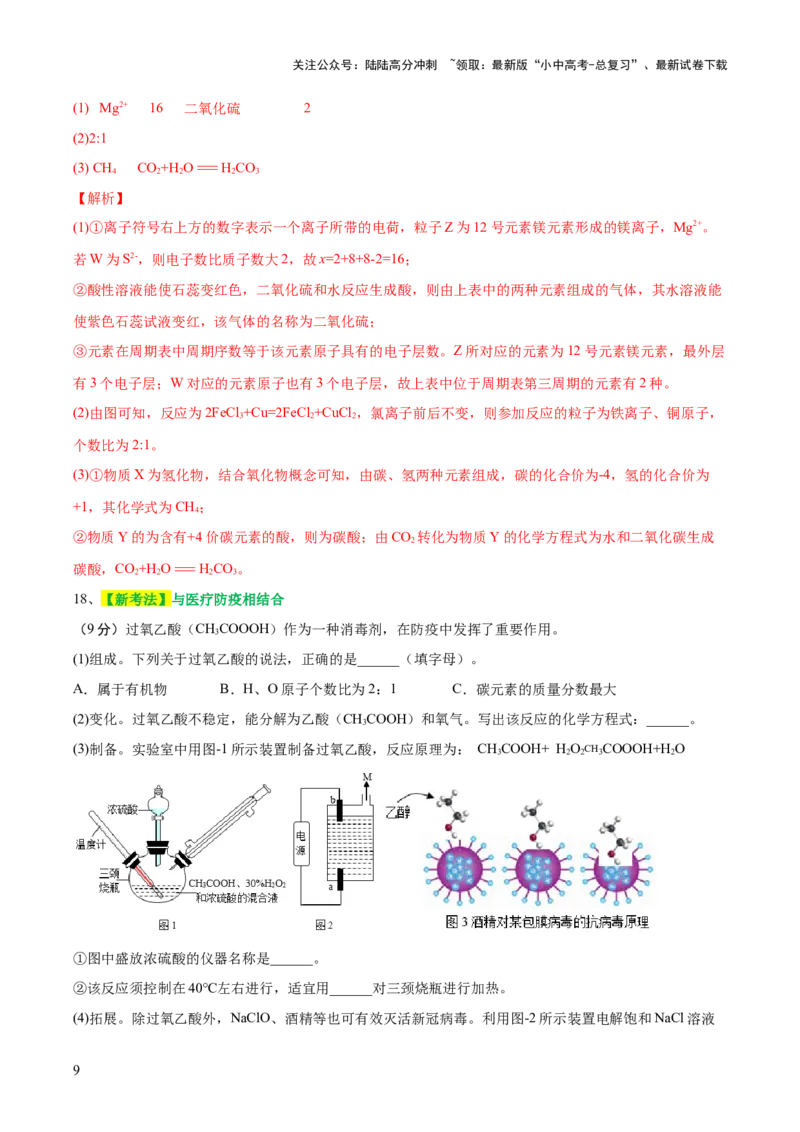
(1) Mg2+ 16 二氧化硫 2
(2)2:1
(3) CH CO+H O=HCO
4 2 2 2 3
【解析】
(1)①离子符号右上方的数字表示一个离子所带的电荷,粒子Z为12号元素镁元素形成的镁离子,Mg2+。
若W为S2-,则电子数比质子数大2,故x=2+8+8-2=16;
②酸性溶液能使石蕊变红色,二氧化硫和水反应生成酸,则由上表中的两种元素组成的气体,其水溶液能
使紫色石蕊试液变红,该气体的名称为二氧化硫;
③元素在周期表中周期序数等于该元素原子具有的电子层数。Z所对应的元素为12号元素镁元素,最外层
有3个电子层;W对应的元素原子也有3个电子层,故上表中位于周期表第三周期的元素有2种。
(2)由图可知,反应为2FeCl +Cu=2FeCl +CuCl ,氯离子前后不变,则参加反应的粒子为铁离子、铜原子,
3 2 2
个数比为2:1。
(3)①物质X为氢化物,结合氧化物概念可知,由碳、氢两种元素组成,碳的化合价为-4,氢的化合价为
+1,其化学式为CH;
4
②物质Y的为含有+4价碳元素的酸,则为碳酸;由CO 转化为物质Y的化学方程式为水和二氧化碳生成
2
碳酸,CO+H O=HCO。
2 2 2 3
18、【新考法】与医疗防疫相结合
(9分)过氧乙酸(CHCOOOH)作为一种消毒剂,在防疫中发挥了重要作用。
3
(1)组成。下列关于过氧乙酸的说法,正确的是______(填字母)。
A.属于有机物 B.H、O原子个数比为2:1 C.碳元素的质量分数最大
(2)变化。过氧乙酸不稳定,能分解为乙酸(CHCOOH)和氧气。写出该反应的化学方程式:______。
3
(3)制备。实验室中用图-1所示装置制备过氧乙酸,反应原理为: CHCOOH+ HOCHCOOOH+H O
3 2 2 3 2
①图中盛放浓硫酸的仪器名称是______。
②该反应须控制在40℃左右进行,适宜用______对三颈烧瓶进行加热。
(4)拓展。除过氧乙酸外,NaClO、酒精等也可有效灭活新冠病毒。利用图-2所示装置电解饱和NaCl溶液
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
可制取少量NaClO消毒液。电解过程中,a极区生成Cl,b极区生成气体单质M和NaOH。
2
①气体M具有可燃性,其化学式为______。
②Cl 与NaOH反应生成NaClO、NaCl和HO,该反应的化学方程式为______。
2 2
③84消毒液【有效成分为次氯酸钠(NaClO)和二氧化氯(ClO )】,其中NaClO中氯元素的化合价为______。
2
④乙醇,俗称酒精,体积分数为75%的酒精溶液常用作消毒剂,酒精抗病毒的原理如图3所示其实质是使
病菌的蛋白质______(填“盐析”、“变性”)。在配制溶液时将75mL酒精和25mL水混合时,发现体
积小于100mL,这是因为______。
【答案】
(1)A
(2)2CH COOOH=2CHCOOH+O↑
3 3 2
(3)分液漏斗 水浴
(4) ①H ②Cl+2NaOH=NaClO+NaCl+HO ③+1 ④变性 分子间有间隔
2 2 2
【解析】
(1)A、由化学式可知,过氧乙酸由碳、氢、氧三种元素组成,符合有机物的特点,属于有机物,选项正确;
B 、由化学式可知,过氧乙酸中,H、O原子个数比为4:3,选项错误;
C 、过氧乙酸中,碳、氢、氧三种元素的质量比=(12×2);(1×4);(16×3) =6;1;12,则过氧乙酸
中,氧元素的质量分数最大,选项错误,故填A。
(2)过氧乙酸分解生成乙酸和氧气,故反应的化学方程式写为:2CHCOOOH=2CH COOH+O ↑。
3 3 2
(3)①由图可知,图中盛放浓硫酸的仪器名称是长颈漏斗。
②该反应须控制在40℃左右进行,加热的温度较低,可用水浴对三颈烧瓶进行加热,故填水浴。
(4)①饱和食盐水中含有钠元素、氯元素、氢元素和氧元素,且反应生成的气体M具有可燃性,则M为氢
气,其化学式为H,故填H。
2 2
②Cl 与NaOH反应生成NaClO、NaCl和HO,故反应的化学方程式写为:
2 2
Cl+2NaOH=NaClO+NaCl+H O。
2 2
③次氯酸钠中钠元素的化合价为+1价,氧元素的化合价为-2价,设氯元素的化合价为x,根据化合物中各
元素的化合价的代数和为零,则+1+x+(-2)=0,x=+1,故填+1。
④乙醇,俗称酒精,体积分数为75%的酒精溶液常用作消毒剂,酒精抗病毒的原理如图3所示,其实质是
使病菌的蛋白质变性,故填变性;
分子间有间隔,75mL酒精和25mL水混合时,酒精分子与水分子相互穿插到对方的分子间隔中,则混合后
的体积小于100mL,故填分子间有间隔。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
11