文档内容
2021 浙江 1 月学考选考
化学试题
可能用到的相对原子质量: H 1 C 12 N 14 O16 Na 23 Mg 24 A1 27 Si 28 S 32
Cl 35.5 K 39 Ca 40 Cr 52 Fe 56 Cu 64 Ag 108 Ba 137
一、选择题(本大题共25小题,每小题2分,共50分。每小题列出的四个备选项中只有一个
是符合题目要求的,不选、多选、错选均不得分)
1. 下列含有共价键的盐是
A. CaCl B. HSO C. Ba(OH) D. NaCO
2 2 4 2 2 3
2. 蒸馏操作中需要用到的仪器是
A. B. C. D.
3. 下列物质属于强电解质的是
A. KOH B. HPO C. SO D. CHCHO
3 4 3 3
4. 下列物质与俗名对应的是
A. 纯碱:NaHCO B. 硫铵:NH HSO
3 4 4
C. TNT: D. 氯仿:CCl
4
5. 下列表示正确的是
A. 甲醛的电子式 B. 乙烯的球棍模型
C. 2-甲基戊烷的键线式 D. 甲酸乙酯的结构简式CHCOOCH
3 3
6. 下列说法不正确的是
A. 联苯( )属于芳香烃,其一溴代物有2种
B. 甲烷与氯气在光照下发生自由基型链反应
C. 沥青来自于石油经减压分馏后的剩余物质D. 煤的气化产物中含有CO、H 和CH 等
2 4
7. 下列说法正确的是
A. 14N 和15N 互为同位素 B. 间二甲苯和苯互为同系物
2 2
C. Fe C和Fe C互为同素异形体 D. 乙醚和乙醇互为同分异构体
2 3
8. 下列说法不正确的是
A. 铁粉与氧化铝发生的铝热反应可用于焊接铁轨
B. 镁燃烧会发出耀眼的白光,可用于制造信号弹和焰火
C. 熟石膏与水混合成糊状后能很快凝固,常用于制作模型和医疗石膏绷带
D. 工业上可用氨水消除燃煤烟气中的二氧化硫
9. 下列说法不正确的是
A. 某些胶态金属氧化物分散于玻璃中可制造有色玻璃
B. 通常以海水提取粗食盐后的母液为原料制取溴
C. 生物炼铜中通常利用某些细菌把不溶性的硫化铜转化为可溶性铜盐
D. 工业制备硝酸的主要设备为沸腾炉、接触室和吸收塔
10. 关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A. NH 中H元素被氧化
3
B. NO 在反应过程中失去电子
2
C. 还原剂与氧化剂的物质的量之比为3:4
D. 氧化产物与还原产物的质量之比为4:3
11. 下列说法不正确的是
A. 用纸层析法分离Fe3+和Cu2+,将滤纸上的试样点完全浸入展开剂可提高分离效果
B. 将CoCl ·6H O晶体溶于95%乙醇,加水稀释,溶液颜色由蓝色逐渐转变为粉红色
2 2
C. 乙酰水杨酸粗产品中加入足量碳酸氢钠溶液,充分反应后过滤,可除去聚合物杂质
D. 某些强氧化剂(如:氯酸钾、高锰酸钾)及其混合物不能研磨,否则可能引起爆炸
12. 下列“类比”合理的是
A. Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H
2 2 2 3 2
B. NaClO溶液与CO 反应生成NaHCO 和HClO,则NaClO溶液与SO 反应生成NaHSO 和HClO
2 3 2 3
C. NaN与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
D. NaOH溶液与少量AgNO 溶液反应生成Ag O和NaNO ,则氨水与少量AgNO 溶液反应生成Ag O和
3 2 3 3 2
NH NO
4 3
13. 下列反应的方程式不正确的是
A. 石灰石与醋酸反应:CO +2CH COOH=2CH COO- +CO ↑+H O
3 3 2 2B. 铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) Ag(阴极)
C. 铜与稀硝酸反应:3Cu+2NO +8H+=3Cu2+ +2NO↑+4HO
2
D. 明矾溶液中加入少量氢氧化钡溶液:2Al3+ +3SO + 3Ba2++6OH-=2Al(OH) ↓+ 3BaSO↓
3 4
14. 下列说法不正确的是
A. 甘氨酸和丙氨酸混合,在一定条件下可生成4种二肽
B. 乙酸、苯甲酸、乙二酸(草酸)均不能使酸性高锰酸钾溶液褪色
C. 纤维素与乙酸酐作用生成的醋酸纤维可用于生产电影胶片片基
D. 工业上通常用植物油与氢气反应生产人造奶油
15. 有关 的说法不正确的是
A. 分子中至少有12个原子共平面
B. 完全水解后所得有机物分子中手性碳原子数目为1个
C. 与FeCl 溶液作用显紫色
3
D. 与足量NaOH溶液完全反应后生成的钠盐只有1种
16. 现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,其中Z、Q在同一周期。相关信息如下
表:
元素 相关信息
X 最外层电子数是核外电子总数的一半
Y 最高化合价和最低化合价之和为零
Z 单质为淡黃色固体,常存在于火山喷口附近
Q 同周期元素中原子半径最小
下列说法正确的是
A. 常温时,X单质能与水发生剧烈反应
B. Y与Q元素组成的YQ 分子,空间构型为正四面体
4
C. Y、Z、Q最高价氧化物对应水化物的酸性依次减弱
D. 第五周期且与Q同主族元素的单质在常温常压下呈液态
17. 25℃时,下列说法正确的是为
A. NaHA溶液呈酸性,可以推测HA 强酸
2
B. 可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C. 0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α 、α ,则α <α
1 2 1 2
D. 100 mL pH=10.00的NaCO 溶液中水电离出H+的物质的量为1.0×10-5mol
2 3
18. 设N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 1 mol NH F晶体中含有的共价键数目为3N
4 A
B. CH 和C H 混合气体2.24L(标准状况)完全燃烧,则消耗O 分子数目为0.25N
4 2 4 2 A
C. 向100mL 0.10mol·L-1FeCl 溶液中加入足量Cu粉充分反应,转移电子数目为0.01N
3 A
D. 0.1 mol CHCOOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目为0.1N
3 3 2 3 2 3 A
19. 取50 mL过氧化氢水溶液,在少量I- 存在下分解:2HO=2H O+O↑。在一定温度下,测得O 的放出
2 2 2 2 2
量,转换成HO 浓度(c)如下表:
2 2
t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是
A. 反应20min时,测得O 体积为224mL(标准状况)
2
B. 20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C. 第30min时的瞬时速率小于第50min时的瞬时速率
D. HO 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
20. 已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/(kJ·mol-1) 436 463
2H(g) + O (g)=2HO(g) ΔH=
热化学方程式 2 2 2
-482kJ·mol-1
则2O(g)=O (g)的ΔH为
2
A. 428 kJ·mol-1 B. -428 kJ·mol-1 C. 498 kJ·mol-1 D. -498 kJ·mol-1
21. 铝硅酸盐型分子筛中有许多笼状空穴和通道(如图),其骨架的基本结构单元是硅氧四面体和铝氧四面体,
化学组成可表示为M[(AlO )·(SiO)]·zHO(M代表金属离子)。
a 2 x 2 y 2下列推测不正确的是
A. 常采用水玻璃、偏铝酸钠在强酸溶液中反应后结晶制得分子筛
B. 若a=x/2,则M为二价阳离子
C. 调节y/x(硅铝比)的值,可以改变分子筛骨架的热稳定性
D. 分子筛中的笼状空穴和通道,可用于筛分分子
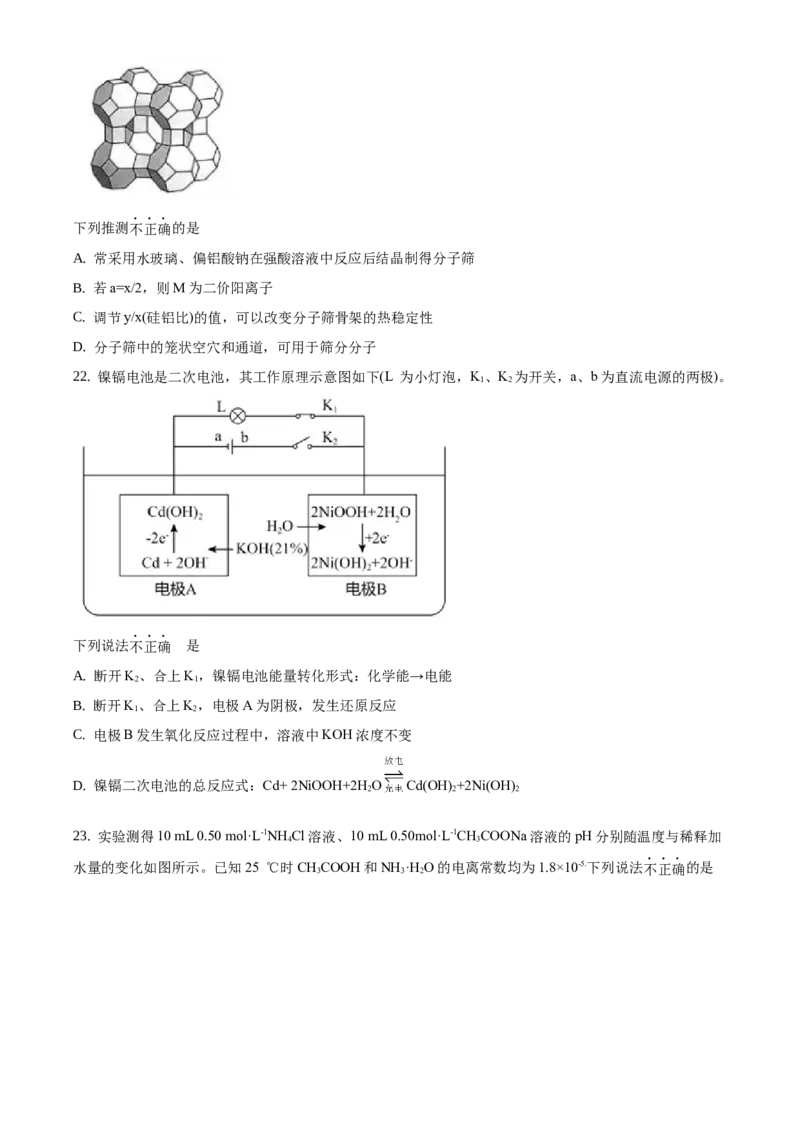
22. 镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,K、K 为开关,a、b为直流电源的两极)。
1 2
下列说法不正确 的是
A. 断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B. 断开K、合上K,电极A为阴极,发生还原反应
1 2
C. 电极B发生氧化反应过程中,溶液中KOH浓度不变
D. 镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Cd(OH) +2Ni(OH)
2 2 2
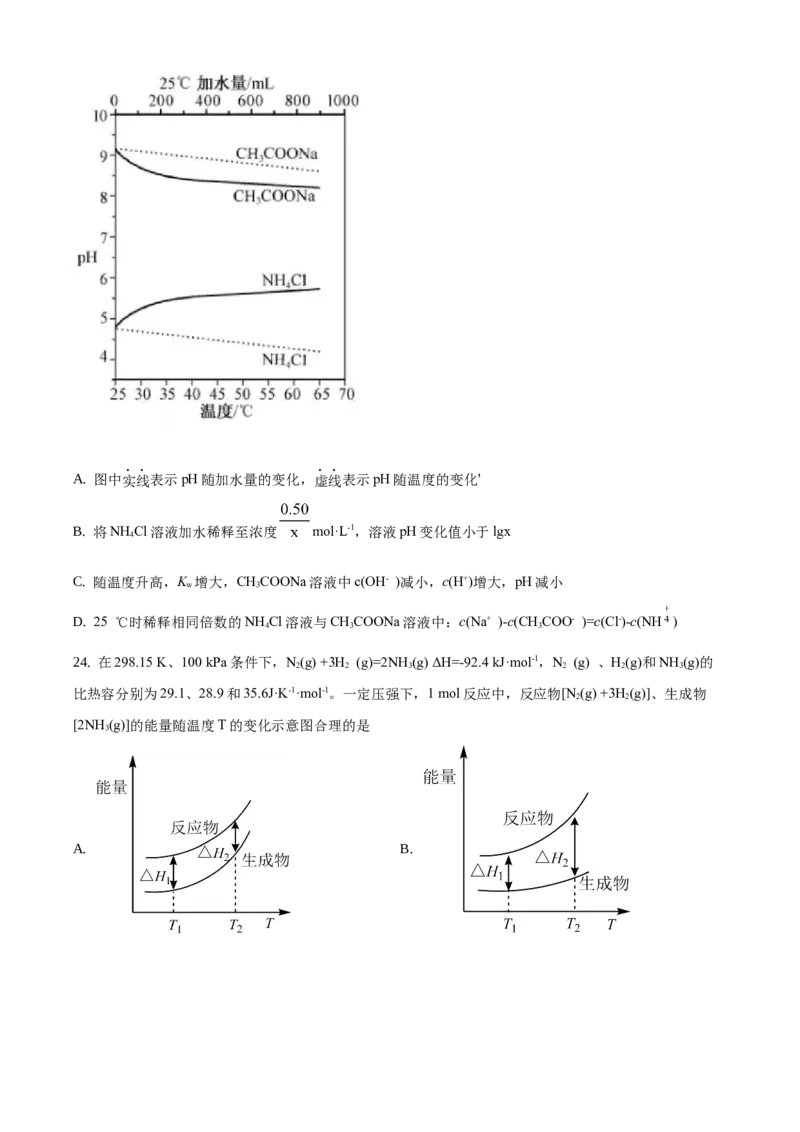
23. 实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液的pH分别随温度与稀释加
4 3
水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为1.8×10-5.下列说法不正确的是
3 3 2A. 图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B. 将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4
C. 随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D. 25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH )
4 3 3
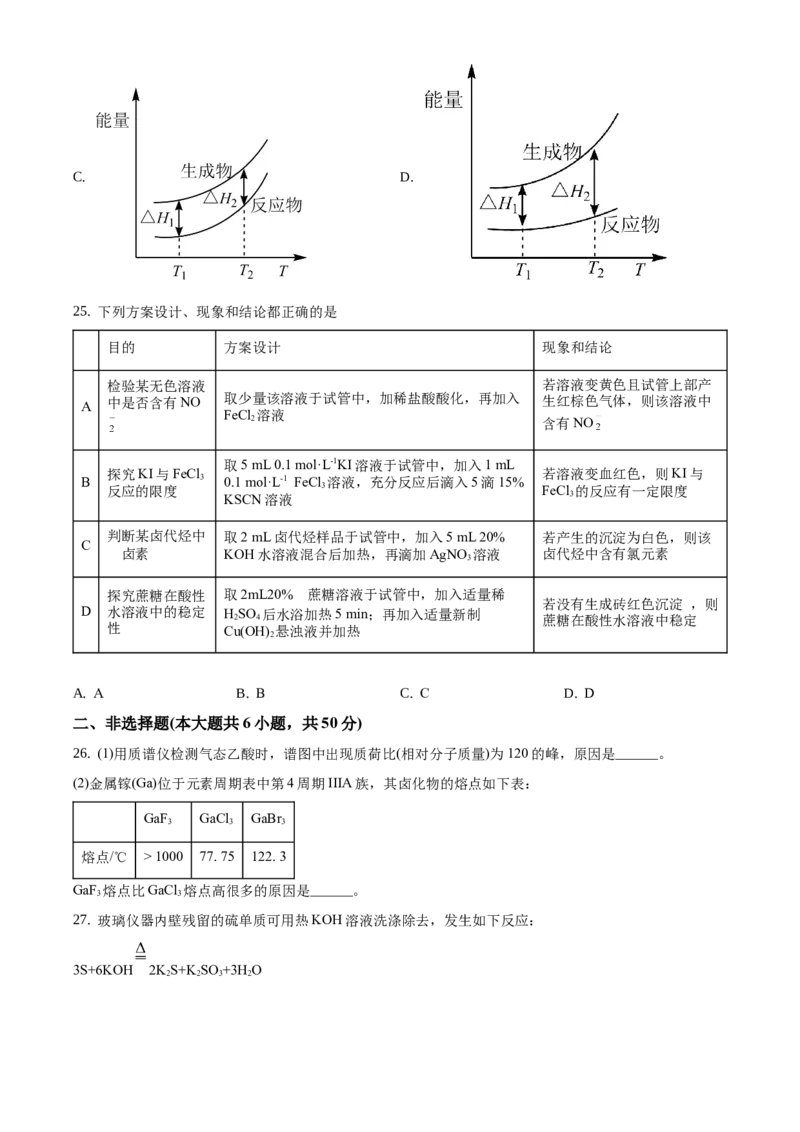
24. 在298.15 K、100 kPa条件下,N(g) +3H (g)=2NH (g) ΔH=-92.4 kJ·mol-1,N (g) 、H(g)和NH (g)的
2 2 3 2 2 3
比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物[N (g) +3H (g)]、生成物
2 2
[2NH (g)]的能量随温度T的变化示意图合理的是
3
A. B.C. D.
25. 下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
检验某无色溶液 若溶液变黄色且试管上部产
中是否含有NO 取少量该溶液于试管中,加稀盐酸酸化,再加入 生红棕色气体,则该溶液中
A
FeCl 溶液
2 含有NO
取5 mL 0.1 mol·L-1KI溶液于试管中,加入1 mL
探究KI与FeCl 若溶液变血红色,则KI与
B 3 0.1 mol·L-1 FeCl 溶液,充分反应后滴入5滴15%
反应的限度 3 FeCl 的反应有一定限度
KSCN溶液 3
判断某卤代烃中 取2 mL卤代烃样品于试管中,加入5 mL 20% 若产生的沉淀为白色,则该
C
的卤素 KOH水溶液混合后加热,再滴加AgNO 溶液 卤代烃中含有氯元素
3
探究蔗糖在酸性 取2mL20% 的蔗糖溶液于试管中,加入适量稀
若没有生成砖红色沉淀 ,则
D 水溶液中的稳定 HSO 后水浴加热5 min;再加入适量新制
2 4 蔗糖在酸性水溶液中稳定
性 Cu(OH) 悬浊液并加热
2
A. A B. B C. C D. D
二、非选择题(本大题共6小题,共50分)
26. (1)用质谱仪检测气态乙酸时,谱图中出现质荷比(相对分子质量)为120的峰,原因是______。
(2)金属镓(Ga)位于元素周期表中第4周期IIIA族,其卤化物的熔点如下表:
GaF GaCl GaBr
3 3 3
熔点/℃ > 1000 77. 75 122. 3
GaF 熔点比GaCl 熔点高很多的原因是______。
3 3
27. 玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S+6KOH 2KS+KSO +3H O
2 2 3 2(x-1)S+KS KS(x=2~6)
2 2 x
S+ K SO KSO
2 3 2 2 3
请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS和KSO ,则V=______。
2 2 3
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS 和KSO,则x=______。
2 x 2 2 3
(写出计算过程)
28. 某兴趣小组对化合物X开展探究实验。
其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶液褪色。请回答:
(1)组成X的3种元素是______(填元素符号),X的化学式是______。
(2)将固体X加入温热的稀HSO 中,产生气体B,该反应的离子方程式是______。
2 4
(3)步骤I,发生反应的化学方程式是______。
(4)步骤II,某同学未加HO 溶液,发现也会缓慢出现白色浑浊,原因是______。
2 2
(5)关于气体B使品红水溶液褪色的原因,一般认为:B不能使品红褪色,而是B与水反应的生成物使品红
褪色。请设计实验证明______。
29. “氯碱工业”以电解饱和食盐水为基础制取氯气等产品, 氯气是实验室和工业上的常用气体。请回答:
(1)电解饱和食盐水制取氯气的化学方程式是______。
(2)下列说法不正确的是______。
A.可采用碱石灰干燥氯气
B.可通过排饱和食盐水法收集氯气
C.常温下,可通过加压使氯气液化而储存于钢瓶中
D.工业上,常用氢气和氯气反应生成的氯化氢溶于水制取盐酸
(3)在一定温度下,氯气溶于水的过程及其平衡常数为:
Cl(g) Cl(aq) K =c(Cl)/p
2 2 1 2
Cl
2
(a⇌q) + H
2
O(l) H+ (aq)+Cl- (aq) + HClO(aq) K
2
⇌的
其中p为Cl(g) 平衡压强,c(Cl )为Cl 在水溶液中的平衡浓度。
2 2 2
①Cl(g) Cl(aq)的焓变ΔH______0。(填”>”、“=”或“<”)
2 2 1
②平衡常⇌数K
2
的表达式为K
2
=______。
③氯气在水中的溶解度(以物质的量浓度表示)为c,则c=______。(用平衡压强p和上述平衡常数表示,忽
略HClO的电离)
(4)工业上,常采用“加碳氯化”的方法以高钛渣(主要成分为TiO)为原料生产TiCl ,相应的化学方程式为;
2 4
I.TiO (s)+2Cl (g) TiCl (g)+O(g) ΔH=181 mol·L-1,K=3.4×10-29
2 2 4 2 I I
II.2C(s)+O
2
(g) 2⇌CO(g) ΔH
II
= - 221 mol·L-1,K
II
=1.2×1048
结合数据说明⇌氯化过程中加碳的理由______ 。
(5)在一定温度下,以I 为催化剂,氯苯和Cl 在CS 中发生平行反应,分别生成邻二氯苯和对二氯苯,两
2 2 2
产物浓度之比与反应时间无关。反应物起始浓度均为0.5 mol·L-1,反应30 min测得氯苯15%转化为邻二氯
苯,25%转化为对二氯苯。保持其他条件不变,若要提高产物中邻二氯苯的比例,可采用的措施是______。
A.适当提高反应温度 B.改变催化剂
C.适当降低反应温度 D.改变反应物浓度
30. 某兴趣小组用铬铁矿[Fe(CrO )]制备KCr O 晶体,流程如下:
2 2 2 2 7
已知:4Fe (CrO ) + 10Na CO+7O 8NaCrO +4NaFeO+10CO
2 2 2 3 2 2 4 2 2
2H++2CrO Cr O +H O
2 2
相关物质的溶解度随温度变化如下图。请回答:
(1)步骤I,将铬铁矿粉碎有利于加快高温氧化的速率,其理由是______。
(2)下列说法正确的是______。
A.步骤II,低温可提高浸取率
B.步骤II,过滤可除去NaFeO 水解产生的Fe(OH)
2 3
C.步骤III,酸化的目的主要是使NaCrO 转变为NaCr O
2 4 2 2 7
D.步骤IV,所得滤渣的主要成分是NaSO 和NaCO
2 4 2 3
(3)步骤V,重结晶前,为了得到杂质较少的KCr O 粗产品,从下列选项中选出合理的操作(操作不能重复
2 2 7
使用)并排序:溶解KCl →______→______→______→______→重结晶。
a.50℃蒸发溶剂;
b.100℃ 蒸发溶剂;
c.抽滤;
d.冷却至室温;
e.蒸发至溶液出现晶膜,停止加热;
f.蒸发至溶液中出现大量晶体,停止加热。
(4)为了测定KCr O 产品的纯度,可采用氧化还原滴定法。
2 2 7
①下列关于滴定分析的操作,不正确的是______。
A.用量筒量取25.00mL待测液转移至锥形瓶
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
②在接近终点时,使用“半滴操作”可提高测量的准确度。其方法是:将旋塞稍稍转动,使半滴溶液悬于管
口,用锥形瓶内壁将半滴溶液沾落,______继续摇动锥形瓶,观察颜色变化。(请在横线上补全操作)
(5)该小组用滴定法准确测得产品中KCr O 的质量分数为98.50%。某同学还用分光光度法测定产品纯度
2 2 7
(K Cr O 溶液的吸光度与其浓度成正比例),但测得的质量分数明显偏低。分析其原因,发现配制KCr O
2 2 7 2 2 7
待测水溶液时少加了一种试剂。该试剂是______,添加该试剂的理由是______。
31. 某课题组合成了一种非天然氨基酸X,合成路线如下(Ph—表示苯基):已知:R —CH=CH—R
1 2
R Br R MgBr
3 3
请回答:
(1)下列说法正确的是______。
A.化合物B的分子结构中含有亚甲基和次甲基
B.1H-NMR谱显示化合物F中有2种不同化学环境的氢原子
C.G→H的反应类型是取代反应
D.化合物X的分子式是C H NO
13 15 2
(2)化合物A的结构简式是______ ;化合物E的结构简式是______。
(3)C→D的化学方程式是______ 。
(4)写出3种同时符合下列条件的化合物H的同分异构体的结构简式(不包括立体异构体)______。
①包含 ;
②包含 (双键两端的C不再连接H)片段;
③除②中片段外只含有1个-CH-
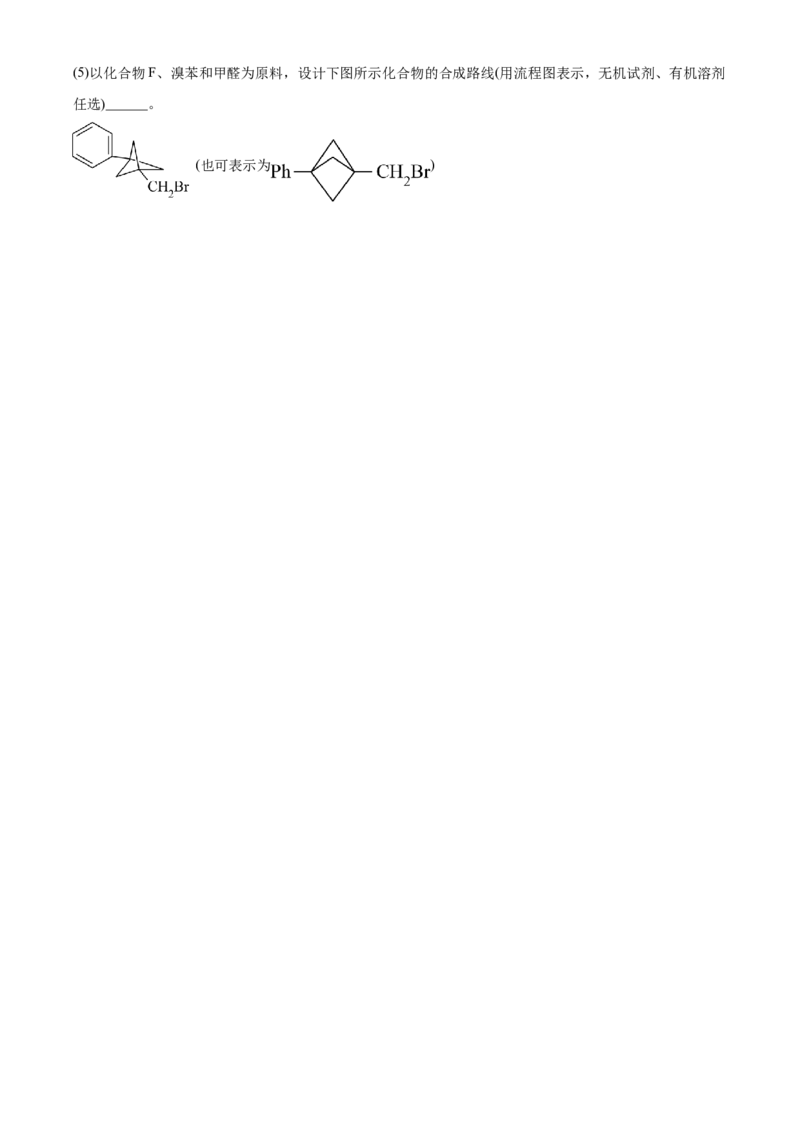
2(5)以化合物F、溴苯和甲醛为原料,设计下图所示化合物的合成路线(用流程图表示,无机试剂、有机溶剂
任选)______。
(也可表示为 )