文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
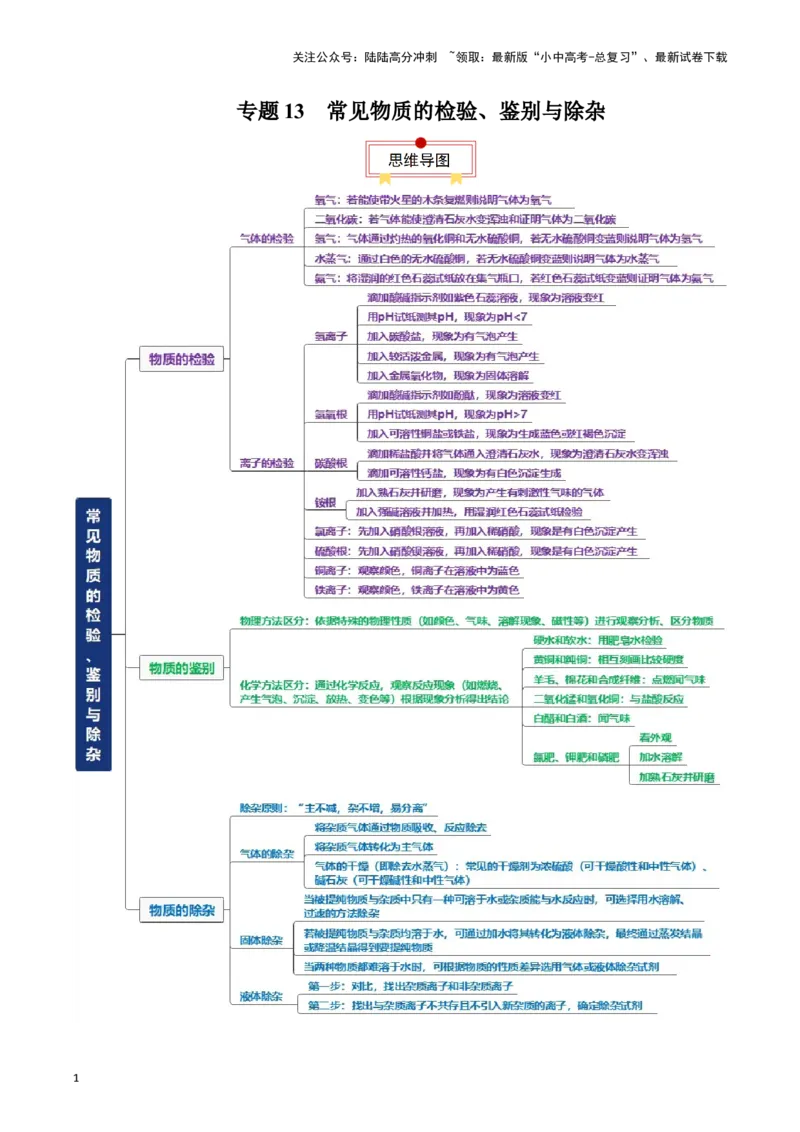
专题 13 常见物质的检验、鉴别与除杂
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识01 物质的检验 方法01 物质检验过程中的干扰和排除
知识02 物质的鉴别 方法02 解答鉴别题的步骤和方法
知识03 物质的除杂
知识 0 1 物质的检验
1.物质检验的一般依据
(1)任何具有明显实验现象差异的物理性质、化学性质都可作为物质检验的依据。
(2)举例:颜色的变化、是否有气体产生、能否溶解、有无沉淀产生、有无吸热或放热等。
2.物质检验的一般步骤
观察物理性质→取少量样品→加入某种试剂→加热、振荡等→观察实验现象→得出结论。
3.常见气体的检验
气体 方法 现象 原理
O 将带火星的木条伸入集气瓶内 木条复燃 氧气具有助燃性
2
点燃气体,在火焰上方罩一个
CO 澄清石灰水变浑浊 2CO+O CO
2 2
内壁涂有澄清石灰水的烧杯
Ca(OH) +CO =CaCO ↓+H O
2 2 3 2
CO 通入澄清石灰水 澄清石灰水变浑浊 Ca(OH) +CO =CaCO ↓+H O
2 2 2 3 2
氢气安静燃烧,产
点燃气体,在火焰上方罩一个
H 生淡蓝色火焰,烧
2
干燥、冷的烧杯 2H+O 2HO
2 2 2
杯内壁有水雾
(1)闻气味
(1)有氨味;
NH (2)将湿润的红色石蕊试纸 NH +H O=NH ·H O
3 3 2 3 2
(2)试纸变蓝
放在盛放氨气的容器口
HO 通过无水硫酸铜 白色粉末变蓝 5HO+CuSO =CuSO ·5H O
2 2 4 4 2
点燃气体,在火焰上方罩一个
产生蓝色火焰;烧
干燥、冷的烧杯,反应一段时
CH 杯内壁有水雾;石 CH+2O CO+2H O
4 4 2 2 2
间后,迅速倒转烧杯,倒入少
灰水变浑浊 Ca(OH) +CO =CaCO ↓+H O
2 2 3 2
量澄清石灰水
HCl (1)用蘸浓氨水的玻璃棒靠 (1)有白烟产生 (1)HCl+NH=NH Cl
3 4
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
近 (2)有白色沉淀
(2)将气体通入硝酸银溶 产生,且沉淀不溶
(2)HCl+AgNO =AgCl↓+HNO
3 3
液,并加稀硝酸 于稀硝酸
4.常见离子的检验
离子 检验方法 现象
Cl- 滴加硝酸银溶液和稀硝酸 产生白色沉淀(AgCl),且沉淀不消失
滴加稀盐酸,将产生的气体通 有气泡(CO )产生,产生的气体能使澄
2
、
入澄清石灰水 清石灰水变浑浊
滴加硝酸钡溶液和稀硝酸 产生白色沉淀(BaSO),且沉淀不消失
4
加入氢氧化钠溶液,用湿润的 有刺激性气味的气体(NH )产生,试纸
3
红色石蕊试纸检验产生的气体 变蓝
Ag+ 滴加稀盐酸和稀硝酸 产生白色沉淀(AgCl),且沉淀不消失
Cu2+ 滴加氢氧化钠溶液 产生蓝色沉淀[Cu(OH) ]
2
Ba2+ 滴加稀硫酸和稀硝酸 产生白色沉淀(BaSO),且沉淀不消失
4
Fe3+ 滴加氢氧化钠溶液 产生红褐色沉淀[Fe(OH) ]
3
①滴加紫色石蕊溶液 ①溶液变蓝
OH-
②滴加无色酚酞溶液 ②溶液变红
①滴加紫色石蕊溶液 ①溶液变红
H+
②加入锌等活泼金属 ②有气泡(H)产生
2
【例1】(2023·贵州贵阳·统考二模)如表设计方案合理的是( )
选项 实验目的 设计方案(主要操作)
A 鉴别化肥KSO 和KNO 分别加水溶解
2 4 3
B 检验溶液中是否含有 取样,加入足量的稀盐酸
探究温度对分子运动速率的影
C 分别向等体积冷水和热水中放入等量品红
响
D 去除粗盐中泥沙 加水溶解、蒸发
A.A B.B C.C D.D
知识 02 物质的鉴别
1.鉴别方法
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)物理方法
根据物质的物理性质不同进行鉴别。
(2)化学方法
根据物质的化学性质的不同进行鉴别。
①利用指示剂或pH试纸进行鉴别。
如鉴别盐酸和氢氧化钠溶液,可利用指示剂或pH试纸鉴别。
②加入其他试剂进行鉴别。
如鉴别NaOH溶液和Ba(OH) 溶液,可分别滴加稀硫酸进行鉴别[产生白色沉淀的即为Ba(OH) 溶液]。
2 2
2.常见物质的物理性质
(1)固体物质的颜色
①紫红色固体:Cu等。
②暗红色固体:红磷等。
③淡黄色固体:S等。
④绿色固体:碱式碳酸铜等。
⑤紫黑色固体:KMnO 等。
4
(2)溶液的颜色
①蓝色溶液:含Cu2+的溶液,如CuSO 溶液。
4
②浅绿色溶液:含Fe2+的溶液,如FeSO 溶液。
4
③黄色溶液:含Fe3+的溶液,如FeCl 溶液。
3
3.常见物质的鉴别
(1)硬水和软水
加肥皂水,硬水产生泡沫较少且有浮渣;软水产生泡沫较少。
(2)化肥
氮肥 钾肥 磷肥
外观 白色晶体 灰白粉末
加水 全部溶于水 大多不溶
灼烧 可燃烧,熔化有气泡或冒烟 不燃烧,跳动或有爆裂声
加熟石灰研磨 放出具有刺激性气味的气体 无气体放出
(3)纤维
纤维种类 燃烧情况 气味 灰烬
棉花(天然植物纤维) 易燃、直接燃烧 烧纸的气味 灰色,细而软
羊毛(天然动物纤维) 起泡成球,不连续燃烧 烧焦羽毛气味 易碎的黑褐色小球
涤纶、锦纶、腈纶(合成纤 先熔化再燃烧,或边熔化边燃
特殊的气味 黑或褐色硬块
维) 烧
(4)热塑性塑料和热固性塑料
加热,能熔化的是热塑性塑料;不能熔化的是热固性塑料。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(5)真假黄金
①灼烧,不变色的是真黄金,变黑的是假黄金。
②加稀盐酸或稀硫酸,有气泡产生的是假黄金,没有气泡产生的是真黄金。
4.区分物质举例
区分物质 试剂或方法 现象及结论
硬水和软水 用肥皂水 产生泡沫多、浮渣较少的是软水,产生泡沫较少、浮渣较多的是硬水
黄铜和纯铜 相互刻画 有明显划痕的为纯铜,反之为黄铜
羊毛、棉花和合 有烧焦羽毛气味的是羊毛;有烧纸气味的是棉花;有特殊气味,产物
灼烧、闻气味
成纤维 是黑色硬球的是合成纤维
二氧化锰和氧化
稀盐酸 无明显现象的是二氧化锰;固体溶解、溶液变为蓝色的是氧化铜
铜
白醋和白酒 闻气味 有刺激性气味的是白醋,有醇香味的是白酒
看外观 氮肥、钾肥都是白色晶体,磷肥是灰白色粉末
氮肥、磷肥、钾
加水溶解 磷肥大多数不溶于水或部分溶于水,氮肥和钾肥全部溶于水
肥
加熟石灰研磨 有刺激性气味放出的是铵态氮肥
【例2】(2024·四川德阳·模拟预测)下列物质的鉴别或除杂所用的操作方法不正确的( )
选项 物质 操作方法
A 除去CO 中的水蒸气 通过碱石灰干燥剂
2
B 除去MnO 粉末中混有的KCl 加水溶解、过滤、烘干
2
C 鉴别合成纤维和羊毛纤维 取样点燃,闻气味
D 鉴别尿素和硝酸铵 加熟石灰研磨闻气味
A.A B.B C.C D.D
知识 0 3 物质的除杂
一、除杂原则
1.主不减:被提纯的物质不能和加入的试剂反应。
2.杂不增:不能引入新的物质。
3.易分离:使被提纯的物质和杂质转化为不同状态(固、液、气),固体和液体的分离方法为过滤。
二、常见物质的除杂
1.气体的除杂
(1)将杂质气体通过物质吸收、反应除去
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
物质 杂质 试剂、方法
O CO 先通过氢氧化钠溶液,再通过浓硫酸
2 2
CO CO 先通过氢氧化钠溶液,再通过浓硫酸
2
CO H 先通过灼热的氧化铜,再通过浓硫酸
2 2
N O 通过灼热的铜网
2 2
H HCl 通过足量的NaOH溶液
2
(2)将杂质气体转化为主气体
物质 杂质 试剂、方法
CO CO 通过灼热的氧化铜,再通过浓硫酸
2
CO HCl 先通过饱和碳酸氢钠溶液,通过浓硫酸
2
(3)气体的干燥(即除去水蒸气)
干燥剂 能干燥的气体
浓硫酸 酸性或中性气体:CO、SO 、HCl、H、O、CO、N、CH 等
2 2 2 2 2 4
生石灰、碱石灰、NaOH固体 碱性或中性气体:NH 、H、O、CO、N、CH 等
3 2 2 2 4
2.固体的除杂
(1)当被提纯物质与杂质中只有一种可溶于水或杂质能与水反应时,可选择用水溶解、过滤的方法除
杂。
(2)若被提纯物质与杂质均溶于水,可通过加水将其转化为液体除杂,最终通过蒸发结晶或降温结晶得
到要提纯物质。
(3)当两种物质都难溶于水时,可根据物质的性质差异选用气体或液体除杂试剂。
常见固体除杂举例
物质 杂质 试剂、方法
Cu Fe 加入足量的稀硫酸或稀盐酸,过滤、洗涤、干燥;或用磁铁吸引
Cu CuO 加足量的稀硫酸或稀盐酸,过滤、洗涤、干燥
KCl MnO 溶解、过滤、蒸发结晶
2
NaCl KNO 溶解、蒸发结晶
3
CaO CaCO 高温煅烧
3
3.液体除杂
第一步:对比,找出杂质离子和非杂质离子
第二步:找出与杂质离子不共存且不引入新杂质的离子,确定除杂试剂
如:除去NaCl溶液中NaCO 的如图所示:
2 3
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
常见液体除杂举例
物质(杂质) 杂质离子 除杂试剂
NaOH溶液(NaCO) Ca(OH)
2 3 2
NaCl溶液(NaSO ) BaCl
2 4 2
NaCl溶液(NaOH) OH- MgCl
2
NaOH溶液[Ca(OH) ] Ca2+ NaCO
2 2 3
CaCl 溶液(HCl) H+ CaCO
2 3
FeSO 溶液(CuSO ) Cu2+ Fe
4 4
NaNO 溶液(CuSO ) Ba(OH)
3 4 Cu2+、 2
【例3】(2022·山东淄博·统考中考真题)除去下列物质中的少量杂质,选用试剂和方法均正确的是(
)
选项 物质 杂质(少量) 试剂和方法
A 氧气 氮气 通过灼热铜粉,收集气体
B 氧化钙 氢氧化钙 加入适量稀盐酸,蒸发
C 氯化钾 二氧化锰 加入适量水溶解,过滤,蒸发
D 盐酸 硫酸 加入适量硝酸钡溶液,过滤
A.A B.B C.C D.D
方法 1 物质检验过程中的干扰和排除
(1)检验中的干扰和排除
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
在物质的检验过程中,由于待检物质中混有杂质,选用试剂不当或试剂不纯以及仪器不洁净、操作有误
等,都会对检验造成干扰,应当予以排除。如鉴定 时,先加盐酸酸化,排除 、Ag+的干扰,再用
氯化钡溶液进行检验。
(2)检验结果的分析和判断
(3)根据检验过程中所观察到的现象确定试样中存在哪些离子,必须把可能存在的离子全部考虑到,再
根据每步检验的现象,肯定或否定某些离子的存在逐步缩小范围,最终得出正确的结论。
【例4】(2023·山东济宁·济宁市联考一模)某固体由Ba2+、Cu2+、Na+、Cl-、 、 中的几种离子构
成,取一定质量的该固体样品,进行如下实验:
①将固体溶于水得无色透明溶液,加入足量BaCl 溶液,过滤后得到5克白色沉淀。
2
②在沉淀中加入过量稀硝酸,仍有3克白色沉淀。
③在滤液中滴加AgNO 溶液,产生白色沉淀。
3
(1)则该固体中一定含有的离子是 ,一定不含的离子是 ;
(2)为验证可能含有的离子如何对以上实验改进 。
方法 2 解答鉴别题的步骤和方法
1.解答鉴别题的步骤和注意事项
(1)解鉴别题的一般步骤:取物质→加试剂→观现象→得结论。
(2)注意。
①不能向被检验物质中直接加人试剂,而应当只取少量试样进行检验,若被检验的物质是固体,而检验时
需要用其溶液时,则应先取少量试样用蒸馏水溶解制成溶液。
②不能把被检验的物质当作已知物质来描述实验现象,即不能未检先知。
③对多种被检验的物质进行并列检验时,要注意避免已加入的试剂对后续实验的影响。
2.鉴别题的常见类型及解答方法
(1)不用任何试剂鉴别一组物质的问题
①可先观察此组物质内有无有特殊颜色、特殊气味的物质,将此类物质作为解决问题的“题眼”。如不用
任何试剂鉴别 MgSO 、Ba(NO )、CuSO 、NaCl 溶液时,CuSO 溶液为“题眼”
4 3 2 4 4
②若无特殊物理性质,可用两两混合列表分析法。先将待测物质编号,分别以一种物质作试剂加入其他物
质中,将产生的现象列表分析,再分别统计每种物质与其他物质反应的现象,最后与表中被标号物质对照,
鉴定出各编号代表哪种物质。
(2)只用一种试剂鉴别一组物质的问题
①如果被鉴别的物质有明显的酸碱性差别,可选用指示剂(或pH试纸)鉴别。
②如果被鉴别的物质溶解性明显不同,以及溶解时时有明显的热现象,可以选用水作检验试剂。
③如果被鉴别的物质存在相同或大多数相同的阴离子,可以考虑选用强碱溶液或含 、 等阴离子
的溶液来检验。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
④如果被鉴别的物质存在相同或大多数相同的金属阳离子,可以选择强酸溶液来鉴别物质中的阴离子。
⑤如果被鉴别的物质是金属单质和金属氧化物,可以选择酸来鉴别。
⑥如果被鉴别的物质组成情况比较复杂,就要考虑区分不同的阴离子需要什么阳离子,区分不同的阴离子
需要什么阳离子,然后把这两种离子组合成一试剂。
(3)综合性鉴别:不限所加试剂种类、不限定实验步骤,利用物理方法或化学方法,根据物质的主要物
理特性(如:固体物质的颜色、沉淀的颜色、溶液的颜色、火焰的颜色、气体的气味等)、化学反应的特征现
象对物质进行区分。
【例5】(2022·湖南益阳·统考中考真题)下列物质的溶液,不另加其他试剂就能相互鉴别出来的一组是(
)
A.HSO NaOH CuSO
2 4 4
B.HCl Ca(OH) NaCl
2
C.NaCO CaCl BaCl
2 3 2 2
D.KNO NaSO FeCl
3 2 4 3
9