文档内容
福建师范大学附属中学2024-2025学年度高考12月模考
化 学
考试总分:100分;考试时间:75分钟;
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
第I卷(选择题)
一、单选题(共40分)
1.(本题4分)生活中处处有化学,下列叙述正确的是
A.苯甲酸钠可作为食品防腐剂是由于其具有酸性
B.竹简的成分之一纤维素属于天然高分子
C.月壤中的“嫦娥石 ” 不含主族金属元素
D.75%的乙醇与84消毒液的消毒原理相同
2.(本题4分)下列化学用语表示不正确的是
A.2,2-二甲基丁烷的结构简式:
B.三氟化硼分子的空间填充模型:
C.次氯酸分子的电子式:
D.基态溴原子的简化电子排布式:[Ar]4s24p5
3.(本题4分)某化学小组在实验室尝试用氨气制备硝酸,过程如下:
。设 为阿伏加德罗常数的值,以下说法正确的是
A.通过加热 和足量 的混合物的方式可以得到 个 分子
B.若要 完全被水吸收,需要额外通入 个 分子
C. 属于氮的固定, 发生该过程转移电子数为
D.25℃下, 的 溶液中 数为4.(本题4分)下述实验方案能达到实验目的的是
A.方案Ⅰ验证金属活泼性:Zn>Cu
B.方案Ⅱ验证Fe电极被保护
C.方案Ⅲ验证平衡移动原理
D.方案Ⅳ验证氯化银在水中存在溶解平衡
5.(本题4分)R、W、X、Y、Z是核电荷数依次增大的短周期主族元素,其形成的某种
甜味剂的阴离子结构如图所示。已知X与W、Y位于同一周期且相邻,Y、Z位于同一主
族。下列说法正确的是
A.简单氢化物热稳定性:Y>Z
B.简单离子半径:Z>Y>X
C.R与W形成的化合物均易溶于水
D.Z的氧化物对应的水化物均为强酸
6.(本题4分)甲酸分子在活性Pd催化剂表面脱氢的反应
历程与能量变化如图所示。
下列说法正确的是
A.该反应历程分3步进行
B.反应达平衡,其他条件相同,升高温度,甲酸浓度减小
C.若用 代替 ,则可制得HD
D.在Pd催化剂表面上有极性键和非极性键的断裂和形成7.(本题4分)某解热镇痛药主要化学成分(M)的结构简式为
。下列有关M的说法错误的是
A.化学式为 B.C原子的杂化方式为 和
C. 最多消耗 D.含酯基和酰胺基两种官能团
8.(本题4分)电有机合成是一种应用广泛的新型有机合成方法。某种3-氯-4-氨基苯酚
的电有机合成装置如图所示,下列说法错误的是
A.Cu2+的价电子排布式为3d9
B. 既可以和酸反应也可以和碱反应
C.电解一段时间后,阴阳两极室中电解质溶液的质量均增
大
D.Cu电极发生反应 +4e-+4H+= +H O
2
9.(本题4分)下列离子方程式书写正确的是
A.用高锰酸钾溶液滴定草酸:
B.用铜电极电解饱和食盐水:
C.向 溶液中加入足量稀硝酸:
D.向 溶液中通入少量的 气体:10.(本题4分)室温下,向 浓度相同的盐酸与醋酸稀溶液中分别滴加同浓度的
溶液,滴加 溶液的体积与 的关系如图所示。已知 表示溶液中水电
离出的 浓度, 。
下列说法正确的是
A.醋酸的初始浓度大于
B.水的电离程度c点小于b点
C.a点溶质为CHCOOH和CHCOONa
3 3
D.a,b点溶液显中性,且存在
第II卷(非选择题)
二、解答题
11.(16分)工业常以黄铁矿(主要成分为 )和软锰矿(主要成分为 ,杂质为 、
、 、 等元素的氧化物)为原料制备 ,其工艺流程如图所示。
已知:常温下, 。相关金属离子 形成氢氧化
物沉淀的 范围如下表所示:
金属离子开始沉淀的
8.1 6.3 1.5 8.9 3.4
完全沉淀的
10.1 8.3 2.8 10.9 4.7
(1)“酸浸”时,滤渣1的成分为 和 (填化学式)。
(2)“氧化”涉及主要反应的化学方程式为 。
(3)“调 ”的目的是除铁和铝,则调节 的合理范围为 。当铁恰好沉淀完全时,
溶液中 = 。
(4)“除镁”时,若溶液 太小会导致除镁不完全,试分析原因: 。
(5)“沉锰”时,涉及主要反应的离子方程式为 。
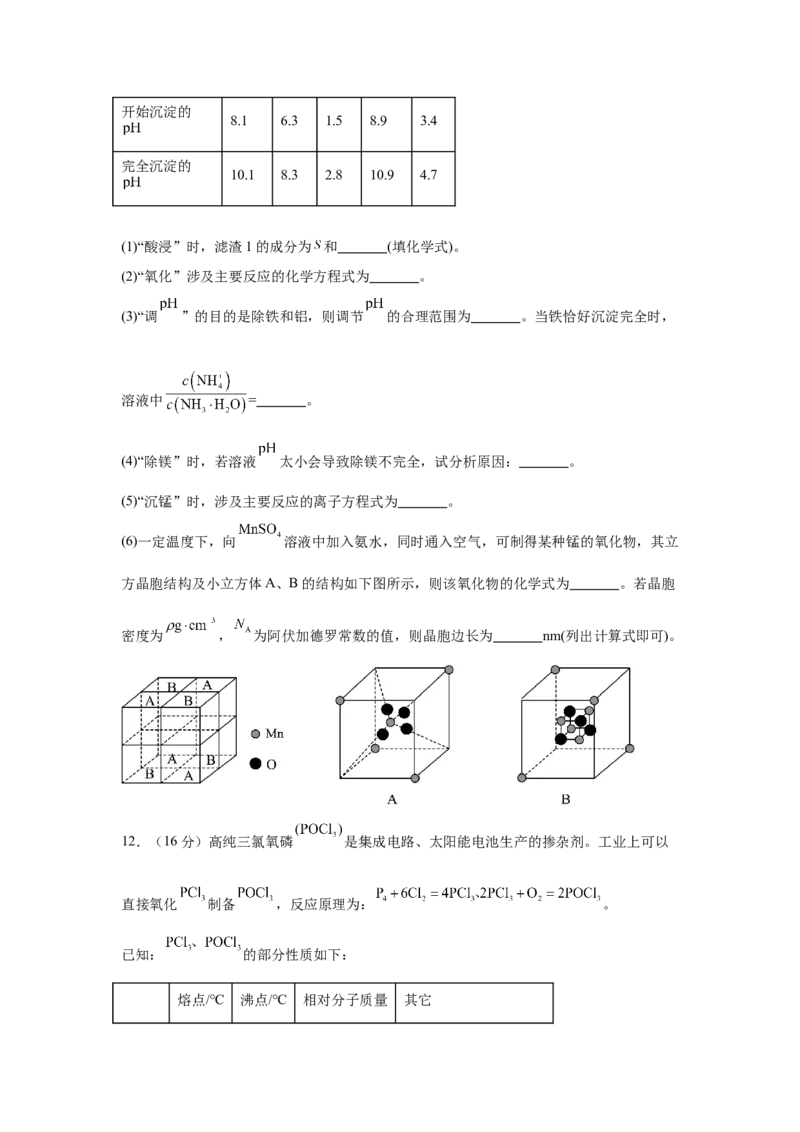
(6)一定温度下,向 溶液中加入氨水,同时通入空气,可制得某种锰的氧化物,其立
方晶胞结构及小立方体A、B的结构如下图所示,则该氧化物的化学式为 。若晶胞
密度为 , 为阿伏加德罗常数的值,则晶胞边长为 nm(列出计算式即可)。
12.(16分)高纯三氯氧磷 是集成电路、太阳能电池生产的掺杂剂。工业上可以
直接氧化 制备 ,反应原理为: 。
已知: 的部分性质如下:
熔点/℃ 沸点/℃ 相对分子质量 其它75.5 137.5 遇水生成 和
2 105.3 153.5 遇水生成 和
某化学兴趣小组模拟该工艺设计实验装置如图(某些夹持装置和加热装置已略去):
实验步骤如下:
i.连接仪器,检查装置气密性。关闭 ,打开 ,点燃酒精灯制备 。
ii.缓慢向B中通入适量 至B中白磷消失,熄灭酒精灯。
iii.关闭 ,打开 ,通入 。
iV.B装置控制反应在 ,最终制得 产品。请回答下列问题:
(1)仪器a的名称为 ;仪器b中盛放药品是 。
(2)D装置制取 的离子方程式为 。
(3)B反映温度应控制在60-65℃,不能过高或过低原因是 。
(4)实验室可通过以下实验步骤测定三氯氧磷产品中氯元素含量,可进一步计算三氯氧磷的
质量分数[假设产品中的杂质只有 。已知:
呈黄色,难溶于水,溶于酸和氨
水]。
步骤i:取 产品置于盛有 溶液(足量)的水解瓶中,摇动至完全水解,将水解液“预处理”并配成 溶液。
步骤ii:取 溶液于锥形瓶中,向其中加入 的 标准溶液 ,使
完全沉淀,再加入 硝基苯,振荡,使沉淀表面被有机物覆盖;然后加入几滴
溶液作指示剂,用 标准溶液滴定过量 至终点,记下所用体
积为 。
滴定终点的现象是 ;
加入硝基苯的作用是 ;步骤ii中若忘记加入硝基苯,则所测 的含量将
(填“偏高”、“偏低”或“不变”)。
(5)所测Cl百分含量为 (只需要列式)。
13.(10分)化合物 是一种具有生物活性的苯并呋喃衍生物,合成路线如图(部分条件忽
略,溶剂未出):
回答下列问题:
(1)B中含氧官能团有 。
(2)A到B的反应类型是 。
(3)反应③和④的顺序不能对换的原因是 。
(4)D结构简式 。
(5)化合物 的合成过程中,经历了取代、加成和消去三步反应,其中加成反应的化学
方程式为 。
14.(18分)3-羟基丙酸乙酯( )高效合成丙烯腈( )的原理如下:
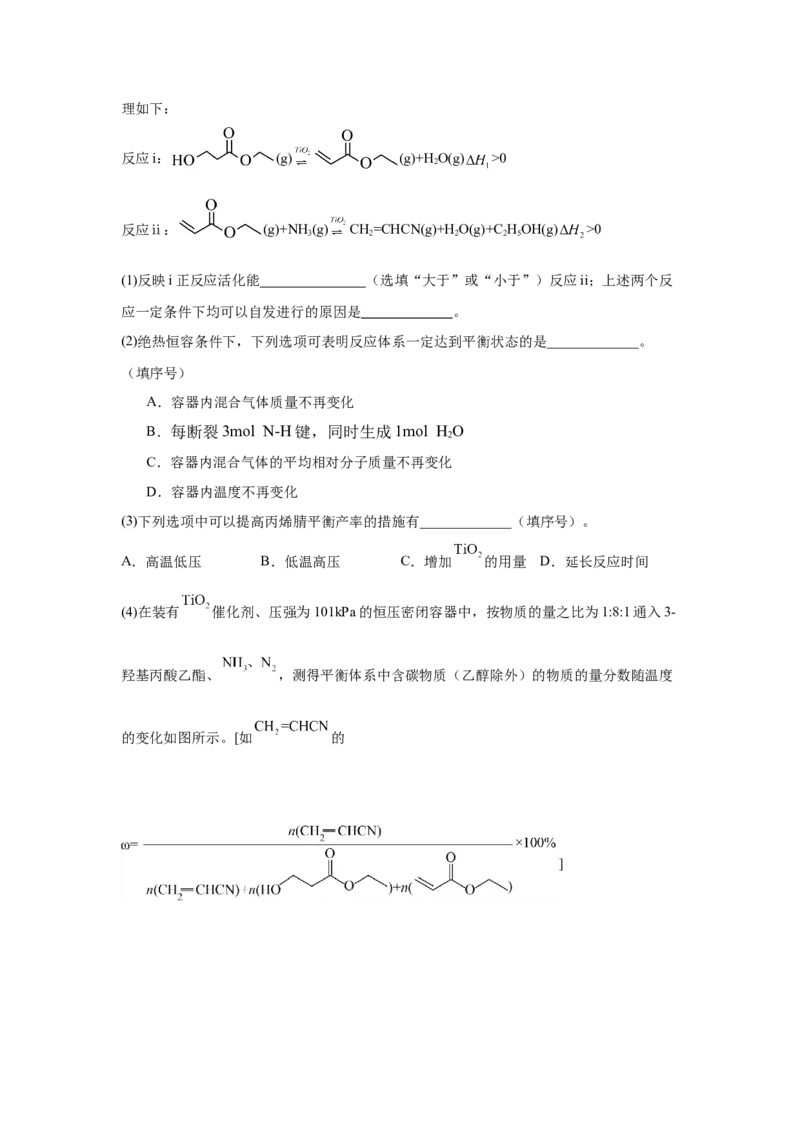
反应i: (g) (g)+HO(g) >0
2
反应ⅱ: (g)+NH (g) CH=CHCN(g)+H O(g)+C HOH(g) >0
3 2 2 2 5
(1)反映i正反应活化能 (选填“大于”或“小于”)反应ii;上述两个反
应一定条件下均可以自发进行的原因是 。
(2)绝热恒容条件下,下列选项可表明反应体系一定达到平衡状态的是_____________。
(填序号)
A.容器内混合气体质量不再变化
B.每断裂3mol N-H键,同时生成1mol H O
2
C.容器内混合气体的平均相对分子质量不再变化
D.容器内温度不再变化
(3)下列选项中可以提高丙烯腈平衡产率的措施有_____________(填序号)。
A.高温低压 B.低温高压 C.增加 的用量 D.延长反应时间
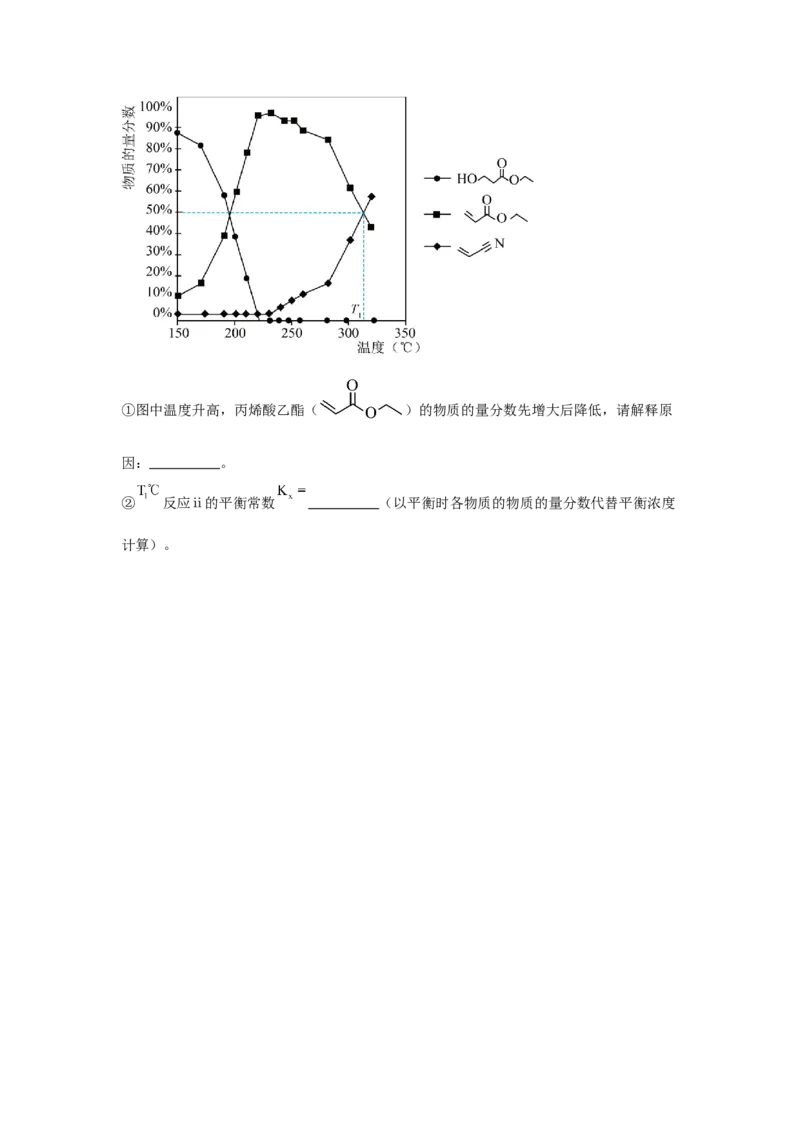
(4)在装有 催化剂、压强为101kPa的恒压密闭容器中,按物质的量之比为1:8:1通入3-
羟基丙酸乙酯、 ,测得平衡体系中含碳物质(乙醇除外)的物质的量分数随温度
的变化如图所示。[如 的
]①图中温度升高,丙烯酸乙酯( )的物质的量分数先增大后降低,请解释原
因: 。
② 反应ⅱ的平衡常数 (以平衡时各物质的物质的量分数代替平衡浓度
计算)。参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B D D D A C C D C C
11.(1)
(2)
(3)
(4)利用反应 除镁,若 太小, 正向移动, 减小,
除镁不完全
(5)
(6)
12.(1) 蒸馏烧瓶 吸收尾气中多余的氯气,防止污染空气,同时可以防止空气
中的水蒸气进入装置B中,使 发生水解
(3)
(4) 向水解液加稀硝酸酸化 滴入最后半滴标准液,溶液变红色,且半分钟不变色
偏高
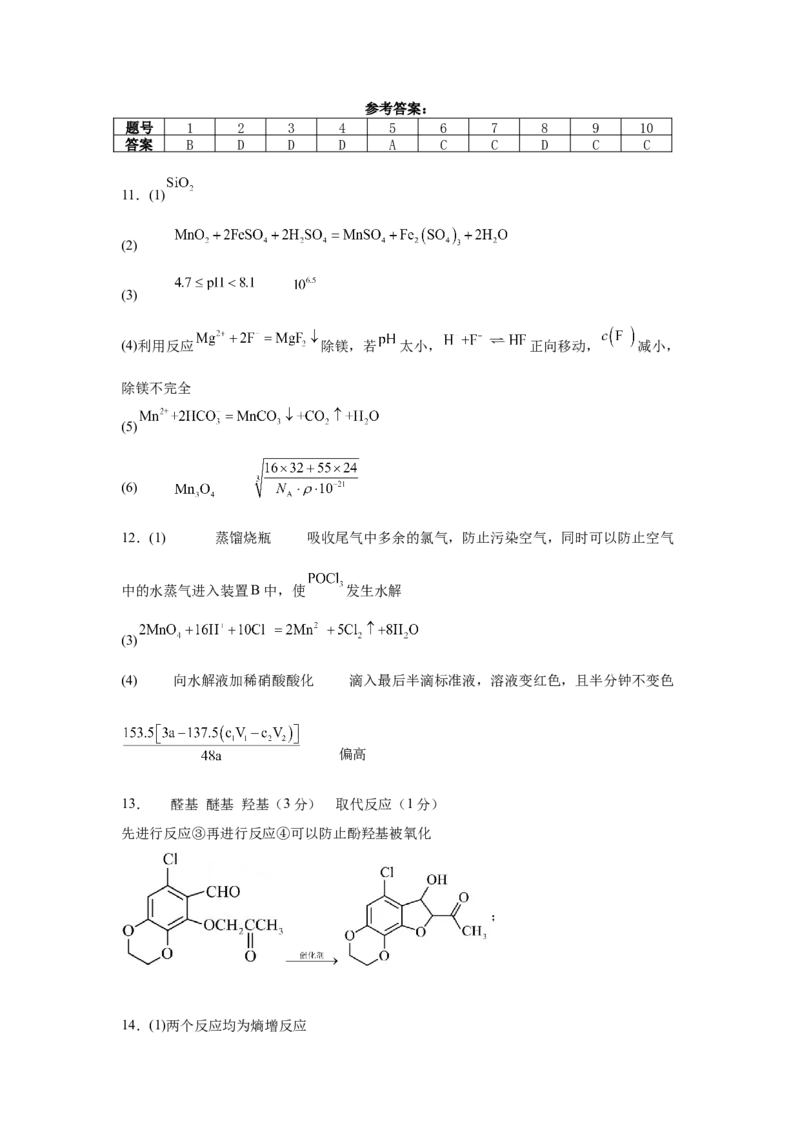
13. 醛基 醚基 羟基(3分) 取代反应(1分)
先进行反应③再进行反应④可以防止酚羟基被氧化
;
14.(1)两个反应均为熵增反应(2)CD
(3)A
(4) 低温时,主要发生反应①,生成丙烯酸乙酯。随着温度升高,反应②占主导,开
始消耗丙烯酸乙酯