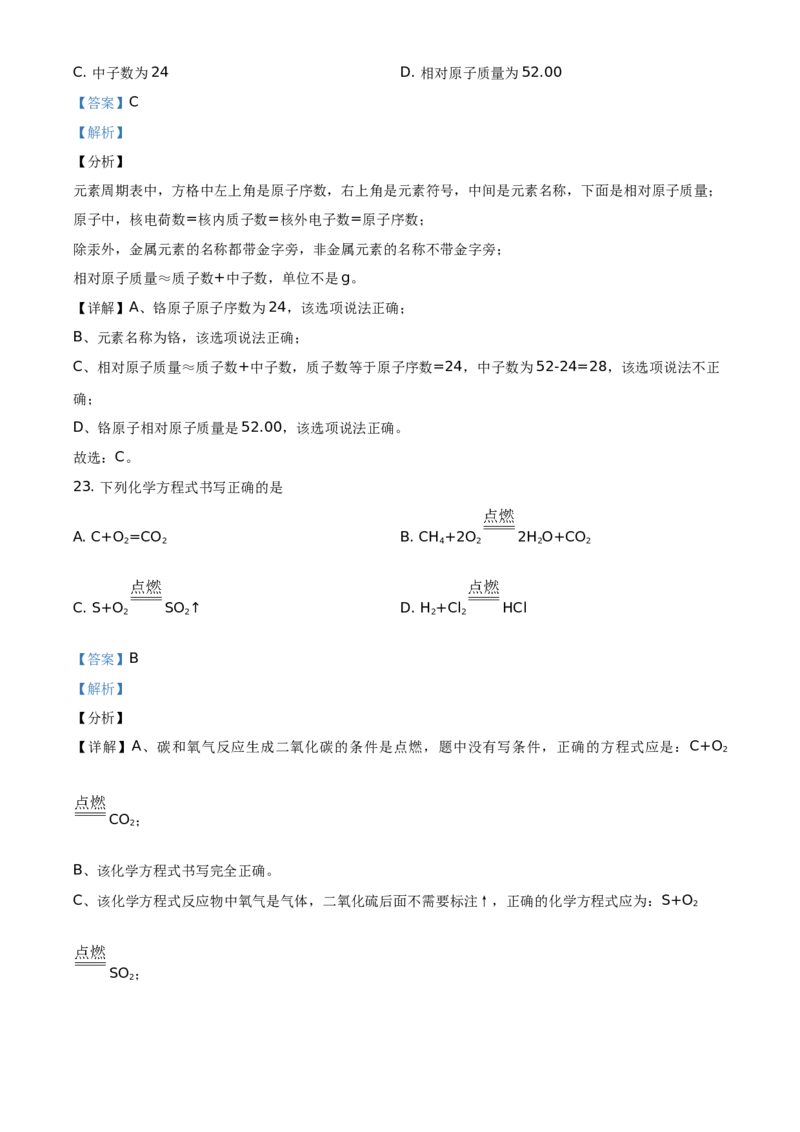文档内容
北京市西城区 2019—2020 学年度第一学期期末试卷
九年级化学
可能用到的相对原子质量:H 1 Li 7 C 12 O 16 Fe 56 Cu 64
一、选择题(共30分,每小题只有1个选项符合题意。每小题1分)
1. 地壳中含量最多的元素是( )
A. 硅 B. 氧 C. 铁 D. 铝
【答案】B
【解析】
本题的对地壳中元素的分布与含量的考查,根据地壳中元素分布图,地壳中元素含量由高到低居前四位的
元素依次是氧、硅、铝、铁。地壳中含量最多的元素是氧。
2. 下列属于物质化学性质的是
A. 密度 B. 可燃性 C. 状态 D. 颜色
【答案】B
【解析】
【分析】
【详解】物质的化学性质是需要通过化学变化才能表现出来的性质,物理性质是不需要发生化学变化就能
表现出来的性质,包括物质的颜色、状态、气味、熔点、沸点、密度、溶解性等,化学性质一般包括可燃
性、氧化性、稳定性、还原性等。
所以选项中属于物质化学性质的是可燃性。
故选:B。
3. 下列金属活动性最弱的是
A. 镁 B. 银 C. 铜 D. 铁
【答案】B
【解析】
【分析】
【详解】根据金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、
Pt、Au,则可知金属活动性大小为:镁>铁>铜>银,所以金属活动性最弱的是银。
故选:B。
【点睛】本题较为简单,熟记金属活动性顺序并且要学会应用。
4. 通过实验测定了空气组成的科学家是A. 门捷列夫
B. 达尔文
C. 拉瓦锡
D. 道尔顿
【答案】C
【解析】
【详解】A、门捷列夫发现了元素周期律并编制出元素周期表,不符合题意;
B、达尔文完整地确立了生物进化学说,不符合题意;
C、通过实验测定了空气组成的科学家是拉瓦锡,符合题意;
D、道尔顿提出原子论,不符合题意。
选C。
5. 下列元素符号书写不正确的是
A. 氖Ne B. 钾K C. 金AU D. 汞Hg
【答案】C
【解析】
【分析】
根据元素符号通常用元素的拉丁名称的第一个字母(大写)来表示,如果几种元素名称的第一个字母相同,
就在第一个字母(必须大写)后面加上元素名称中另一个字母(必须小写)以示区别,进行解答本题。
【详解】A、氖的元素符号书写是正确的;
B、钾的元素符号书写是正确的;
C、金的元素符号应该是Au,错误;
D、汞的元素符号书写正确。
故选:C。
6. 下列仪器不能加热的是
A. 烧杯 B. 试管 C. 量筒 D. 燃烧匙
【答案】C
【解析】
【分析】
【详解】烧杯、试管、燃烧匙都是反应仪器都可以加热,量筒是专用于量取液体体积的仪器,不能加热,
故选:C。
7. 下列属于氧气用途的是
A. 灭火 B. 作燃料 C. 光合作用 D. 医疗急救
【答案】D【解析】
【分析】
【详解】A、氧气能支持燃烧,不能用于灭火,故选项错误。
B、氧气不具有可燃性,不能作燃料,故选项错误。
C、二氧化碳是光合作用的原料之一,可用于光合作用,氧气是光合作用的产物,故选项错误。
D、氧气能供给呼吸,可用于医疗抢救,故选项正确。
故选:D。
8. “含氟牙膏”中的“氟”指的是
A. 分子 B. 原子 C. 单质 D. 元素
【答案】D
【解析】
【分析】
【详解】元素是有相同质子数的同一类原子的总称,“含氟牙膏”中的“氟”指的是元素。故选D。
9. 下列物质中,含有金属元素的是
A. Al O B. P O C. NO D. H SO
2 3 2 5 2 2 4
【答案】A
【解析】
【分析】
【详解】A、Al O 是由铝元素和氧元素组成的,其中铝元素属于金属元素,故选项正确。
2 3
B、P O 是由磷元素和氧元素组成的,不含金属元素,故选项错误。
2 5
C、NO 是由氮元素和氧元素组成的,不含金属元素,故选项错误。
2
D、H SO 是由氢元素、硫元素和氧元素组成的,不含金属元素,故选项错误。
2 4
故选:A。
10. 下列物质在空气中燃烧,生成大量白烟的是
A. 硫 B. 木炭 C. 酒精 D. 红磷
【答案】D
【解析】
【分析】
【详解】A、硫在空气中燃烧,发出淡蓝色火焰,产生一种具有刺激性气味的气体,故选项错误。
B、木炭在空气中燃烧,只能烧至红热,生成能使澄清石灰水变浑浊的气体,故选项错误。
C、酒精在空气中燃烧,产生蓝色火焰,不会产生白烟,故选项错误。
D、红磷在空气中燃烧,产生大量的白烟,故选项正确。
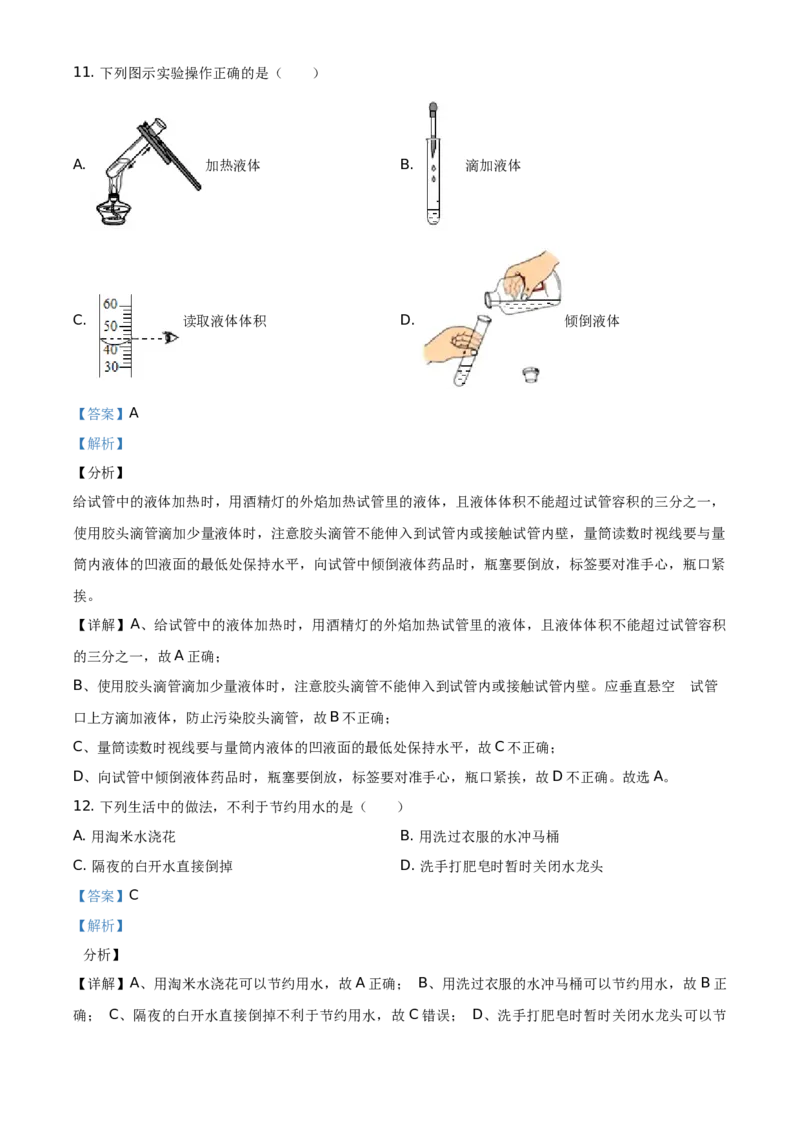
故选:D。11. 下列图示实验操作正确的是( )
A. 加热液体 B. 滴加液体
C. 读取液体体积 D. 倾倒液体
【答案】A
【解析】
【分析】
给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的三分之一,
使用胶头滴管滴加少量液体时,注意胶头滴管不能伸入到试管内或接触试管内壁,量筒读数时视线要与量
筒内液体的凹液面的最低处保持水平,向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧
挨。
【详解】A、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积
的三分之一,故A正确;
B、使用胶头滴管滴加少量液体时,注意胶头滴管不能伸入到试管内或接触试管内壁。应垂直悬空 在试管
口上方滴加液体,防止污染胶头滴管,故B不正确;
C、量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,故C不正确;
D、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,故D不正确。故选A。
12. 下列生活中的做法,不利于节约用水的是( )
A. 用淘米水浇花 B. 用洗过衣服的水冲马桶
C. 隔夜的白开水直接倒掉 D. 洗手打肥皂时暂时关闭水龙头
【答案】C
【解析】
【分析】
【详解】A、用淘米水浇花可以节约用水,故A正确; B、用洗过衣服的水冲马桶可以节约用水,故B正
确; C、隔夜的白开水直接倒掉不利于节约用水,故 C错误; D、洗手打肥皂时暂时关闭水龙头可以节约用水,故D正确,故选C。
13. 某原子的原子核内有1个质子和2个中子,则该原子的核外电子数为
A. 3 B. 2 C. 1 D. 0
【答案】C
【解析】
【分析】
【详解】因为原子中:核电荷数=核内质子数=核外电子数,由题意已知一种氢原子的原子核内有1个质
子,故该原子的原子核外电子数为1。
故选:C。
14. 有关空气中主要成分的说法不正确的是
A. 氮气可作保护气 B. 稀有气体可用于制作霓虹灯
C. 氧气可与多种物质发生反应 D. 二氧化碳是一种空气污染物
【答案】D
【解析】
【分析】
【详解】A.氮气的化学性质不活泼,可作保护气,所以说法正确;
B.稀有气体通电时会发出有色光,所以稀有气体可用于制作霓虹灯,所以说法正确;
C.氧气化学性质活泼,可以与多种物质发生反应,所以说法正确;
D.二氧化碳是空气的成分之一,没有毒性,不属于空气污染物,所以说法错误;
故选:D。
15. 氢元素与氧元素的本质区别是( )
A. 质子数不同
B. 电子数不同
C. 中子数不同
D. 最外层电子数不同
【答案】A
【解析】
【详解】根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,所以氧元素与氢元素之间的
本质区别是质子数不同。故选:A。
16. 下列配制与使用火药的过程中,主要发生化学变化的是A. 精磨配料 B. 称量配料 C. 混合配料
D. 点燃火药
【答案】D
【解析】
【分析】
【详解】A、精磨配料只是形状发生了变化,没有新物质生成,属于物理变化;
B、称量配料过程中没有新物质生成,属于物理变化;
C、混合配料过程中没有新物质生成,属于物理变化;
D、点燃火药过程中有新物质二氧化碳等生成,属于化学变化;
故选:D。
17. 下列符号表示2个氢原子的是
A. 2H B. 2H+ C. H D. 2H
2 2
【答案】A
【解析】
试题分析:下列符号中,表示两个氢原子的是2H,2H +表示两个氢离子,2H 表示两个氢分子,H 表示
2 2
宏观的物质和微观的分子。故选A.
考点:符号的意义
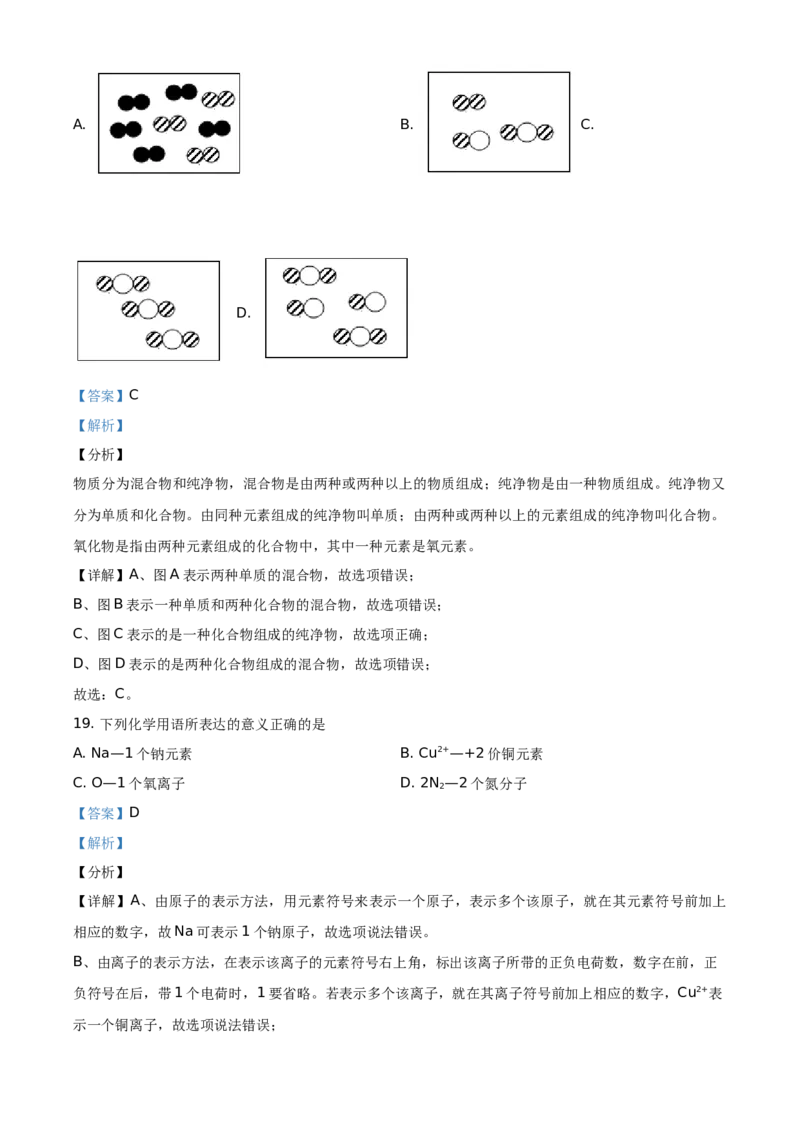
18. 以下各图能表示纯净物的是(图中不同小球代表不同原子)A. B. C.
D.
【答案】C
【解析】
【分析】
物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成。纯净物又
分为单质和化合物。由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物。
氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素。
【详解】A、图A表示两种单质的混合物,故选项错误;
B、图B表示一种单质和两种化合物的混合物,故选项错误;
C、图C表示的是一种化合物组成的纯净物,故选项正确;
D、图D表示的是两种化合物组成的混合物,故选项错误;
故选:C。
19. 下列化学用语所表达的意义正确的是
A. Na—1个钠元素 B. Cu2+—+2价铜元素
C. O—1个氧离子 D. 2N —2个氮分子
2
【答案】D
【解析】
【分析】
【详解】A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上
相应的数字,故Na可表示1个钠原子,故选项说法错误。
B、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正
负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,Cu2+表
示一个铜离子,故选项说法错误;C、O表示一个氧原子,故选项说法错误。
D、由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,
则2 N 可表示2个氮分子,故选项说法正确。
2
故选:D。
20. 下列灭火方法不正确的是
A. 电器起火—用水浇灭 B. 森林起火—砍伐树木形成隔离带
C. 油锅起火—用锅盖盖灭 D. 图书起火—用二氧化碳灭火器灭火
【答案】A
【解析】
【分析】
【详解】A、电器着火不能用水浇灭,以免发生触电,故选项说法错误。
B、森林起火,砍伐树木形成隔离带,是利用了清除可燃物的灭火原理,故选项说法正确。
C、油锅起火,用锅盖盖灭,是利用了隔绝氧气的灭火原理,故选项说法正确。
D、图书档案着火不能用水基型灭火器,以防损坏档案,应用二氧化碳灭火器,故选项说法正确。
故选:A。
【点睛】本题难度不大,掌握灭火的原理(清除或隔离可燃物,隔绝氧气或空气,使温度降到可燃物的着
火点以下)并能灵活运用是正确解答本题的关键。
21. 下列物质的化学式书写正确的是
A. 氧化铁 FeO B. 氯化铝 AlCl C. 硫酸钠 Na SO D. 氢氧化镁MgOH
2 4
【答案】C
【解析】
【分析】
【详解】A、氧化铁中铁元素的化合价为+3,氧元素的化合价为-2,化学式为:Fe O ;故错误
2 3
B、氯元素的化合价为-1,铝元素的化合价为+3,氯化铝化学式为 AlCl ;故错误;
3
C、硫酸钠中钠元素显+1价,硫酸根显-2价,其化学式为:Na SO ,故正确;
2 4
D、氢氧化镁中,镁离子显+2价,氢氧根显-1价,其化学式为:Mg(OH) ,故错误;
2
故选:C。
22. 铬在元素周期表中信息如右图所示。下列有关铬元素的说法不正确的是
A. 原子序数为24 B. 元素名称为铬C. 中子数为24 D. 相对原子质量为52.00
【答案】C
【解析】
【分析】
元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量;
原子中,核电荷数=核内质子数=核外电子数=原子序数;
除汞外,金属元素的名称都带金字旁,非金属元素的名称不带金字旁;
相对原子质量≈质子数+中子数,单位不是g。
【详解】A、铬原子原子序数为24,该选项说法正确;
B、元素名称为铬,该选项说法正确;
C、相对原子质量≈质子数+中子数,质子数等于原子序数=24,中子数为52-24=28,该选项说法不正
确;
D、铬原子相对原子质量是52.00,该选项说法正确。
故选:C。
23. 下列化学方程式书写正确的是
A. C+O =CO B. CH +2O 2H O+CO
2 2 4 2 2 2
C. S+O SO ↑ D. H +Cl HCl
2 2 2 2
【答案】B
【解析】
【分析】
【详解】A、碳和氧气反应生成二氧化碳的条件是点燃,题中没有写条件,正确的方程式应是:C+O
2
CO ;
2
B、该化学方程式书写完全正确。
C、该化学方程式反应物中氧气是气体,二氧化硫后面不需要标注↑,正确的化学方程式应为:S+O
2
SO ;
2D、该方程式没有配平,正确的方程式应为:H +Cl 2HCl;
2 2
故选:B。
24. 改善环境质量,推动绿色发展。下列做法不符合该理念的是
A. 多用一次性餐具 B. 垃圾分类处理
C. 选择公交出行 D. 注意人走灯灭
【答案】A
【解析】
【分析】
【详解】A.一次性餐具制作过程消耗能源和资源,多用一次性餐具,能增大消耗的能量、二氧化碳的排
放、白色污染等,故选项不符合该理念。
B.垃圾分类回收可以改善环境质量、有利于节约资源,故选项符合该理念;
C.选择公交方式出行,能减少燃油、燃气等交通工具的使用,从而减少二氧化碳的排放,故选项符合该
理念;
D.注意人走灯灭,可以节约能源,故选项符合该理念。
故选:A。
25. 关于净水器(如图)的说法不正确的是
A. 能除去难溶性杂质 B. 不能杀菌消毒
C. 能除去颜色和异味 D. 能得到蒸馏水
【答案】D
【解析】
【分析】
【详解】A、该装置可以把不溶于水的固体杂质通过多层过滤而除去,故A正确;
B、杀菌消毒需要消毒杀菌剂,该装置中没有使用消毒剂,不能杀菌消毒,故B正确;
C、该装置有活性炭,能吸附水中色素及异味,故C正确;
D、通过蒸馏才能得到蒸馏水,该装置净化后的水中仍然含有一些溶于水的物质,不能得到蒸馏水,故D错误;
故选:D。
26. 蔗糖存在于多种植物的果实中,其化学式为C H O 。下列有关蔗糖的说法正确的是
12 22 11
A. 属于混合物
B. 由12个碳原子、22个氢原子和11个氧原子构成
C. 由碳、氢、氧三种元素组成
D. 碳、氧元素质量比为12:11
【答案】C
【解析】
【分析】
【详解】A、蔗糖是由蔗糖一种物质组成的,属于纯净物,故错误。
B、蔗糖是由蔗糖分子构成的,而不是由原子直接构成的,故错误;
C、由蔗糖的化学式C H O 可知,蔗糖是由碳、氢、氧三种元素组成的,故正确;
12 22 11
D、蔗糖中,碳元素与氧元素的质量比为:(12×12):(16×11)≠12:11,故错误。
故选:C。
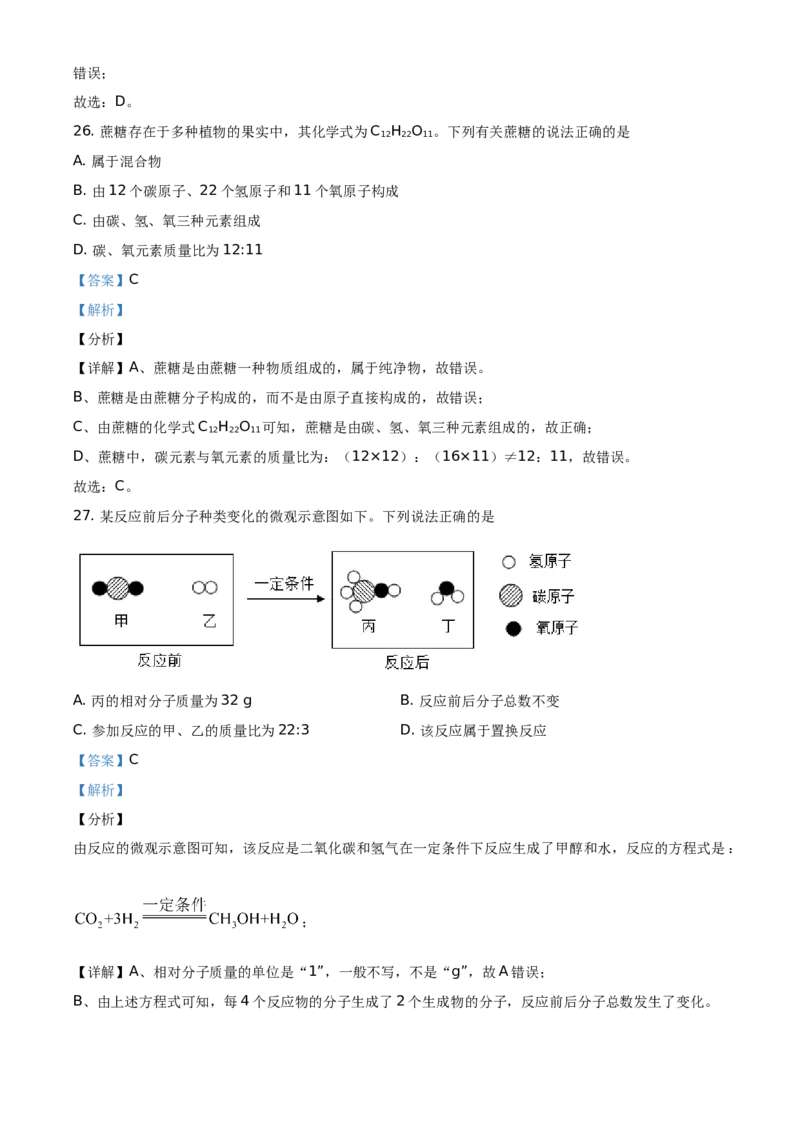
27. 某反应前后分子种类变化的微观示意图如下。下列说法正确的是
A. 丙的相对分子质量为32 g B. 反应前后分子总数不变
C. 参加反应的甲、乙的质量比为22:3 D. 该反应属于置换反应
【答案】C
【解析】
【分析】
由反应的微观示意图可知,该反应是二氧化碳和氢气在一定条件下反应生成了甲醇和水,反应的方程式是:
;
【详解】A、相对分子质量的单位是“1”,一般不写,不是“g”,故A错误;
B、由上述方程式可知,每4个反应物的分子生成了2个生成物的分子,反应前后分子总数发生了变化。故B错误;
C、由反应的方程式可知,发生反应的甲和乙的质量比为44:(3×1×2)=22:3,故C正确;
D、由上述方程式可知,生成物为两种化合物,不属于置换反应,故D错误;
故选:C。
28. 下图为金刚石、石墨和石墨烯的结构模型(图中小球代表碳原子)。下列说法正确的是
①三种物质分别在足量的氧气中完全燃烧均生成CO
2
②金刚石和石墨烯是元素组成相同但结构不同的两种物质
③石墨烯有超强的导电性和导热性,说明石墨烯的化学性质和金属相似
A. ①②③ B. ①② C. ①③ D. ②③
【答案】B
【解析】
【分析】
【详解】①这三种物质都是由碳元素组成的,完全燃烧后的产物都是CO ,正确;
2
②金刚石和石墨烯是组成相同但结构不同的两种物质,正确;
③石墨烯有超强的导电性和导热性,说明石墨烯的物理性质和金属相似,错误;
故选:B。
29. 下列实验方法一定能达到实验目的的是
选项 实验目的 实验方法
A 鉴别H 和CH 分别点燃,在火焰上方罩一干冷烧杯
2 4
B 鉴别双氧水和水 加入适量的二氧化锰
C 除去CO 中的少量CO 点燃
2
除去 Cu(NO ) 溶液中的少量
D 3 2 加入过量Zn粉,过滤
AgNO
3
A. A B. B C. C D. D
【答案】B
【解析】
【分析】【详解】A、H 和CH 燃烧都有水生成 ,分别点燃,在火焰上方罩一干冷烧杯,烧杯内壁都会出现水
2 4
雾,现象相同,不能鉴别,选项错误;
B、过氧化氢在二氧化锰的作用下分解生成氧气,分别向双氧水(过氧化氢溶液)和水中加入适量的二氧
化锰,能产生气泡的是过氧化氢溶液,无明显现象的是水,可以区分,选项正确;
C、二氧化碳不可燃、不助燃,不能点燃CO 中的少量CO ,故不能用点燃的方法除掉二氧化碳中的少
2
量一氧化碳,选项错误;
D、锌的活动性比铜和银的都强,与 Cu(NO ) 和AgNO 溶液都能反应,加入过量Zn粉,过滤,所得溶
3 2 3
液是硝酸锌溶液,选项错误。故选B。
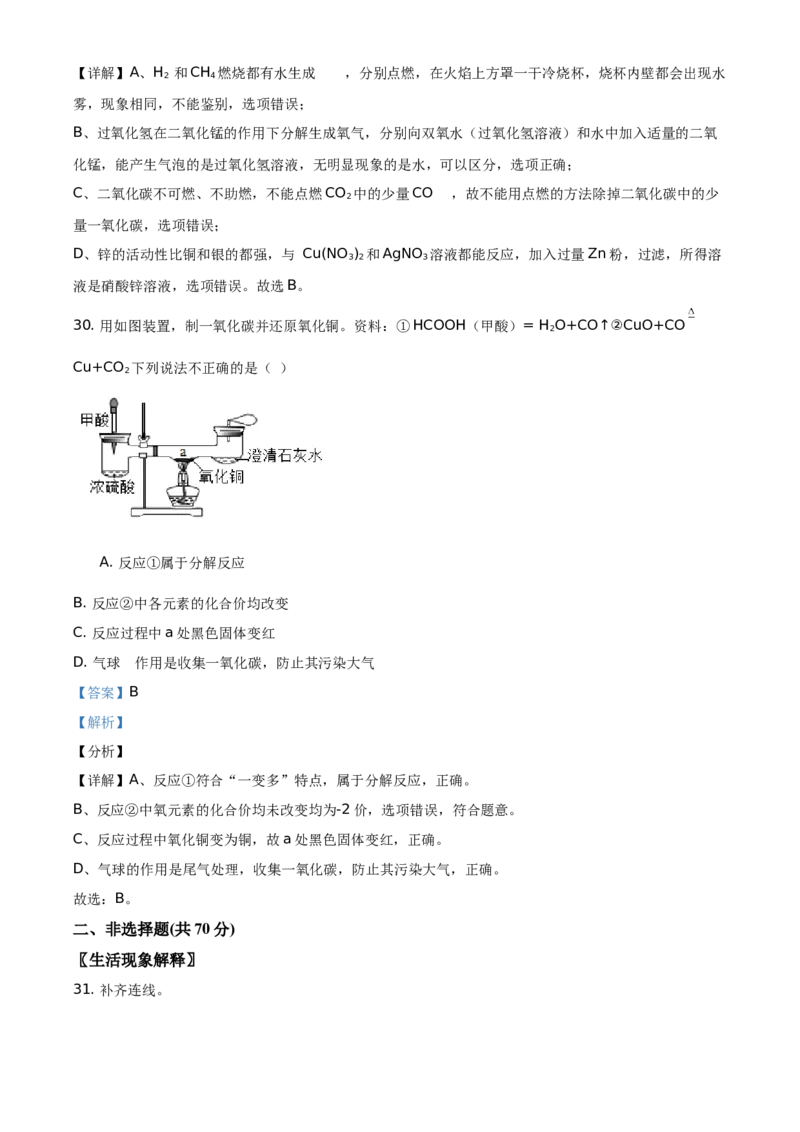
30. 用如图装置,制一氧化碳并还原氧化铜。资料:①HCOOH(甲酸)= H O+CO↑②CuO+CO
2
Cu+CO 下列说法不正确的是( )
2
A. 反应①属于分解反应
B. 反应②中各元素的化合价均改变
C. 反应过程中a处黑色固体变红
D. 气球 的作用是收集一氧化碳,防止其污染大气
【答案】B
【解析】
【分析】
【详解】A、反应①符合“一变多”特点,属于分解反应,正确。
B、反应②中氧元素的化合价均未改变均为-2价,选项错误,符合题意。
C、反应过程中氧化铜变为铜,故a处黑色固体变红,正确。
D、气球的作用是尾气处理,收集一氧化碳,防止其污染大气,正确。
故选:B。
二、非选择题(共70分)
〖生活现象解释〗
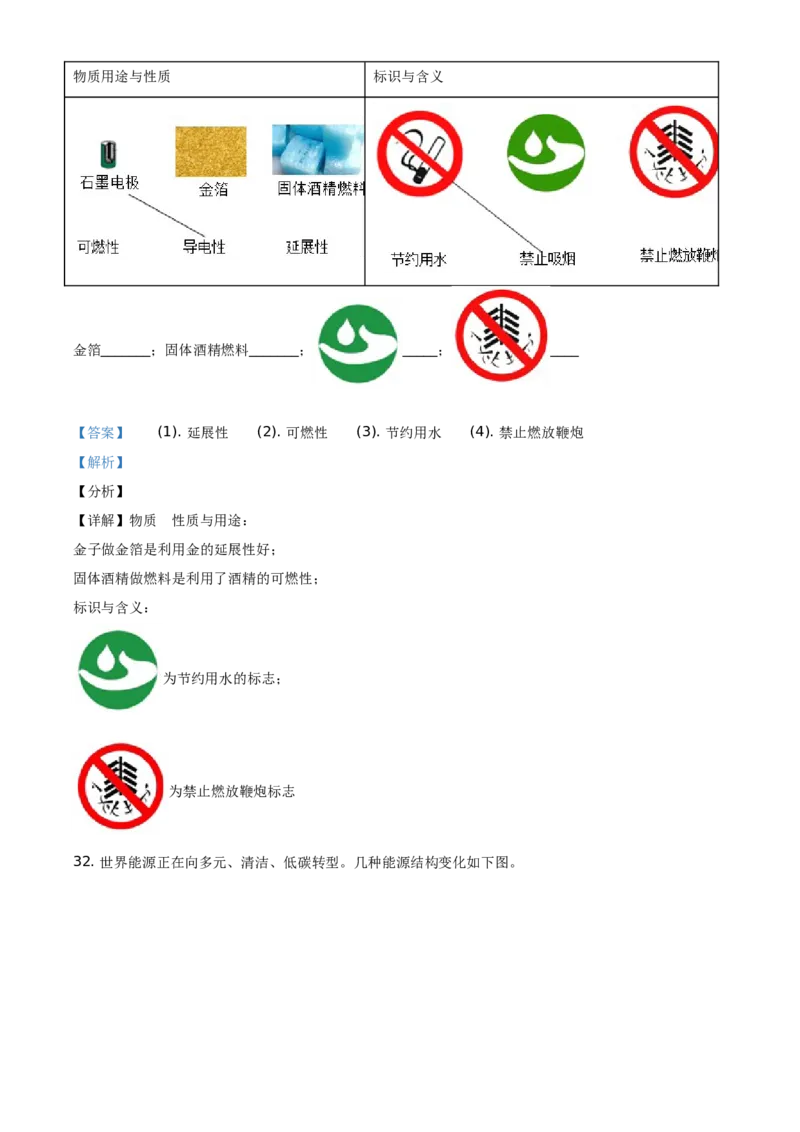
31. 补齐连线。物质用途与性质 标识与含义
金箔_______;固体酒精燃料_______; _____; ____
【答案】 (1). 延展性 (2). 可燃性 (3). 节约用水 (4). 禁止燃放鞭炮
【解析】
【分析】
【详解】物质 的性质与用途:
金子做金箔是利用金的延展性好;
固体酒精做燃料是利用了酒精的可燃性;
标识与含义:
为节约用水的标志;
为禁止燃放鞭炮标志
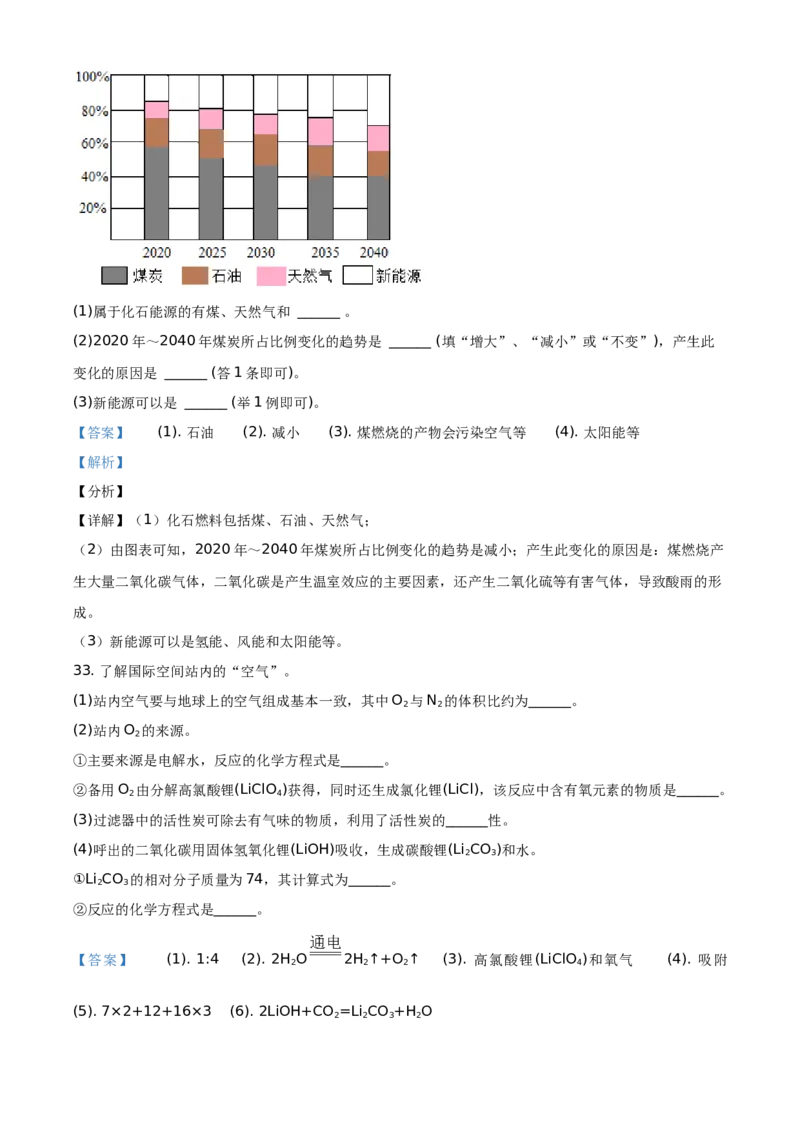
32. 世界能源正在向多元、清洁、低碳转型。几种能源结构变化如下图。(1)属于化石能源的有煤、天然气和 ______ 。
(2)2020年~2040年煤炭所占比例变化的趋势是 ______ (填“增大”、“减小”或“不变”),产生此
变化的原因是 ______ (答1条即可)。
(3)新能源可以是 ______ (举1例即可)。
【答案】 (1). 石油 (2). 减小 (3). 煤燃烧的产物会污染空气等 (4). 太阳能等
【解析】
【分析】
【详解】(1)化石燃料包括煤、石油、天然气;
(2)由图表可知,2020年~2040年煤炭所占比例变化的趋势是减小;产生此变化的原因是:煤燃烧产
生大量二氧化碳气体,二氧化碳是产生温室效应的主要因素,还产生二氧化硫等有害气体,导致酸雨的形
成。
(3)新能源可以是氢能、风能和太阳能等。
33. 了解国际空间站内的“空气”。
(1)站内空气要与地球上的空气组成基本一致,其中O 与N 的体积比约为______。
2 2
(2)站内O 的来源。
2
①主要来源是电解水,反应的化学方程式是______。
②备用O 由分解高氯酸锂(LiClO )获得,同时还生成氯化锂(LiCl),该反应中含有氧元素的物质是______。
2 4
(3)过滤器中的活性炭可除去有气味的物质,利用了活性炭的______性。
(4)呼出的二氧化碳用固体氢氧化锂(LiOH)吸收,生成碳酸锂(Li CO )和水。
2 3
①Li CO 的相对分子质量为74,其计算式为______。
2 3
②反应的化学方程式是______。
【答案】 (1). 1:4 (2). 2H O 2H ↑+O ↑ (3). 高氯酸锂(LiClO )和氧气 (4). 吸附
2 2 2 4
(5). 7×2+12+16×3 (6). 2LiOH+CO =Li CO +H O
2 2 3 2【解析】
【分析】
【详解】(1)从空气的成分按体积分数计算大约是:大约是氮气占(78%),氧气占(21%),O 与
2
N 的体积比约为1:4;
2
(2)①水通电分解成水和氧气,反应方程式为:2H O 2H ↑+O ↑;
2 2 2
②备用O 由分解高氯酸锂(LiClO )获得,同时还生成氯化锂(LiCl),该反应中含有氧元素的物质是高氯酸
2 4
锂(LiClO )和氧气;
4
(3)过滤器中的活性炭可除去有气味的物质,利用了活性炭的吸附性;
(4)①Li CO 的相对分子质量为74,其计算式为:7×2+12+16×3;
2 3
②二氧化碳用固体氢氧化锂(LiOH)吸收,生成碳酸锂(Li CO )和水,反应方程式为:
2 3
2LiOH+CO =Li CO +H O。
2 2 3 2
34. 食品包装袋内常有下列物品。
(1)用化学方程式表示石灰干燥剂的吸水原理______。
(2)铁粉脱氧剂的保鲜原理与铁生锈相同。铁生锈的条件是______。
(3)酒精保鲜片以淀粉、二氧化硅(SiO )为载体,吸附酒精制成。
2
①SiO 属于______(填序号,下同)。
2
A 混合物 B 单质 C 氧化物
②酒精挥发过程中不发生改变的是______。
A 分子的种类 B 分子间的间隔 C 分子质量
【答案】 (1). CaO+H O=Ca(OH) (2). 接触水和氧气 (3). C (4). AC
2 2
【解析】
【分析】
【详解】(1)石灰干燥剂有效成分为氧化钙,氧化钙与水反应生成氢氧化钙,反应方程式为:
CaO+H O=Ca(OH) ;
2 2(2)铁生锈需要与水蒸气和氧气同时接触;
(3)①二氧化硅由硅和氧两种元素组成,属于氧化物;故选:C。
②酒精挥发,是由液态变成气态,分子的种类、分子的质量不会发生改变,发生改变的是分子间的间隔,
故选:AC。
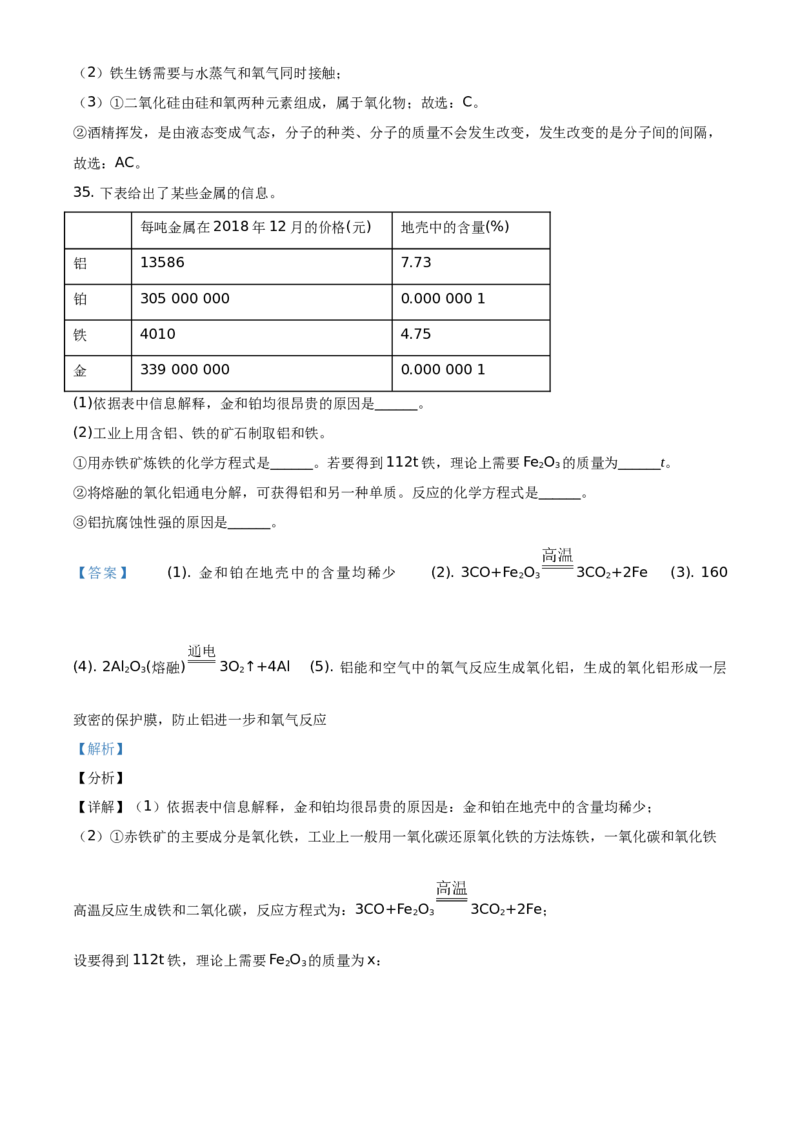
35. 下表给出了某些金属的信息。
每吨金属在2018年12月的价格(元) 地壳中的含量(%)
铝 13586 7.73
铂 305 000 000 0.000 000 1
铁 4010 4.75
金 339 000 000 0.000 000 1
(1)依据表中信息解释,金和铂均很昂贵的原因是______。
(2)工业上用含铝、铁的矿石制取铝和铁。
①用赤铁矿炼铁的化学方程式是______。若要得到112t铁,理论上需要Fe O 的质量为______t。
2 3
②将熔融的氧化铝通电分解,可获得铝和另一种单质。反应的化学方程式是______。
③铝抗腐蚀性强的原因是______。
【答案】 (1). 金和铂在地壳中的含量均稀少 (2). 3CO+Fe O 3CO +2Fe (3). 160
2 3 2
(4). 2Al O (熔融) 3O ↑+4Al (5). 铝能和空气中的氧气反应生成氧化铝,生成的氧化铝形成一层
2 3 2
致密的保护膜,防止铝进一步和氧气反应
【解析】
【分析】
【详解】(1)依据表中信息解释,金和铂均很昂贵的原因是:金和铂在地壳中的含量均稀少;
(2)①赤铁矿的主要成分是氧化铁,工业上一般用一氧化碳还原氧化铁的方法炼铁,一氧化碳和氧化铁
高温反应生成铁和二氧化碳,反应方程式为:3CO+Fe O 3CO +2Fe;
2 3 2
设要得到112t铁,理论上需要Fe O 的质量为x:
2 3x=160t
②根据质量守恒定律,化学反应前后原子的种类和数目不变,可知生成的另一种单质是氧气,反应的方程
式为:2Al O (熔融) 3O ↑+4Al;
2 3 2
③铝的抗腐蚀性强的原因是因为铝能和空气中的氧气反应生成氧化铝,生成的氧化铝形成一层致密的保护
膜,防止铝进一步和氧气反应。
〖科普阅读理解〗
36. 阅读下面科普短文。
葡萄是深受人们喜爱的水果之一。但由于葡萄果皮薄、果肉柔软,难以保存。葡萄的保鲜方法很多,常用
的有冰温高湿保鲜法、SO 保鲜法等。
2
冰温高湿保鲜法。在贮藏过程中,葡萄中的糖(C H O )、VC(C H O )、水份等含量会因温度和湿度的波
6 12 6 6 8 6
动而变化。将葡萄贮藏在其冻结点(0℃以下)的范围内、湿度保持在90%以上,能使其生理活性降至最低,
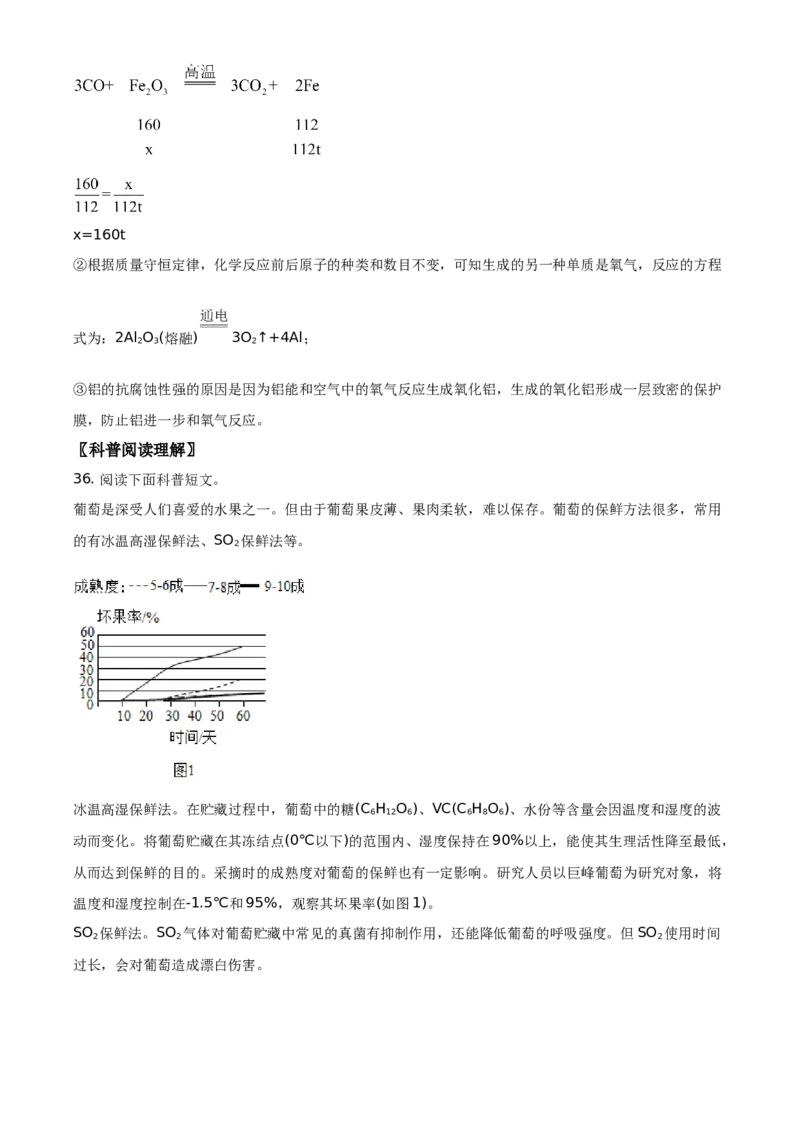
从而达到保鲜的目的。采摘时的成熟度对葡萄的保鲜也有一定影响。研究人员以巨峰葡萄为研究对象,将
温度和湿度控制在-1.5℃和95%,观察其坏果率(如图1)。
SO 保鲜法。SO 气体对葡萄贮藏中常见的真菌有抑制作用,还能降低葡萄的呼吸强度。但SO 使用时间
2 2 2
过长,会对葡萄造成漂白伤害。表1不同葡萄品种出现漂白伤害的时间(0℃)
红宝石 红地球 玫瑰香 龙眼
时间(天) 24 32 58 72
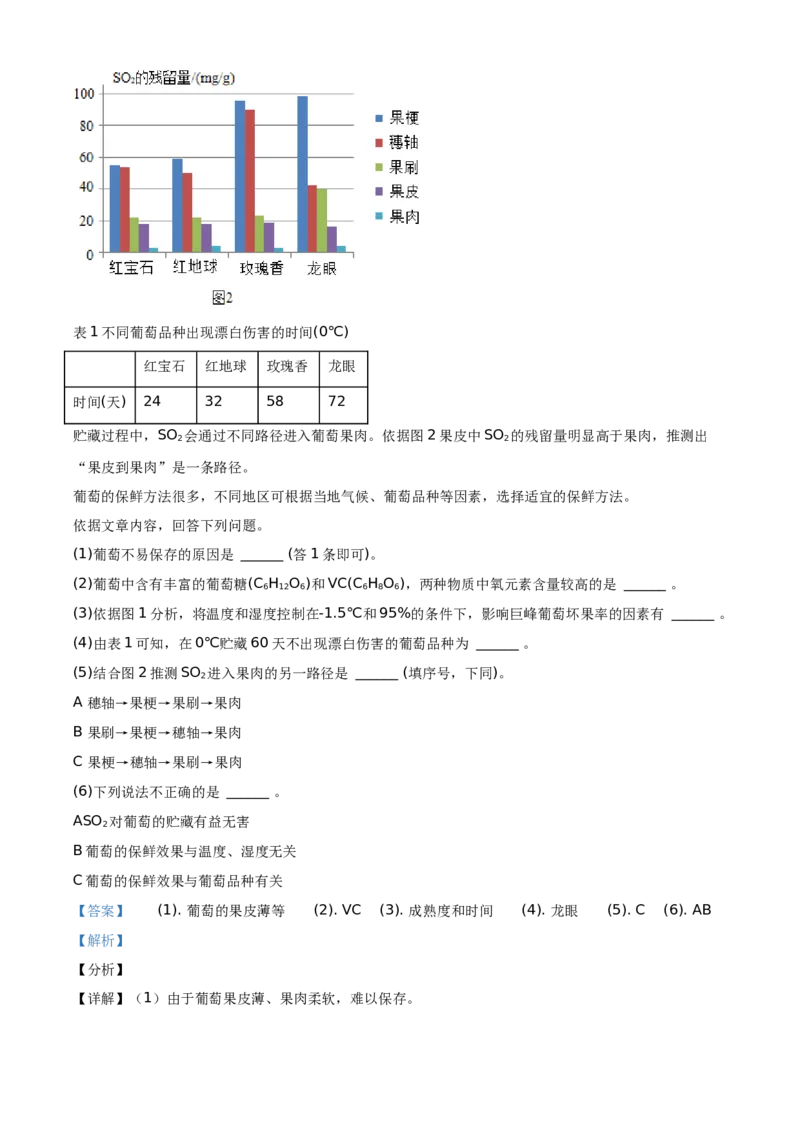
贮藏过程中,SO 会通过不同路径进入葡萄果肉。依据图2果皮中SO 的残留量明显高于果肉,推测出
2 2
“果皮到果肉”是一条路径。
葡萄的保鲜方法很多,不同地区可根据当地气候、葡萄品种等因素,选择适宜的保鲜方法。
依据文章内容,回答下列问题。
(1)葡萄不易保存的原因是 ______ (答1条即可)。
(2)葡萄中含有丰富的葡萄糖(C H O )和VC(C H O ),两种物质中氧元素含量较高的是 ______ 。
6 12 6 6 8 6
(3)依据图1分析,将温度和湿度控制在-1.5℃和95%的条件下,影响巨峰葡萄坏果率的因素有 ______ 。
(4)由表1可知,在0℃贮藏60天不出现漂白伤害的葡萄品种为 ______ 。
(5)结合图2推测SO 进入果肉的另一路径是 ______ (填序号,下同)。
2
A 穗轴→果梗→果刷→果肉
B 果刷→果梗→穗轴→果肉
C 果梗→穗轴→果刷→果肉
(6)下列说法不正确的是 ______ 。
ASO 对葡萄的贮藏有益无害
2
B葡萄的保鲜效果与温度、湿度无关
C葡萄的保鲜效果与葡萄品种有关
【答案】 (1). 葡萄的果皮薄等 (2). VC (3). 成熟度和时间 (4). 龙眼 (5). C (6). AB
【解析】
【分析】
【详解】(1)由于葡萄果皮薄、果肉柔软,难以保存。(2)葡萄糖(C H O )中氧元素质量分数为:
6 12 6
VC(C H O ) 中氧元素质量分数为:
6 8 6
通过比较可知VC中氧元素的含量高。
(3)从图表可以看出随着时间的增长坏果率增多,且9-10成成熟的葡萄明显坏果率高,所以影响巨峰葡
萄坏果率的因素有成熟度和时间;
(4)由表1可知,在0℃贮藏60天不出现漂白伤害的葡萄品种为龙眼,在贮藏72天后才出现漂白伤害;
(5)由图2各部位二氧化硫含量推测SO 进入果肉的另一路径是:果梗→穗轴→果刷→果肉,故选:
2
C。
(6)A SO 使用时间过长,会对葡萄造成漂白伤害,故选项错误;
2
B在贮藏过程中,葡萄中的糖(C H O )、VC(C H O )、水份等含量会因温度和湿度的波动而变化,所以
6 12 6 6 8 6
葡萄的保鲜效果与温度、湿度有关,故选项错误;
C表1不同葡萄品种出现漂白伤害的时间不同,可知葡萄的保鲜效果与葡萄品种有关,故选项正确;
故选;AB.
〖生产实际分析〗
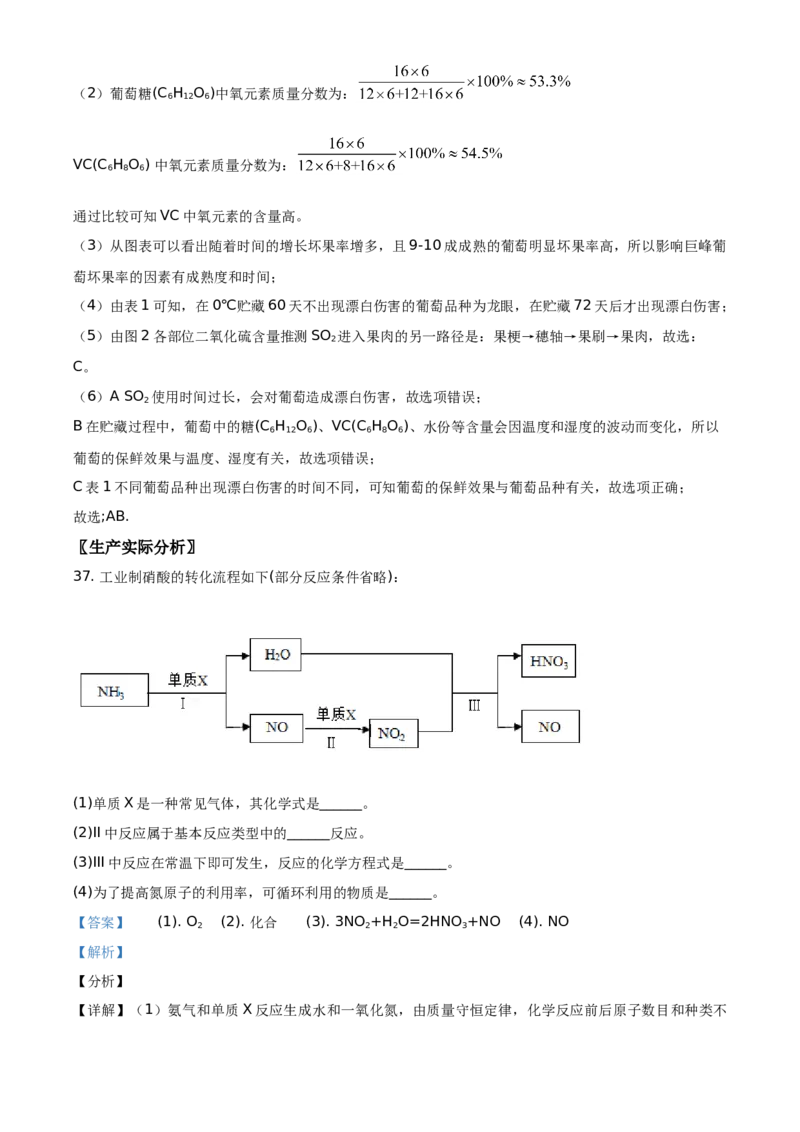
37. 工业制硝酸的转化流程如下(部分反应条件省略):
(1)单质X是一种常见气体,其化学式是______。
(2)II中反应属于基本反应类型中的______反应。
(3)III中反应在常温下即可发生,反应的化学方程式是______。
(4)为了提高氮原子的利用率,可循环利用的物质是______。
【答案】 (1). O (2). 化合 (3). 3NO +H O=2HNO +NO (4). NO
2 2 2 3
【解析】
【分析】
【详解】(1)氨气和单质X反应生成水和一氧化氮,由质量守恒定律,化学反应前后原子数目和种类不发生改变可知,单质X是氧气,因为生成物中有氮元素、氢元素和氧元素,反应物中氮元素和氢元素,所
以氧元素来自于X,单质X为O 。
2
(2)II为一氧化氮和氧气反应生成二氧化氮,反应物两种生成物一种,属于化合反应;
(3)反应III为水和二氧化氮反应生成硝酸和一氧化氮,反应方程式为:3NO +H O=2HNO +NO;
2 2 3
(4)由流程图可知,可循环利用的物质是一氧化氮。
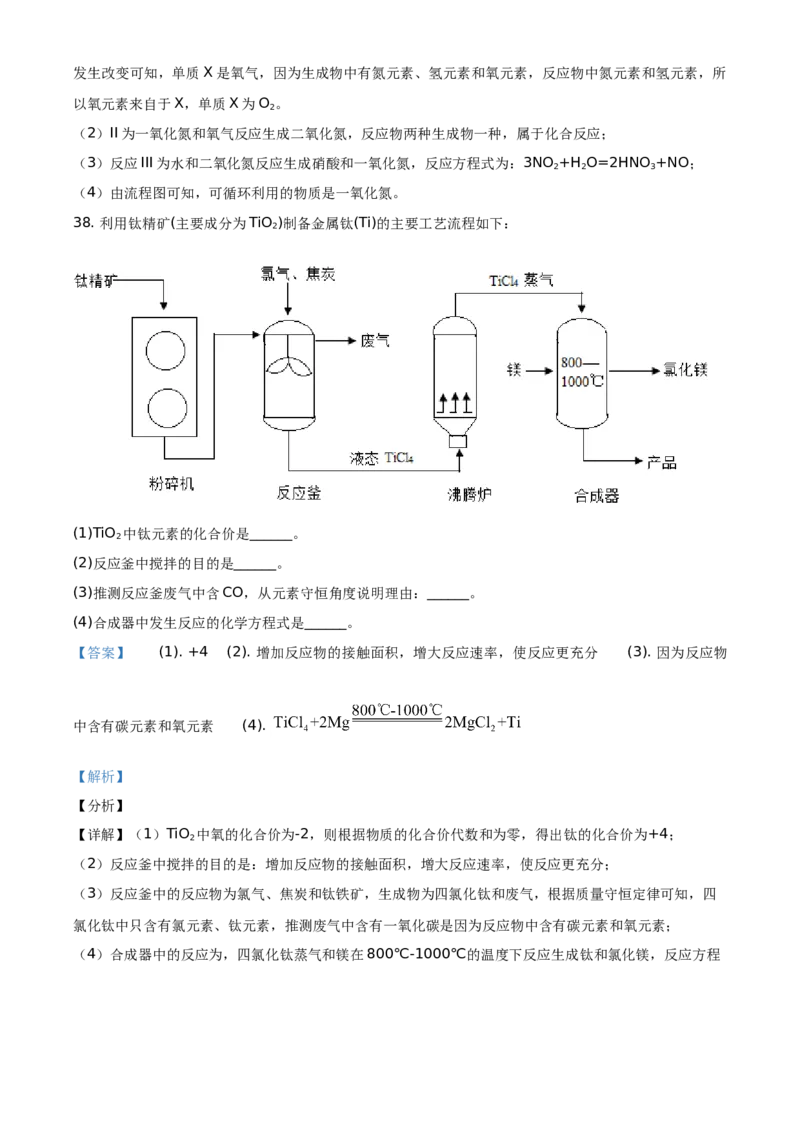
38. 利用钛精矿(主要成分为TiO )制备金属钛(Ti)的主要工艺流程如下:
2
(1)TiO 中钛元素的化合价是______。
2
(2)反应釜中搅拌的目的是______。
(3)推测反应釜废气中含CO,从元素守恒角度说明理由:______。
(4)合成器中发生反应的化学方程式是______。
【答案】 (1). +4 (2). 增加反应物的接触面积,增大反应速率,使反应更充分 (3). 因为反应物
中含有碳元素和氧元素 (4).
【解析】
【分析】
【详解】(1)TiO 中氧的化合价为-2,则根据物质的化合价代数和为零,得出钛的化合价为+4;
2
(2)反应釜中搅拌的目的是:增加反应物的接触面积,增大反应速率,使反应更充分;
(3)反应釜中的反应物为氯气、焦炭和钛铁矿,生成物为四氯化钛和废气,根据质量守恒定律可知,四
氯化钛中只含有氯元素、钛元素,推测废气中含有一氧化碳是因为反应物中含有碳元素和氧元素;
(4)合成器中的反应为,四氯化钛蒸气和镁在800℃-1000℃的温度下反应生成钛和氯化镁,反应方程式为: 。
〖基本实验及其原理分析〗
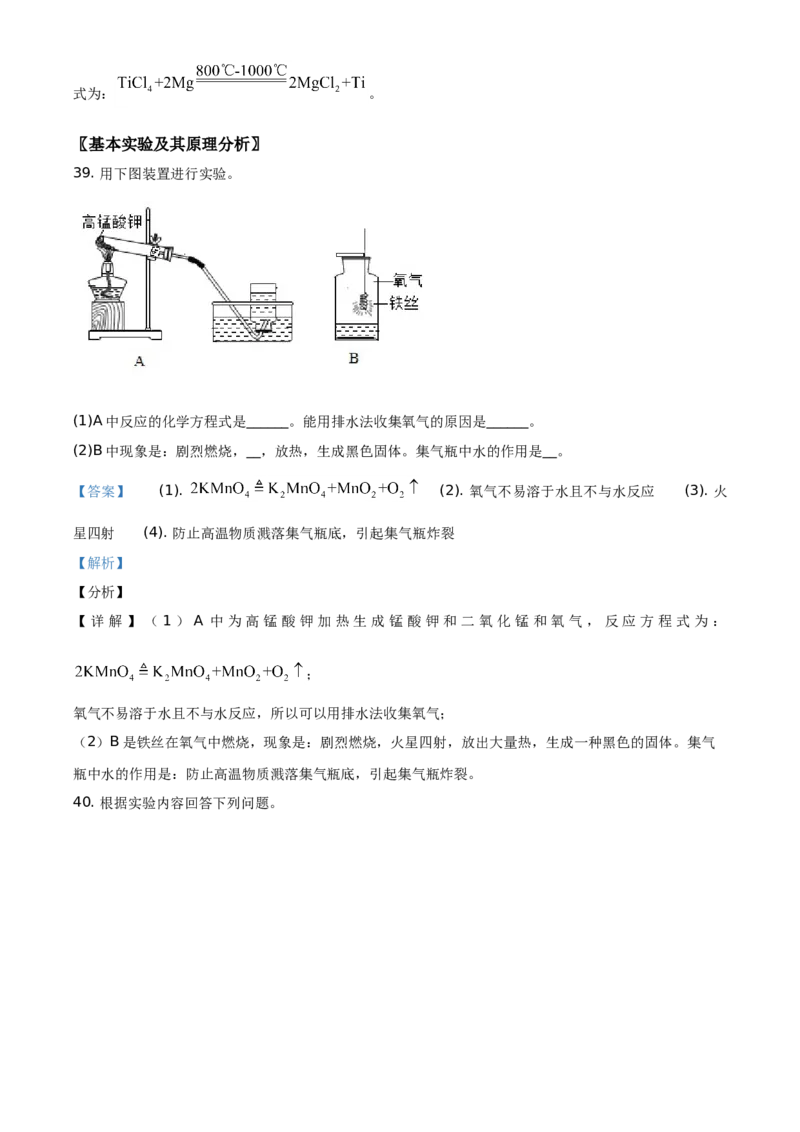
39. 用下图装置进行实验。
(1)A中反应的化学方程式是______。能用排水法收集氧气的原因是______。
(2)B中现象是:剧烈燃烧,__,放热,生成黑色固体。集气瓶中水的作用是__。
【答案】 (1). (2). 氧气不易溶于水且不与水反应 (3). 火
星四射 (4). 防止高温物质溅落集气瓶底,引起集气瓶炸裂
【解析】
【分析】
【详解】( 1)A 中为高锰酸钾加热生成锰酸钾和二氧化锰和氧气,反应方程式为:
;
氧气不易溶于水且不与水反应,所以可以用排水法收集氧气;
(2)B是铁丝在氧气中燃烧,现象是:剧烈燃烧,火星四射,放出大量热,生成一种黑色的固体。集气
瓶中水的作用是:防止高温物质溅落集气瓶底,引起集气瓶炸裂。
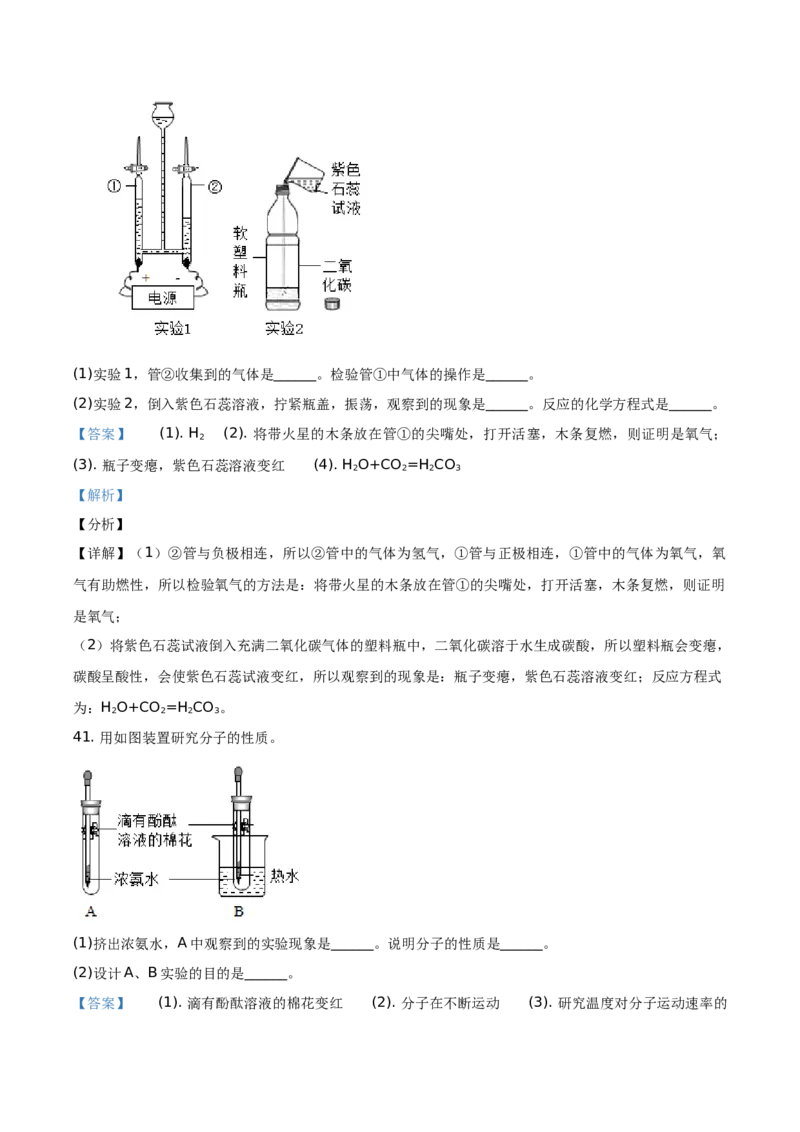
40. 根据实验内容回答下列问题。(1)实验1,管②收集到的气体是______。检验管①中气体的操作是______。
(2)实验2,倒入紫色石蕊溶液,拧紧瓶盖,振荡,观察到的现象是______。反应的化学方程式是______。
【答案】 (1). H (2). 将带火星的木条放在管①的尖嘴处,打开活塞,木条复燃,则证明是氧气;
2
(3). 瓶子变瘪,紫色石蕊溶液变红 (4). H O+CO =H CO
2 2 2 3
【解析】
【分析】
【详解】(1)②管与负极相连,所以②管中的气体为氢气,①管与正极相连,①管中的气体为氧气,氧
气有助燃性,所以检验氧气的方法是:将带火星的木条放在管①的尖嘴处,打开活塞,木条复燃,则证明
是氧气;
(2)将紫色石蕊试液倒入充满二氧化碳气体的塑料瓶中,二氧化碳溶于水生成碳酸,所以塑料瓶会变瘪,
碳酸呈酸性,会使紫色石蕊试液变红,所以观察到的现象是:瓶子变瘪,紫色石蕊溶液变红;反应方程式
为:H O+CO =H CO 。
2 2 2 3
41. 用如图装置研究分子的性质。
(1)挤出浓氨水,A中观察到的实验现象是______。说明分子的性质是______。
(2)设计A、B实验的目的是______。
【答案】 (1). 滴有酚酞溶液的棉花变红 (2). 分子在不断运动 (3). 研究温度对分子运动速率的影响
【解析】
【分析】
【详解】(1)氨水呈碱性,会使酚酞溶液变红,所以挤出浓氨水,A中观察到的实验现象是:滴有酚酞
溶液的棉花变红;说明分子的性质是:分子在不断运动;
(2)A与B的唯一变量是温度,同时挤入浓氨水,B中的棉花比A中棉花先变红,证明B中分子比A中
的分子运动的快,对比实验的目的是:研究温度对分子运动速率的影响。
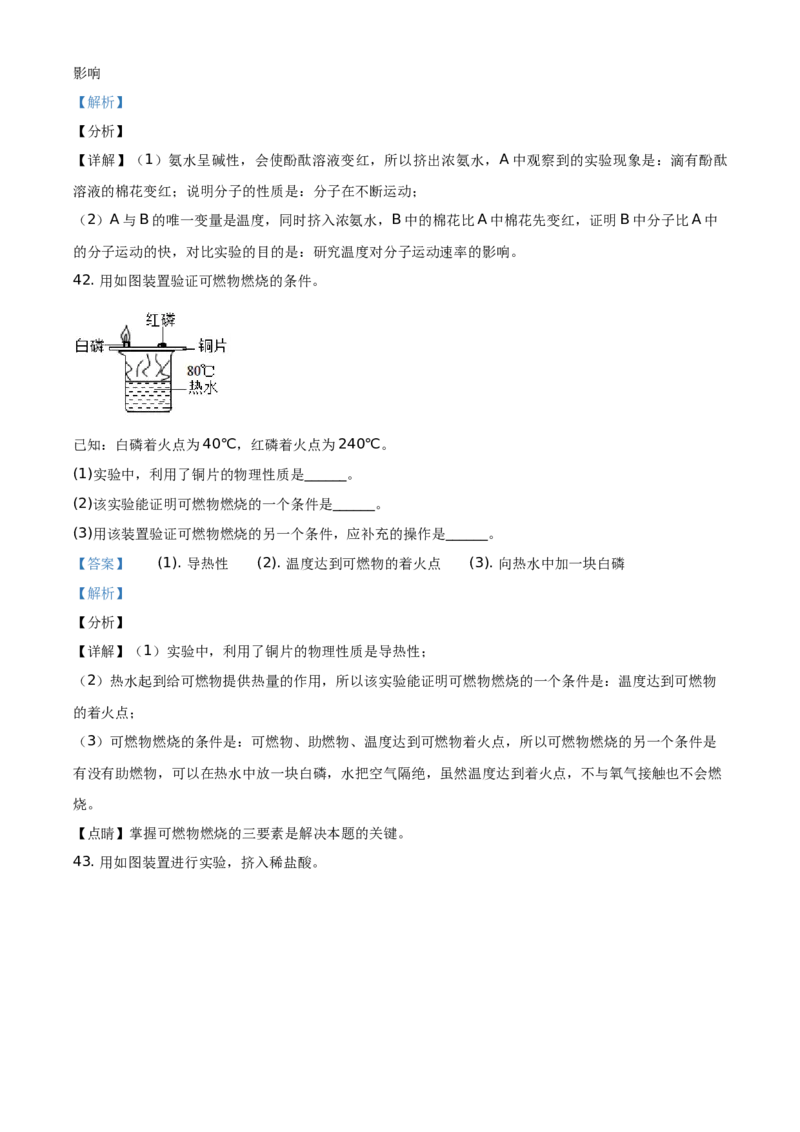
42. 用如图装置验证可燃物燃烧的条件。
已知:白磷着火点为40℃,红磷着火点为240℃。
(1)实验中,利用了铜片的物理性质是______。
(2)该实验能证明可燃物燃烧的一个条件是______。
(3)用该装置验证可燃物燃烧的另一个条件,应补充的操作是______。
【答案】 (1). 导热性 (2). 温度达到可燃物的着火点 (3). 向热水中加一块白磷
【解析】
【分析】
【详解】(1)实验中,利用了铜片的物理性质是导热性;
(2)热水起到给可燃物提供热量的作用,所以该实验能证明可燃物燃烧的一个条件是:温度达到可燃物
的着火点;
(3)可燃物燃烧的条件是:可燃物、助燃物、温度达到可燃物着火点,所以可燃物燃烧的另一个条件是
有没有助燃物,可以在热水中放一块白磷,水把空气隔绝,虽然温度达到着火点,不与氧气接触也不会燃
烧。
【点睛】掌握可燃物燃烧的三要素是解决本题的关键。
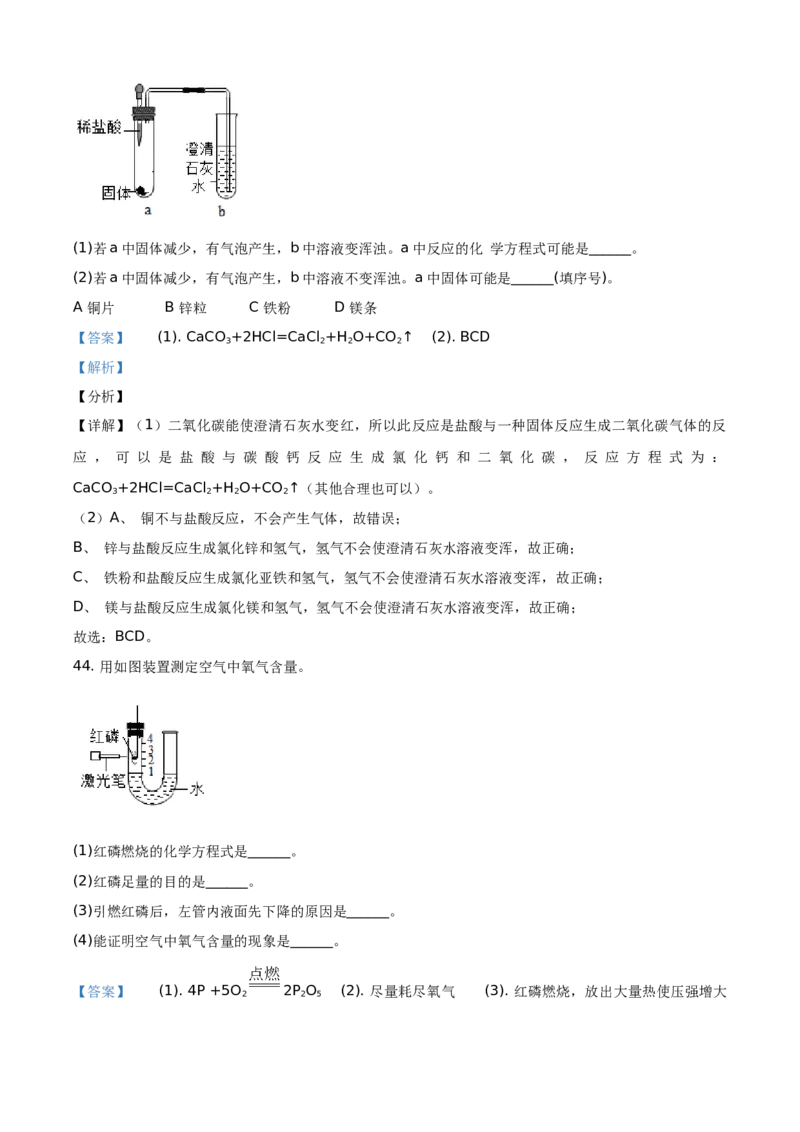
43. 用如图装置进行实验,挤入稀盐酸。(1)若a中固体减少,有气泡产生,b中溶液变浑浊。a中反应的化 学方程式可能是______。
(2)若a中固体减少,有气泡产生,b中溶液不变浑浊。a中固体可能是______(填序号)。
A 铜片 B 锌粒 C 铁粉 D 镁条
【答案】 (1). CaCO +2HCl=CaCl +H O+CO ↑ (2). BCD
3 2 2 2
【解析】
【分析】
【详解】(1)二氧化碳能使澄清石灰水变红,所以此反应是盐酸与一种固体反应生成二氧化碳气体的反
应 , 可 以 是 盐 酸 与 碳 酸 钙 反 应 生 成 氯 化 钙 和 二 氧 化 碳 , 反 应 方 程 式 为 :
CaCO +2HCl=CaCl +H O+CO ↑(其他合理也可以)。
3 2 2 2
(2)A、 铜不与盐酸反应,不会产生气体,故错误;
B、 锌与盐酸反应生成氯化锌和氢气,氢气不会使澄清石灰水溶液变浑,故正确;
C、 铁粉和盐酸反应生成氯化亚铁和氢气,氢气不会使澄清石灰水溶液变浑,故正确;
D、 镁与盐酸反应生成氯化镁和氢气,氢气不会使澄清石灰水溶液变浑,故正确;
故选:BCD。
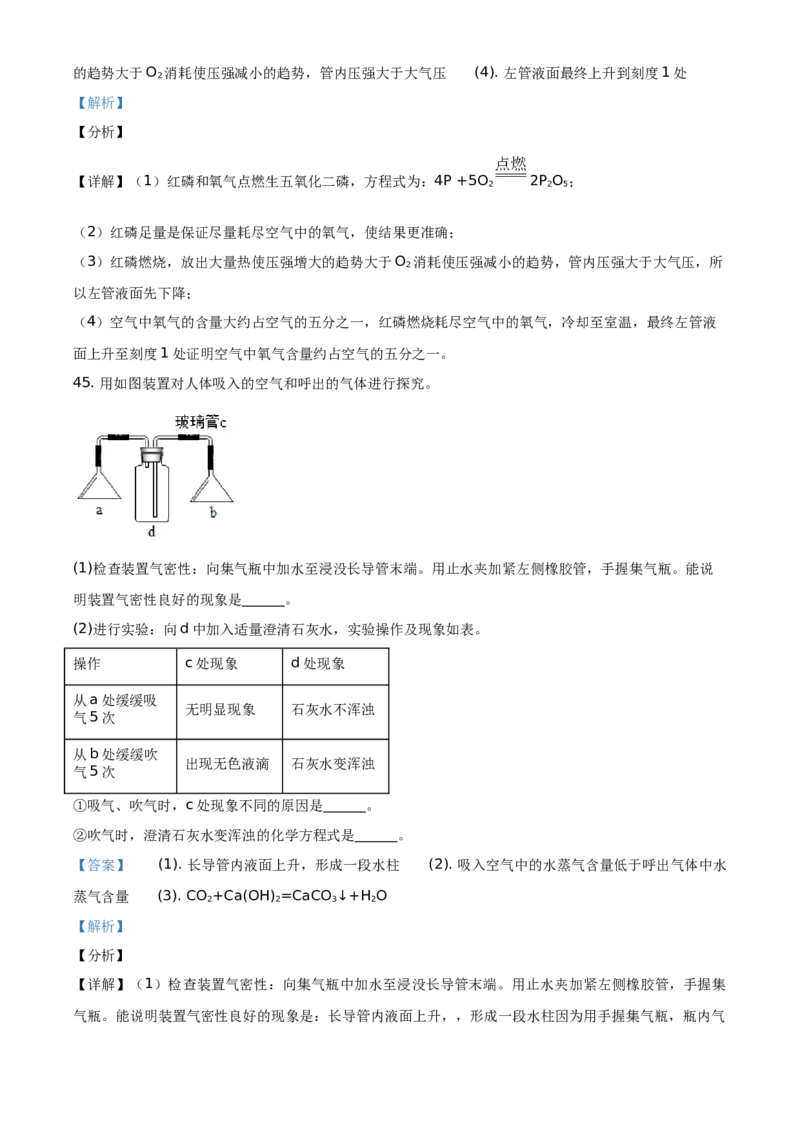
44. 用如图装置测定空气中氧气含量。
(1)红磷燃烧的化学方程式是______。
(2)红磷足量的目的是______。
(3)引燃红磷后,左管内液面先下降的原因是______。
(4)能证明空气中氧气含量的现象是______。
【答案】 (1). 4P +5O 2P O (2). 尽量耗尽氧气 (3). 红磷燃烧,放出大量热使压强增大
2 2 5的趋势大于O 消耗使压强减小的趋势,管内压强大于大气压 (4). 左管液面最终上升到刻度1处
2
【解析】
【分析】
【详解】(1)红磷和氧气点燃生五氧化二磷,方程式为:4P +5O 2P O ;
2 2 5
(2)红磷足量是保证尽量耗尽空气中的氧气,使结果更准确;
(3)红磷燃烧,放出大量热使压强增大的趋势大于O 消耗使压强减小的趋势,管内压强大于大气压,所
2
以左管液面先下降;
(4)空气中氧气的含量大约占空气的五分之一,红磷燃烧耗尽空气中的氧气,冷却至室温,最终左管液
面上升至刻度1处证明空气中氧气含量约占空气的五分之一。
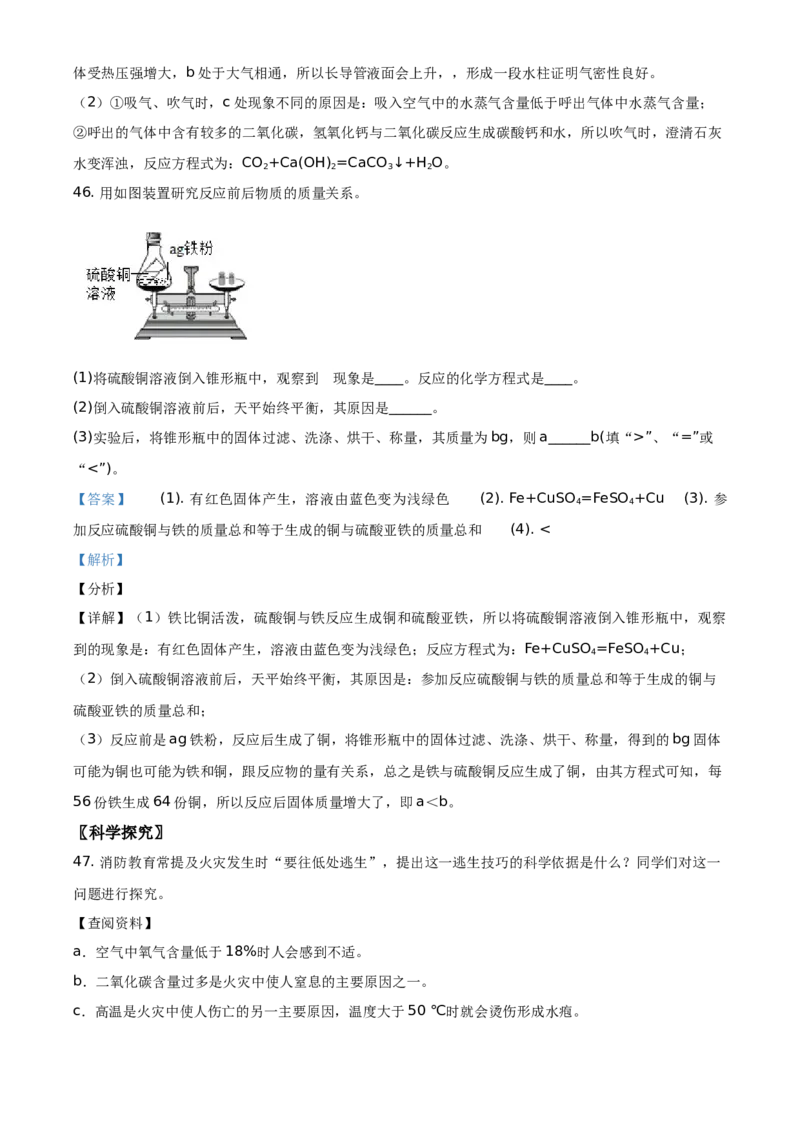
45. 用如图装置对人体吸入的空气和呼出的气体进行探究。
(1)检查装置气密性:向集气瓶中加水至浸没长导管末端。用止水夹加紧左侧橡胶管,手握集气瓶。能说
明装置气密性良好的现象是______。
(2)进行实验:向d中加入适量澄清石灰水,实验操作及现象如表。
操作 c处现象 d处现象
从a处缓缓吸
无明显现象 石灰水不浑浊
气5次
从b处缓缓吹
出现无色液滴 石灰水变浑浊
气5次
①吸气、吹气时,c处现象不同的原因是______。
②吹气时,澄清石灰水变浑浊的化学方程式是______。
【答案】 (1). 长导管内液面上升,形成一段水柱 (2). 吸入空气中的水蒸气含量低于呼出气体中水
蒸气含量 (3). CO +Ca(OH) =CaCO ↓+H O
2 2 3 2
【解析】
【分析】
【详解】(1)检查装置气密性:向集气瓶中加水至浸没长导管末端。用止水夹加紧左侧橡胶管,手握集
气瓶。能说明装置气密性良好的现象是:长导管内液面上升,,形成一段水柱因为用手握集气瓶,瓶内气体受热压强增大,b处于大气相通,所以长导管液面会上升,,形成一段水柱证明气密性良好。
(2)①吸气、吹气时,c处现象不同的原因是:吸入空气中的水蒸气含量低于呼出气体中水蒸气含量;
②呼出的气体中含有较多的二氧化碳,氢氧化钙与二氧化碳反应生成碳酸钙和水,所以吹气时,澄清石灰
水变浑浊,反应方程式为:CO +Ca(OH) =CaCO ↓+H O。
2 2 3 2
46. 用如图装置研究反应前后物质的质量关系。
(1)将硫酸铜溶液倒入锥形瓶中,观察到 的现象是____。反应的化学方程式是____。
(2)倒入硫酸铜溶液前后,天平始终平衡,其原因是______。
(3)实验后,将锥形瓶中的固体过滤、洗涤、烘干、称量,其质量为bg,则a______b(填“>”、“=”或
“<”)。
【答案】 (1). 有红色固体产生,溶液由蓝色变为浅绿色 (2). Fe+CuSO =FeSO +Cu (3). 参
4 4
加反应硫酸铜与铁的质量总和等于生成的铜与硫酸亚铁的质量总和 (4). <
【解析】
【分析】
【详解】(1)铁比铜活泼,硫酸铜与铁反应生成铜和硫酸亚铁,所以将硫酸铜溶液倒入锥形瓶中,观察
到的现象是:有红色固体产生,溶液由蓝色变为浅绿色;反应方程式为:Fe+CuSO =FeSO +Cu;
4 4
(2)倒入硫酸铜溶液前后,天平始终平衡,其原因是:参加反应硫酸铜与铁的质量总和等于生成的铜与
硫酸亚铁的质量总和;
(3)反应前是ag铁粉,反应后生成了铜,将锥形瓶中的固体过滤、洗涤、烘干、称量,得到的bg固体
可能为铜也可能为铁和铜,跟反应物的量有关系,总之是铁与硫酸铜反应生成了铜,由其方程式可知,每
56份铁生成64份铜,所以反应后固体质量增大了,即a<b。
〖科学探究〗
47. 消防教育常提及火灾发生时“要往低处逃生”,提出这一逃生技巧的科学依据是什么?同学们对这一
问题进行探究。
【查阅资料】
a.空气中氧气含量低于18%时人会感到不适。
b.二氧化碳含量过多是火灾中使人窒息的主要原因之一。
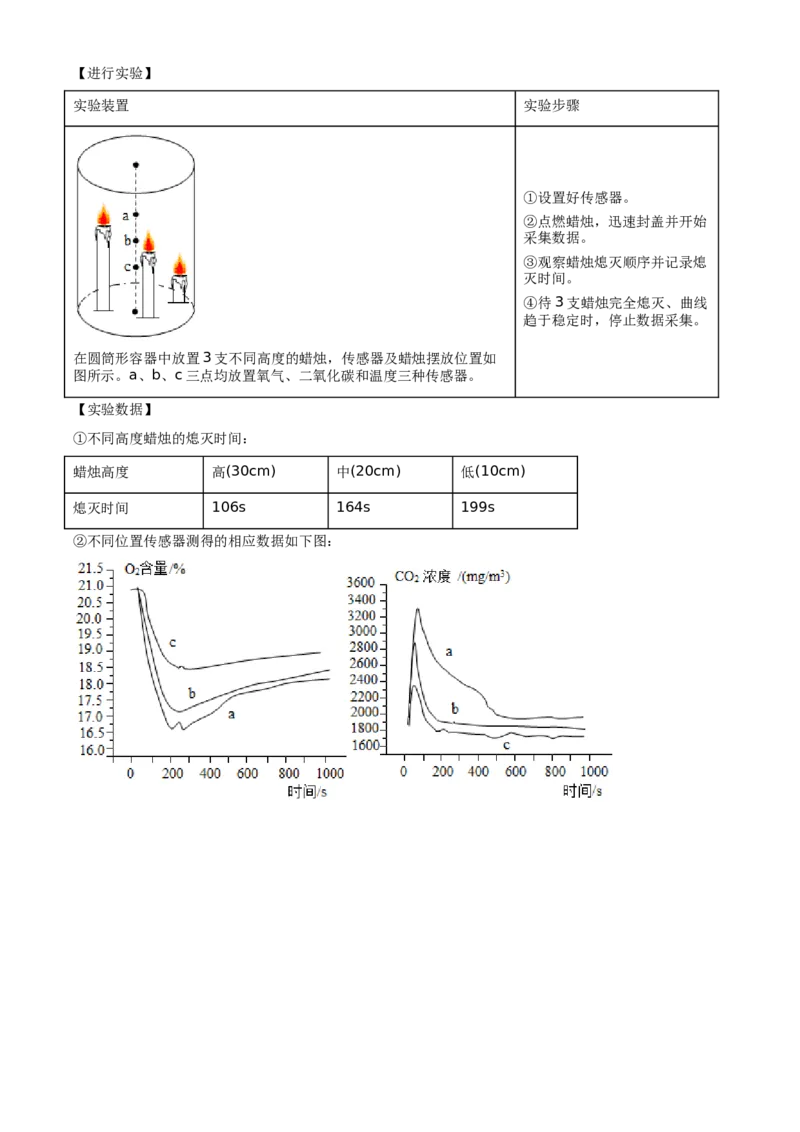
c.高温是火灾中使人伤亡的另一主要原因,温度大于50 ℃时就会烫伤形成水疱。【进行实验】
实验装置 实验步骤
①设置好传感器。
②点燃蜡烛,迅速封盖并开始
采集数据。
③观察蜡烛熄灭顺序并记录熄
灭时间。
④待3支蜡烛完全熄灭、曲线
趋于稳定时,停止数据采集。
在圆筒形容器中放置3支不同高度的蜡烛,传感器及蜡烛摆放位置如
图所示。a、b、c三点均放置氧气、二氧化碳和温度三种传感器。
【实验数据】
①不同高度蜡烛的熄灭时间:
蜡烛高度 高(30cm) 中(20cm) 低(10cm)
熄灭时间 106s 164s 199s
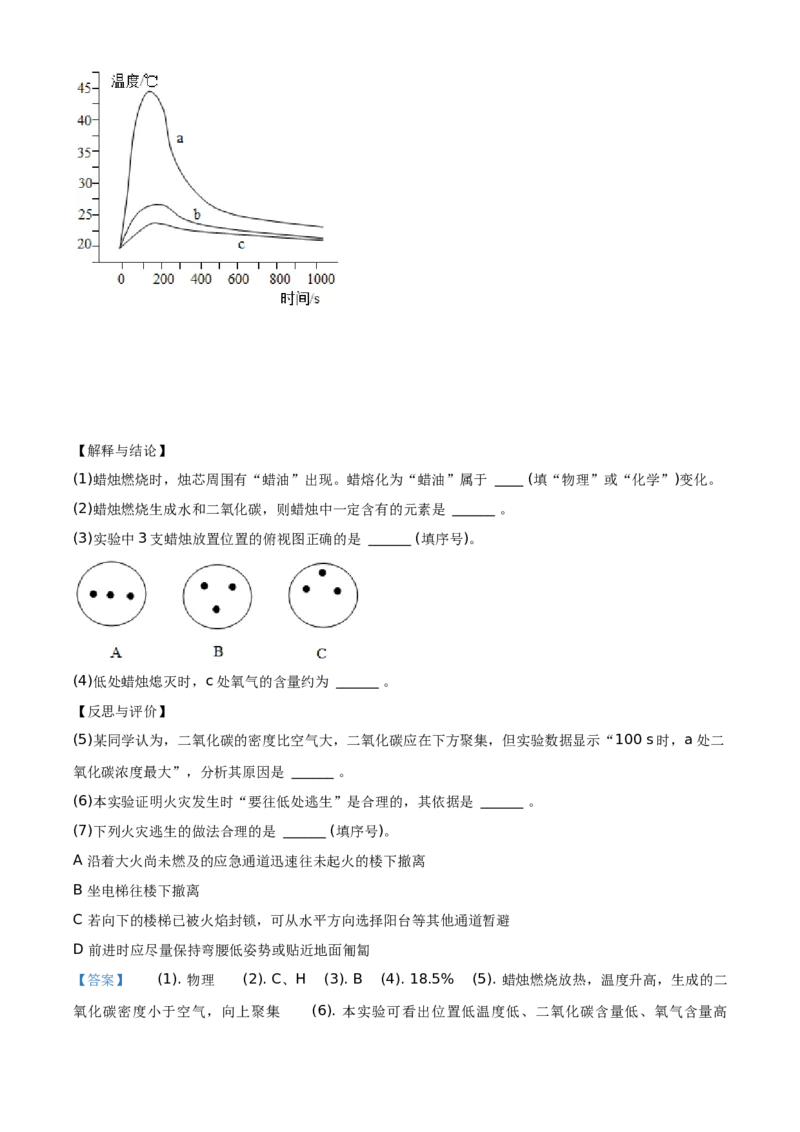
②不同位置传感器测得的相应数据如下图:【解释与结论】
(1)蜡烛燃烧时,烛芯周围有“蜡油”出现。蜡熔化为“蜡油”属于 ____ (填“物理”或“化学”)变化。
(2)蜡烛燃烧生成水和二氧化碳,则蜡烛中一定含有的元素是 ______ 。
(3)实验中3支蜡烛放置位置的俯视图正确的是 ______ (填序号)。
(4)低处蜡烛熄灭时,c处氧气的含量约为 ______ 。
【反思与评价】
(5)某同学认为,二氧化碳的密度比空气大,二氧化碳应在下方聚集,但实验数据显示“100 s时,a处二
氧化碳浓度最大”,分析其原因是 ______ 。
(6)本实验证明火灾发生时“要往低处逃生”是合理的,其依据是 ______ 。
(7)下列火灾逃生的做法合理的是 ______ (填序号)。
A 沿着大火尚未燃及的应急通道迅速往未起火的楼下撤离
B 坐电梯往楼下撤离
C 若向下的楼梯已被火焰封锁,可从水平方向选择阳台等其他通道暂避
D 前进时应尽量保持弯腰低姿势或贴近地面匍匐
【答案】 (1). 物理 (2). C、H (3). B (4). 18.5% (5). 蜡烛燃烧放热,温度升高,生成的二
氧化碳密度小于空气,向上聚集 (6). 本实验可看出位置低温度低、二氧化碳含量低、氧气含量高(7). ACD
【解析】
【分析】
【详解】(1)蜡烛熔化只是物质的状态发生了改变,没有新物质生成,属于物理变化;
(2)蜡烛燃烧生成水和二氧化碳,反应物中有氧气,水中含有氢元素和氧元素,二氧化碳中含有氧元素
和碳元素,根据质量守恒可知,化学反应前后原子数目及种类不变,生成物中含有C、H、O,反应物中
有氧气,那么C、H肯定来自于蜡烛,所以蜡烛中肯定含有C、H,可能含有O。
(3)由实验装置可以看出,实验中3支蜡烛放置位置的俯视图应该是B。
(4)由数据图可知,低处蜡烛熄灭时,c处氧气的含量约为18.25%;
(5)实验数据显示“100 s时,a处二氧化碳浓度最大”,原因是:蜡烛燃烧放热,温度升高,生成的二
氧化碳密度小于空气,向上聚集;
(6)由数据图可以看出,c处位置最低,c处的二氧化碳浓度最低,氧气含量最高,温度最低,所以火灾
发生时要往低处逃生。
(7)A 沿着大火尚未燃及的应急通道迅速往未起火的楼下撤离,正确;
B 发生火灾时可能会停电,所以不能乘坐电梯逃生,故错误;
C 若向下的楼梯已被火焰封锁,可从水平方向选择阳台等其他通道暂避,正确;
D 前进时应尽量保持弯腰低姿势或贴近地面匍匐,匍匐前进,防止被烟呛到,便于寻找安全出口,正确;
故选:ACD。本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635