文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
微专题 5 溶解度曲线及溶解度表分析
考向一 溶解度曲线分析
1、解答此类题目的关键
(1)明确溶解度曲线上点的含义(某点是在某温度时某物质的溶解度是多少g。交点是在某温度时,两物
质的溶解度相等。线上方的点表示是饱和溶液,下方的点表示不饱和溶液);
(2)明确物质的溶解度随温度变化的趋势(线越陡,表示该物质溶解度受温度影响较大);
(3)明确饱和溶液中溶质的质量大小的判断方法;
(4)明确判断溶质的质量分数大小关系的方法。
2、溶解度曲线:线的含义:三线:
①“陡升型” :大多数固体物的溶解度随温度升高而升高。如KNO;
3
② “缓升型”:少数固体物质的溶解度受温度的影响很小。如NaCl;
③“下降型”:极少数物质溶解度随温度升高而降低。如Ca(OH) 。
2
3、点的含义:四点:
①曲线上的点:所示某温度下某物质的溶解度是多少(该温度下饱和状态)。
②两曲线的交点:表示在该点所示的温度下,两种物质的溶解度相等。
③线上方的点表示:在该温度下,该溶液是饱和且有部分晶体;
④线下方的点表示:该温度下,该溶液是不饱和溶液。
1. 【2023四川内江真题】甲、乙两种物质的溶解度曲线如图所示,下列有关说法错误的是( )
A. 两种物质的溶解度都随温度升高而增大
B. t°C时,甲、乙两物质的溶液中溶质质量分数一定相等
1
C. 通常采用蒸发结晶的方法从乙的溶液中获得晶体
D. t°C时,在100g水中加入25g甲,可形成甲的不饱和溶液
2
【答案】B
【解析】A. 由溶解度曲线可知,两种物质的溶解度都随温度升高而增大,此选项正确;
B. t °C时,甲、乙两物质的溶解度相等,则t°C时,甲、乙两物质的饱和溶液中溶质质量分数一定相等,
1 1
此选项错误;
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C. 乙的溶解度受温度影响不大,对于溶解度受温度影响不大的物质,一般采用蒸发结晶法从溶液中获取晶
体,此选项正确;
D. 由溶解度曲线可知,t°C时,甲的溶解度大于25g,则在100g水中加入25g甲,可形成甲的不饱和溶
2
液,此选项正确。
故选B
2. 【2023四川乐山真题】气体的溶解度通常指压强为101 kPa和一定温度时,在1体积水里溶解达到饱和
状态时的气体体积。如图是甲、乙两种气体在101 kPa时的溶解度曲线,下列说法正确的是
A. 甲的溶解度大于乙的溶解度 B. 两种气体的溶解度都随温度升高而增大
C. 甲气体的溶解度受温度的影响小于乙 D. T℃时,气体乙的溶解度为2 g
【答案】C
【解析】A、溶解度比较,应指明温度,否则无法比较,不符合题意;
B、由图可知,两种气体的溶解度都随温度升高而减小,不符合题意;
C、由图可知,两种气体的溶解度都随温度升高而减小,且甲的溶解度受温度影响比乙小,符合题意;
D、气体的溶解度通常指压强为101 kPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积,单
位不是“g”,不符合题意。
故选C。
3. 【2023湖南郴州真题】甲、乙、丙三种固体物质的溶解度曲线如下图所示。回答下列问题:
(1)T℃时,甲、乙、丙的溶解度由大到小的顺序是_______。
3
(2)甲和乙溶解度相同时,对应的温度是_______。
(3)图中表示甲不饱和溶液的点是_______。
(4)图中与气体溶解度变化规律相似的曲线是_______。
(5)T℃时,将50g甲放入100g水里,充分溶解,所得溶液的质量为_______g。
1
【答案】(1)甲>乙=丙
(2)T℃
1
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)D
(4)丙物质的溶解度曲线
(5)125
【解析】(1)据图可知,T℃时,甲、乙、丙的溶解度由大到小的顺序是甲>乙=丙。
3
(2)据图可知,T℃时,甲和乙溶解度相同。
1
(3)A点、C点位于甲物质溶解度曲线上,表示甲物质溶液恰好饱和;B点位于甲物质溶解度曲线的上
方,表示甲物质溶液已经达到饱和,且还有未溶解的固体;D点位于甲物质溶解度曲线的下方,表示的是
甲物质的不饱和溶液。故填:D。
(4)气体溶解度随温度升高而减小,据图可知,丙物质的溶解度随温度升高而减小,所以图中与气体溶
解度变化规律相似的曲线是丙物质的溶解度曲线。
(5)据图可知,T℃时,甲物质溶解度是25g,即100g水里最多溶解甲物质25g。所以T℃时,将50g甲
1 1
放入100g水里,充分溶解,只能溶解甲25g,所得溶液的质量=100g+25g=125g。
考向二 溶解度表分析
1、固体的溶解度
概念 固体物质溶解度指的是在 一定温度下 ,某固态物质在 100 g 溶剂 里达到 饱和状态 时所
溶解的质量。
四要素 ①、条件 : 一定温度 ②、标准 : 100 g 溶剂 ③、状态 : 饱和状态 ④、单位 : g 。
影响因素 内因 溶剂种类、溶质种类;
外因 温度。
变化规律 大多数固体物质的溶解度随温度升高而升高。 如KNO。
3
少数固体物质的溶解度受温度的影响很小。 如NaCl。
极少数固体物质的溶解度随温度升高而降低。 如Ca(OH) 。
2
2、气体的溶解度
概念 气体的溶解度是指气体物质在 _ 一定压强 _ 、一定温度下一体积水最多溶解气体的体积分数来表
示。
影响 内因 溶剂种类、溶质种类;
因素
外因 温 在一定压强下,温度越高气体的溶解度越小,温度越低气体的溶解度越大;
度。
压 在一定温度下,压强越大气体的溶解度越大,压强越小气体的溶解度越小
强。
1. 【2022四川泸州】已知:温度超过35℃时,NH HCO 开始分解,其溶解度表如下。下列说法正确的是
4 3
( )
温度/℃ 0 10 20 30
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
NH HCO 溶解度(g/100g水) 11.9 15.8 21.0 27.0
4 3
A. 用NH HCO 晶体配制浓溶液时,可加热煮沸以加快溶解
4 3
B. NH HCO 是铵态复合肥料,与其它肥料都可以混合使用
4 3
C. 20℃时,50.0g蒸馏水就能使11.0g NH HCO 晶体完全溶解
4 3
D. 127.0g NH HCO 饱和溶液,由30℃降至20℃可析出6.0g晶体
4 3
【答案】D
【解析】A、温度超过35℃时,NH HCO 开始分解。所以用碳酸氢铵晶体配制浓溶液时,不能加热煮沸,
4 3
以防止碳酸氢铵受热分解,故A错误;
B、复合肥中含有氮、磷、钾元素中的两种及以上的营养元素,而碳酸氢铵中所含有的营养元素只有氮元
素,故碳酸氢铵属于氮肥,不是复合肥;铵态氮肥和碱性物质混用时,会有氨气移出,从而降低铵态氮肥
肥效,故碳酸氢铵不能和碱性物质混用,故B错误;
C、20℃时碳酸氢铵的溶解度为21.0g,即该温度下100g水中最多溶解碳酸氢铵的质量为21.0g,所以该温
度下50g水中对多溶解的碳酸氢铵质量为10.5g<11.0g,故碳酸氢铵晶体不能完全溶解,故C错误;
D、30℃时127.0g 碳酸氢铵饱和溶液中,含有溶质碳酸氢铵质量为27.0g,溶剂水的质量为100g。该饱和
溶液由30℃降至20℃时,碳酸氢铵溶解度由27.0g降低到21.0g,所以30℃时127.0g的碳酸氢铵饱和溶液
降温到20℃时,可析出6.0g晶体,故D正确;
故选D。
2.【2023湖北武汉真题】化学兴趣小组探究碳酸氢钠、氯化钾、氯化钠和氯化铵的溶解性时,查阅资料如
下:
表1物质在不同温度时的溶解度
温度/℃ 0 10 20 30
NaHCO 6.9 8.2 9.6 11.1
3
KCl 27.6 31.0 34.0 37.0
溶解度/g
NaCl 35.7 35.8 36.0 36.3
NH Cl 29.4 33.3 37.2 41.4
4
表2溶解度的相对大小(20℃)
溶解度/g 一般称为
<0.01 难溶
0.01~1 微溶
1~10 可溶
>10 易溶
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
回答下列问题:
(1)10℃时,NaCl的溶解度为______。
(2)根据20℃时上述四种物质的溶解度,判断其中属于“可溶”的物质是______。
(3)将30℃时上述四种物质的饱和溶液各ag分别降温到0℃,析出同体质量最大的物质是______。
(4)20℃时,将氯化钠和氯化铵各mg分别放入两只烧杯中,再分别加入ng水,充分搅拌。下列说法正
确的是______。(填标号)
A. 若两只烧杯中均无固体剩余,则所得氯化铵溶液一定是不饱和溶液
B. 若两只烧杯中均有固体剩余,则所得溶液中溶质的质量分数:氯化铵>氯化钠
C. 若m≤0.36,则所得溶液中溶质的质量分数:氯化铵=氯化钠
D. 若所得溶液中只有一种是饱和溶液,则0.36n≤m≤0.372n
【答案】(1)35.8g
(2)碳酸氢钠或NaHCO
3
(3)氯化铵或NH Cl
4
(4)AB
【解析】(1)由表1知,10℃时,NaCl的溶解度为35.8g;
(2)20℃时,固体物质的溶解度为1~10g,为可溶,由表1可知,20℃时,NaHCO 的溶解度为9.6g,为
3
可溶;
(3)由表1可知,0℃~30℃氯化铵的溶解度受温度影响最大,所以将30℃时上述四种物质的饱和溶液各
ag分别降温到0℃,析出同体质量最大的物质是NH Cl;
4
(4)A、20℃时,氯化铵的溶解度比氯化钠的溶解度大,若两只烧杯中均无固体剩余,则所得氯化铵溶液
一定是不饱和溶液,故选项说法正确;
B、20℃时,氯化铵的溶解度比氯化钠的溶解度大,若两只烧杯中均有固体剩余,则所得溶液中溶质的质
量分数:氯化铵>氯化钠,故选项说法正确;
C、若m≤0.36,由于20℃时,氯化铵的溶解度大于36.0g,氯化钠的溶解度为36.0g,只给了ng水,但不
知道具体的量,如果固体全部溶解溶质质量分数相等,但无法判断是否全部溶解,故选项说法错误;
D、20℃时,氯化铵的溶解度为37.2g,氯化钠的溶解度为36.0g,若所得溶液中只有一种是饱和溶液,则
饱和溶液一定是氯化钠饱和溶液,氯化铵不饱和,则0.36n≤m<0.372n,故选项说法错误;
故选:AB。
1. 【2023湖南永州真题】甲、乙两种物质的溶解度曲线如下图所示。下列说法正确的是( )
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A. 阴影部分的任意点表明甲、乙两种溶液都是饱和溶液
B. P点时,甲、乙两种溶液的溶质质量分数相等
C. t℃时,在100g水中加入60g甲,形成不饱和溶液
2
D. t℃时,甲、乙的饱和溶液升温至t℃,溶液的溶质质量分数甲>乙
1 2
【答案】B
【解析】A、图中阴影部分中的点在甲曲线的上部,是甲的饱和溶液,在乙曲线的下部,是乙的不饱和溶
液,故选项说法不正确;
B、由图可知,t℃时,甲、乙两物质相交于P点,因此P点时,甲、乙两种溶液的溶解度相等,P点表示
1
两溶液的饱和状态,则P点时,甲、乙两种溶液的溶质质量分数相等,故选项说法正确;
C、t℃时,甲的溶解度为60g,则t℃时,在100g水中加入60g甲,只能溶解50g甲,形成饱和溶液,故
2 2
选项说法不正确;
D、甲、乙的溶解度都温度的升高而增大,t℃时,乙的溶解度大于甲的溶解度,此时溶质的质量分数:乙
1
>甲,将t℃时,甲、乙的饱和溶液升温至t℃,溶液都变成不饱和溶液,溶液组成不变,溶质的质量分
1 2
数不变,则升温至t℃,溶液的溶质质量分数乙>甲,故选项说法不正确。
2
故选B。
2. 【2023江苏连云港真题】 和 的溶解度曲线如图所示。下列说法中正确的是( )
A. 的溶解度比 的大
B. 的溶解度受温度的影响比 的大
C. 时 的饱和溶液,升温到 时仍是饱和溶液
D. 时,在100g水中加入 ,形成不饱和溶液
【答案】B
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解析】A、由于没有确定温度,不能比较两种物质的溶解度大小,错误;
B、根据溶解度曲线可知, 的溶解度曲线较陡,受温度的影响较大,正确;
C、根据溶解度曲线可知, 溶解度随温度升高而增大, 时 的饱和溶液,升温到
时变成不饱和溶液,错误。
D、根据溶解度曲线可知, 时,NaCl溶解度小于40g,根据溶解度概念可知, 时,在100g水中
最多溶解的NaCl质量小于40g,在100g水中加入 ,形成饱和溶液,错误。
故选B。
3. 【2023山东济南真题】我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。
和NaCl的溶解度曲线如下图所示。下列叙述中,不正确的是( )(双选)
A. 时,NaCl饱和溶液的溶质质量分数为30%
B. 时,将10g 固体放入50g水中,充分溶解后得到溶液的质量为60g
C. 将 时 的饱和溶液升温到 时,溶液的溶质质量分数变大
D. 当 中混有少量NaCl时,可采用冷却热饱和溶液的方法提纯
【答案】AC
【解析】A、由图可知, 时,NaCl的溶解度为36g,则 时,NaCl饱和溶液的溶质质量分数为
×100%≈26.5%,故选项说法不正确;
B、由图可知, 时, 的溶解度为21.8g,则 时,将10g 固体放入50g水中,10g
固体全部溶解,所得溶液的质量为50g+10g=60g,故选项说法正确;
C、由图可知, 到 时, 的溶解度随温度的升高而增大,因此将 时 的饱和溶
液升温到 时,溶液变为不饱和溶液,但溶液组成不变,则溶液的溶质质量分数不变,故选项说法不正
确;
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、由图可知, 的溶解度受温度影响较大,而NaCl的溶解度受温度影响较小,当 中混有
少量NaCl时,可采用冷却热饱和溶液的方法提纯 ,故选项说法正确。
故选AC。
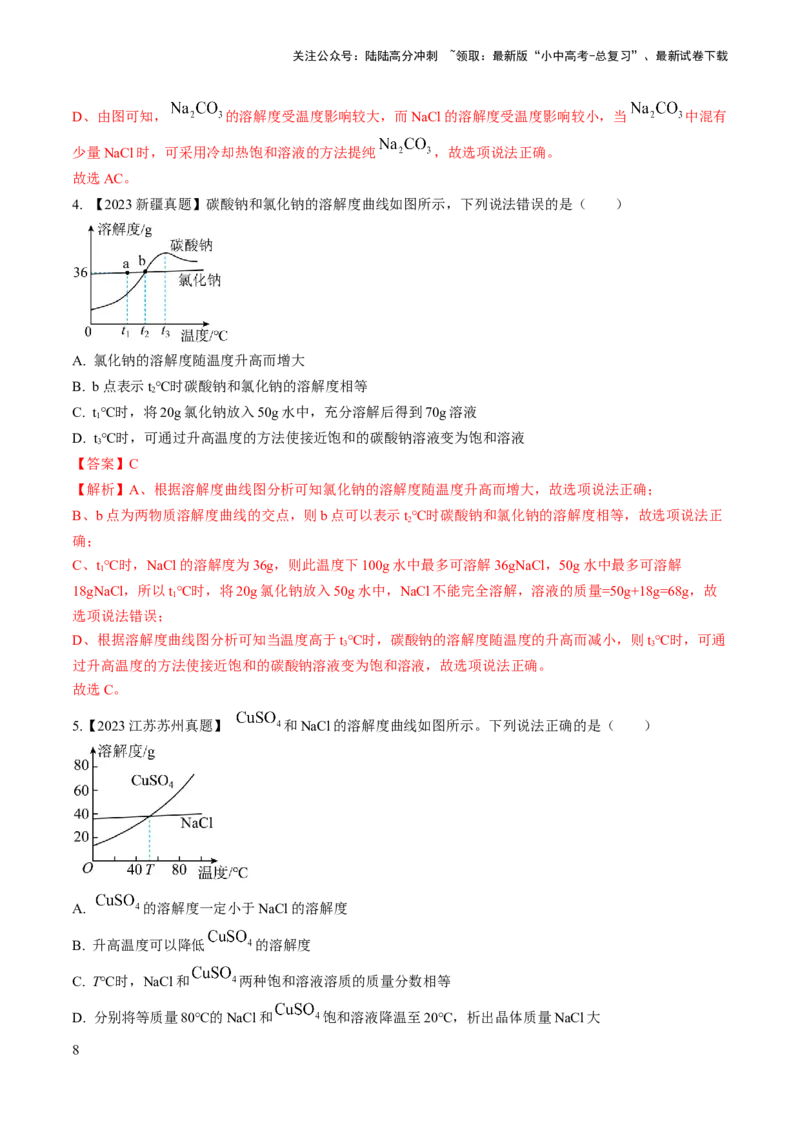
4. 【2023新疆真题】碳酸钠和氯化钠的溶解度曲线如图所示,下列说法错误的是( )
A. 氯化钠的溶解度随温度升高而增大
B. b点表示t℃时碳酸钠和氯化钠的溶解度相等
2
C. t℃时,将20g氯化钠放入50g水中,充分溶解后得到70g溶液
1
D. t℃时,可通过升高温度的方法使接近饱和的碳酸钠溶液变为饱和溶液
3
【答案】C
【解析】A、根据溶解度曲线图分析可知氯化钠的溶解度随温度升高而增大,故选项说法正确;
B、b点为两物质溶解度曲线的交点,则b点可以表示t℃时碳酸钠和氯化钠的溶解度相等,故选项说法正
2
确;
C、t℃时,NaCl的溶解度为36g,则此温度下100g水中最多可溶解36gNaCl,50g水中最多可溶解
1
18gNaCl,所以t℃时,将20g氯化钠放入50g水中,NaCl不能完全溶解,溶液的质量=50g+18g=68g,故
1
选项说法错误;
D、根据溶解度曲线图分析可知当温度高于t℃时,碳酸钠的溶解度随温度的升高而减小,则t℃时,可通
3 3
过升高温度的方法使接近饱和的碳酸钠溶液变为饱和溶液,故选项说法正确。
故选C。
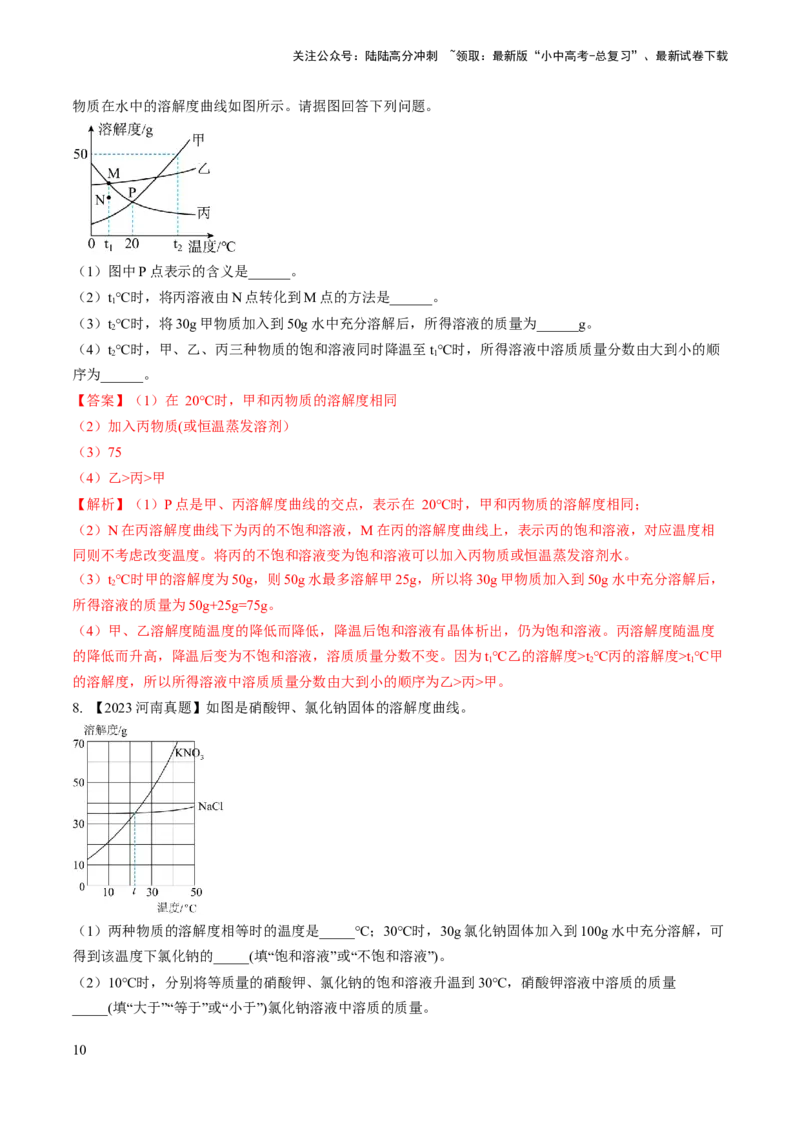
5.【2023江苏苏州真题】 和NaCl的溶解度曲线如图所示。下列说法正确的是( )
A. 的溶解度一定小于NaCl的溶解度
B. 升高温度可以降低 的溶解度
C. T℃时,NaCl和 两种饱和溶液溶质的质量分数相等
D. 分别将等质量80℃的NaCl和 饱和溶液降温至20℃,析出晶体质量NaCl大
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【答案】C
【解析】A、在0-T℃,NaCl的溶解度大于CuSO ,在高于T℃,CuSO 的溶解度大于NaCl,选项错误;
4 4
B、CuSO 的溶解度随温度的升高而增大,选项错误;
4
C、T℃时,NaCl和 CuSO 的溶解度相等,所以T℃时, NaCl和 CuSO 两种饱和溶液溶质的质量分数相
4 4
等,选项正确;
D、分别将等质量80℃的NaCl和 CuSO 饱和溶液降温至20℃,CuSO 溶解度降低更多,析出晶体质量
4 4
CuSO 大,选项错误;
4
故选:C。
6. 【2023山西真题】浓度为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。下图为配制氯化钠杀菌
液的过程,结合图表信息,有关分析正确的一项是( )
NaCl在不同温度时的溶解度
温度/°C 0 10 20 30 40 60 80 90 100
氯化钠溶解度/g 35.7 35.8 36.0 36.3 36.6 37.3 38.4 39.0 39.8
A. 图1中搅拌可增大氯化钠的溶解度
B. 图2中溶液为20℃氯化钠的不饱和溶液
C. 图2中溶液对葡萄球菌有明显的杀菌效果
D. 从氯化钠溶液中得到氯化钠均可采用降温结晶的方法
【答案】B
【解析】A、溶解过程中玻璃棒的作用是搅拌,只能加快溶解速率,不能增大氯化钠的溶解度,故选项说
法错误;
B、由表中数据可知,20℃时,氯化钠的溶解度是36g,所以该温度下,将10g氯化钠溶解在100g水中得
到的是氯化钠的不饱和溶液,故选项说法正确;
C、图2中溶液的浓度为: 小于10%,所以对葡萄球菌没有明显的杀菌效果,
故选项说法错误;
D、氯化钠的溶解度受温度影响变化不大,可以采用蒸发结晶的方法把氯化钠从它的饱和溶液中结晶出
来,故选项说法错误。
故选B。
7. 【2023甘肃金昌真题】学会从图表中获取关键信息是学习化学的一种重要能力。甲、乙、丙三种固体
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
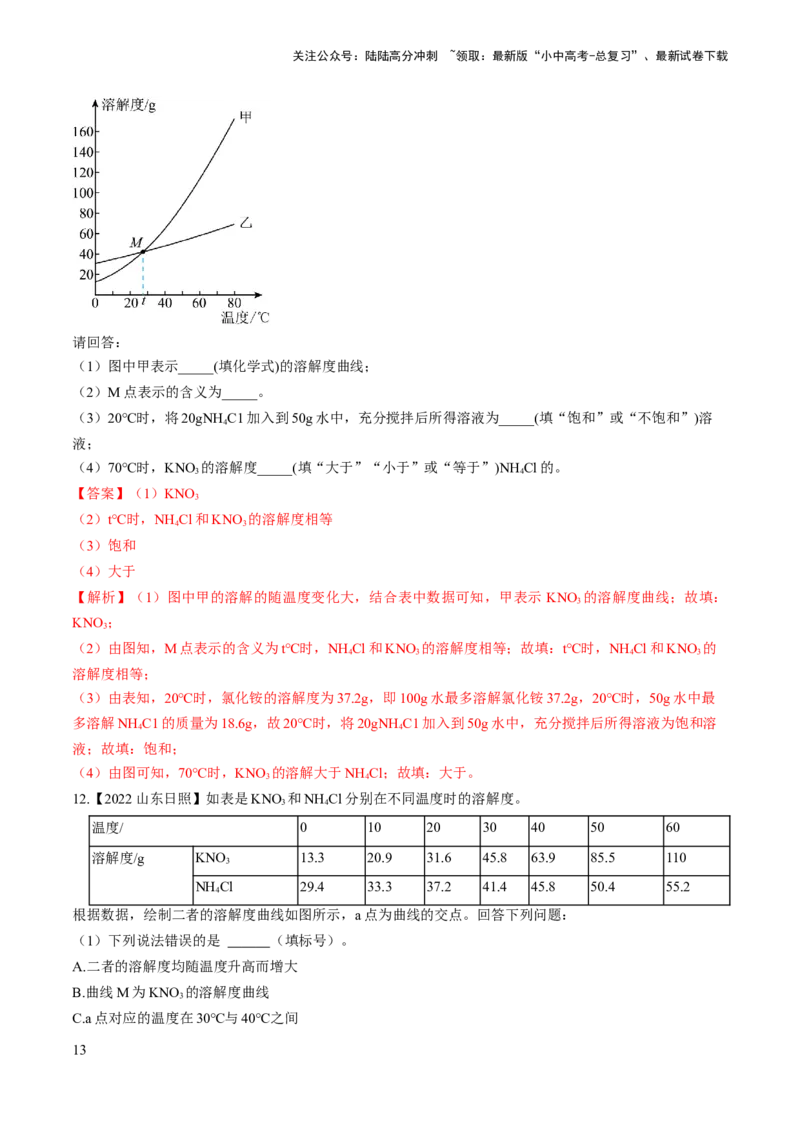
物质在水中的溶解度曲线如图所示。请据图回答下列问题。
(1)图中P点表示的含义是______。
(2)t℃时,将丙溶液由N点转化到M点的方法是______。
1
(3)t℃时,将30g甲物质加入到50g水中充分溶解后,所得溶液的质量为______g。
2
(4)t℃时,甲、乙、丙三种物质的饱和溶液同时降温至t℃时,所得溶液中溶质质量分数由大到小的顺
2 1
序为______。
【答案】(1)在 20℃时,甲和丙物质的溶解度相同
(2)加入丙物质(或恒温蒸发溶剂)
(3)75
(4)乙˃丙˃甲
【解析】(1)P点是甲、丙溶解度曲线的交点,表示在 20℃时,甲和丙物质的溶解度相同;
(2)N在丙溶解度曲线下为丙的不饱和溶液,M在丙的溶解度曲线上,表示丙的饱和溶液,对应温度相
同则不考虑改变温度。将丙的不饱和溶液变为饱和溶液可以加入丙物质或恒温蒸发溶剂水。
(3)t℃时甲的溶解度为50g,则50g水最多溶解甲25g,所以将30g甲物质加入到50g水中充分溶解后,
2
所得溶液的质量为50g+25g=75g。
(4)甲、乙溶解度随温度的降低而降低,降温后饱和溶液有晶体析出,仍为饱和溶液。丙溶解度随温度
的降低而升高,降温后变为不饱和溶液,溶质质量分数不变。因为t℃乙的溶解度>t℃丙的溶解度>t℃甲
1 2 1
的溶解度,所以所得溶液中溶质质量分数由大到小的顺序为乙˃丙˃甲。
8. 【2023河南真题】如图是硝酸钾、氯化钠固体的溶解度曲线。
(1)两种物质的溶解度相等时的温度是_____℃;30℃时,30g氯化钠固体加入到100g水中充分溶解,可
得到该温度下氯化钠的_____(填“饱和溶液”或“不饱和溶液”)。
(2)10℃时,分别将等质量的硝酸钾、氯化钠的饱和溶液升温到30℃,硝酸钾溶液中溶质的质量
_____(填“大于”“等于”或“小于”)氯化钠溶液中溶质的质量。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【答案】(1) ①. t ②. 不饱和 (2)小于
【解析】(1)溶解度曲线的交点表示该温度下,固体物质溶解度相等,由硝酸钾、氯化钠固体的溶解度
曲线可知:两种物质的溶解度相等时的温度是t℃;30℃时,氯化钠的溶解度大约36g,该温度下,30g氯
化钠固体加入到100g水中充分溶解,可得到该温度下氯化钠的不饱和溶液;
(2)10℃时,硝酸钾的溶解度小于氯化钠的溶解度,且两种物质的溶解度随温度的升高而增大,分别将
等质量的硝酸钾、氯化钠的饱和溶液升温到30℃,该过程中溶剂质量不变,溶质质量不变,硝酸钾溶液中
溶质的质量小于氯化钠溶液中溶质的质量。
9. 【2023湖北宜昌真题】下图是两种固体物质的溶解度随温度变化的曲线图,据图回答:
(1) ℃时乙的溶解度是______g。
(2) ℃时把30 g物质甲加入到50 g水中充分搅拌,形成的是______溶液(填“饱和”或“不饱
和”),升温到 ℃时,溶液的质量是______g。
(3)分别将 ℃时100 g甲、乙饱和溶液降温到 ℃,下列叙述正确的是______。
A. 甲、乙仍是饱和溶液 B. 溶剂质量:甲等于乙
C. 溶液质量:甲大于乙 D. 溶质质量分数:甲小于乙
【答案】(1)50 (2) ①. 饱和 ②. 75 (3)BD
【解析】(1)由溶解度曲线图可知, ℃时乙的溶解度是50g,故填:50。
(2)由溶解度曲线图可知, ℃时物质甲的溶解度为40g, ℃时50 g水中最多能溶解20g甲物质,所以
℃时把30 g物质甲加入到50 g水中充分搅拌,形成的是饱和溶液;物质甲的溶解度随温度的升高而增
大,升温到 ℃时,溶解度为50g,50g水中最多能溶解25g甲物质,一共加入30g甲物质,则溶液质量
为:25g+50g=75g。故填:饱和;75。
(3)A.由溶解度曲线图可知,物质甲的溶解度随温度的降低而减小,物质乙的溶解度随温度的降低而增
大,分别将 ℃时100 g甲、乙饱和溶液降温到 ℃,甲仍是饱和溶液,乙变为不饱和溶液,故A错误;
B.降温过程中,甲、乙溶液中溶剂的质量不变,与 ℃时饱和溶液中溶剂的质量相等,由溶解度曲线图可
知, ℃时,甲、乙的溶解度相等,等质量的饱和溶液中所含的溶剂质量相等,分别将 ℃时100 g甲、
乙饱和溶液降温到 ℃,溶剂质量:甲等于乙,故B正确;
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.甲溶液中有晶体析出,溶液质量减小,乙溶液中无晶体析出,溶液质量不变,所以分别将 ℃时100 g
甲、乙饱和溶液降温到 ℃,溶液质量:甲小于乙,故C错误;
D.由溶解度曲线图可知, ℃时,甲、乙的溶解度相等,根据饱和溶液溶质质量分数=
,可知 ℃时甲、乙饱和溶液溶质的质量分数相等,分别将 ℃时100g甲、乙饱
和溶液降温到 ℃,甲溶液中有晶体析出,溶质质量分数减小,乙溶液中无晶体析出,溶质质量分数不
变,所以 ℃时溶质质量分数:甲小于乙,故D正确。
故选:BD。
10. 【2023内蒙古包头】下表是硝酸钾和氯化钠在不同温度时的溶解度。根据此表回答:
温度/℃ 0 20 40 60 80
13.3 31.6 63.9 110 169
溶解度/g
NaCl 35.7 36.0 36.6 37.3 38.4
(1)两种物质的溶解度受温度变化影响较大的是___________。
(2)40℃时,向两只各盛有100g蒸馏水的烧杯中分别加入50g NaC1和50gKNO 固体,充分溶解,能达
3
到饱和状态的是___________溶液。此时NaCl的溶质质量分数___________ KNO 的溶质质量分数(填“>”
3
“=”或“<”)。
【答案】(1)KNO##硝酸钾 (2) ①. NaCl##氯化钠 ②. <
3
【解析】(2)由表中数据可知,硝酸钾的溶解度受温度影响比较大。
(2)40℃时,硝酸钾和氯化钠的溶解度分别为63.9g和36.6g,则向两只各盛有100g蒸馏水的烧杯中分别
加入50g NaC1和50gKNO 固体,氯化钠能形成饱和溶液,但硝酸钾不能;
3
但由于形成的氯化钠溶液中,溶质质量只有36.6g,而硝酸钾溶液中,溶质质量为50g,则氯化钠的溶质质
量分数小于硝酸钾。
11. 【2023湖南益阳真题】下面是NH Cl、KNO 在不同温度时的溶解度以及相应的溶解度曲线。
4 3
温度/℃ 10 20 30 40 60 80
NH Cl 33.3 37.2 41.4 45.8 55.2 65.6
4
溶解度/g
KNO 20.9 31.6 45.8 63.9 110 169
3
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
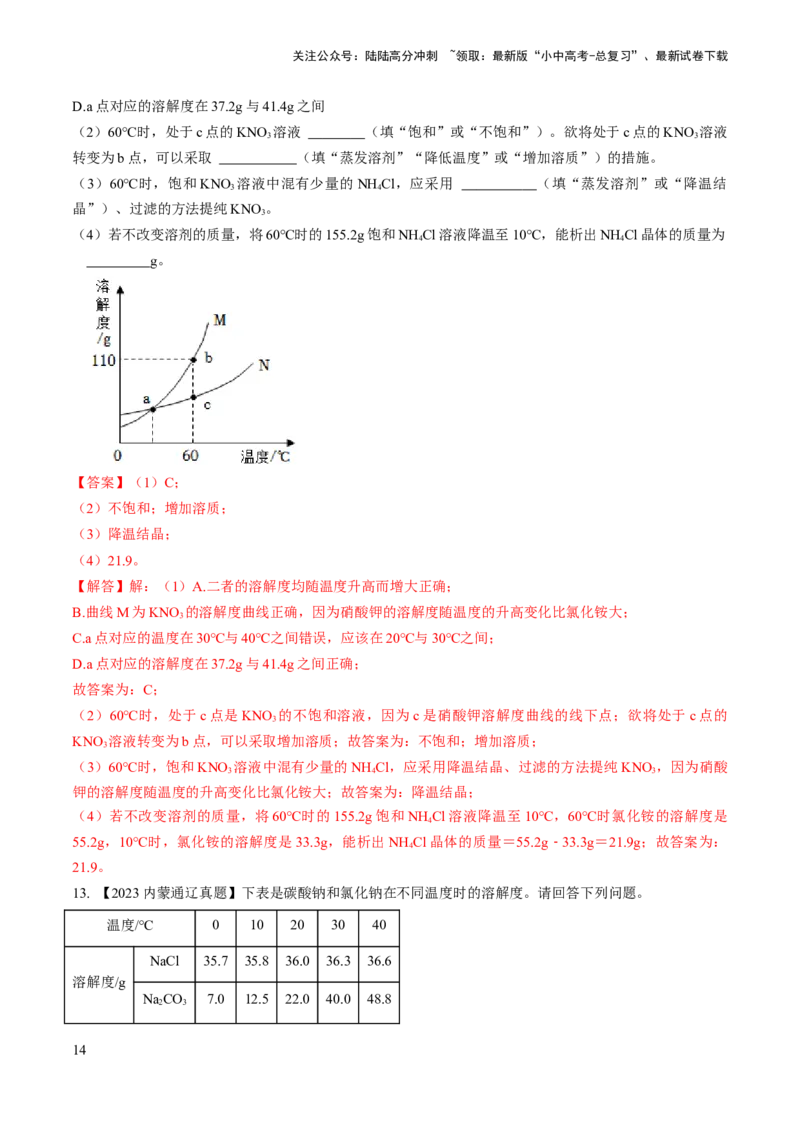
请回答:
(1)图中甲表示_____(填化学式)的溶解度曲线;
(2)M点表示的含义为_____。
(3)20℃时,将20gNH C1加入到50g水中,充分搅拌后所得溶液为_____(填“饱和”或“不饱和”)溶
4
液;
(4)70℃时,KNO 的溶解度_____(填“大于”“小于”或“等于”)NH Cl的。
3 4
【答案】(1)KNO
3
(2)t℃时,NH Cl和KNO 的溶解度相等
4 3
(3)饱和
(4)大于
【解析】(1)图中甲的溶解的随温度变化大,结合表中数据可知,甲表示 KNO 的溶解度曲线;故填:
3
KNO;
3
(2)由图知,M点表示的含义为t℃时,NH Cl和KNO 的溶解度相等;故填:t℃时,NH Cl和KNO 的
4 3 4 3
溶解度相等;
(3)由表知,20℃时,氯化铵的溶解度为37.2g,即100g水最多溶解氯化铵37.2g,20℃时,50g水中最
多溶解NH C1的质量为18.6g,故20℃时,将20gNH C1加入到50g水中,充分搅拌后所得溶液为饱和溶
4 4
液;故填:饱和;
(4)由图可知,70℃时,KNO 的溶解大于NH Cl;故填:大于。
3 4
12.【2022山东日照】如表是KNO 和NH Cl分别在不同温度时的溶解度。
3 4
温度/ 0 10 20 30 40 50 60
溶解度/g KNO 13.3 20.9 31.6 45.8 63.9 85.5 110
3
NH Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.2
4
根据数据,绘制二者的溶解度曲线如图所示,a点为曲线的交点。回答下列问题:
(1)下列说法错误的是 (填标号)。
A.二者的溶解度均随温度升高而增大
B.曲线M为KNO 的溶解度曲线
3
C.a点对应的温度在30℃与40℃之间
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.a点对应的溶解度在37.2g与41.4g之间
(2)60℃时,处于c点的KNO 溶液 (填“饱和”或“不饱和”)。欲将处于c点的KNO 溶液
3 3
转变为b点,可以采取 (填“蒸发溶剂”“降低温度”或“增加溶质”)的措施。
(3)60℃时,饱和KNO 溶液中混有少量的NH Cl,应采用 (填“蒸发溶剂”或“降温结
3 4
晶”)、过滤的方法提纯KNO。
3
(4)若不改变溶剂的质量,将60℃时的155.2g饱和NH Cl溶液降温至10℃,能析出NH Cl晶体的质量为
4 4
g。
【答案】(1)C;
(2)不饱和;增加溶质;
(3)降温结晶;
(4)21.9。
【解答】解:(1)A.二者的溶解度均随温度升高而增大正确;
B.曲线M为KNO 的溶解度曲线正确,因为硝酸钾的溶解度随温度的升高变化比氯化铵大;
3
C.a点对应的温度在30℃与40℃之间错误,应该在20℃与30℃之间;
D.a点对应的溶解度在37.2g与41.4g之间正确;
故答案为:C;
(2)60℃时,处于c点是KNO 的不饱和溶液,因为c是硝酸钾溶解度曲线的线下点;欲将处于c点的
3
KNO 溶液转变为b点,可以采取增加溶质;故答案为:不饱和;增加溶质;
3
(3)60℃时,饱和KNO 溶液中混有少量的NH Cl,应采用降温结晶、过滤的方法提纯KNO ,因为硝酸
3 4 3
钾的溶解度随温度的升高变化比氯化铵大;故答案为:降温结晶;
(4)若不改变溶剂的质量,将60℃时的155.2g饱和NH Cl溶液降温至10℃,60℃时氯化铵的溶解度是
4
55.2g,10℃时,氯化铵的溶解度是33.3g,能析出NH Cl晶体的质量=55.2g﹣33.3g=21.9g;故答案为:
4
21.9。
13. 【2023内蒙通辽真题】下表是碳酸钠和氯化钠在不同温度时的溶解度。请回答下列问题。
温度/℃ 0 10 20 30 40
NaCl 35.7 35.8 36.0 36.3 36.6
溶解度/g
NaCO 7.0 12.5 22.0 40.0 48.8
2 3
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)40℃时,将16g氯化钠溶解在50g水中,得到______(填“饱和”或“不饱和”)溶液。
(2)取30℃时碳酸钠和氯化钠的饱和溶液各100g,降温至20℃,析出碳酸钠的质量______(填“大于”
或“小于”)氯化钠的质量。
(3)海水晒盐是利用______的方法获得晶体。
(4)将接近饱和的碳酸钠溶液变为饱和溶液,可采用的方法是______(写出一种即可)。
【答案】(1)不饱和 (2)大于 (3)蒸发结晶 (4)加碳酸钠固体
【解析】(1)据表格可知,40℃时氯化钠的溶解度为36.6g,其涵义是40℃时,100g水中最多溶解36.6g
氯化钠,溶液达到饱和状态,即该温度下,50g水中最多能溶解氯化钠18.3g。所以40℃时,将16g氯化钠
溶解在50g水中,得到不饱和溶液。故填:不饱和。
(2)降温后溶解度减小的多的析出的晶体就多,由表格可知将30℃时碳酸钠和氯化钠的饱和溶液各
100g,降温至20℃,碳酸钠的溶解度减小的多,所以析出的多。即析出碳酸钠的质量大于氯化钠的质量。
故填:大于。
(3)食盐的溶解度受温度变化的影响较小,从食盐溶液中获得食盐主要利用阳光和风力蒸发水分,使海
水中的水分蒸发掉,使氯化钠结晶出来,利用的是蒸发溶剂的方法。即海水晒盐是利用“蒸发结晶”的方
法来得到食盐晶体的。故填:蒸发结晶。
(4)据表格可知,碳酸钠的溶解度随着温度的升高而增大,将接近饱和的碳酸钠溶液转化为饱和溶液,
可采用增加碳酸钠、蒸发溶剂、降低温度等方法,其中增加碳酸钠是最可靠的方法。故填:加碳酸钠固
体。
15