文档内容
查补易混易错 07 元素周期表和元素周期律
元素周期律与元素周期表是近几年高考中每年必考的内容,题型主要是以选择题形式考查,考查内容主要
是元素的推断、元素周期表和元素周期律的应用、物质结构、元素重要单质及其化合物的主要性质,主要
的考查方向为非金属性或金属性强弱、原子半径大小比较、气态氢化物稳定性强弱、最高价氧化物的水化
物的酸性或碱性强弱、化学键与化合物的类型、物质的性质间的关系等问题,新高考模式下,可能会出现
电子排布式、不成对或成对电子数、第一电离能或电负性大小、原子的杂化方式、空间构型、分子的极性
等内容的考查与分析,原子核外电子排布的周期性变化是元素周期律变化的原因,掌握元素的单质及化合
物的结构、反应条件、物质的物理性质、化学性质等是进行元素及化合物推断的关键。
易错01 元素周期表的结构
①基态原子最外层电子排布相同的原子对应元素不一定处于同主族,如He、Be的最外层均有2个电子,
前者处于0族,后者处于第IIA族。
②第IA族和0族不是含元素种类最多的族,应是第ⅢB族,共有32种元素。
③第VIII族属于副族,但表示时仍表示“VIII族”;过渡元素包括8个副族,全部是金属元素,原子最外
层电子数不超过2个。
易错02周期表的分区
分区 价层电子排布
s区 ns1~2
p区 ns2np1~6(除He外)
d区 (n-1)d1~9ns1~2(除钯外)
ds区 (n-1)d10ns1~2
f区 (n-2)f0~14(n-1)d0~2ns2
易错03 电离能和电负性
(1)电离能:同周期从左到右,第一电离能呈增大的趋势,稀有气体的第一电离能最大,碱金属的第一
电离能最小;同主族从上到下,第一电离能逐渐减小。
①判断元素金属性的强弱:第一电离能越小,金属越容易失去电子,金属性越强;反之越弱。
②判断元素的化合价(I、I……表示各级电离能):如果某元素的I I,则该元素的常见化合价为+n。
1 2 n+1 n
≫例如,钠元素的I I,故钠元素的化合价为+1。
2 1
③判断核外电子的分层排布情况:多电子原子中,元素的各级电离能逐级增大,有一定的规律性。当电离
≫
能的变化出现突变时,电子层数就可能发生变化。
④第二、三、四周期中,第IIA族、第VA族元素的第一电离能比相邻主族元素都大。
(2)电负性:一般来说,同周期元素从左至右,元素的电负性逐渐变大;同族元素从上至下,元素的电
负性逐渐变小。金属元素的电负性一般小于1.8,非金属元素的电负性一般大于1.8,而位于非金属三角区
边界的“类金属”(如锗、锑等)的电负性则在1.8左右,它们既有金属性又有非金属性。
易错04 元素金属性(非金属性)相对强弱的判断规律
元素的性质 本质 判断的一般依据
元素的原子失电子 与水或酸(非氧化性)反应置换出氢的难易
的能力(与失电子的数
最高价氧化物对应水化物的碱性强弱
目无关),原子越容易
失去电子,元素金属性 水溶液中单质间的置换反应
元素金属性
越强;反之则弱
原电池中的正负极(Mg—Al---NaOH溶液例外)
阳离子在电解池中阴极上的放电顺序
元素的原子得电子 与氢气化合的难易
的能力(与得电子的数
气态氢化物的稳定性
目无关),原子越容易
得到电子,元素非金属 最高价氧化物对应水化物的酸性强弱
元素的非金属性
性越强;反之则弱。
水溶液中单质间的置换反应(单质作氧化剂)
阴离子的还原性
易错05 微粒半径大小比较中的规律
同周期 随原子序数递增,原子半径减小。如:r(Na)>r( Mg)>r(Al)>r(Si)>r
M
(P)>r(S)>r(Cl)
随原子序数递增,原子或离子半径减小。如:r(Li)<r(Na)<r(k)<r(Rb)<r
(Cs),r(Li+)<r(Na+)<r(k+)<r(Rb+)<r(Cs+),r(F—)<r(Cl—)<r(Br
同主族
—)<r(I—)
同电子层 核电荷数越大,离子半径越小。如:r(O2—)>r(F—)>r(Na+)>r(Mg2+)>r
(Al3+)
同元素 阴离子大于原子,原子大于阳离子,低价阳离子大于高价阳离子。如:r(Cl-)>r
(Cl),r(Fe)>r(Fe2+)>r(Fe3+)
易错06 共价键的类型
分类依据 类型
形成共价键的原子 σ键 电子云“头碰头”重叠
轨道重叠方式 π键 电子云“肩并肩”重叠
形成共价键的电子 极性键 共用电子对发生偏移
对是否偏移 非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对
双键 原子间有两对共用电子对的数目 三键 原子间有三对共用电子对
1.(2023·浙江·高考真题)下列化学用语表示正确的是
A.中子数为18的氯原子:
B.碳的基态原子轨道表示式:
C. 的空间结构: (平面三角形)
D. 的形成过程:
2.(2022·河北·高考真题)中子轰击 X原子的核反应为 X+ n→ Y+ H,其中 Y可用于测定文物年代。
下列说法错误的是
A.原子半径:Y>X B.YH 的电子式为:
C.最高价含氧酸的酸性:Y>X D.X与Y均能形成多种氢化物
3.(2022·福建·统考高考真题)某非线性光学晶体由钾元素(K)和原子序数依次增大的X、Y、Z、W四种
短周期元素组成。X与Y、Z与W均为同周期相邻元素,X的核外电子总数为最外层电子数的2倍,Z为
地壳中含量最多的元素。下列说法正确的是
A.简单氢化物沸点: B. 分子的空间构型为三角锥形
C.原子半径: D.最高价氧化物对应水化物的碱性:
4.(2022·重庆·统考高考真题)R、X、Y、Z均为短周期主族元素,Y与Z同主族且Z的原子序数大于
Y。R和X的原子获得1个电子均可形成稀有气体原子的电子层结构,R的最高化合价为+1。1mol化合物
RZY X含58mol电子。下列说法正确的是
3
A.R与X形成的化合物水溶液呈碱性 B.X是四种元素中原子半径最大的C.Y单质的氧化性比Z单质的弱 D.Z的原子最外层电子数为6
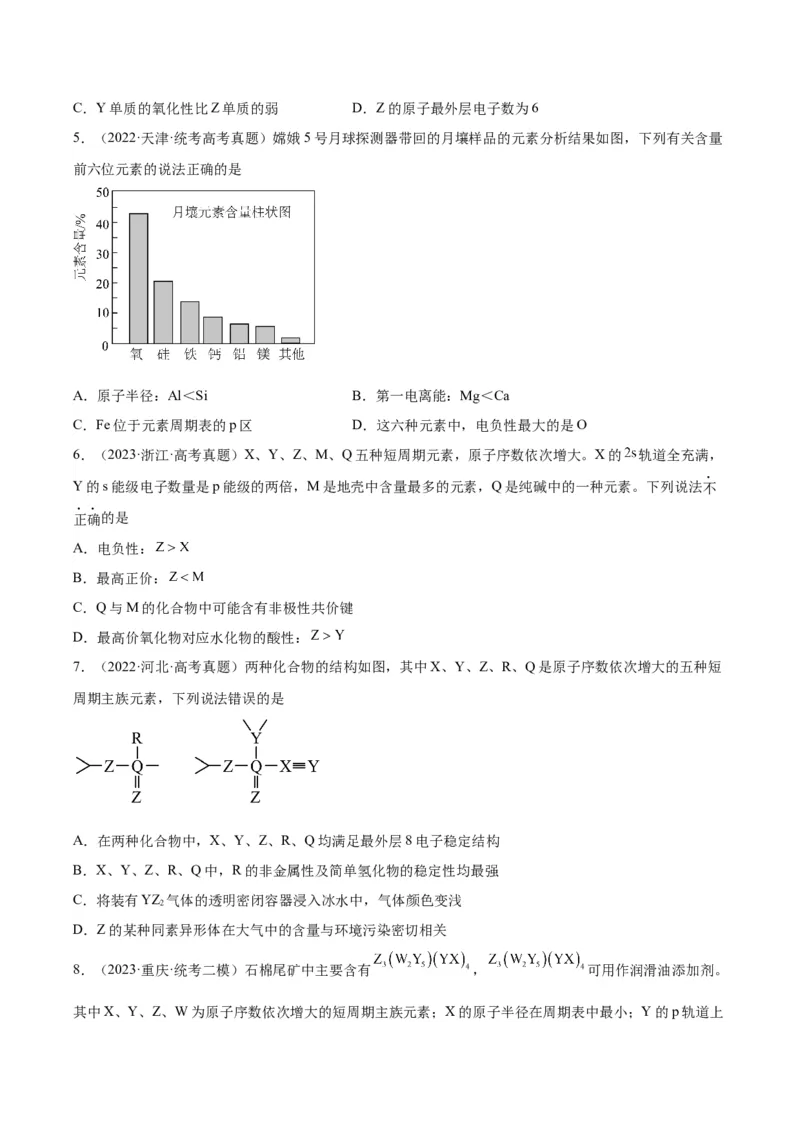
5.(2022·天津·统考高考真题)嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关含量
前六位元素的说法正确的是
A.原子半径:Al<Si B.第一电离能:Mg<Ca
C.Fe位于元素周期表的p区 D.这六种元素中,电负性最大的是O
6.(2023·浙江·高考真题)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X的 轨道全充满,
Y的s能级电子数量是p能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说法不
正确的是
A.电负性:
B.最高正价:
C.Q与M的化合物中可能含有非极性共价键
D.最高价氧化物对应水化物的酸性:
7.(2022·河北·高考真题)两种化合物的结构如图,其中X、Y、Z、R、Q是原子序数依次增大的五种短
周期主族元素,下列说法错误的是
A.在两种化合物中,X、Y、Z、R、Q均满足最外层8电子稳定结构
B.X、Y、Z、R、Q中,R的非金属性及简单氢化物的稳定性均最强
C.将装有YZ 气体的透明密闭容器浸入冰水中,气体颜色变浅
2
D.Z的某种同素异形体在大气中的含量与环境污染密切相关
8.(2023·重庆·统考二模)石棉尾矿中主要含有 , 可用作润滑油添加剂。
其中X、Y、Z、W为原子序数依次增大的短周期主族元素;X的原子半径在周期表中最小;Y的p轨道上自旋方向不同的电子数之比为3∶1;W是地壳中含量第二的元素。下列说法正确的是
A.离子半径:
B.Y和W形成的化合物不与酸反应
C.X和Z形成的化合物能与水反应生成一种不溶物和气体
D.X和Y两元素形成的化合物中,一定不含非极性键
9.(2023·云南·统考二模)X、Y、Z、W是原子序数依次增大的前四周期元素,X元素的简单氢化物能与
其最高价氧化物对应水化物反应生成盐; Y元素原子的核外电子只有8种运动状态;Z为短周期金属元素,
其简单离子的半径在同周期中最小;基态W原子的未成对电子数为6。下列说法错误的是
A.第一电离能: X>Y> Z
B.键角 >
C.W为第四周期d区元素
D.X和Y的最简单气态氢化物中,前者更易液化
10.(2023·河北沧州·统考一模)X、Y、Z、Q、R为原子序数依次增大的1~36号元素,基态X原子核外
最外层有2个未成对的电子,且没有空轨道,Y的简单离子在同周期中离子半径最小,Z和X同主族,Q
的一种氧化物常用作水处理剂,R原子的M层全充满,且最高能层只有一个电子,下列说法错误的是
A. 为含有非极性键和极性键的极性分子
B.简单氢化物的键角:
C.Z单质和R单质直接化合生成
D. 分子中存在配位键
11.(2023·安徽蚌埠·统考三模)X、Y、Z、W是前4周期原子序数依次增大的主族元素,X在周期表中
非金属性最强,Y的周期序数与族序数相等,Z原子次外层电子数是核外电子总数的一半,基态W原子核
外16个轨道上填有电子。下列说法正确的是
A.原子半径:r(X) Y
C.Z元素的第一电离能比同周期相邻元素的大
D.与M同族元素的基态原子最高能级的电子云轮廓图呈球形
21.(2023·宁夏中卫·统考二模)某种由六种元素形成的抗癌药物的结构简式如图所示,其中W、X、Y、
Z是原子序数依次增大的短周期主族元素,W、Y同主族,Y、Z的最外层电子数之和是X的最外层电子数
的2倍,下列叙述不正确的是
A.W的最简单氢化物与Z的单质混合后可产生白烟
B.简单气态氢化物稳定性:XX>Y
C.W的气态氢化物沸点比T气态氢化物沸点低
D.T的氧化物对应水化物的酸性一定比Z的氧化物对应水化物的酸性强
24.(2023·广东梅州·统考二模)常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶
液(浓度均为 )的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
A.第一电离能:
B. 含有极性共价键和非极性共价键
C.工业上通过电解XZ的水溶液来制取X的单质
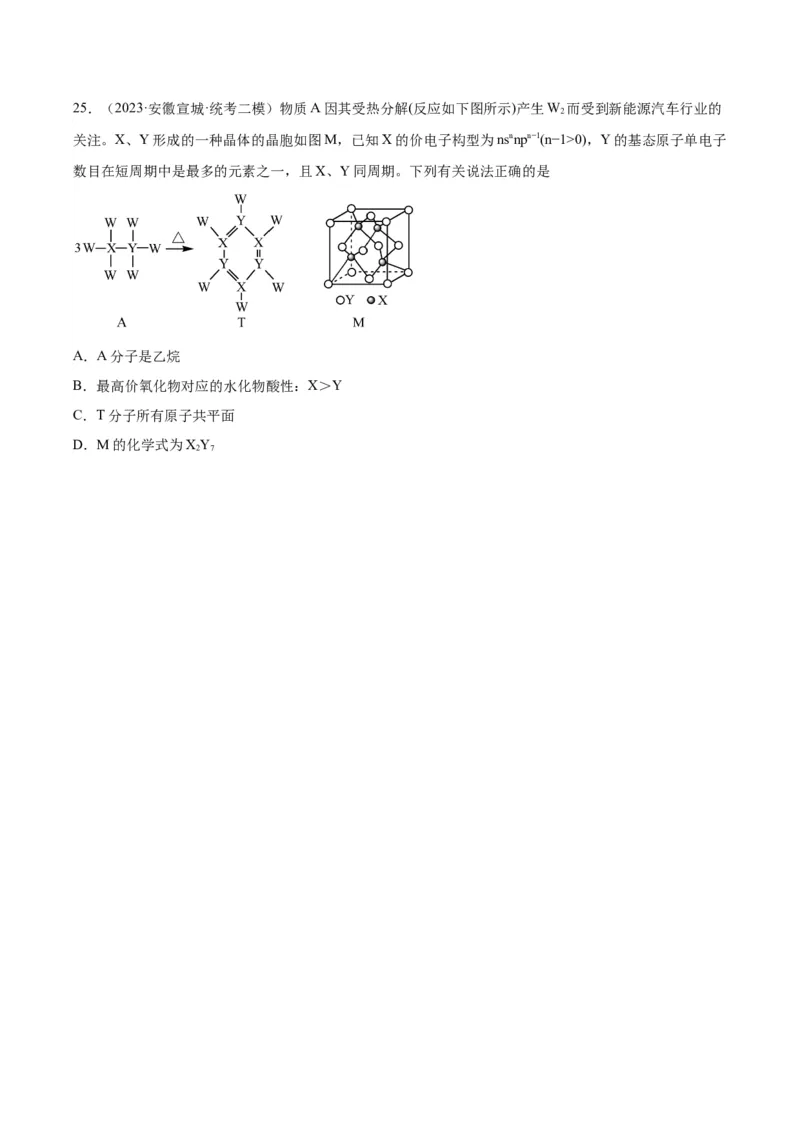
D.Z的单质具有强氧化性和漂白性25.(2023·安徽宣城·统考二模)物质A因其受热分解(反应如下图所示)产生W 而受到新能源汽车行业的
2
关注。X、Y形成的一种晶体的晶胞如图M,已知X的价电子构型为nsnnpn−1(n−1>0),Y的基态原子单电子
数目在短周期中是最多的元素之一,且X、Y同周期。下列有关说法正确的是
A.A分子是乙烷
B.最高价氧化物对应的水化物酸性:X>Y
C.T分子所有原子共平面
D.M的化学式为XY
2 7