文档内容
第 4 讲 氧化还原反应(上)
达标练习01.
★☆☆☆☆
氧化还原反应的实质是( )
A.物质跟氧气反应
B.有氧原子得失
C.有元素化合价升降
D.有电子得失或电子对偏移
【考点】氧化还原反应的实质
【答案】D
【解答】解:电子的得失或共用电子对的偏移是氧化还原反应的实质,也是氧化
还原反应中化合价变化的原因,故D选。
达标练习02.
★☆☆☆☆
判断一个反应是否为氧化还原反应的标准是( )
A.是否有氧气参加
B.是否为置换反应
C.是否有化合价的变化
D.是否为化合反应或者分解反应
【考点】氧化还原反应的判断
【答案】C
【解答】解:A.有的氧化还原反应中没有氧气参与,如氢气与氧化铜的反应,
则是否有氧气参加不是判断氧化还原反应的标准,故A错误;
B.置换反应一定为氧化还原反应,但氧化还原反应不一定为置换反应,故是否
为置换反应不是判断氧化还原反应的标准,故B 错误;
C.化合价变化为氧化还原反应的特征,是否有化合价的变化为判断氧化还原反
应的标准,故C 正确;
D.化合反应和分解反应不一定为氧化还原反应,二者不是判断氧化还原反应的
标准,故D错误;
故选:C。
第1页(共8页)达标练习03.
★☆☆☆☆
下列不属于氧化还原反应的是( )
A.H +CuO Cu+H O
2 2
B.AgNO +NaCl==AgCl↓+NaNO
3 3
C.3CO+Fe O 2Fe+3CO
2 3 2
通电
D.MgCl (熔融) Mg+Cl ↑
2 2
【考点】氧化还原反应的判断
【答案】B
【解答】解:A.该反应中H 元素化合价由0价变为+1价、Cu 元素化合价由+2
价变为0价,所以属于氧化还原反应,故A错误;
B.该反应中所有元素化合价不变,不属于氧化还原反应,故B正确;
C.该反应中C元素化合价由+2 价变为+4 价、Fe 元素化合价由+3价变为 0价,
所以属于氧化还原反应,故C 错误;
D.该反应中 Mg元素化合价由+2 价变为0价、Cl元素化合价由﹣1价变为0价,
所以属于氧化还原反应,故D错误;故选:B。
达标练习04.
★☆☆☆☆
下列说法正确的是( )
A.化合反应都是氧化还原反应
B.分解反应都是氧化还原反应
C.置换反应都是氧化还原反应
D.复分解反应都是氧化还原反应
【考点】氧化还原反应与四种基本反应类型的关系
【答案】C
【解答】解:A.化合反应中可能没有元素的化合价变化,如二氧化硫与水反应
生成亚硫酸为非氧化还原反应,故A错误;
B.分解反应中不一定有元素的化合价变化,如水分解生成单质为氧化还原反应,
而碳酸钙分解生成CaO和二氧化碳不属于氧化还原反应,故B 错误;
C.置换反应一定是氧化还原反应,故C正确;
第2页(共8页)D.复分解反应中一定不存在元素的化合价变化,则一定不是氧化还原反应,故
D错误;故选:C。
达标练习05.
★☆☆☆☆
下列既属于氧化还原反应,又属于分解反应的是( )
A.2KBr+Cl ═2KCl+Br
2 2
B.2NaHCO Na CO +CO ↑+H O
3 2 3 2 2
C.SO +H O ═H SO
2 2 2 2 4
D.4HNO 2H O+4NO +O ↑
3 2 2 2
【考点】氧化还原反应与四种基本反应类型的关系
【答案】D
【解答】解:A.该反应中 Br 元素化合价由﹣1价变为0价、Cl 元素化合价由0
价变为﹣1价,则属于氧化还原反应,但该反应又属于置换反应,故A错误;
B.该反应属于分解反应,但该反应中没有电子转移,所以不属于氧化还原反应,
故B 错误;
C.S 元素化合价从+4 价变为+6 价、H O 中O 元素化合价由-1 价变为﹣2 价,
2 2
所以属于氧化还原反应,但该反应属于化合反应,故C 错误;
D.该反应中N元素化合价由+5 价变为+4价、O元素化合价由﹣2价变为0价,
则属于氧化还原反应,且是由一种物质生成三种物质,所以为分解反应,故 D
正确;
故选:D。
达标练习06.
★★☆☆☆
黑火药的爆炸反应为 2KNO +S+3C K S+N ↑+3CO ↑,其中被还原的元素是
3 2 2 2
( )
A.N 和 O B.C 和 O C.N 和 S D.N 和 C
【考点】氧化还原反应基本概念理解与区分
【答案】C
【解答】2KNO +S+3C K S+N ↑+3CO ↑反应中,化合价变化的元素为:
3 2 2 2
第3页(共8页)KNO →N ,氮元素化合价降低,被还原;S→K S,硫元素化合价降低被还原;
3 2 2
C→CO ,碳元素化合价升高,被氧化,所以被还原的元素是氮元素和硫元素,
2
故选:C。
达标练习07.
★★☆☆☆
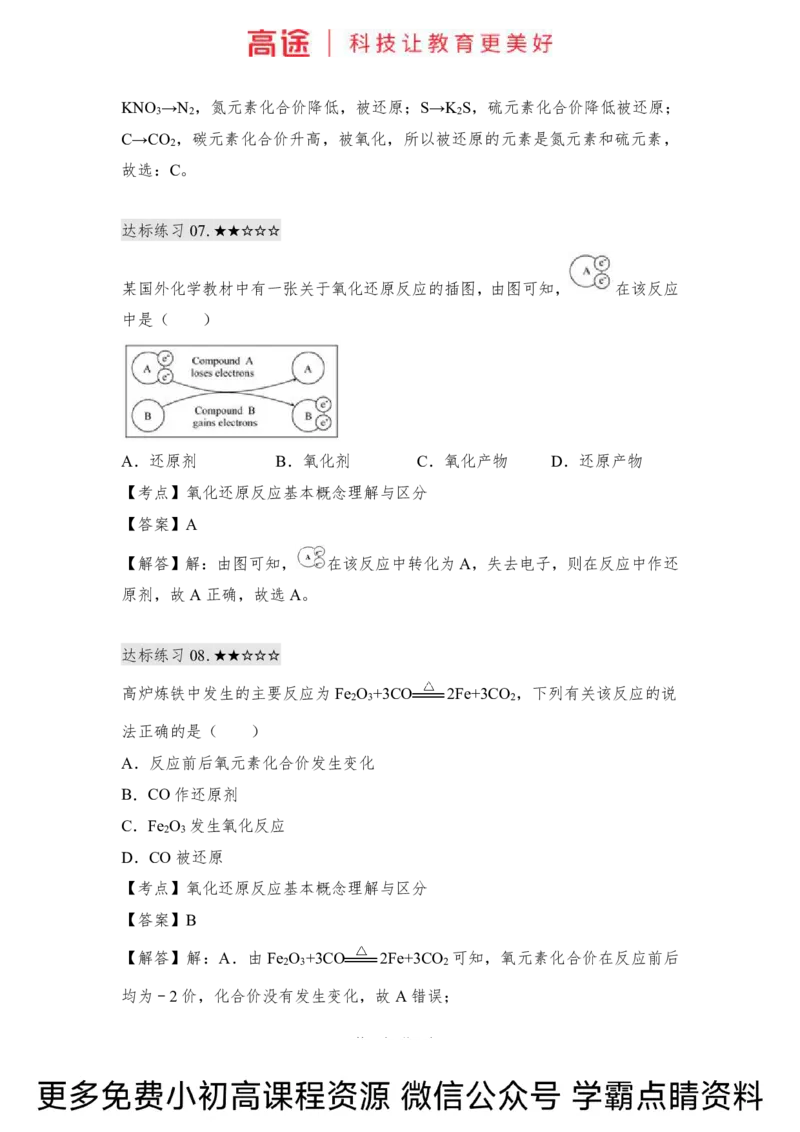
某国外化学教材中有一张关于氧化还原反应的插图,由图可知, 在该反应
中是( )
A.还原剂 B.氧化剂 C.氧化产物 D.还原产物
【考点】氧化还原反应基本概念理解与区分
【答案】A
【解答】解:由图可知, 在该反应中转化为 A,失去电子,则在反应中作还
原剂,故A正确,故选A。
达标练习08.
★★☆☆☆
高炉炼铁中发生的主要反应为Fe O +3CO 2Fe+3CO ,下列有关该反应的说
2 3 2
法正确的是( )
A.反应前后氧元素化合价发生变化
B.CO作还原剂
C.Fe O 发生氧化反应
2 3
D.CO被还原
【考点】氧化还原反应基本概念理解与区分
【答案】B
【解答】解:A.由 Fe O +3CO 2Fe+3CO 可知,氧元素化合价在反应前后
2 3 2
均为﹣2价,化合价没有发生变化,故A错误;
第4页(共8页)B.由 Fe O +3CO 2Fe+3CO 可知,CO中的 C 元素的化合价由+2 价失电子
2 3 2
升高到+4 价,被氧化,发生氧化反应,则CO是还原剂,故B 正确;
C.由 Fe O +3CO 2Fe+3CO 可知,氧化铁中铁元素化合价由+3 价得电子降
2 3 2
低到0价,被还原,发生还原反应,故C 错误;
D.由 Fe O +3CO 2Fe+3CO 可知,CO 中的 C 元素的化合价由+2 价失电子
2 3 2
升高到+4 价,被氧化,发生氧化反应,故D错误;故选:B。
达标练习09.
★★☆☆☆
实验室制取少量的氮气,常利用的反应是 NaNO +NH Cl NaCl+N ↑+2H O。
2 4 2 2
关于该反应说法正确的是( )
A.NaNO 是还原剂 B.N 只是氧化产物
2 2
C.NH Cl中的氮元素被氧化 D.N 既是氧化剂又是还原剂
4 2
【考点】氧化还原反应基本概念理解与区分
【答案】C
【解答】解:A.NaNO 中N元素的化合价降低,为氧化剂,故A错误;
2
B.N 既是氧化产物又是还原产物,故B 错误;
2
C.NH Cl中的N 元素化合价升高,失去电子,被氧化,故C 正确;
4
D.此反应中N 是产物,氧化剂和还原剂为反应物,故 D 错误;故选:C。
2
达标练习10.
★★☆☆☆
下列对X+Y ═XY (XY 中含X2+和Y﹣)的叙述正确的是( )
2 2 2
A.Y被还原,X2+是还原产物
B.Y被还原,X发生氧化反应
C.X是还原剂,Y被氧化
D.X被氧化,X显氧化性
【考点】氧化还原反应基本概念理解与区分
【答案】B
【解答】解:A.Y 化合价从 0 变为﹣1,化合价降低,被还原,X 化合价从 0
第5页(共8页)变为+2,化合价升高,被氧化,则X2+是氧化产物,故A错误;
B.Y 化合价从 0 变为﹣1,化合价降低,被还原,X 化合价从 0 变为+2,化合
价升高,被氧化,发生氧化反应,故B 正确;
C.X化合价从0变为+2,化合价升高,被氧化,为还原剂,Y的化合价降低,
被还原,故C 错误;
D.X元素化合价升高,被氧化,为还原剂,还原剂表现还原性,故D错误;故
选:B。
达标练习11.
★★☆☆☆
下列反应中,需加还原剂才能完成的是( )
A.HCl→Cl B.CO →CO C.CO →CaCO D.Al3+→A1O ﹣
2 2 2 3 2
【考点】氧化还原反应基本概念理解与区分
【答案】B
【解答】解:A.HCl→Cl 中 Cl 元素的化合价升高,需加氧化剂才完成,故 A
2
不选;
B、CO →CO 中C元素的化合价降低,需加还原剂才完成,故B 选;
2
C、二氧化碳与石灰水反应生成碳酸钙,没有化合价变化,非氧化还原反应,故
C 不选;
D、铝离子生成偏铝酸根(A1O ﹣),化合价没有变化,非氧化还原反应,故 D
2
不选;故选:B。
达标练习12.
★★☆☆☆
下列转化必须加入氧化剂才能进行的是( )
A.HCO ﹣→CO B.MnO ﹣→Mn2+ C.Fe2+→Fe3+ D.H O →O
3 2 4 2 2 2
【考点】氧化还原反应基本概念理解与区分
【答案】C
【解答】解:A.从HCO ﹣→CO ,元素化合价没有发生变化,不是氧化还原反
3 2
应,故A错误;
B.B中反应,Mn 元素化合价降低,被还原,应加入还原剂,故B 错误;
C.C中反应,Fe 元素化合价升高,被氧化,应加入氧化剂,故C 正确;
第6页(共8页)D.D中反应,过氧化氢分解生成氧气和水,反应中过氧化氢既是氧化剂也是还
原剂,故D错误。故选:C。
达标练习13.
★★☆☆☆
下列反应中,H O 既不做氧化剂又不做还原剂的是( )
2
通电
A.2H O 2H ↑+O ↑ B.2F +2H O═4HF+O
2 2 2 2 2 2
C.NaH+H O═NaOH+H ↑ D.SO +H O H SO
2 2 2 2 2 3
【考点】氧化还原反应基本概念理解与区分
⇌
【答案】D
通电
【解答】解:A.反应 2H O 2H ↑+O ↑中,水中H、O元素化合价均发生变
2 2 2
化,水既是氧化剂又是还原剂,故A错误;
B.2F +2H O═4HF+O 中,水分子中 O 元素从﹣2 价变为 0 价,水作还原剂,故
2 2 2
B 错误;
C.NaH+H O═NaOH+H ↑中,水中H 元素的化合价从+1 变为0 价,水作氧化剂,
2 2
故C 错误;
D.SO +H O H SO 不属于氧化还原反应,则 H O既不做氧化剂又不作还原剂,
2 2 2 3 2
故D正确;
⇌
故选:D。
达标练习14.
★★☆☆☆
下列微粒通常只具有氧化性的是( )
A.Na B.Fe2+ C.H+ D.Cl
2
【考点】氧化还原反应基本概念理解与区分
【答案】C
【解答】解:A.Na 中元素的化合价为0,为金属元素的最低价,只有还原性,
故A不选;
B.Fe2+中元素的化合价为+2价,为铁元素的中间价态,既有氧化性又有还原性,
故B 不选;
C.H+中元素的化合价为+1 价,为H元素的最高价,只有氧化性,故C选;
第7页(共8页)D.Cl 中Cl元素化合价为0,为中间价态,既有氧化性又有还原性,故D不选;
2
故选:C。
达标练习15.
★★★☆☆
人体血红蛋白中含有Fe2+,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使
Fe2+转变为Fe3+,血红蛋白转变为高铁血红蛋白而丧失与O 结合的能力,服用
2
维生素C 可缓解亚硝酸盐的中毒。下列说法正确的( )
A.亚硝酸盐表现出还原性
B.维生素C可被亚硝酸盐氧化
C.维生素C表现出氧化性
D.中毒时亚硝酸盐被Fe2+氧化成硝酸盐
【考点】氧化还原反应基本概念应用
【答案】B
【解答】解:A.由分析可知维生素 C具有还原性,起还原剂的作用,是还原剂,
则亚硝酸盐是氧化剂,表现出氧化性,故A错误;
B.由分析可知维生素 C是还原剂,亚硝酸盐是氧化剂,维生素C可被亚硝酸盐
氧化,故B 正确;
C.由分析可知维生素C具有还原性,起还原剂的作用,是还原剂,故C 错误;
D.亚硝酸盐会使 Fe2+转变为Fe3+,Fe2+是还原剂,中毒时亚硝酸盐被 Fe2+还原,
故D错误;故选:B。
第8页(共8页)