文档内容
第3讲 热力学定律与能量守恒定律
素养目标 1.能认识物质的运动形式有多种,不同运动形式对应不同形式的能,各种
形式的能在一定条件下可以相互转化.(物理观念) 2.认识热力学第一定律、热力学第二定
律及两类永动机.(物理观念) 3.理解热力学第一定律与能量守恒定律的关系.(科学思维) 4.
能应用热力学第一定律分析有关实际问题.(科学思维)
一、热力学第一定律
1.改变物体内能的两种方式
(1)做功;(2)热传递.
2.热力学第一定律
(1)内容:一个热力学系统的内能增量等于外界向它传递的热量与外界对它所做的功的
和.
(2)表达式:ΔU= Q + W .
(3)表达式中的正、负号法则
符号 W Q ΔU
+ 外界对物体做功 物体吸收热量 内能增加
- 物体对外界做功 物体放出热量 内能减少
二、能量守恒定律
1.内容
能量既不会凭空产生,也不会凭空消失,它只能从一种形式转化为另一种形式,或者
是从一个物体转移到别的物体,在转化或转移的过程中,能量的总量保持不变.
2.条件性
能量守恒定律是自然界的普遍规律,某一种形式的能是否守恒是有条件的.
3.第一类永动机是不可能制成的,它违背了能量守恒定律.
三、热力学第二定律
1.热力学第二定律的两种表述
(1)克劳修斯表述:热量不能自发地从低温物体传到高温物体.
(2)开尔文表述:不可能从单一热库吸收热量,使之完全变成功,而不产生其他影响.
或表述为“第二类永动机是不可能制成的”.
直
观
情
境
2.用熵的概念表述热力学第二定律在任何自然过程中,一个孤立系统的总熵不会减小.
3.热力学第二定律的微观意义
一切自发过程总是沿着分子热运动的无序性增大的方向进行.
4.第二类永动机不可能制成的原因是违背了热力学第二定律.
1.思维辨析
(1)做功和热传递的实质是相同的.( )
(2)绝热过程中,外界压缩气体做功20 J,气体的内能一定减少. ( )
(3)物体吸收热量,同时对外做功,内能可能不变.( )
(4)电冰箱的工作过程表明,热量可以从低温物体向高温物体传递. ( )
2.关于热力学定律,下列说法正确的是( )
A.在一定条件下,物体的温度可以降到0 K
B.物体从单一热源吸收的热量可全部用于做功
C.吸收了热量的物体,其内能一定增加
D.压缩气体总能使气体的温度升高
3.一定质量的理想气体,从某一状态开始,经过一系列变化后又回到初始状态.W
1
表示外界对气体做的功,W 表示气体对外界做的功,Q 表示气体吸收的热量,Q 表示气体
2 1 2
放出的热量.在整个过程中一定有( )
A.Q-Q=W-W B.Q=Q
1 2 2 1 1 2
C.W=W D.Q>Q
1 2 1
考点 热力学第一定律
1.热力学第一定律 Δ U = Q + W
(1)符号法则
符号 W Q ΔU
+ 外界对物体做功 物体吸收热量 内能增加
- 物体对外界做功 物体放出热量 内能减小
(2)三种特殊情况
过程 含义 内能变化 物理意义
绝热 Q=0 Δ U = W 外界对物体做的功等于物体内能的增加
等容 W=0 Q = Δ U 物体吸收的热量等于物体内能的增加
等温 ΔU=0 W=-Q 外界对物体做的功,等于物体放出的热量
2.温度、内能、热量、功的比较
项目 含义 特点
表示物体的冷热程度,是物体分子平均动能大小的标
温度 状态量
志,它是大量分子热运动的集体表现,对个别分子来说,温度没有意义
物体内所有分子动能和势能的总和,它是由大量分子的
内能 状态量
热运动和分子的相对位置所决定的能
指在热力学系统与外界之间依靠温差传递的能量,热量
热量 是过程量,只能说“吸收”“放出”,不能说“含有”
“具有” 过程量
做功过程是机械能或其他形式的能和内能之间的转化过
功
程
典例1 (2023·全国甲卷)(多选)在一汽缸中用活塞封闭着一定量的理想气体,发生下列
缓慢变化过程,气体一定与外界有热量交换的过程是( )
A.气体的体积不变,温度升高
B.气体的体积减小,温度降低
C.气体的体积减小,温度升高
D.气体的体积增大,温度不变
E.气体的体积增大,温度降低
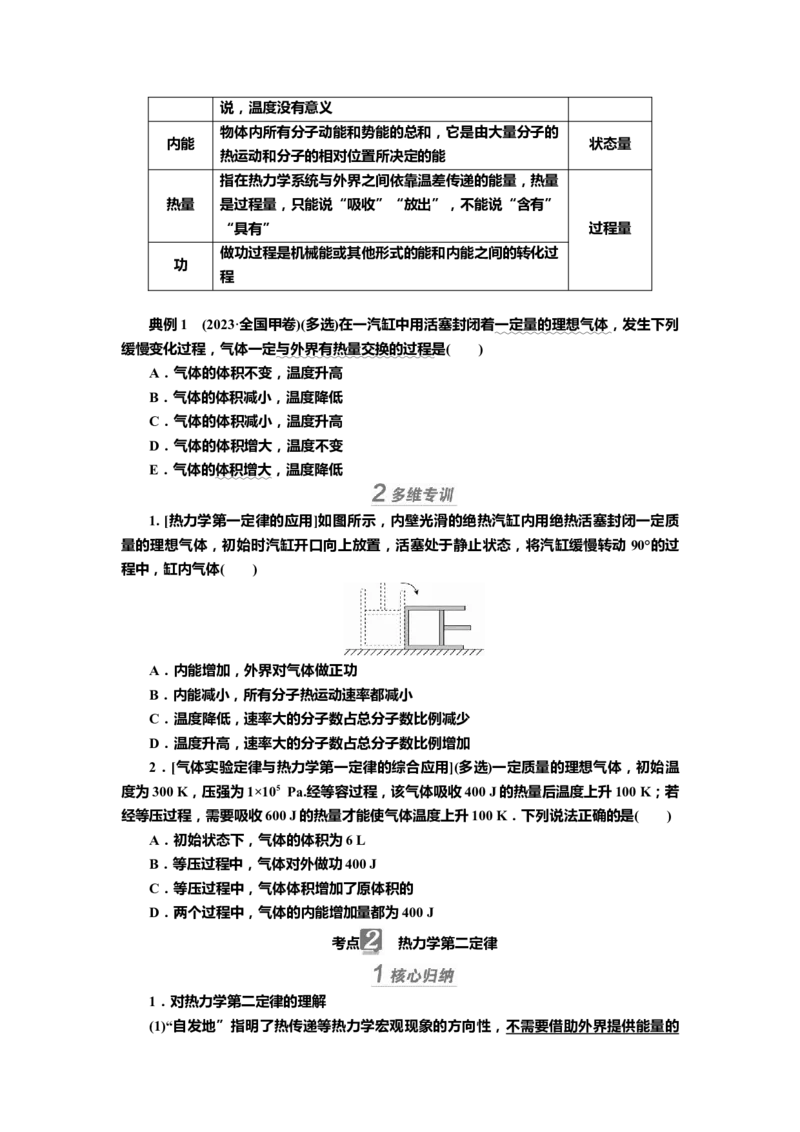
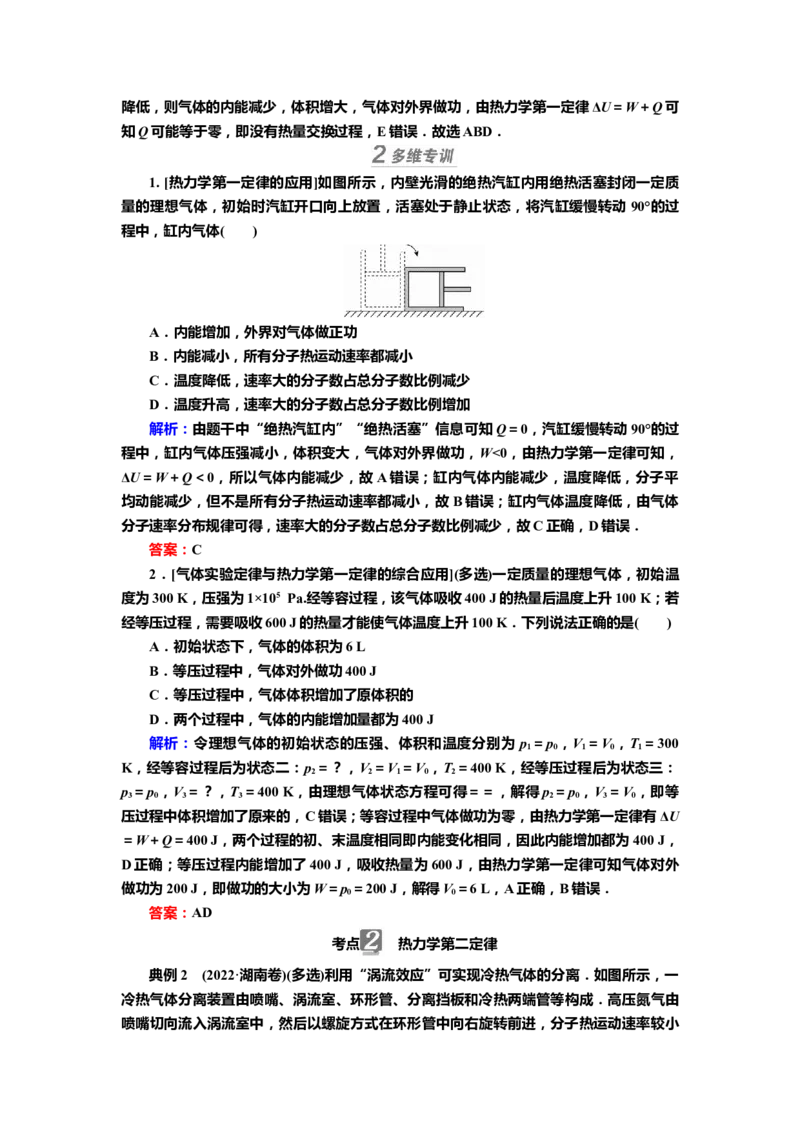
1. [热力学第一定律的应用]如图所示,内壁光滑的绝热汽缸内用绝热活塞封闭一定质
量的理想气体,初始时汽缸开口向上放置,活塞处于静止状态,将汽缸缓慢转动 90°的过
程中,缸内气体( )
A.内能增加,外界对气体做正功
B.内能减小,所有分子热运动速率都减小
C.温度降低,速率大的分子数占总分子数比例减少
D.温度升高,速率大的分子数占总分子数比例增加
2.[气体实验定律与热力学第一定律的综合应用](多选)一定质量的理想气体,初始温
度为300 K,压强为1×105 Pa.经等容过程,该气体吸收400 J的热量后温度上升100 K;若
经等压过程,需要吸收600 J的热量才能使气体温度上升100 K.下列说法正确的是( )
A.初始状态下,气体的体积为6 L
B.等压过程中,气体对外做功400 J
C.等压过程中,气体体积增加了原体积的
D.两个过程中,气体的内能增加量都为400 J
考点 热力学第二定律
1.对热力学第二定律的理解
(1)“自发地”指明了热传递等热力学宏观现象的方向性,不需要借助外界提供能量的帮助.
(2)“不产生其他影响”的涵义是发生的热力学宏观过程只在本系统内完成,对周围环
境不产生热力学方面的影响.如吸热、放热、做功等.
2.热力学第二定律的实质
自然界中进行的涉及热现象的宏观过程都具有方向性.
(1)高温物体低温物体.
(2)功热.
(3)气体体积V 气体体积V (较大).
1 2
(4)不同气体A和B混合气体AB.
3.两类永动机的比较
第一类永动机 第二类永动机
不需要任何动力或燃料,却能不断地对外做 从单一热源吸收热量,使之完全变成功,而
功的机器 不产生其他影响的机器
不违背能量守恒定律,但违背热力学第二定
违背能量守恒定律,不可能制成
律,不可能制成
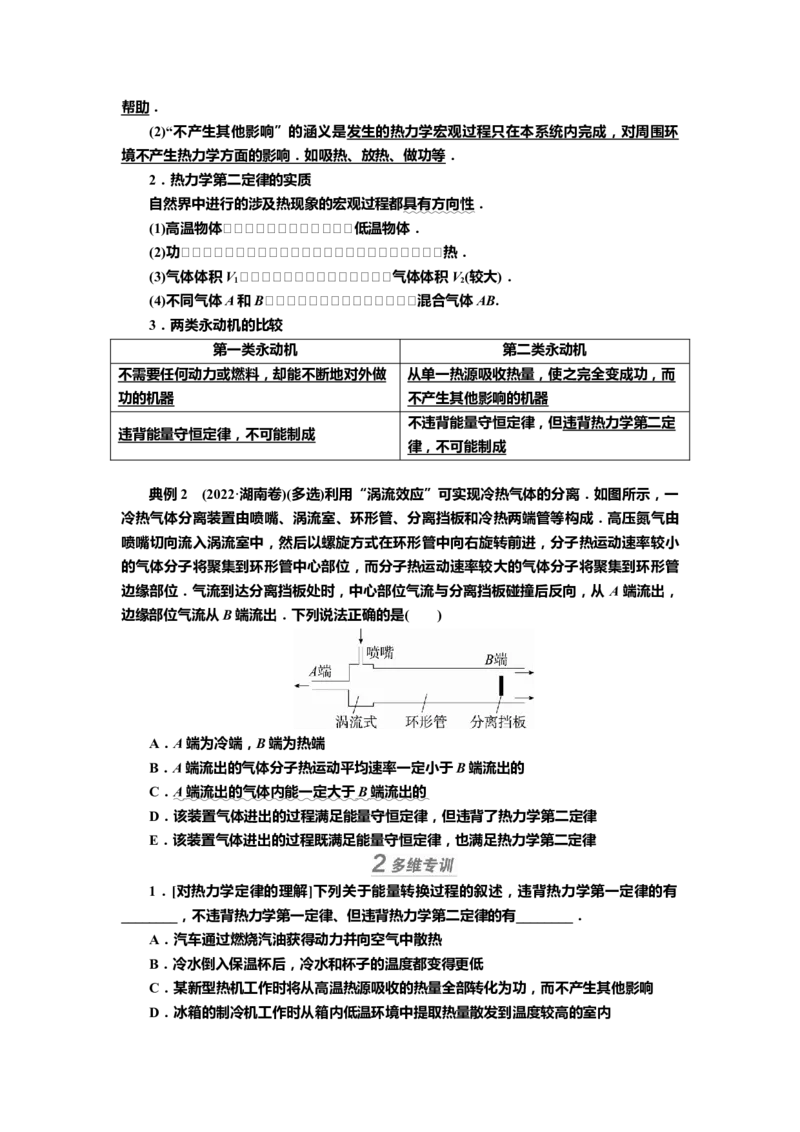
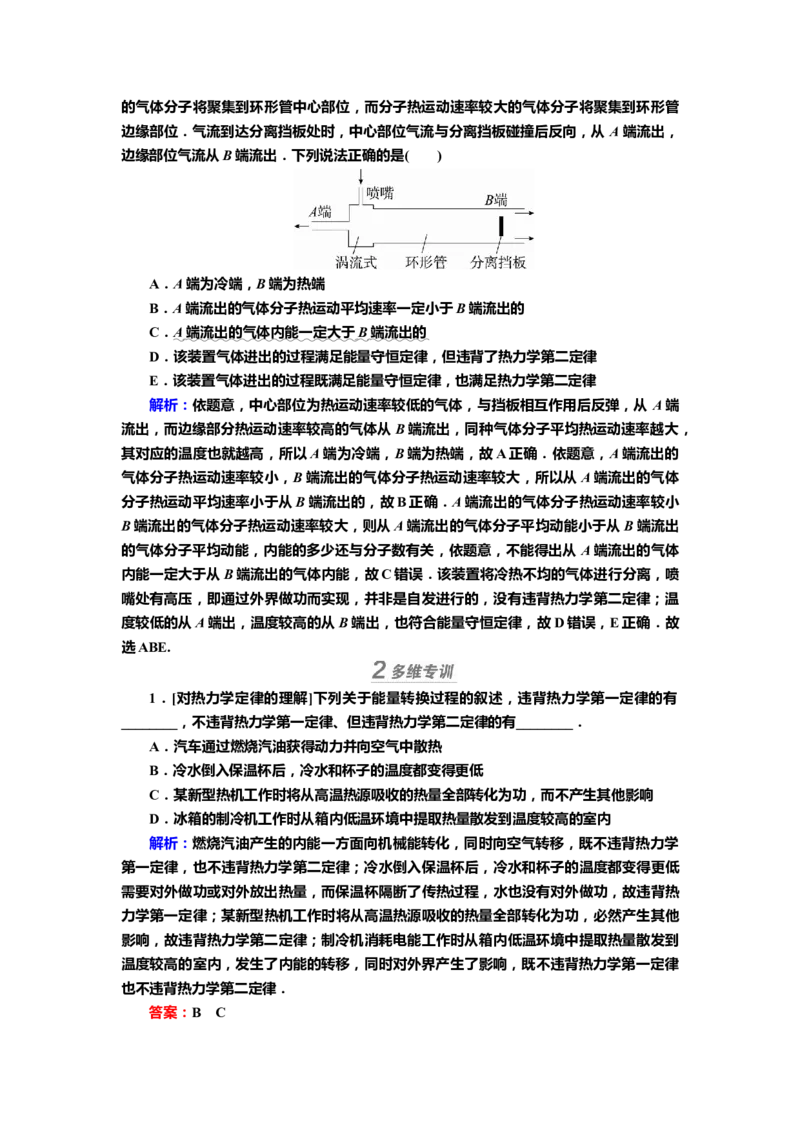
典例2 (2022·湖南卷)(多选)利用“涡流效应”可实现冷热气体的分离.如图所示,一
冷热气体分离装置由喷嘴、涡流室、环形管、分离挡板和冷热两端管等构成.高压氮气由
喷嘴切向流入涡流室中,然后以螺旋方式在环形管中向右旋转前进,分子热运动速率较小
的气体分子将聚集到环形管中心部位,而分子热运动速率较大的气体分子将聚集到环形管
边缘部位.气流到达分离挡板处时,中心部位气流与分离挡板碰撞后反向,从 A端流出,
边缘部位气流从B端流出.下列说法正确的是( )
A.A端为冷端,B端为热端
B.A端流出的气体分子热运动平均速率一定小于B端流出的
C. A 端流出的气体内能一定大于 B 端流出的
D.该装置气体进出的过程满足能量守恒定律,但违背了热力学第二定律
E.该装置气体进出的过程既满足能量守恒定律,也满足热力学第二定律
1.[对热力学定律的理解]下列关于能量转换过程的叙述,违背热力学第一定律的有
________,不违背热力学第一定律、但违背热力学第二定律的有________.
A.汽车通过燃烧汽油获得动力并向空气中散热
B.冷水倒入保温杯后,冷水和杯子的温度都变得更低
C.某新型热机工作时将从高温热源吸收的热量全部转化为功,而不产生其他影响
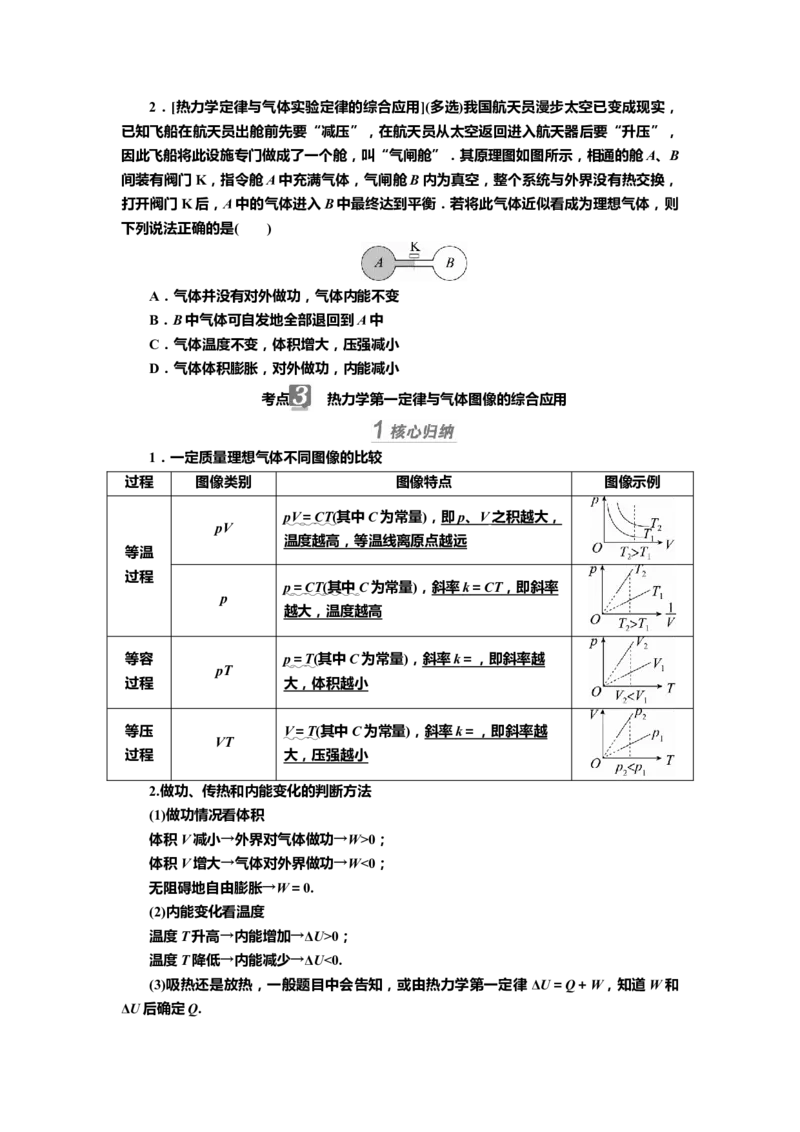
D.冰箱的制冷机工作时从箱内低温环境中提取热量散发到温度较高的室内2.[热力学定律与气体实验定律的综合应用](多选)我国航天员漫步太空已变成现实,
已知飞船在航天员出舱前先要“减压”,在航天员从太空返回进入航天器后要“升压”,
因此飞船将此设施专门做成了一个舱,叫“气闸舱”.其原理图如图所示,相通的舱A、B
间装有阀门K,指令舱A中充满气体,气闸舱B内为真空,整个系统与外界没有热交换,
打开阀门K后,A中的气体进入B中最终达到平衡.若将此气体近似看成为理想气体,则
下列说法正确的是( )
A.气体并没有对外做功,气体内能不变
B.B中气体可自发地全部退回到A中
C.气体温度不变,体积增大,压强减小
D.气体体积膨胀,对外做功,内能减小
考点 热力学第一定律与气体图像的综合应用
1.一定质量理想气体不同图像的比较
过程 图像类别 图像特点 图像示例
pV = CT (其中C为常量), 即 p 、 V 之积越大,
pV
温度越高,等温线离原点越远
等温
过程
p = CT ( 其中 C为常量), 斜率 k = CT ,即斜率
p
越大,温度越高
等容 p = T (其中C为常量), 斜率 k =,即斜率越
pT
过程 大,体积越小
等压 V = T (其中C为常量), 斜率 k =,即斜率越
VT
过程 大,压强越小
2.做功、传热和内能变化的判断方法
(1)做功情况看体积
体积V减小→外界对气体做功→W>0;
体积V增大→气体对外界做功→W<0;
无阻碍地自由膨胀→W=0.
(2)内能变化看温度
温度T升高→内能增加→ΔU>0;
温度T降低→内能减少→ΔU<0.
(3)吸热还是放热,一般题目中会告知,或由热力学第一定律 ΔU=Q+W,知道W和
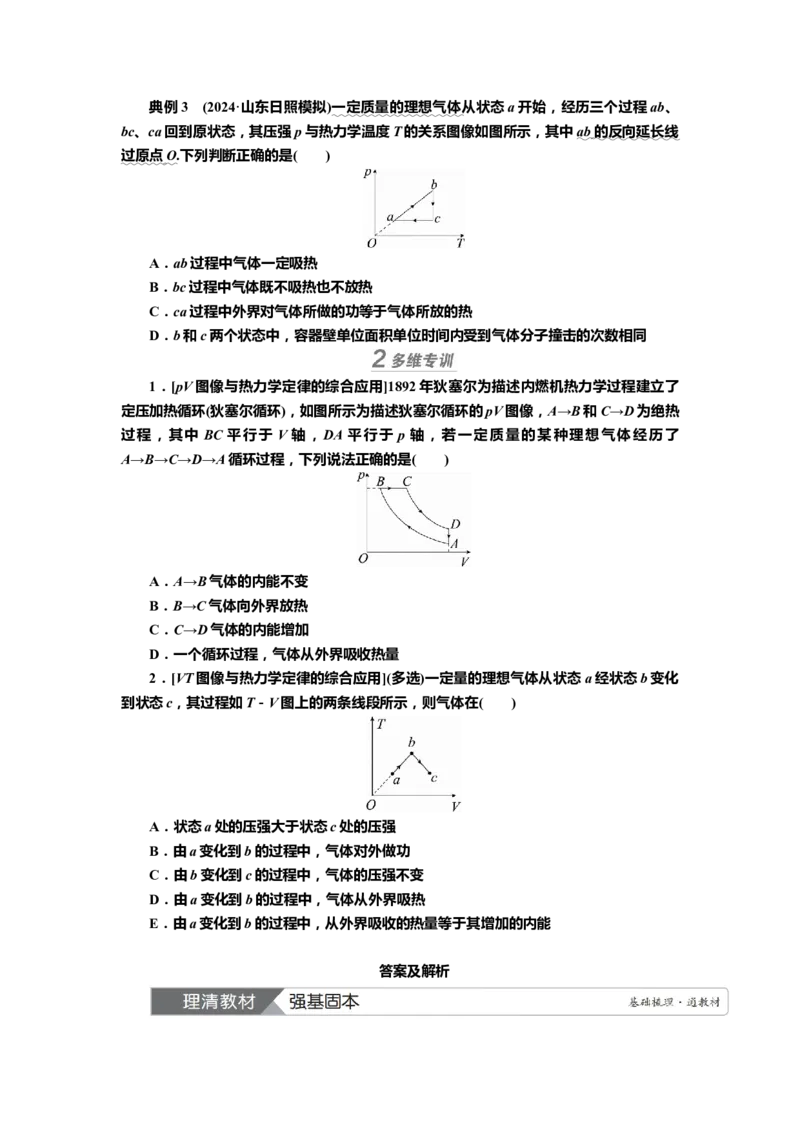
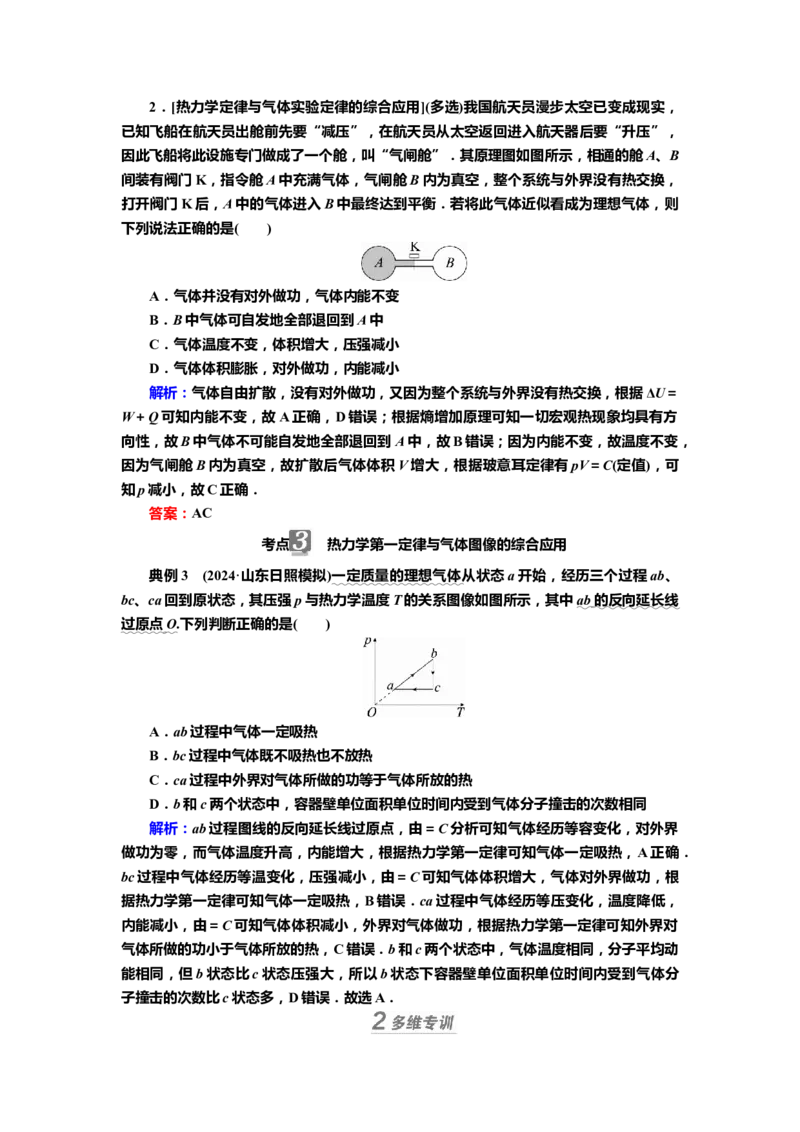
ΔU后确定Q.典例3 (2024·山东日照模拟)一定质量的理想气体从状态a开始,经历三个过程ab、
bc、ca回到原状态,其压强p与热力学温度T的关系图像如图所示,其中 ab 的反向延长线
过原点 O .下列判断正确的是( )
A.ab过程中气体一定吸热
B.bc过程中气体既不吸热也不放热
C.ca过程中外界对气体所做的功等于气体所放的热
D.b和c两个状态中,容器壁单位面积单位时间内受到气体分子撞击的次数相同
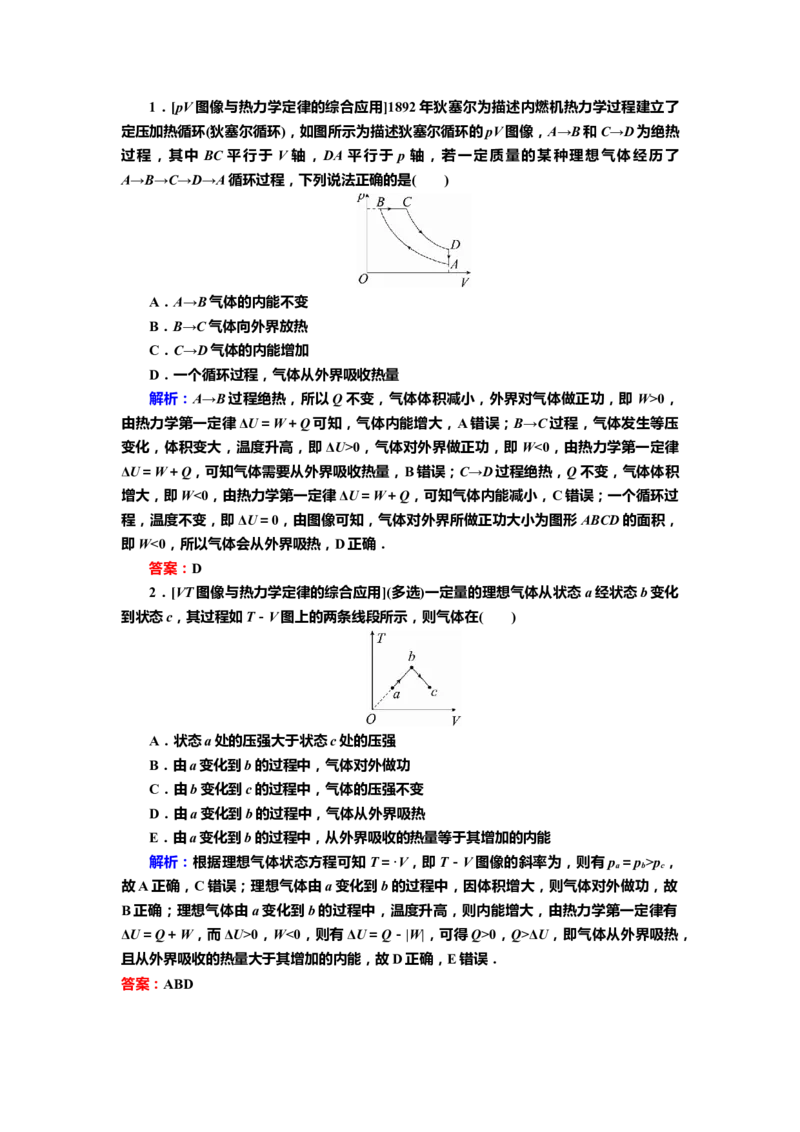
1.[pV图像与热力学定律的综合应用]1892年狄塞尔为描述内燃机热力学过程建立了
定压加热循环(狄塞尔循环),如图所示为描述狄塞尔循环的pV图像,A→B和C→D为绝热
过程,其中 BC 平行于 V 轴,DA 平行于 p 轴,若一定质量的某种理想气体经历了
A→B→C→D→A循环过程,下列说法正确的是( )
A.A→B气体的内能不变
B.B→C气体向外界放热
C.C→D气体的内能增加
D.一个循环过程,气体从外界吸收热量
2.[VT图像与热力学定律的综合应用](多选)一定量的理想气体从状态a经状态b变化
到状态c,其过程如T-V图上的两条线段所示,则气体在( )
A.状态a处的压强大于状态c处的压强
B.由a变化到b的过程中,气体对外做功
C.由b变化到c的过程中,气体的压强不变
D.由a变化到b的过程中,气体从外界吸热
E.由a变化到b的过程中,从外界吸收的热量等于其增加的内能
答案及解析1.思维辨析
(1)做功和热传递的实质是相同的.(×)
(2)绝热过程中,外界压缩气体做功20 J,气体的内能一定减少. (×)
(3)物体吸收热量,同时对外做功,内能可能不变.(√)
(4)电冰箱的工作过程表明,热量可以从低温物体向高温物体传递. (√)
2.关于热力学定律,下列说法正确的是( )
A.在一定条件下,物体的温度可以降到0 K
B.物体从单一热源吸收的热量可全部用于做功
C.吸收了热量的物体,其内能一定增加
D.压缩气体总能使气体的温度升高
解析:热力学的绝对零度不可能达到,A错误;根据热力学第二定律,物体从单一热
源吸收的热量可全部用于对外做功,但会引起其他变化,B正确;物体从外界吸收了热量,
若全部用来对外界做功,其内能不变,C错误;压缩气体的过程对气体做功,若气体同时
向外界释放热量,根据能量守恒定律可知,气体的内能可能减少,温度可能降低,D错误.
答案:B
3.一定质量的理想气体,从某一状态开始,经过一系列变化后又回到初始状态.W
1
表示外界对气体做的功,W 表示气体对外界做的功,Q 表示气体吸收的热量,Q 表示气体
2 1 2
放出的热量.在整个过程中一定有( )
A.Q-Q=W-W B.Q=Q
1 2 2 1 1 2
C.W=W D.Q>Q
1 2 1
解析:根据题意可知,W 为正功,W 为负功,Q 为正,Q 为负,故W=W -W ,Q
1 2 1 2 1 2
=Q-Q,因为气体从某一状态开始,经过一系列变化后又回到开始的状态,所以 ΔU=W
1 2
+Q=0,即(W-W)+(Q-Q)=0,所以A正确.
1 2 1 2
答案:A
考点 热力学第一定律
典例1 (2023·全国甲卷)(多选)在一汽缸中用活塞封闭着一定量的理想气体,发生下列
缓慢变化过程,气体一定与外界有热量交换的过程是( )
A.气体的体积不变,温度升高
B.气体的体积减小,温度降低
C.气体的体积减小,温度升高
D.气体的体积增大,温度不变
E.气体的体积增大,温度降低
解析:气体的温度升高,则气体的内能增多,体积不变,气体做功为零,因此气体吸
收热量,A正确;气体的温度降低,则气体的内能减少,体积减小,外界对气体做功,由
热力学第一定律ΔU=W+Q可知气体对外放热,B正确;气体的温度升高,则气体的内能
增多,体积减小,外界对气体做功,由热力学第一定律ΔU=W+Q可知Q可能等于零,即
没有热量交换过程,C错误;气体的温度不变,则气体的内能不变,体积增大,气体对外
界做功,由热力学第一定律ΔU=W+Q可知Q>0,即气体吸收热量,D正确;气体的温度降低,则气体的内能减少,体积增大,气体对外界做功,由热力学第一定律ΔU=W+Q可
知Q可能等于零,即没有热量交换过程,E错误.故选ABD.
1. [热力学第一定律的应用]如图所示,内壁光滑的绝热汽缸内用绝热活塞封闭一定质
量的理想气体,初始时汽缸开口向上放置,活塞处于静止状态,将汽缸缓慢转动 90°的过
程中,缸内气体( )
A.内能增加,外界对气体做正功
B.内能减小,所有分子热运动速率都减小
C.温度降低,速率大的分子数占总分子数比例减少
D.温度升高,速率大的分子数占总分子数比例增加
解析:由题干中“绝热汽缸内”“绝热活塞”信息可知Q=0,汽缸缓慢转动90°的过
程中,缸内气体压强减小,体积变大,气体对外界做功,W<0,由热力学第一定律可知,
ΔU=W+Q<0,所以气体内能减少,故A错误;缸内气体内能减少,温度降低,分子平
均动能减少,但不是所有分子热运动速率都减小,故B错误;缸内气体温度降低,由气体
分子速率分布规律可得,速率大的分子数占总分子数比例减少,故C正确,D错误.
答案:C
2.[气体实验定律与热力学第一定律的综合应用](多选)一定质量的理想气体,初始温
度为300 K,压强为1×105 Pa.经等容过程,该气体吸收400 J的热量后温度上升100 K;若
经等压过程,需要吸收600 J的热量才能使气体温度上升100 K.下列说法正确的是( )
A.初始状态下,气体的体积为6 L
B.等压过程中,气体对外做功400 J
C.等压过程中,气体体积增加了原体积的
D.两个过程中,气体的内能增加量都为400 J
解析:令理想气体的初始状态的压强、体积和温度分别为 p =p ,V =V ,T =300
1 0 1 0 1
K,经等容过程后为状态二:p =?,V =V =V ,T =400 K,经等压过程后为状态三:
2 2 1 0 2
p =p ,V =?,T =400 K,由理想气体状态方程可得==,解得p =p ,V =V ,即等
3 0 3 3 2 0 3 0
压过程中体积增加了原来的,C错误;等容过程中气体做功为零,由热力学第一定律有ΔU
=W+Q=400 J,两个过程的初、末温度相同即内能变化相同,因此内能增加都为400 J,
D正确;等压过程内能增加了400 J,吸收热量为600 J,由热力学第一定律可知气体对外
做功为200 J,即做功的大小为W=p=200 J,解得V =6 L,A正确,B错误.
0 0
答案:AD
考点 热力学第二定律
典例2 (2022·湖南卷)(多选)利用“涡流效应”可实现冷热气体的分离.如图所示,一
冷热气体分离装置由喷嘴、涡流室、环形管、分离挡板和冷热两端管等构成.高压氮气由
喷嘴切向流入涡流室中,然后以螺旋方式在环形管中向右旋转前进,分子热运动速率较小的气体分子将聚集到环形管中心部位,而分子热运动速率较大的气体分子将聚集到环形管
边缘部位.气流到达分离挡板处时,中心部位气流与分离挡板碰撞后反向,从 A端流出,
边缘部位气流从B端流出.下列说法正确的是( )
A.A端为冷端,B端为热端
B.A端流出的气体分子热运动平均速率一定小于B端流出的
C. A 端流出的气体内能一定大于 B 端流出的
D.该装置气体进出的过程满足能量守恒定律,但违背了热力学第二定律
E.该装置气体进出的过程既满足能量守恒定律,也满足热力学第二定律
解析:依题意,中心部位为热运动速率较低的气体,与挡板相互作用后反弹,从 A端
流出,而边缘部分热运动速率较高的气体从B端流出,同种气体分子平均热运动速率越大,
其对应的温度也就越高,所以A端为冷端,B端为热端,故A正确.依题意,A端流出的
气体分子热运动速率较小,B端流出的气体分子热运动速率较大,所以从A端流出的气体
分子热运动平均速率小于从B端流出的,故B正确.A端流出的气体分子热运动速率较小
B端流出的气体分子热运动速率较大,则从A端流出的气体分子平均动能小于从B端流出
的气体分子平均动能,内能的多少还与分子数有关,依题意,不能得出从 A端流出的气体
内能一定大于从B端流出的气体内能,故C错误.该装置将冷热不均的气体进行分离,喷
嘴处有高压,即通过外界做功而实现,并非是自发进行的,没有违背热力学第二定律;温
度较低的从A端出,温度较高的从B端出,也符合能量守恒定律,故D错误,E正确.故
选ABE.
1.[对热力学定律的理解]下列关于能量转换过程的叙述,违背热力学第一定律的有
________,不违背热力学第一定律、但违背热力学第二定律的有________.
A.汽车通过燃烧汽油获得动力并向空气中散热
B.冷水倒入保温杯后,冷水和杯子的温度都变得更低
C.某新型热机工作时将从高温热源吸收的热量全部转化为功,而不产生其他影响
D.冰箱的制冷机工作时从箱内低温环境中提取热量散发到温度较高的室内
解析:燃烧汽油产生的内能一方面向机械能转化,同时向空气转移,既不违背热力学
第一定律,也不违背热力学第二定律;冷水倒入保温杯后,冷水和杯子的温度都变得更低
需要对外做功或对外放出热量,而保温杯隔断了传热过程,水也没有对外做功,故违背热
力学第一定律;某新型热机工作时将从高温热源吸收的热量全部转化为功,必然产生其他
影响,故违背热力学第二定律;制冷机消耗电能工作时从箱内低温环境中提取热量散发到
温度较高的室内,发生了内能的转移,同时对外界产生了影响,既不违背热力学第一定律
也不违背热力学第二定律.
答案:B C2.[热力学定律与气体实验定律的综合应用](多选)我国航天员漫步太空已变成现实,
已知飞船在航天员出舱前先要“减压”,在航天员从太空返回进入航天器后要“升压”,
因此飞船将此设施专门做成了一个舱,叫“气闸舱”.其原理图如图所示,相通的舱A、B
间装有阀门K,指令舱A中充满气体,气闸舱B内为真空,整个系统与外界没有热交换,
打开阀门K后,A中的气体进入B中最终达到平衡.若将此气体近似看成为理想气体,则
下列说法正确的是( )
A.气体并没有对外做功,气体内能不变
B.B中气体可自发地全部退回到A中
C.气体温度不变,体积增大,压强减小
D.气体体积膨胀,对外做功,内能减小
解析:气体自由扩散,没有对外做功,又因为整个系统与外界没有热交换,根据ΔU=
W+Q可知内能不变,故A正确,D错误;根据熵增加原理可知一切宏观热现象均具有方
向性,故B中气体不可能自发地全部退回到A中,故B错误;因为内能不变,故温度不变,
因为气闸舱B内为真空,故扩散后气体体积V增大,根据玻意耳定律有pV=C(定值),可
知p减小,故C正确.
答案:AC
考点 热力学第一定律与气体图像的综合应用
典例3 (2024·山东日照模拟)一定质量的理想气体从状态a开始,经历三个过程ab、
bc、ca回到原状态,其压强p与热力学温度T的关系图像如图所示,其中 ab 的反向延长线
过原点 O .下列判断正确的是( )
A.ab过程中气体一定吸热
B.bc过程中气体既不吸热也不放热
C.ca过程中外界对气体所做的功等于气体所放的热
D.b和c两个状态中,容器壁单位面积单位时间内受到气体分子撞击的次数相同
解析:ab过程图线的反向延长线过原点,由=C分析可知气体经历等容变化,对外界
做功为零,而气体温度升高,内能增大,根据热力学第一定律可知气体一定吸热,A正确.
bc过程中气体经历等温变化,压强减小,由=C可知气体体积增大,气体对外界做功,根
据热力学第一定律可知气体一定吸热,B错误.ca过程中气体经历等压变化,温度降低,
内能减小,由=C可知气体体积减小,外界对气体做功,根据热力学第一定律可知外界对
气体所做的功小于气体所放的热,C错误.b和c两个状态中,气体温度相同,分子平均动
能相同,但b状态比c状态压强大,所以b状态下容器壁单位面积单位时间内受到气体分
子撞击的次数比c状态多,D错误.故选A.1.[pV图像与热力学定律的综合应用]1892年狄塞尔为描述内燃机热力学过程建立了
定压加热循环(狄塞尔循环),如图所示为描述狄塞尔循环的pV图像,A→B和C→D为绝热
过程,其中 BC 平行于 V 轴,DA 平行于 p 轴,若一定质量的某种理想气体经历了
A→B→C→D→A循环过程,下列说法正确的是( )
A.A→B气体的内能不变
B.B→C气体向外界放热
C.C→D气体的内能增加
D.一个循环过程,气体从外界吸收热量
解析:A→B过程绝热,所以Q不变,气体体积减小,外界对气体做正功,即 W>0,
由热力学第一定律ΔU=W+Q可知,气体内能增大,A错误;B→C过程,气体发生等压
变化,体积变大,温度升高,即ΔU>0,气体对外界做正功,即W<0,由热力学第一定律
ΔU=W+Q,可知气体需要从外界吸收热量,B错误;C→D过程绝热,Q不变,气体体积
增大,即W<0,由热力学第一定律ΔU=W+Q,可知气体内能减小,C错误;一个循环过
程,温度不变,即ΔU=0,由图像可知,气体对外界所做正功大小为图形ABCD的面积,
即W<0,所以气体会从外界吸热,D正确.
答案:D
2.[VT图像与热力学定律的综合应用](多选)一定量的理想气体从状态a经状态b变化
到状态c,其过程如T-V图上的两条线段所示,则气体在( )
A.状态a处的压强大于状态c处的压强
B.由a变化到b的过程中,气体对外做功
C.由b变化到c的过程中,气体的压强不变
D.由a变化到b的过程中,气体从外界吸热
E.由a变化到b的过程中,从外界吸收的热量等于其增加的内能
解析:根据理想气体状态方程可知T=·V,即T-V图像的斜率为,则有p =p>p,
a b c
故A正确,C错误;理想气体由a变化到b的过程中,因体积增大,则气体对外做功,故
B正确;理想气体由a变化到b的过程中,温度升高,则内能增大,由热力学第一定律有
ΔU=Q+W,而ΔU>0,W<0,则有ΔU=Q-|W|,可得Q>0,Q>ΔU,即气体从外界吸热,
且从外界吸收的热量大于其增加的内能,故D正确,E错误.
答案:ABD