文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点提分训练(十四)粗盐中难溶性杂质的去除
一、选择题
1.食盐的主要成分是氯化钠,下列关于粗盐提纯实验的叙述中不正确的是( )
A.提纯后的精盐仍是混合物
B.精盐中氯化钠的纯度比粗盐大
C.通过粗盐提纯实验可除去粗盐中全部杂质
D.该提纯实验不能去除粗盐中可溶性杂质
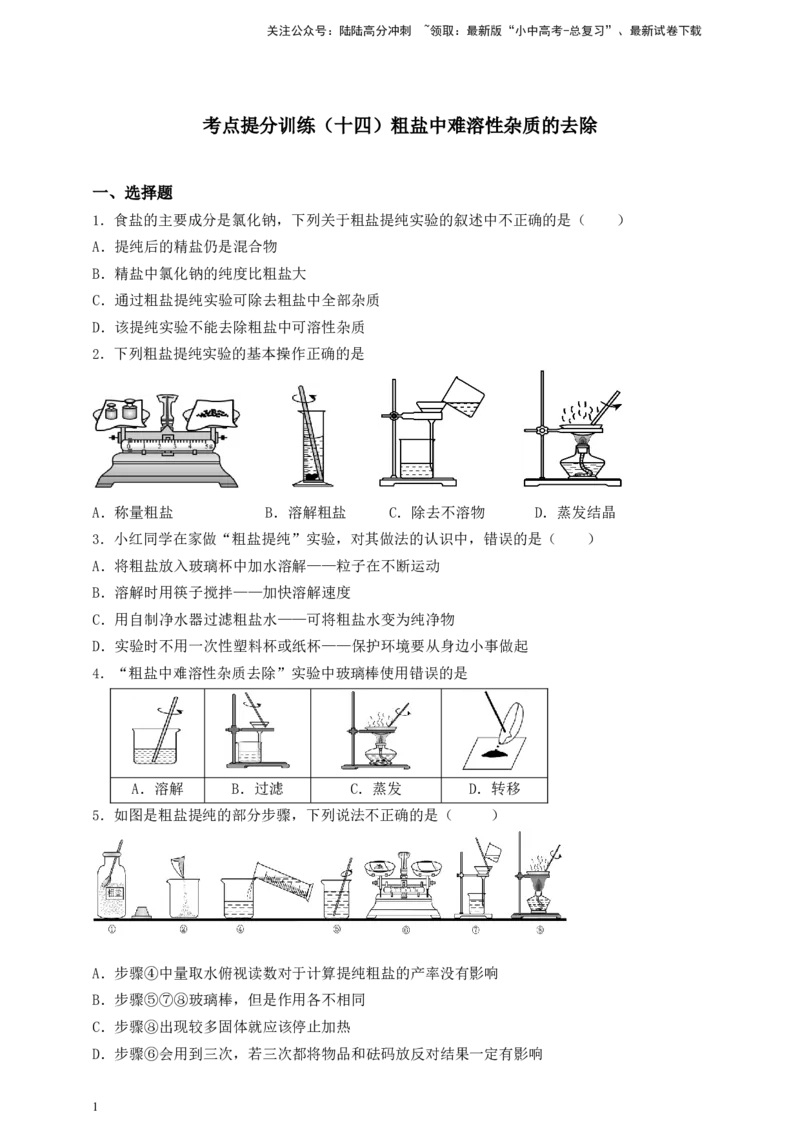
2.下列粗盐提纯实验的基本操作正确的是
A.称量粗盐 B.溶解粗盐 C.除去不溶物 D.蒸发结晶
3.小红同学在家做“粗盐提纯”实验,对其做法的认识中,错误的是( )
A.将粗盐放入玻璃杯中加水溶解——粒子在不断运动
B.溶解时用筷子搅拌——加快溶解速度
C.用自制净水器过滤粗盐水——可将粗盐水变为纯净物
D.实验时不用一次性塑料杯或纸杯——保护环境要从身边小事做起
4.“粗盐中难溶性杂质去除”实验中玻璃棒使用错误的是
A.溶解 B.过滤 C.蒸发 D.转移
5.如图是粗盐提纯的部分步骤,下列说法不正确的是( )
A.步骤④中量取水俯视读数对于计算提纯粗盐的产率没有影响
B.步骤⑤⑦⑧玻璃棒,但是作用各不相同
C.步骤⑧出现较多固体就应该停止加热
D.步骤⑥会用到三次,若三次都将物品和砝码放反对结果一定有影响
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
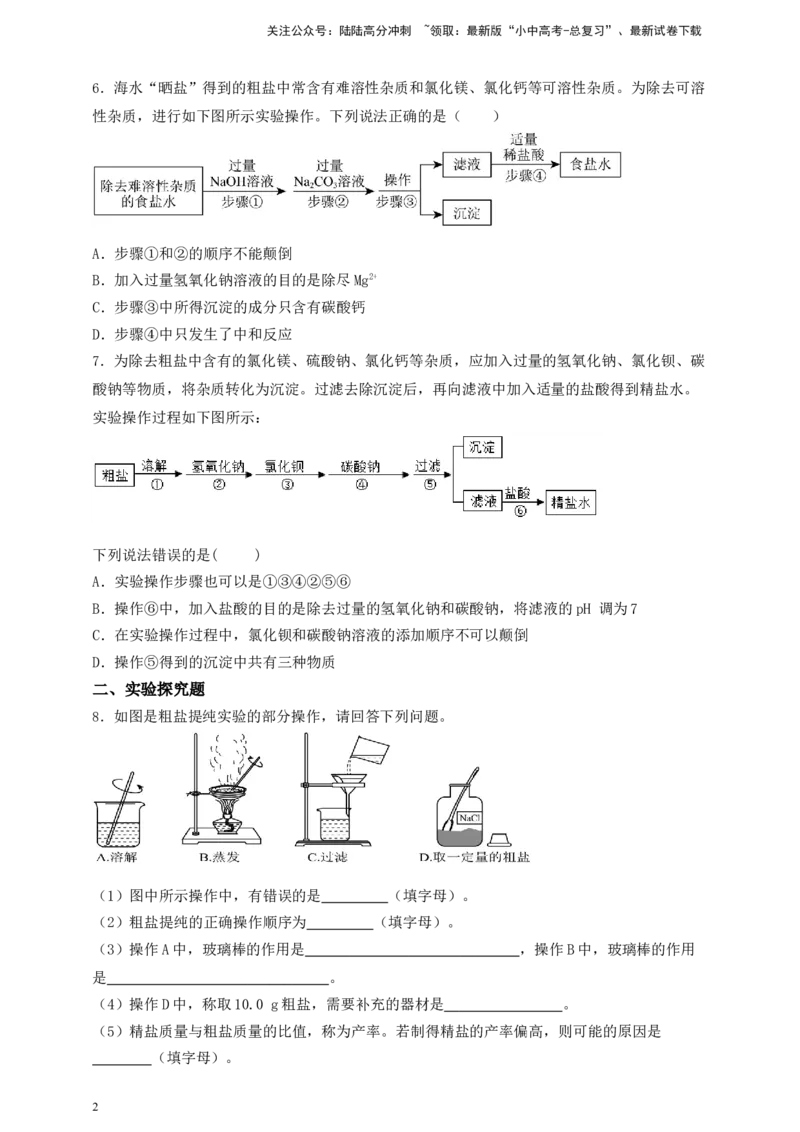
6.海水“晒盐”得到的粗盐中常含有难溶性杂质和氯化镁、氯化钙等可溶性杂质。为除去可溶
性杂质,进行如下图所示实验操作。下列说法正确的是( )
A.步骤①和②的顺序不能颠倒
B.加入过量氢氧化钠溶液的目的是除尽Mg2+
C.步骤③中所得沉淀的成分只含有碳酸钙
D.步骤④中只发生了中和反应
7.为除去粗盐中含有的氯化镁、硫酸钠、氯化钙等杂质,应加入过量的氢氧化钠、氯化钡、碳
酸钠等物质,将杂质转化为沉淀。过滤去除沉淀后,再向滤液中加入适量的盐酸得到精盐水。
实验操作过程如下图所示:
下列说法错误的是( )
A.实验操作步骤也可以是①③④②⑤⑥
B.操作⑥中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH 调为7
C.在实验操作过程中,氯化钡和碳酸钠溶液的添加顺序不可以颠倒
D.操作⑤得到的沉淀中共有三种物质
二、实验探究题
8.如图是粗盐提纯实验的部分操作,请回答下列问题。
(1)图中所示操作中,有错误的是 (填字母)。
(2)粗盐提纯的正确操作顺序为 (填字母)。
(3)操作A中,玻璃棒的作用是 ,操作B中,玻璃棒的作用
是 。
(4)操作D中,称取10.0 g粗盐,需要补充的器材是 。
(5)精盐质量与粗盐质量的比值,称为产率。若制得精盐的产率偏高,则可能的原因是
(填字母)。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含有泥沙的粗盐时,加入的水量不足
D.最终所得精盐比较潮湿
9.中国制盐的历史,至少可以追溯到5000年前。古人从海水制盐主要有煮盐和晒盐两种方
法,宋代以前的海盐制造都出于煎炼,到了清末海盐各产区大都改用晒制之法。
(1)煮盐和晒盐等同于实验室中的 操作。
(2)从能源、效率或便捷性的角度考虑,煮盐有不受环境天气限制、较为方便等优点,而晒盐
的优点是(写出一点即可) 。
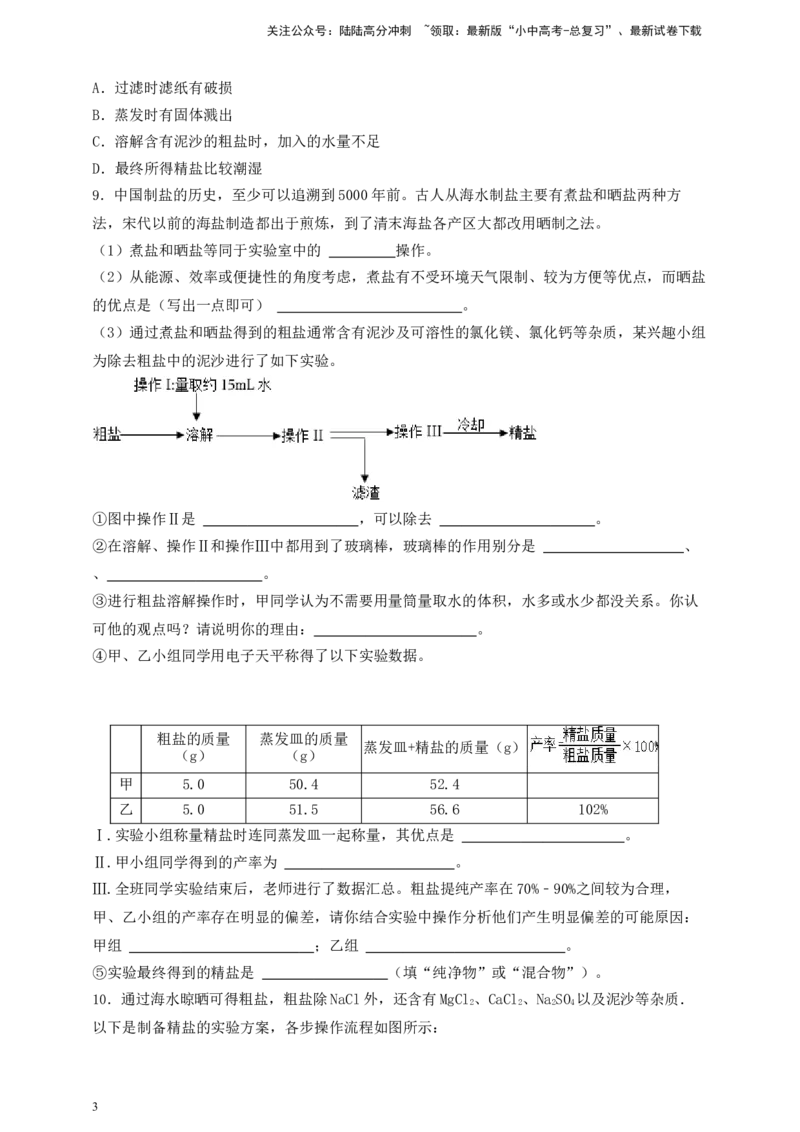
(3)通过煮盐和晒盐得到的粗盐通常含有泥沙及可溶性的氯化镁、氯化钙等杂质,某兴趣小组
为除去粗盐中的泥沙进行了如下实验。
①图中操作Ⅱ是 ,可以除去 。
②在溶解、操作Ⅱ和操作Ⅲ中都用到了玻璃棒,玻璃棒的作用别分是 、
、 。
③进行粗盐溶解操作时,甲同学认为不需要用量筒量取水的体积,水多或水少都没关系。你认
可他的观点吗?请说明你的理由: 。
④甲、乙小组同学用电子天平称得了以下实验数据。
粗盐的质量 蒸发皿的质量
蒸发皿+精盐的质量(g)
(g) (g)
甲 5.0 50.4 52.4
乙 5.0 51.5 56.6 102%
Ⅰ.实验小组称量精盐时连同蒸发皿一起称量,其优点是 。
Ⅱ.甲小组同学得到的产率为 。
Ⅲ.全班同学实验结束后,老师进行了数据汇总。粗盐提纯产率在70%﹣90%之间较为合理,
甲、乙小组的产率存在明显的偏差,请你结合实验中操作分析他们产生明显偏差的可能原因:
甲组 ;乙组 。
⑤实验最终得到的精盐是 (填“纯净物”或“混合物”)。
10.通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl、CaCl、NaSO 以及泥沙等杂质.
2 2 2 4
以下是制备精盐的实验方案,各步操作流程如图所示:
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)在第①步粗盐溶解操作中要用 搅拌,作用是 .
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是
除去滤液中的 。
(3)第②步与第④步不能颠倒顺序,理由是 。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是 。
(5)实验所得精盐质量 粗盐中氯化钠质量(选填“大于”、“小于”或“等
于”)。
答案解析
1.C
2.D
【解析】A、用托盘天平称量药品时应左物右码,该操作错误,不符合题意;B、量筒只能用于
量取液体体积,不能作配制溶液的容器,该操作错误,不符合题意;C、过滤时应使用玻璃棒引
流,该操作错误,不符合题意;D、蒸发结晶时用玻璃棒搅拌来加快蒸发速度同时防止液滴飞
溅,该操作正确,符合题意。故答案为:D.
3.C
【解析】A、 将粗盐放入玻璃杯中加水溶解,是粒子的不断运动 ,不符合题意;B、 溶解时用
筷子搅拌可加快溶解速度 ,不符合题意;C、 用自制净水器过滤粗盐水,只能除去粗盐水中难
溶性物质,不能除去可溶性物质,不能将粗盐水变为纯净物 ,符合题意;D、 实验时不用一次
性塑料杯或纸杯,以减小浪费且保护环境,不符合题意;故答案为: C。
4.B
5.D
【解析】A:步骤④量取水俯视读数,实际水量偏少,但产率计算与水量无关(仅影响溶解
量),若粗盐全溶,对产率无影响,正确。B:步骤⑤(溶解,搅拌加速溶解)、⑦(过滤,引
流)、⑧(蒸发,搅拌防飞溅),玻璃棒作用不同,正确。C:蒸发时出现较多固体应停止加
热,利用余热蒸干,正确。D:步骤⑥(称量)若物品和砝码放反,使用游码时结果偏大,未使
用游码时无影响(如称10g盐,放反且无游码,质量仍为10g),选项“一定有影响”错误。
6.B
【解析】A:步骤①(加NaOH除Mg2+)和②(加Na CO 除Ca2+和过量Ba2+,若有BaCl )顺序可颠
2 3 2
倒,但若用BaCl 除SO ² ,则Na CO 需在BaCl 后,本题未提BaCl ,故顺序可颠倒,选项说法
2 4 ⁻ 2 3 2 2
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
错误。B:NaOH与Mg2+反应生成Mg(OH) 沉淀,过量目的是除尽Mg2+,正确。
2
C:步骤③加Na CO ,若含Ca2+和过量Ba2+(若有BaCl ),沉淀为CaCO 和BaCO ,成分不止一
2 3 2 3 3
种,错误。D:步骤④加稀盐酸,除与 NaOH 发生中和反应外,还与 Na CO 反应(复分解反
2 3
应),错误。
7.D
【解析】A. 除去硫酸根离子用钡离子沉淀,除去镁离子用氢氧根离子进行沉淀,除去钙离子用
碳酸根离子进行沉淀,过量的钡离子需要用碳酸根离子除去,实验操作步骤改为
①③④②⑤⑥③④不会影响形成沉淀和效果,故正确,不符合题意;B. ⑥操作中,加入适量盐
酸的目的是除去过量的氢氧化钠和碳酸钠从而得到氯化钠溶液呈中性,故正确,不符合题意;
C. 氯化钡和碳酸钠溶液的添加顺序颠倒会影响除掉多余的钡离子而形成沉淀,故正确,不符合
题意;D. 加入过量的氯化钡溶液,可以将硫酸根离子转化为沉淀,加过量碳酸钠溶液,可以将
钙离子和反应剩余的钡离子转化为沉淀,加过量氢氧化钠溶液,可以将镁离子转化为沉淀,所
以⑤操作中得到的沉淀共有四种,故错误,符合题意。故答案为:D。
8.(1)C
(2)DACB
(3)搅拌,加速溶解;搅拌,防止因局部温度过高,造成液滴飞溅
(4)托盘天平
(5)
9.(1)蒸发
(2)节约能源(合理即可)
(3)过滤;泥沙;搅拌,加速溶解;引流;搅拌,防止局部温度过高引起液滴飞溅;不认可;
水多蒸发时间长,浪费能源,水少不能将粗盐完全溶解,影响精盐产率;减少误差;40%;粗盐
没有完全溶解;水分没有蒸发完;混合物
【解析】(1)煮盐和晒盐等同于实验室中的蒸发操作,都是将水分蒸发;
(2)晒盐的优点是节约能源;
(3)①图中操作Ⅱ是过滤,可以除去难溶性杂质;
②在溶解、过滤和蒸发中都用到了玻璃棒,溶解过程中,玻璃棒的作用是:搅拌,加速溶解;
过滤操作中,玻璃棒的作用是:引流;蒸发操作中玻璃棒的作用是:搅拌,防止局部温度过高
引起液滴飞溅;
③进行粗盐溶解操作时,需要用量筒量取水的体积,因为水多蒸发时间长,浪费能源,水少不
能将粗盐完全溶解,影响精盐产率;
④Ⅰ.实验小组称量精盐时连同蒸发皿一起称量,其优点是减小误差,因为精盐可能粘在蒸发皿
上;
52.4g−50.4g
Ⅱ.甲小组同学得到的产率为 ×100%=40%;
5g
Ⅲ. 甲组实验产生误差的原因可能是:粗盐没有完全溶解或者在蒸发过程中液体飞溅,造成氯
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
化钠的损失;乙组产生误差的原因可能是:水分没有蒸发完;
⑤实验最终得到的精盐是混合物,因为粗盐中的可溶性杂质没有除去,只除去了难溶性杂质。
10.(1)玻璃棒;加快溶解速率
(2)NaSO;NaOH、NaCO
2 4 2 3
(3)过量的BaCl 无法除去
2
(4)引入新的杂质KCl
(5)大于
【解析】(1)粗盐提纯的第一步是溶解,搅拌时要用到玻璃棒,以加快粗盐溶解;(2)氯化
钡和硫酸钠反应会生成硫酸钡沉淀和氯化钠,所以第②步操作的目的是除去粗盐中的NaSO,
2 4
氢氧化钠和盐酸反应会生成氯化钠和水,碳酸钠和盐酸反应会生成氯化钠、水和二氧化碳,所
以第⑥步操作的目的是除去滤液中的NaOH、NaCO;(3)碳酸钠和氯化钡反应会生成碳酸钡沉
2 3
淀和氯化钠,所以第②步与第④步不能颠倒顺序,理由是:过量的BaCl 无法除去;(4)氢氧
2
化钾和氯化镁反应生成的氯化钾对于氯化钠也是杂质;(5)除杂过程都会生成氯化钠,所以实
验所得精盐质量等于粗盐中氯化钠质量,故答案为:(1)玻璃棒,加快溶解速率;(2)
NaSO,NaOH、NaCO;(3)过量的BaCl 无法除去;(4)引入新的杂质KCl;(5)大于
2 4 2 3 2
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
7