文档内容
【基础知识】原子结构与性质
考点四 元素周期律
【必备知识】
一、主族元素周期性变化规律
1、原子结构与元素性质
项目 同周期(从左到右) 同主族(从上到下)
电子层数
原子结
最外层电子数
构
原子半径
金属性
非金属性
元素性
最高正化合价:+1→+7(O、F除
质
相同,最高正化合价=
化合价 外),
(O、F除外)
负化合价= (H为-1价)
2、定性判断金属性、非金属性的一般方法
①单质与水或非氧化性酸反应制取氢气越 ,金属性越强
金属性 ②单质还原性越 或阳离子氧化性越 金属性越强
③最高价氧化物对应水化物的碱性越 ,金属性越强
①与H 化合越 ,气态氢化物越 ,非金属性越强
2
非金属性 ②单质氧化性越 或阴离子还原性越 ,非金属性越强
③最高价氧化物对应水化物的酸性越 ,非金属性越强
例1、根据元素周期律比较下列各组性质(用“>”或“<”填空):
(1)金属性:K________Na________Mg;非金属性:F________O________S。
(2)碱性:Mg(OH) ________Ca(OH) ______KOH。
2 2
(3)酸性:HClO________HSO ________HClO。
4 2 4
(4)热稳定性:CH________NH ________HO。
4 3 2
(5)还原性:HBr________HCl,I-________S2-。
(6)氧化性:Fe3+________Cu2+________Fe2+。
例2、下列实验方案设计合理的是 。选
实验目的 实验方案
项
A 证明非金属性S>C 将SO 气体通入NaHCO 溶液,生成CO
2 3 2
B 证明金属性Fe>Cu 向CuSO 溶液中加入铁粉
4
C 证明非金属性Cl>S 向NaS溶液中滴加盐酸
2
D 证明非金属性C>S 测同浓度NaSO 与NaCO 溶液的pH
2 3 2 3
E 证明金属性Mg>Al 测同浓度MgCl 与Al (SO ) 溶液的pH
2 2 4 3
F 证明金属性Fe>Cu 将Fe、Cu分别与稀盐酸反应
G 证明非金属性Cl>Br Cl、Br 分别与H 反应
2 2 2
二、电离能
(1)第一电离能概念:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的 能量 ,通
常用I 表示,单位: kJ·mol - 1 。
1
(2)规律
①同周期元素:从左往右,元素第一电离能呈 的趋势,其中 元素的第一电离能出现反
常。第三周期主族元素第一电离能排序 。
②同族元素:从上至下第一电离能逐渐 。
③过渡元素的第一电离能变化不太规则,同一周期,从左至右,第一电离能略有增加。
④同种原子:逐级电离能越来越大(即I> (5倍以上突
1 2 3
变),对主族元素而言,最外层有 个电子,最高化合价为 。
思考1:请结合核外电子排布相关知识解释,第一电离能:C小于O。思考2:为什么第ⅡA族、第ⅤA族元素的第一电离能反常,以Be和B、N和O为例。
思考3:已知电离能:I(Ti)=1 310 kJ·mol-1,I(K)=3 051 kJ·mol-1。为什么I(Ti)O>F>C。( )
7、钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能。( )
8、电负性大小可以作为判断元素非金属性强弱的依据。( )
9、共价化合物中,电负性大的成键元素表现为负价。( )
10、电负性大于1.8的一定为非金属,小于1.8的一定为金属。( )
【 跟踪练习】
1、现有四种元素的基态原子的核外电子排布式如下:
①1s22s22p63s23p4; ②1s22s22p63s23p3; ③1s22s22p3; ④1s22s22p5
下列有关判断正确的是( )
A.第一电离能:④>③>②>① B.原子半径:④>③>②>①
C.电负性:④>③>②>① D.最高正化合价:④>③=②>①
2、(2021·北京,4)下列性质的比较,不能用元素周期律解释的是( )
A.酸性:HClO>HSO >HSiO B.碱性:KOH>NaOH>LiOH
4 2 3 2 3
C.热稳定性:HO>HS>PH D.非金属性:F>O>N
2 2 3
3、(2019·全国I卷)下列状态的镁中,电离最外层一个电子所需能量最大的是( )
A. B. C. D.
4、(2022·广东,7)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应
的水化物为强酸。下列说法不正确的是( )
A.原子半径:丁>戊>乙 B.非金属性:戊>丁>丙
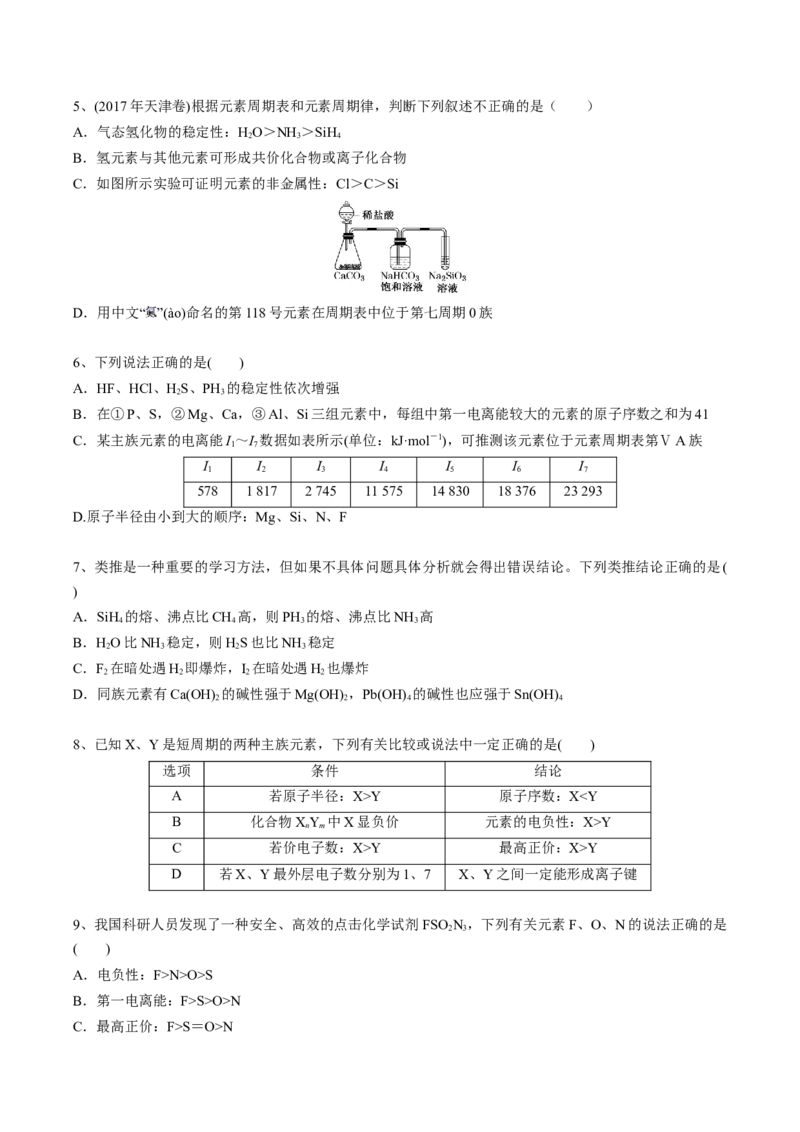
C.甲的氢化物遇氯化氢一定有白烟产生 D.丙的最高价氧化物对应的水化物一定能与强碱反应5、(2017年天津卷)根据元素周期表和元素周期律,判断下列叙述不正确的是( )
A.气态氢化物的稳定性:HO>NH >SiH
2 3 4
B.氢元素与其他元素可形成共价化合物或离子化合物
C.如图所示实验可证明元素的非金属性:Cl>C>Si
D.用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族
6、下列说法正确的是( )
A.HF、HCl、HS、PH 的稳定性依次增强
2 3
B.在①P、S,②Mg、Ca,③Al、Si三组元素中,每组中第一电离能较大的元素的原子序数之和为41
C.某主族元素的电离能I~I 数据如表所示(单位:kJ·mol-1),可推测该元素位于元素周期表第ⅤA族
1 7
I I I I I I I
1 2 3 4 5 6 7
578 1 817 2 745 11 575 14 830 18 376 23 293
D.原子半径由小到大的顺序:Mg、Si、N、F
7、类推是一种重要的学习方法,但如果不具体问题具体分析就会得出错误结论。下列类推结论正确的是(
)
A.SiH 的熔、沸点比CH 高,则PH 的熔、沸点比NH 高
4 4 3 3
B.HO比NH 稳定,则HS也比NH 稳定
2 3 2 3
C.F 在暗处遇H 即爆炸,I 在暗处遇H 也爆炸
2 2 2 2
D.同族元素有Ca(OH) 的碱性强于Mg(OH) ,Pb(OH) 的碱性也应强于Sn(OH)
2 2 4 4
8、已知X、Y是短周期的两种主族元素,下列有关比较或说法中一定正确的是( )
选项 条件 结论
A 若原子半径:X>Y 原子序数:XY
n m
C 若价电子数:X>Y 最高正价:X>Y
D 若X、Y最外层电子数分别为1、7 X、Y之间一定能形成离子键
9、我国科研人员发现了一种安全、高效的点击化学试剂 FSO N,下列有关元素F、O、N的说法正确的是
2 3
( )
A.电负性:F>N>O>S
B.第一电离能:F>S>O>N
C.最高正价:F>S=O>ND.以上物质涉及元素的原子中,N原子的基态原子核外未成对电子数最多
10、根据下表中五种元素的电离能数据(单位:kJ·mol-1),下列说法不正确的是( )
电离能
I I I I
1 2 3 4
元素代号
Q 2 080 4 000 6 100 9 400
R 500 4 600 6 900 9 500
S 740 1 500 7 700 10 500
T 580 1 800 2 700 11 600
U 420 3 100 4 400 5 900
A.T的氯化物最可能的化学式为TCl B.氦元素最有可能与Q元素位于同一族
3
C.在周期表中,最可能处于同一族的是R和U D.U元素最有可能为K,R元素最有可能为Li
11、下列有关元素性质的说法不正确的是( )
A.具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4,电负性最大的是③
B.某主族元素气态基态原子的逐级电离能(kJ·mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、
21 703,当它与氯气反应时可能生成的阳离子是X2+
C.①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的第一电离能随原子序数增大而递
增的是④
D.具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4,原子
半径最大的是①
12、简答题
(1)[2020·全国卷Ⅰ,35(2)]Li及其周期表中相邻元素的第一电离能(I)如表所示。I(Li)> I(Na),原因是
1 1 1
___________________ 。 I(Be)> I(B)> I(Li) , 原 因 是
1 1 1
______________________________________________。
I/(kJ·mol-1)
1
Li 520 Be 900 B 801
Na 496 Mg 738 Al 578
(2)[2018·全国卷Ⅲ,35(2)]黄铜是人类最早使用的合金之一,主要由 Zn 和 Cu 组成。第一电离能
I(Zn)_______________(填“大于”或“小于”)I(Cu)。原因是_________________________。
1 1
(3)[2016·全国卷Ⅱ,37(3)节选]元素铜与镍的第二电离能分别为 I =1 958 kJ·mol-1,I =1 753 kJ·mol-
Cu Ni
1,I >I 的原因是_________________________________________________________________。
Cu Ni
(4)[2016·全国卷Ⅲ,37(2)]根据元素周期律,原子半径 Ga________As,第一电离能 Ga________(填“大
于”或“小于”)As。
(5)[2022·河北,17)]Cu与Zn相比,第二电离能与第一电离能差值更大的是________________,原因是
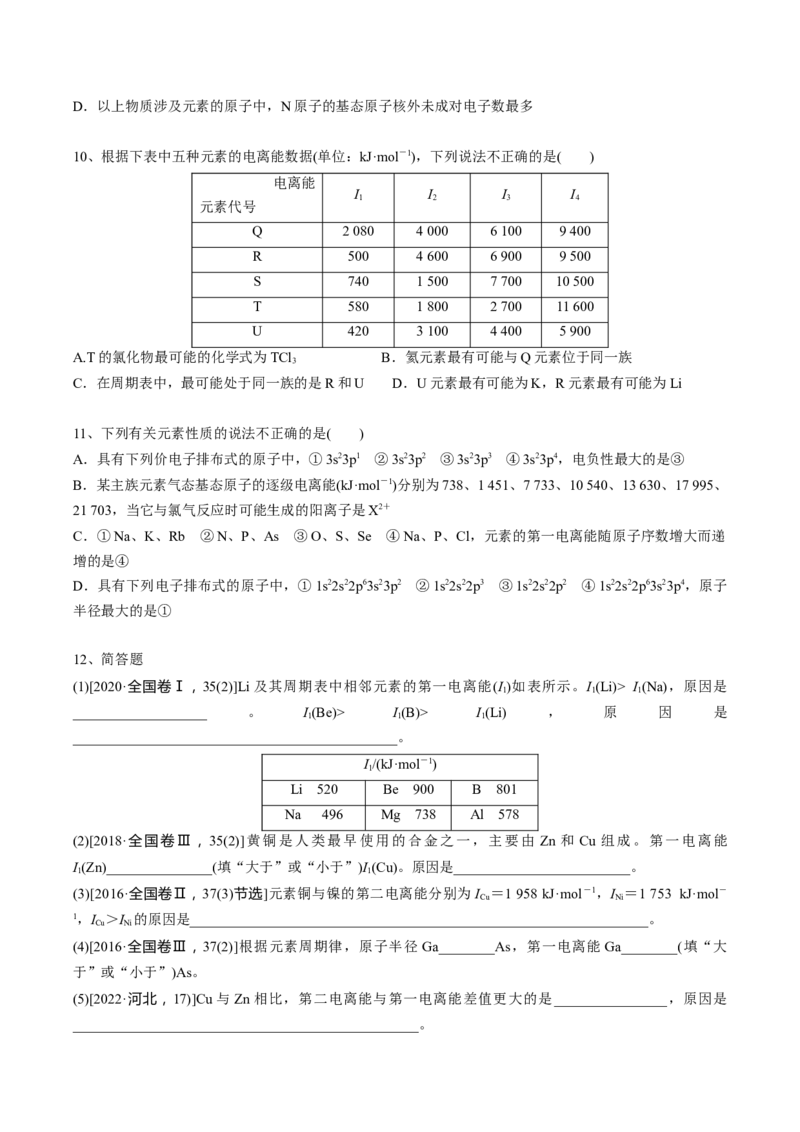
_________________________________________________。(6)[2022·全国甲卷,35]图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。
第一电离能的变化图是____________(填标号),判断的根据是_________________________________;第三
电离能的变化图是________(填标号)。
(7)NH BH 分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺
3 3
序是________________。
(8)CaTiO 的组成元素的电负性大小顺序是________________。
3
(9)对于呋喃( 和吡咯 )所含的元素中,电负性最大的是________,最小的是________;第一电离
能最大的是________
(10)砷与硒的第一电离能较大的是________。
(11)元素Mn与O中,第一电离能较大的是________。
(12)K[Fe(CN) ]中所涉及的元素的基态原子核外未成对电子数最多的是____________,各元素的第一电离
3 6
能由大到小的顺序为________________
(13)光催化还原CO 制备CH 反应中,带状纳米ZnGeO 是该反应的良好催化剂。Zn、Ge、O电负性由大
2 4 2 4
至小的顺序是________
(14)下图表示碳、硅和磷元素的四级电离能变化趋势,其中表示磷的曲线是________。
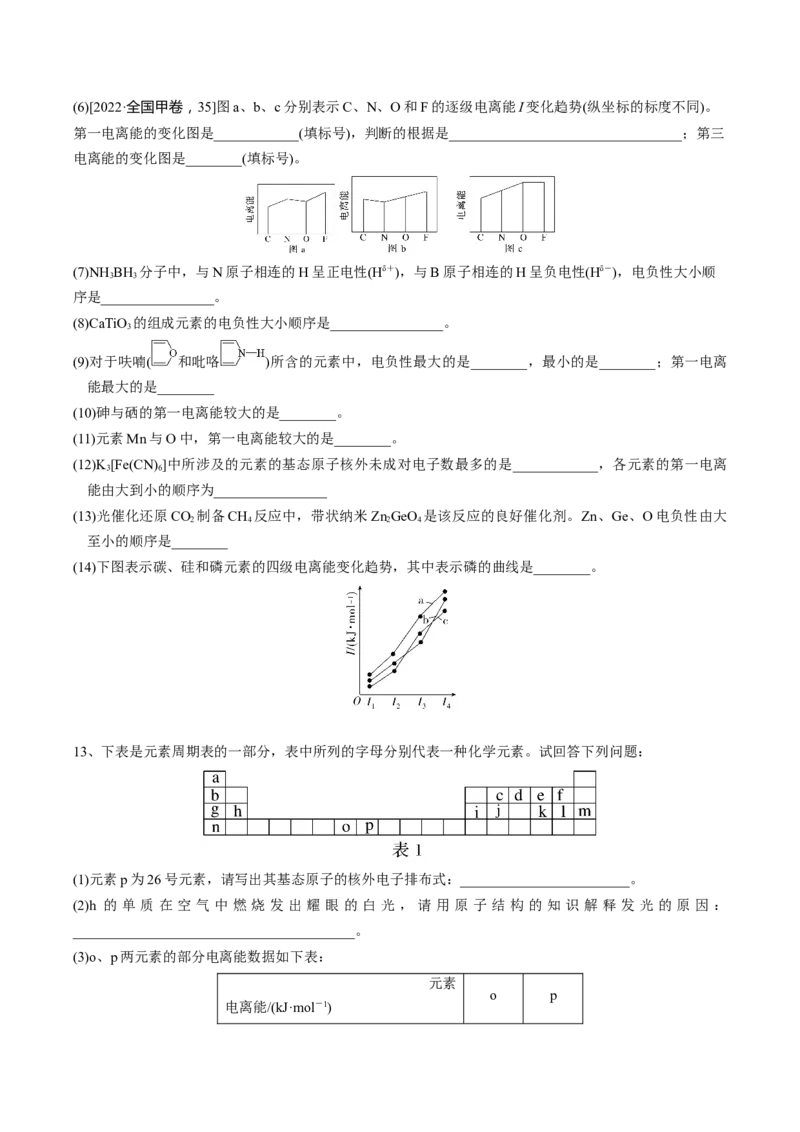
13、下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)元素p为26号元素,请写出其基态原子的核外电子排布式:________________________。
(2)h 的 单 质 在 空 气 中 燃 烧 发 出 耀 眼 的 白 光 , 请 用 原 子 结 构 的 知 识 解 释 发 光 的 原 因 :
________________________________________。
(3)o、p两元素的部分电离能数据如下表:
元素
o p
电离能/(kJ·mol-1)I 717 759
1
I 1 509 1 561
2
I 3 248 2 957
3
比较两元素的I 、I 可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是
2 3
________________________________________________________________________。
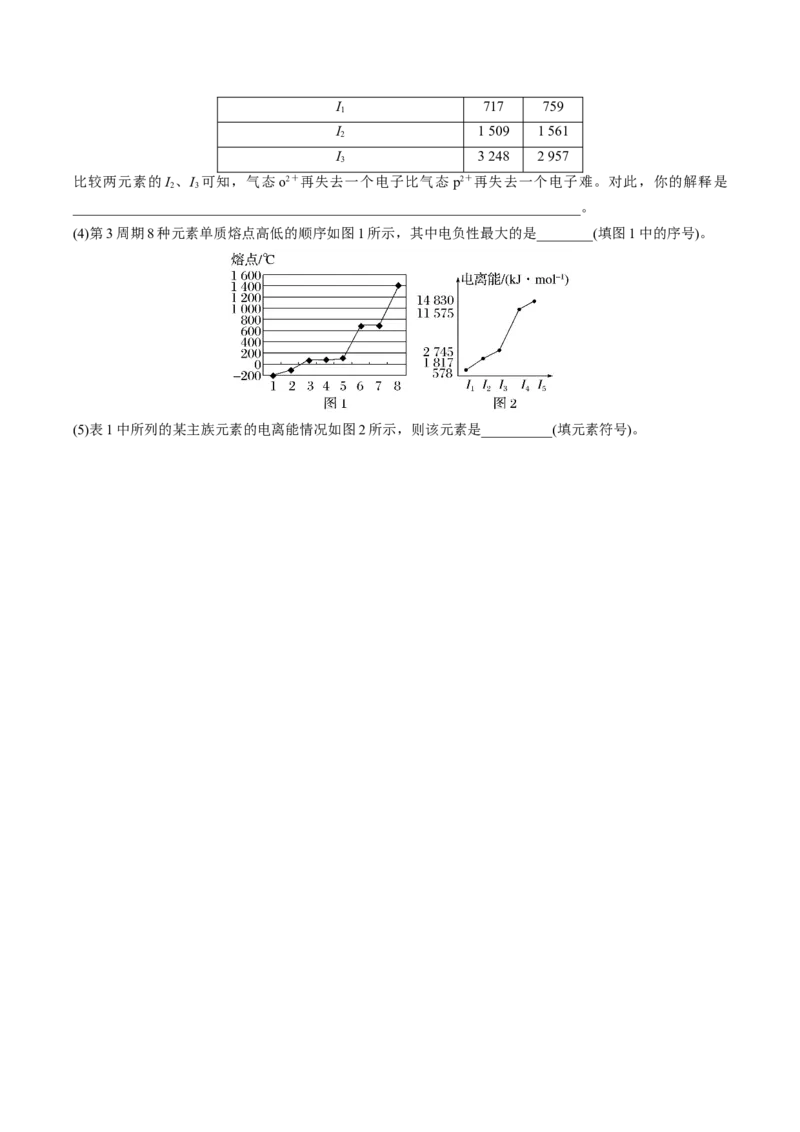
(4)第3周期8种元素单质熔点高低的顺序如图1所示,其中电负性最大的是________(填图1中的序号)。
(5)表1中所列的某主族元素的电离能情况如图2所示,则该元素是__________(填元素符号)。