文档内容
【基础知识】分子结构与性质
考点一 化学键与化合物类型 电子式
【 必备知识】
1、化学键类型及比较
化学键 离子键 共价键 金属键
阴、阳离子间通过静电作用形 原子间通过共用电子形成, 金属阳离子与自由电子
形成
成,包括静电引力和静电斥力。 分为极性键和非极性键。 间的强的作用
特征 无方向性、饱和性 有方向性、饱和性 无方向性、饱和性
表示方式
—
(电子式)
①阴阳离子半径的大小、 ①金属离子半径的大小
强弱比较 ①键能和②键长
②离子所带电荷数的多少 ②所带电荷数的多少
活泼金属离子、或NH +与非金
4
存在 一般存在非金属原子间 金属单质、合金
属离子间
2、如何判断离子化合物和共价化合物
项目 离子化合物 共价化合物
化学键类型 含有离子键的化合物 只含有共价键的化合物
活泼金属元素、或NH +与非金属元素形成
4
化合物类型 非金属原子形成的化合物或单质
化合物
化合物性质 在熔融状态下能导电的化合物 在熔融状态下不能导电
例1、现有下列物质:①NaCl ②NaO ③NaO ④NaOH ⑤AlCl ⑥HO ⑦N ⑧NH Cl
2 2 2 3 2 2 4
⑨CO ⑩HO
2 2 2
(1)只含离子键的物质有________(填序号,下同),只含共价键的物质有__________。
(2)属于离子化合物的有__________,其中含非极性键的离子化合物有__________,含有非极性键的共价化
合物有__________。
【答案】 (1)①② ⑤⑥⑦⑨⑩ (2)①②③④⑧ ③ ⑩
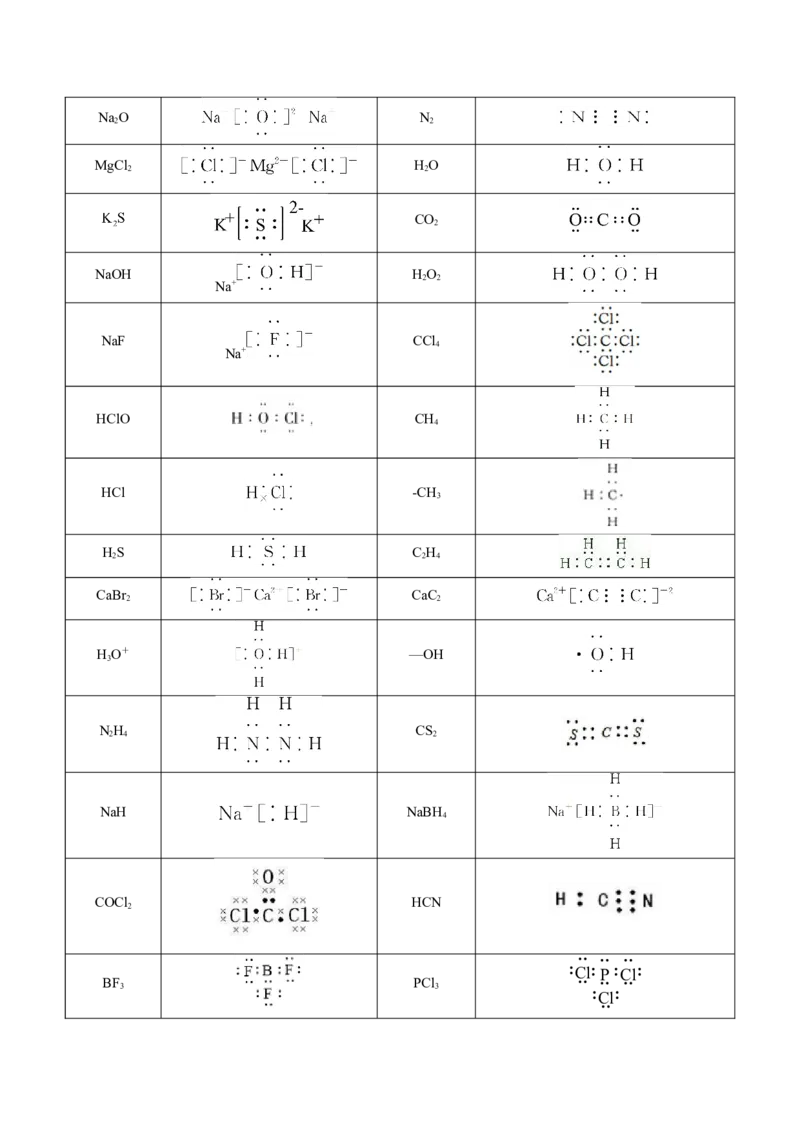
例2、写出下列物质的电子式(首先判断有无离子键)
物质 电子式 物质 电子式
NaO Cl
2 2 2NaO N
2 2
MgCl HO
2 2
CO
2
NaOH HO
2 2
Na+
NaF CCl
4
Na+
HClO CH
4
HCl -CH
3
HS C H
2 2 4
CaBr CaC
2 2
HO+ —OH
3
NH CS
2 4 2
NaH NaBH
4
COCl HCN
2
Cl P Cl
BF PCl
3 3
Cl例3、指出下列电子式书写错误的原因
①氮气,N⋮⋮N( ); ②氨气, ( );
③氯化钠, ( ); ④HF, ( )
⑤次氯酸, ( )(2019浙江) ⑥HCl 的电子式: (2018江苏)
⑦CaCl 的电子式: (2017江苏) ⑧NaS的电子式 (2016江苏)
2 2
⑨NH Br的电子式: (2012海南) ⑩NH Cl:
4 4
例4、用电子式表示化合的形成过程(反应物用原子的电子式表示)
MgBr :
2
NaCl:
HO:
2
HCl:
例5、下列粒子中,所有原子的最外层都满足8电子结构的分子是 (填序号)
①BF ②NCl ③HO+ ④SiCl ⑤PCl ⑥PCl ⑦NO ⑧XeF ⑨SO ⑩HClO ⑪N ⑫NH ⑬CO
3 3 3 4 3 5 2 4 2 2 2 4 2
【答案】②④⑤⑪⑬
【技巧】8电子稳定结构的判断方法
1、最外层电子数+|化合价|=8,说明该原子达8电子结构。
2、H原子一定不是8电子结构。
【概念辨析】
1、物质中一定存在化学键。( )
2、化学键是一种静电作用。( )
3、化学键是相邻原子之间强烈的相互吸引。( )
4、由活泼金属元素与活泼非金属元素形成的化学键都是离子键。( )
5、离子化合物中一定含有金属元素,共价化合物中一定不含有金属元素。( )
6、HCl的水溶液能导电,因为HCl是离子化合物。( )
7、含共价键的一定是共价化合物。( )8、熔融状态下能导电的一定是离子化合物。( )
9、钠与N、O、Cl分别形成的化合物中只含有离子键(2018·全国卷Ⅱ,10B改编)( )
10、NaO 与ClO 均含有非极性共价键(2018·全国卷Ⅲ,13C改编)( )
2 2 2
11、氢元素与其他元素可形成共价化合物或离子化合物(2017·天津,5B)( )
12、金属键是金属阳离子和自由电子间的强烈的静电吸引力。( )
13、有阳离子的晶体一定是化合物。( )
【答案】 1.× 2.× 3.× 4.× 5.× 6.× 7.× 8.× 9.× 10.× 11.√ 12.× 13.×
【跟踪练习】
1、一定条件下,氨与氟气发生反应:4NH +3F===NF +3NH F,其中NF 的空间结构与NH 相似。下列
3 2 3 4 3 3
有关说法错误的是( )
A.除F 单质外,反应物和生成物均为共价化合物 B.NF 中各原子均满足8电子稳定结构
2 3
C.NF 中只含极性共价键 D.NH F中既含有离子键又含有共价键
3 4
【答案】 A
【解析】 NF 为共价化合物,NH F为离子化合物。
3 4
2、下列各分子中所有原子都满足最外层为8电子结构的是( )
A.HCl B.BF C.PCl D.CO
3 5 2
【答案】 D
3、(2023 江苏卷)反应NH Cl+NaNO =NaCl+N↑+2HO应用于石油开采。下列说法正确的是( )
4 2 2 2
A. NH+的电子式为 B. NO N元素的化合价为+5
4 中
C. N 分子中存在N≡N键 D. HO为非极性分子
2 2
【答案】C
【解析】A.NH +的电子式为[ ]+,A错误;B.NO 分子中存在N≡N键,C正
4 中N元素的化合价为+3,B错误;C.N2
确;D.HO 为V形分子,分子中正负电荷中心未重合,为极性分子,D错误。
2
4、(2023届广东湛江一模)下列各组中的每种物质内既有离子键又有共价键的一组是
A.HO B.CaCl C.NH Cl D.CO
2 2 2 4 2
【答案】C
【解析】A.HO 中只存在共价键不存在离子键,A错误;
2 2
B.CaCl 中只存在离子键不存在共价键,B错误;
2
C.NH Cl中铵根离子和氯离子间存在离子键,铵根离子内部存在共价键,C正确;
4
D.CO 中只存在共价键不存在离子键,D错误;
25、下列表达正确的是( )
A.HClO的电子式为 B.HS的电子式可表示为
2
C.用电子式表示NaO的形成过程:
2
D.BaCl 的电子式为
2
【答案】 D
【解析】 HClO分子中,氧原子分别与氢原子和氯原子形成共价键,电子式为 ,故A错误;
HS是共价化合物,电子式可表示为 ,故B错误;用电子式表示NaO的形成过程时,2个Na+
2 2
不能合并,正确的表达方式为 ,故C错误;BaCl 是离子化合物,电子
2
式为 ,故D正确。
6、北京大学和中国科学院的化学工作者已成功研制出碱金属与 C 形成的球碳盐KC 。实验测知该物质
60 3 60
属于离子化合物,具有良好的超导性。下列有关分析正确的是( )
A.KC 中只有离子键 B.KC 中不含共价键
3 60 3 60
C.该晶体在熔融状态下能导电 D.C 与12C互为同素异形体
60
【答案】 C
7、(2022·浙江1月)下列表示不正确的是( )
A.乙炔的结构简式HC≡CH B.KOH的电子式
C.乙烷的球棍模型: D.氯离子的结构示意图:
【答案】 D
8、氯胺(NH Cl)是一种长效缓释有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的 4~5倍,下
2
列有关氯胺的说法一定不正确的是( )
A.氯胺的水解产物为NH OH(羟氨)和HCl B.氯胺的电子式为
2
C.氯胺中氯的化合价为+1 D.氯胺的消毒原理与漂白粉相似
【答案】 A
【解析】NH Cl+HO NH +HClO,反应生成的HClO能杀菌消毒。该水解反应是一个可逆反应,
2 2 3
HClO杀菌后浓度减小,平衡向右移动,氯胺转化成HClO;相反,当HClO浓度较高时,平衡向左移动,
转化为氯胺,相当于暂时“贮存”,避免其分解损失,这样就延长了消毒时间。9、研究表明:三硫化四磷分子中没有不饱和键,且各原子的最外层均已达到了八电子的稳定结构。在一
个三硫化四磷分子中含有的P-S共价键个数是( )
A.6个 B.7个 C.8个 D.9个
【答案】 A
【解析】一个硫形成二个P-S共价键,则三个硫形成6个P-S共价键,A项正确。
10、“珍珠项链靠线穿,芝麻成球靠糖粘;微观粒子聚一起,全靠一种超魔力”,这种超魔力实际就是化
学键。下列关于化学键的说法错误的是( )
A.CO和O生成具有极性共价键的CO
2
B. 既含极性键,又含非极性键
C.只含H、N、O三种元素的化合物,可能形成含有共价键的离子化合物,也可能形成共价化合物
D.含有离子键的物质不可能是单质
【答案】 B
【解析】 CO 中C与O形成极性共价键; 中只含有极性键;H、N、O可以形成NH NO ,
2 4 3
为离子化合物,也可以形成HNO,为共价化合物;离子键的形成必须有阴、阳离子。
3