文档内容
9 提取卤素单质的化工流程
1.氯的提取——氯碱工业
海水―→粗盐――→饱和食盐水――→
化学方程式为2NaCl+2HO=====2NaOH+H↑+Cl↑。
2 2 2
2.海水提取溴
(1)工艺流程
――→―――――→―――――→――→――→
(2)发生反应的化学方程式
①2NaBr+Cl===Br +2NaCl;
2 2
②Br +SO +2HO===2HBr+HSO ;
2 2 2 2 4
③2HBr+Cl===2HCl+Br 。
2 2
3.海带中提取碘
(1)工艺流程
HO Cl
2 2
↓ ↓
海带――→―→――→――→――→
(2)发生反应的离子方程式:Cl+2I-===I+2Cl-。
2 2
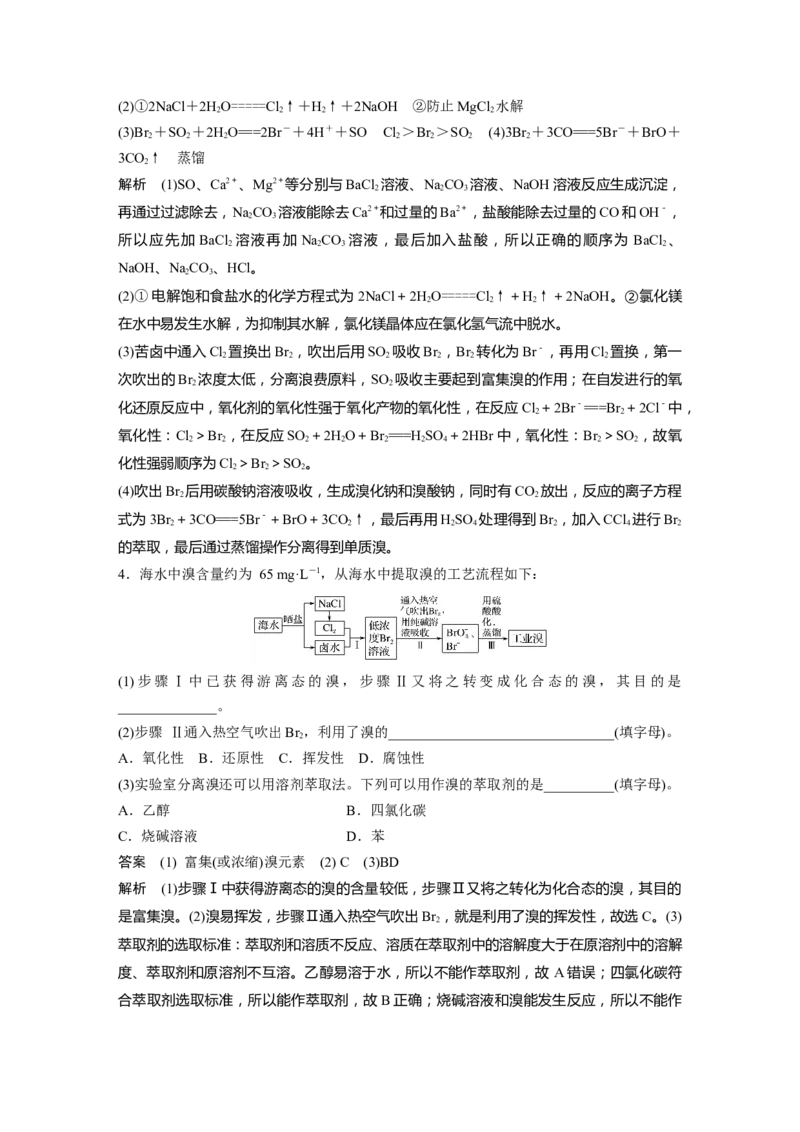
1.(2020·顺义区模拟)为了从海带浸取液中提取碘,某同学设计了如图实验方案,下列说法
正确的是( )
A.①中反应的离子方程式:2I-+HO===I+2OH-
2 2 2
B.②中分液时含I 的CCl 溶液从分液漏斗上口倒出
2 4
C.③中得到的上层溶液中含有I-
D.操作Z的名称是加热
答案 C
解析 反应为酸性环境,①中反应的离子方程式:2I-+2H++HO===I +2HO,故A错误;
2 2 2 2
四氯化碳比水的密度大,在下层,②中分液时含I 的CCl 溶液从分液漏斗下口放出,故B
2 4
错误;操作Z的名称是过滤,故D错误。2.(2020·武汉调研)从淡化海水中提取溴的流程如下:
下列有关说法不正确的是( )
A.X试剂可用NaSO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:2Br-+Cl===2Cl-+Br
2 2
C.工业上每获得1 mol Br ,需要消耗Cl 44.8 L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏
答案 C
解析 NaSO +Br +HO===NaSO +2HBr,A正确;步骤Ⅲ根据氯的非金属性比溴的强,
2 3 2 2 2 4
利用置换反应制取Br ,B正确;反应Ⅰ和反应Ⅲ均使用到Cl ,故制取1 mol Br 消耗2 mol
2 2 2
氯气,但未标明氯气所处的温度和压强,C错误;从浓溴水中提取溴,可利用有机溶剂(如
苯)萃取溴,然后分液得到溴的有机溶液,再经蒸馏可得纯净的溴,D正确。
3.海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原
料。如图是海水综合利用的部分流程图,据图回答问题:
(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO等离子,为除去这些离子,所加试剂及其先
后顺序为(填化学式):__________________________________________________________。
(2)①电解饱和食盐水的化学方程式为____________________________________________。
②制取MgCl 的过程中涉及反应:MgCl ·6H O=====MgCl +6HO,该反应要在HCl气氛中
2 2 2 2 2
进行,原因是___________________________________________________________________。
(3)苦卤中通入Cl 置换出Br ,吹出后用SO 吸收,写出用SO 吸收发生反应的离子方程式:
2 2 2 2
______________________________________________________________________________,
由此判断Cl、Br 、SO 的氧化性由强到弱的顺序为__________________。
2 2 2
(4)也有工艺是在吹出Br 后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,同时有CO 放出,该
2 2
反应的离子方程式是
________________________________________________________________________;
最后再用HSO 处理得到Br ,之后加入CCl 进行Br 的萃取,最终用________法得到单质
2 4 2 4 2
Br 。
2
答案 (1)BaCl 、NaOH、NaCO 、HCl(只要 NaCO 在 BaCl 之后加,HCl 最后加皆可)
2 2 3 2 3 2(2)①2NaCl+2HO=====Cl↑+H↑+2NaOH ②防止MgCl 水解
2 2 2 2
(3)Br +SO +2HO===2Br-+4H++SO Cl >Br >SO (4)3Br +3CO===5Br-+BrO+
2 2 2 2 2 2 2
3CO↑ 蒸馏
2
解析 (1)SO、Ca2+、Mg2+等分别与BaCl 溶液、NaCO 溶液、NaOH溶液反应生成沉淀,
2 2 3
再通过过滤除去,NaCO 溶液能除去Ca2+和过量的Ba2+,盐酸能除去过量的CO和OH-,
2 3
所以应先加 BaCl 溶液再加 NaCO 溶液,最后加入盐酸,所以正确的顺序为 BaCl 、
2 2 3 2
NaOH、NaCO、HCl。
2 3
(2)①电解饱和食盐水的化学方程式为2NaCl+2HO=====Cl↑+H↑+2NaOH。②氯化镁
2 2 2
在水中易发生水解,为抑制其水解,氯化镁晶体应在氯化氢气流中脱水。
(3)苦卤中通入Cl 置换出Br ,吹出后用SO 吸收Br ,Br 转化为Br-,再用Cl 置换,第一
2 2 2 2 2 2
次吹出的Br 浓度太低,分离浪费原料,SO 吸收主要起到富集溴的作用;在自发进行的氧
2 2
化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,在反应 Cl +2Br-===Br +2Cl-中,
2 2
氧化性:Cl >Br ,在反应SO +2HO+Br ===HSO +2HBr中,氧化性:Br >SO ,故氧
2 2 2 2 2 2 4 2 2
化性强弱顺序为Cl>Br >SO 。
2 2 2
(4)吹出Br 后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,同时有CO 放出,反应的离子方程
2 2
式为3Br +3CO===5Br-+BrO+3CO↑,最后再用HSO 处理得到Br ,加入CCl 进行Br
2 2 2 4 2 4 2
的萃取,最后通过蒸馏操作分离得到单质溴。
4.海水中溴含量约为 65 mg·L-1,从海水中提取溴的工艺流程如下:
(1)步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是
______________。
(2)步骤 Ⅱ通入热空气吹出Br ,利用了溴的________________________________(填字母)。
2
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)实验室分离溴还可以用溶剂萃取法。下列可以用作溴的萃取剂的是__________(填字母)。
A.乙醇 B.四氯化碳
C.烧碱溶液 D.苯
答案 (1) 富集(或浓缩)溴元素 (2) C (3)BD
解析 (1)步骤Ⅰ中获得游离态的溴的含量较低,步骤Ⅱ又将之转化为化合态的溴,其目的
是富集溴。(2)溴易挥发,步骤Ⅱ通入热空气吹出Br ,就是利用了溴的挥发性,故选C。(3)
2
萃取剂的选取标准:萃取剂和溶质不反应、溶质在萃取剂中的溶解度大于在原溶剂中的溶解
度、萃取剂和原溶剂不互溶。乙醇易溶于水,所以不能作萃取剂,故 A错误;四氯化碳符
合萃取剂选取标准,所以能作萃取剂,故B正确;烧碱溶液和溴能发生反应,所以不能作萃取剂,故C错误;苯符合萃取剂选取标准,所以能作萃取剂,故D正确。