文档内容
第 32 讲 多池、多室的电化学装置
复习目标 1.掌握多池连接的分析应用。2.了解离子交换膜的分类及特点。3.理解离子交换
膜在装置中的作用。4.熟悉电化学综合计算中的常用方法。
考点一 多池串联的两大模型及原理分析
1.常见串联装置图
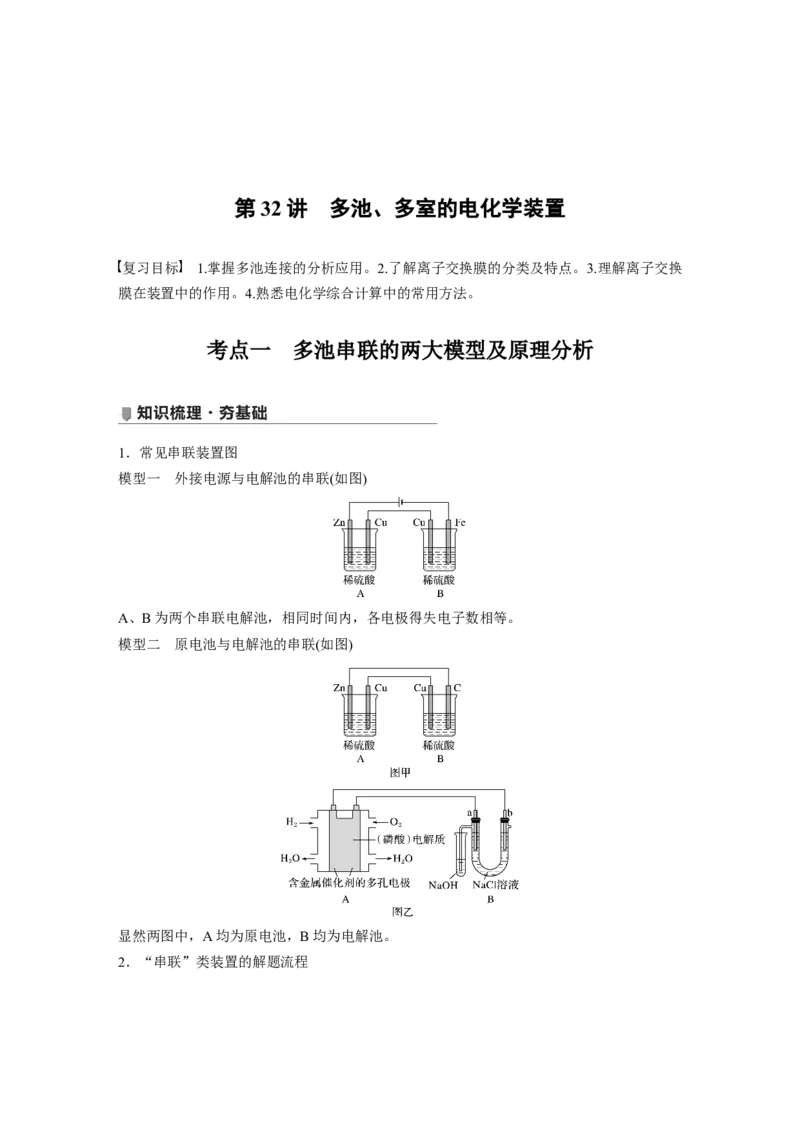
模型一 外接电源与电解池的串联(如图)
A、B为两个串联电解池,相同时间内,各电极得失电子数相等。
模型二 原电池与电解池的串联(如图)
显然两图中,A均为原电池,B均为电解池。
2.“串联”类装置的解题流程1.(2020·长春质检)下图装置中a、b、c、d均为Pt电极。电解过程中,电极b和d上没有气
体逸出,但质量均增大,且增重b>d。符合上述实验结果的盐溶液是( )
选项 X Y
A MgSO CuSO
4 4
B AgNO Pb(NO )
3 3 2
C FeSO Al (SO )
4 2 4 3
D CuSO AgNO
4 3
答案 B
解析 A项,当 X为MgSO 时,b极上生成 H ,电极质量不增加,错误;C 项,X为
4 2
FeSO ,Y为Al (SO ) ,b、d极上均产生气体,错误;D项,b极上析出Cu,d极上析出
4 2 4 3
Ag,其中d极增加的质量大于b极增加的质量,错误。
2.如图所示装置可间接氧化工业废水中含氮离子(NH)。下列说法不正确的是( )A.乙是电能转变为化学能的装置
B.含氮离子氧化时的离子方程式为3Cl+2NH===N+6Cl-+8H+
2 2
C.若生成H 和N 的物质的量之比为3∶1,则处理后废水的pH减小
2 2
D.电池工作时,甲池中的Na+移向Mg电极
答案 D
3.某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观
察到电流表的指针发生了偏转。
请回答下列问题:
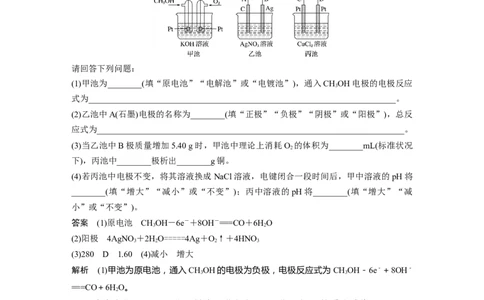
(1)甲池为________(填“原电池”“电解池”或“电镀池”),通入CHOH电极的电极反应
3
式为________________________________________________________________________。
(2)乙池中A(石墨)电极的名称为________(填“正极”“负极”“阴极”或“阳极”),总反
应式为________________________________________________________________________。
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗O 的体积为________mL(标准状况
2
下),丙池中________极析出________g铜。
(4)若丙池中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将
________(填“增大”“减小”或“不变”);丙中溶液的pH将________(填“增大”“减
小”或“不变”)。
答案 (1)原电池 CHOH-6e-+8OH-===CO+6HO
3 2
(2)阳极 4AgNO+2HO=====4Ag+O↑+4HNO
3 2 2 3
(3)280 D 1.60 (4)减小 增大
解析 (1)甲池为原电池,通入CHOH的电极为负极,电极反应式为CHOH-6e-+8OH-
3 3
===CO+6HO。
2
(2)乙池中电解 AgNO 溶液,其中 C 作阳极,Ag 作阴极,总反应式为 4AgNO +
3 3
2HO=====4Ag+O↑+4HNO。
2 2 3
(3)根据各电极上转移的电子数相同,得 n(Ag)=4n(O )=2n(Cu),故V(O )=××22.4 L=0.28
2 2
L=280 mL,m(Cu)=××64 g=1.60 g。(4)若丙中电极不变,将其溶液换成NaCl溶液,根据
丙中总反应2NaCl+2HO=====2NaOH+H↑+Cl↑,则溶液pH增大,而甲中总反应为
2 2 2
2CHOH+3O+4KOH===2KCO+6HO,溶液pH减小。
3 2 2 3 2
多池串联的装置中,先根据电极反应物和电解质溶液判断哪个是原电池,其余装置一般为电解池;与原电池正极相连的电极为电解池阳极,与原电池负极相连的电极为电解池阴极,据
此判断各池中发生的反应。
考点二 多室隔膜在电化学中的应用
常见的离子交换膜
1.含义和作用
(1)含义:离子交换膜又叫隔膜,由高分子特殊材料制成。
(2)作用:①能将两极区隔离,阻止两极区产生的物质接触,防止发生化学反应。
②能选择性的通过离子,起到平衡电荷、形成闭合回路的作用。
2.分类和应用
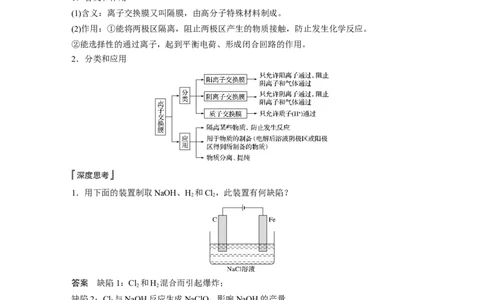
1.用下面的装置制取NaOH、H 和Cl,此装置有何缺陷?
2 2
答案 缺陷1:Cl 和H 混合而引起爆炸;
2 2
缺陷2:Cl 与NaOH反应生成NaClO,影响NaOH的产量。
2
2.用下图装置电解饱和食盐水,其中阳离子交换膜的作用有哪些?
答案 (1)平衡电荷,形成闭合回路;(2)防止Cl 和H 混合而引起爆炸;
2 2
(3)避免Cl 与NaOH反应生成NaClO,影响NaOH的产量;
2
(4)避免Cl-进入阴极区导致制得的NaOH不纯。
题组一 “隔膜”在新型电池中的应用
1.(2020·黔东南州模拟)二甲醚(CHOCH )燃料电池的工作原理如图,下列有关叙述正确的
3 3
是( )
A.该装置能实现化学能100%转化为电能
B.电子移动方向:a极→b极→质子交换膜→a极
C.a电极的电极反应式为:CHOCH +3HO-12e-===2CO+12H+
3 3 2 2
D.当b电极消耗22.4 L O 时,质子交换膜有4 mol H+通过
2
答案 C
解析 A项,化学能转化为热能和电能,不可能 100%转化为电能,错误;B项,电子不能
经过电解质溶液,所以电子由a极――→b极,错误;C项,a为负极,发生氧化反应,电
极反应式为CHOCH -12e-+3HO===2CO +12H+,正确;D项,气体所处状况不知,无
3 3 2 2
法由体积求物质的量,所以通过H+的物质的量无法求出,错误。
2.(2020·青岛高三模拟)2019年3月,我国科学家研发出一种新型的锌碘单液流电池,其原
理图所示。下列说法不正确的是( )
A.放电时,B电极反应式:I+2e-===2I-
2
B.放电时,电解质储罐中离子总浓度增大
C.M为阳离子交换膜,N为阴离子交换膜
D.充电时,A极增重65 g时,C区增加的离子数为4N
A
答案 C解析 放电时,B电极为正极,I 得到电子生成I-,电极反应式为I+2e-===2I-,A项正确;
2 2
放电时,左侧即负极,电极反应式为Zn-2e-===Zn2+,所以电解质储罐中的离子总浓度增
大,B项正确;离子交换膜的作用是防止I 、Zn接触发生反应,负极区生成Zn2+,正极区
2
生成
I-,所以Cl-通过M膜进入负极区,K+通过N膜进入正极区,所以M为阴离子交换膜,N
为阳离子交换膜,C项错误;充电时,A极的电极反应式为Zn2++2e-===Zn,A极增重65
g,转移2 mol电子,所以C区增加2 mol K+、2 mol Cl-,离子总数为4N ,D正确。
A
题组二 “双室”电解池的应用
3.(2020·合肥第一次教学质量检测)利用LiOH和钴氧化物可制备锂离子电池正极材料。可
用电解LiCl溶液制备LiOH,装置如图所示。下列说法正确的是( )
A.电极B连接电源正极
B.A极区电解液为LiCl溶液
C.阳极反应式为2HO+2e-===H↑+2OH-
2 2
D.每生成1 mol H ,有1 mol Li+通过该离子交换膜
2
答案 B
解析 由题意知,电解LiCl溶液制备LiOH,由于电极B生成氢气,A与B用阳离子交换膜
隔开,所以B为阴极,B极区为LiOH溶液,A极区为LiCl溶液,A项错误,B项正确;阳
极反应式为2Cl--2e-===Cl↑,C项错误;每生成1 mol H ,有2 mol Li+通过该离子交换
2 2
膜,D项错误。
4.(2020·四川宜宾诊断)连二亚硫酸钠(Na SO)俗称保险粉,是一种强还原剂。工业常用惰
2 2 4
性电极电解亚硫酸氢钠的方法制备连二亚硫酸钠,原理及装置如图所示,下列说法正确的是
( )
A.b电极应该接电源的负极
B.a电极的电极反应式2HSO+2H++2e-===SO+2HO
2 2
C.装置中所用离子交换膜为阴离子交换膜
D.电路中每转移1 mol电子,消耗SO 的体积为11.2 L
2答案 B
解析 NaHSO 在a电极被还原生成NaSO ,则a电极是阴极,b电极是阳极,故b电极接
3 2 2 4
电源的正极,A错误;a电极发生还原反应,HSO被还原生成SO,电极反应式为2HSO+
2
2H++2e-===SO+2HO,B正确;b电极是阳极,电极反应式为SO +2HO-2e-===4H++
2 2 2 2
SO,阳极生成H+,阴极消耗H+,为维持溶液呈电中性,H+透过离子交换膜向阴极迁移,
则该离子交换膜是阳离子交换膜,C错误;电路中每转移1 mol电子,阳极消耗0.5 mol
SO ,在标准状况下的体积为11.2 L,题目未指明SO 是否处于标准状况下,D错误。
2 2
题组三 “多室”电解池的应用
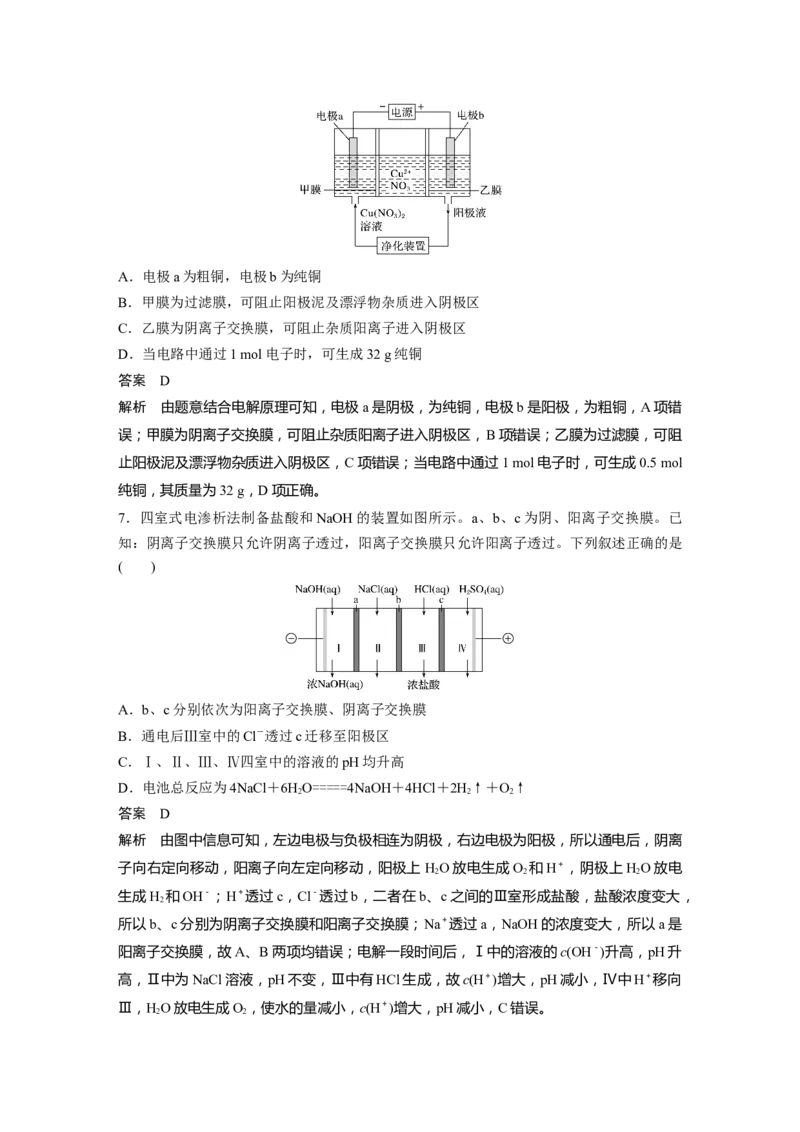
5.(2020·长春质检)某科研小组研究采用BMED膜堆(示意图如下),模拟以精制浓海水为原
料直接制备酸碱。BMED膜堆包括阳离子交换膜、阴离子交换膜和双极膜(A、D)。已知:
在直流电源的作用下,双极膜内中间界面层发生水的解离,生成H+和OH-。下列说法错误
的是( )
A.电极a连接电源的正极
B.B为阳离子交换膜
C.电解质溶液采用NaSO 溶液可避免有害气体的产生
2 4
D.Ⅱ口排出的是淡水
答案 B
解析 根据题干信息确定该装置为电解池,阴离子向阳极移动,阳离子向阴极移动,所以电
极a为阳极,连接电源的正极,A正确;水在双极膜A解离后,氢离子吸引阴离子透过B膜
到左侧形成酸,B为阴离子交换膜,B错误;电解质溶液采用NaSO 溶液,电解时生成氢
2 4
气和氧气,可避免有害气体的产生,C正确;海水中的阴、阳离子透过两侧交换膜向两侧移
动,淡水从Ⅱ口排出,D正确。
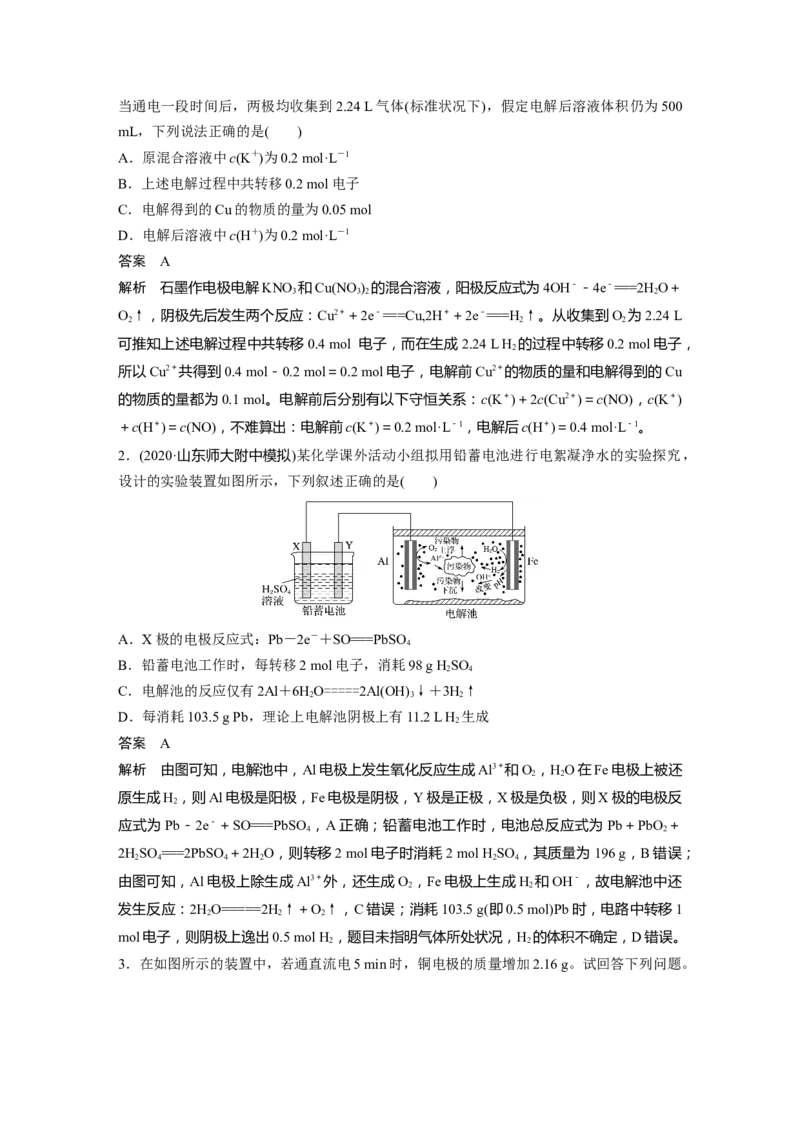
6.(2020·河南天一大联考阶段检测)普通电解精炼铜的方法所制备的铜中仍含杂质,利用下
面的双膜(阴离子交换膜和过滤膜)电解装置可制备高纯度的Cu。下列有关叙述正确的是(
)A.电极a为粗铜,电极b为纯铜
B.甲膜为过滤膜,可阻止阳极泥及漂浮物杂质进入阴极区
C.乙膜为阴离子交换膜,可阻止杂质阳离子进入阴极区
D.当电路中通过1 mol电子时,可生成32 g纯铜
答案 D
解析 由题意结合电解原理可知,电极a是阴极,为纯铜,电极b是阳极,为粗铜,A项错
误;甲膜为阴离子交换膜,可阻止杂质阳离子进入阴极区,B项错误;乙膜为过滤膜,可阻
止阳极泥及漂浮物杂质进入阴极区,C项错误;当电路中通过1 mol电子时,可生成0.5 mol
纯铜,其质量为32 g,D项正确。
7.四室式电渗析法制备盐酸和NaOH的装置如图所示。a、b、c为阴、阳离子交换膜。已
知:阴离子交换膜只允许阴离子透过,阳离子交换膜只允许阳离子透过。下列叙述正确的是
( )
A.b、c分别依次为阳离子交换膜、阴离子交换膜
B.通电后Ⅲ室中的Cl-透过c迁移至阳极区
C.Ⅰ、Ⅱ、Ⅲ、Ⅳ四室中的溶液的pH均升高
D.电池总反应为4NaCl+6HO=====4NaOH+4HCl+2H↑+O↑
2 2 2
答案 D
解析 由图中信息可知,左边电极与负极相连为阴极,右边电极为阳极,所以通电后,阴离
子向右定向移动,阳离子向左定向移动,阳极上 HO放电生成O 和H+,阴极上HO放电
2 2 2
生成H 和OH-;H+透过c,Cl-透过b,二者在b、c之间的Ⅲ室形成盐酸,盐酸浓度变大,
2
所以b、c分别为阴离子交换膜和阳离子交换膜;Na+透过a,NaOH的浓度变大,所以a是
阳离子交换膜,故A、B两项均错误;电解一段时间后,Ⅰ中的溶液的c(OH-)升高,pH升
高,Ⅱ中为NaCl溶液,pH不变,Ⅲ中有HCl生成,故c(H+)增大,pH减小,Ⅳ中H+移向
Ⅲ,HO放电生成O,使水的量减小,c(H+)增大,pH减小,C错误。
2 2(1)含离子交换膜电化学装置题的解题步骤
(2)在原电池中应用离子交换膜,起到替代盐桥的作用,一方面能起到平衡电荷、导电的作
用,另一方面能防止电解质溶液中的离子与电极直接反应,提高电流效率;在电解池中使用
选择性离子交换膜的主要目的是限制某些离子(或分子)的定向移动,避免电解质溶液中的离
子或分子与电极产物反应,提高产品纯度或防止造成危险等。
考点三 电化学原理的相关计算
电化学综合计算的三种常用方法
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中
转移的电子数相等。
②用于混合溶液中电解的分阶段计算。
(3)根据关系式计算
根据得失电子守恒定律建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4 mol e-为桥梁可构建如下关系式:
4e-~ ~
阳极产物 阴极产物
(式中M为金属,n为其离子的化合价数值)
该关系式具有总揽电化学计算的作用和价值,熟记电极反应式,灵活运用关系式便能快速解
答常见的电化学计算问题。
1.500 mL KNO 和Cu(NO ) 的混合溶液中c(NO)=0.6 mol·L-1,用石墨作电极电解此溶液,
3 3 2当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500
mL,下列说法正确的是( )
A.原混合溶液中c(K+)为0.2 mol·L-1
B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol
D.电解后溶液中c(H+)为0.2 mol·L-1
答案 A
解析 石墨作电极电解KNO 和Cu(NO ) 的混合溶液,阳极反应式为4OH--4e-===2HO+
3 3 2 2
O↑,阴极先后发生两个反应:Cu2++2e-===Cu,2H++2e-===H↑。从收集到O 为2.24 L
2 2 2
可推知上述电解过程中共转移0.4 mol 电子,而在生成2.24 L H 的过程中转移0.2 mol电子,
2
所以Cu2+共得到0.4 mol-0.2 mol=0.2 mol电子,电解前Cu2+的物质的量和电解得到的Cu
的物质的量都为0.1 mol。电解前后分别有以下守恒关系:c(K+)+2c(Cu2+)=c(NO),c(K+)
+c(H+)=c(NO),不难算出:电解前c(K+)=0.2 mol·L-1,电解后c(H+)=0.4 mol·L-1。
2.(2020·山东师大附中模拟)某化学课外活动小组拟用铅蓄电池进行电絮凝净水的实验探究,
设计的实验装置如图所示,下列叙述正确的是( )
A.X极的电极反应式:Pb-2e-+SO===PbSO
4
B.铅蓄电池工作时,每转移2 mol电子,消耗98 g HSO
2 4
C.电解池的反应仅有2Al+6HO=====2Al(OH) ↓+3H↑
2 3 2
D.每消耗103.5 g Pb,理论上电解池阴极上有11.2 L H 生成
2
答案 A
解析 由图可知,电解池中,Al电极上发生氧化反应生成Al3+和O ,HO在Fe电极上被还
2 2
原生成H ,则Al电极是阳极,Fe电极是阴极,Y极是正极,X极是负极,则X极的电极反
2
应式为Pb-2e-+SO===PbSO ,A正确;铅蓄电池工作时,电池总反应式为 Pb+PbO +
4 2
2HSO ===2PbSO +2HO,则转移2 mol电子时消耗2 mol H SO ,其质量为196 g,B错误;
2 4 4 2 2 4
由图可知,Al电极上除生成Al3+外,还生成O ,Fe电极上生成H 和OH-,故电解池中还
2 2
发生反应:2HO=====2H↑+O↑,C错误;消耗103.5 g(即0.5 mol)Pb时,电路中转移1
2 2 2
mol电子,则阴极上逸出0.5 mol H,题目未指明气体所处状况,H 的体积不确定,D错误。
2 2
3.在如图所示的装置中,若通直流电5 min时,铜电极的质量增加2.16 g。试回答下列问题。(1)电源中X电极为直流电源的________极。
(2)pH变化:A________,B________,C________。(填“增大”“减小”或“不变”)
(3)通电5 min时,B中共收集224 mL(标准状况下)气体,溶液体积为 200 mL,则通电前
CuSO 溶液的物质的量浓度为________(设电解前后溶液体积无变化)。
4
(4)常温下,若 A 中 KCl 足量且溶液的体积也是 200 mL,电解后,溶液的 pH 为
__________(设电解前后溶液体积无变化)。
答案 (1)负 (2)增大 减小 不变
(3)0.025 mol·L-1 (4)13
解析 (1)三个装置是串联的电解池。电解 AgNO 溶液时,Ag+在阴极发生还原反应变为
3
Ag,所以质量增加的铜电极是阴极,则银电极是阳极,Y是正极,X是负极。
(2)电解KCl溶液生成KOH,溶液pH增大;电解CuSO 溶液生成HSO ,溶液pH减小;电
4 2 4
解AgNO 溶液,银为阳极,不断溶解,Ag+浓度基本不变,pH不变。
3
(3)通电5 min时,C中析出0.02 mol Ag,电路中通过0.02 mol电子。B中共收集0.01 mol气
体,若该气体全为氧气,则电路中需通过0.04 mol电子,电子转移不守恒,因此,B中电解
分为两个阶段,先电解CuSO 溶液,生成O ,后电解水,生成O 和H ,B中收集到的气体
4 2 2 2
是O 和H 的混合物。设电解CuSO 溶液时生成O 的物质的量为x,电解HO时生成O 的
2 2 4 2 2 2
物质的量为y,则4x+4y=0.02 mol(电子转移守恒),x+3y=0.01 mol(气体体积之和),解得
x=y=0.002 5 mol,所以n(CuSO )=2×0.002 5 mol=0.005 mol,c(CuSO )==0.025 mol·L-
4 4
1。(4)通电5 min时,A中放出0.01 mol H ,溶液中生成0.02 mol KOH,c(OH-)==0.1
2
mol·L-1,pH=13。
(1)同一原电池的正、负极的电极反应得、失电子数相等。
(2)同一电解池的阴、阳极电极反应中得、失电子数相等。
(3)串联电路中的各个电极反应得、失电子数相等。
上述三种情况下,在写电极反应式时,得、失电子数要相等,在计算电解产物的量时,应按
得、失电子数相等计算。
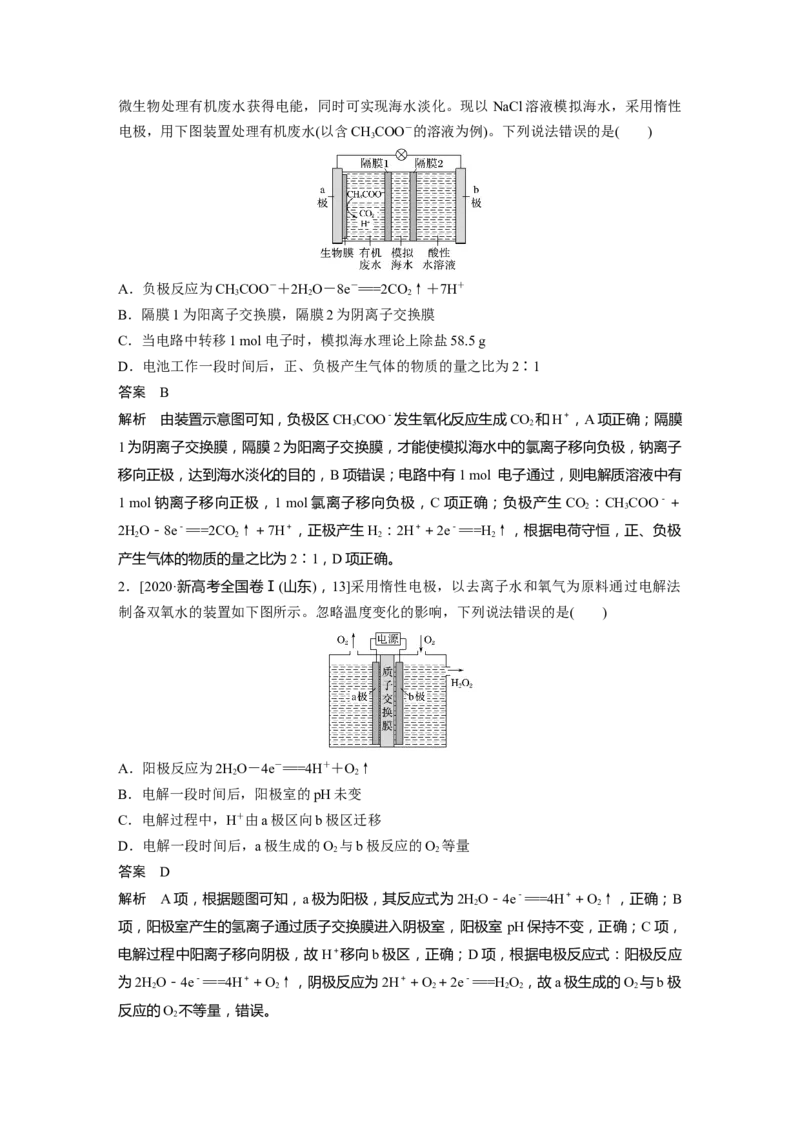
1.[2020·新高考全国卷Ⅰ(山东),10]微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以 NaCl溶液模拟海水,采用惰性
电极,用下图装置处理有机废水(以含CHCOO-的溶液为例)。下列说法错误的是( )
3
A.负极反应为CHCOO-+2HO-8e-===2CO↑+7H+
3 2 2
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1
答案 B
解析 由装置示意图可知,负极区CHCOO-发生氧化反应生成CO 和H+,A项正确;隔膜
3 2
1为阴离子交换膜,隔膜2为阳离子交换膜,才能使模拟海水中的氯离子移向负极,钠离子
移向正极,达到海水淡化的目的,B项错误;电路中有1 mol 电子通过,则电解质溶液中有
1 mol钠离子移向正极,1 mol氯离子移向负极,C项正确;负极产生CO :CHCOO-+
2 3
2HO-8e-===2CO↑+7H+,正极产生H :2H++2e-===H↑,根据电荷守恒,正、负极
2 2 2 2
产生气体的物质的量之比为2∶1,D项正确。
2.[2020·新高考全国卷Ⅰ(山东),13]采用惰性电极,以去离子水和氧气为原料通过电解法
制备双氧水的装置如下图所示。忽略温度变化的影响,下列说法错误的是( )
A.阳极反应为2HO-4e-===4H++O↑
2 2
B.电解一段时间后,阳极室的pH未变
C.电解过程中,H+由a极区向b极区迁移
D.电解一段时间后,a极生成的O 与b极反应的O 等量
2 2
答案 D
解析 A项,根据题图可知,a极为阳极,其反应式为2HO-4e-===4H++O↑,正确;B
2 2
项,阳极室产生的氢离子通过质子交换膜进入阴极室,阳极室 pH保持不变,正确;C项,
电解过程中阳离子移向阴极,故H+移向b极区,正确;D项,根据电极反应式:阳极反应
为2HO-4e-===4H++O↑,阴极反应为2H++O +2e-===HO ,故a极生成的O 与b极
2 2 2 2 2 2
反应的O 不等量,错误。
23.[2018·全国卷Ⅰ,27(3)]焦亚硫酸钠(Na SO)在医药、橡胶、印染、食品等方面应用广泛。
2 2 5
回答下列问题:
制备NaSO 可采用三室膜电解技术,装置如图所示,其中SO 碱吸收液中含有NaHSO 和
2 2 5 2 3
NaSO 。阳极的电极反应式为___________________。电解后,____________室的NaHSO
2 3 3
浓度增加。将该室溶液进行结晶脱水,可得到NaSO。
2 2 5
答案 2HO-4e-===4H++O↑ a
2 2
解析 阳极上HO放电生成O 和H+,电极反应式为2HO-4e-===O↑+4H+,电解过程
2 2 2 2
中H+透过阳离子交换膜进入a室,故a室中NaHSO 浓度增加。
3
4.[2019·北京,27(2)]可利用太阳能光伏电池电解水制高纯氢,工作示意图如图。通过控制
开关连接K 或K,可交替得到H 和O。
1 2 2 2
①制H 时,连接________。产生H 的电极反应式是______________________________。
2 2
②改变开关连接方式,可得O。
2
③结合①和②中电极3的电极反应,说明电极3的作用:___________________________
________________________________________________________________________。
答案 ①K 2HO+2e-===H↑+2OH- ③制H 时,电极3发生反应:Ni(OH) +OH--
1 2 2 2 2
e-===NiOOH+HO。制O 时,上述电极反应逆向进行,使电极3得以循环使用
2 2
解析 ①电解碱性电解液时,HO电离出的H+在阴极得到电子产生H ,根据题图可知电极
2 2
1与电池负极连接,为阴极,所以制 H 时,连接K ,产生H 的电极反应式为2HO+2e-
2 1 2 2
===H↑+2OH-。③制备O 时碱性电解液中的OH-失去电子生成O,连接K,O 在电极2
2 2 2 2 2
上产生。连接K 时,电极3为电解池的阳极,Ni(OH) 失去电子生成NiOOH,电极反应式
1 2
为Ni(OH) -e-+OH-===NiOOH+HO,连接K 时,电极3为电解池的阴极,电极反应式
2 2 2
为NiOOH+e-+HO===Ni(OH) +OH-,使电极3得以循环使用。
2 21.(2020·山东师大附中期中)某种酒精检测仪的传感器采用Pt作为电极,其燃烧室内充满特
种催化剂。某同学用该乙醇燃料电池作为电源设计如图所示电解实验装置。
下列说法不正确的是( )
A.a电极为负极,d电极为阴极
B.b电极的电极反应式为O+4H++4e-===2HO
2 2
C.当装置Ⅱ中生成11.2 L(标准状况)Cl 时,有0.5 mol H+通过装置Ⅰ中的质子交换膜
2
D.当装置Ⅰ中生成6.0 g CH COOH时,装置Ⅲ中CuSO 溶液的质量减少16 g
3 4
答案 C
解析 乙醇燃料电池中,O 通入b电极区,乙醇蒸气通入a电极区,则a电极是负极,b电
2
极是正极,从而推知,d电极是阴极,A正确;b电极是正极,O 得电子发生还原反应,电
2
解液呈酸性,则正极反应式为O +4H++4e-===2HO,B正确;装置Ⅱ中电解饱和氯化钠
2 2
溶液,生成标准状况下11.2 L Cl (即0.5 mol),电路中通过1 mol电子,据得失电子守恒和溶
2
液呈电中性可知,装置Ⅰ中有1 mol H+透过质子交换膜向右迁移,C错误;装置Ⅰ中负极反
应式为CHCHOH+HO-4e-===CHCOOH+4H+,生成6.0 g CH COOH(即0.1 mol)时,
3 2 2 3 3
电路中通过0.4 mol电子,装置Ⅲ中阳极反应式为2HO-4e-===4H++O↑,阴极反应式为
2 2
Cu2++2e-===Cu,据得失电子守恒推知,放出0.1 mol O 、析出0.2 mol Cu,故装置Ⅲ中溶
2
液减少的质量为0.1 mol×32 g·mol-1+0.2 mol×64 g·mol-1=16 g,D正确。
2.(2020·山东菏泽模拟)用石墨烯锂硫电池电解制备Fe(OH) 的装置如图所示。电池放电时
2
的反应为16Li+xS===8LiS(2≤x≤8),电解池两极材料分别为Fe和石墨,工作一段时间后,
8 2 x
右侧玻璃管中产生大量的白色沉淀。下列说法不正确的是( )
A.X是铁电极,发生氧化反应
B.电子流动的方向:B→Y,X→A
C.正极可发生反应:2LiS+2Li++2e-===3LiS
2 6 2 4
D.锂电极减重0.14 g时,电解池中溶液减重0.18 g答案 D
解析 电解法制备Fe(OH) ,则铁作阳极,根据题给总反应可知,金属锂发生氧化反应,作
2
电池的负极,所以Y为阴极,故X是铁电极,故A项正确;电子从原电池的负极流至电解
池的阴极,然后从电解池的阳极流回到原电池的正极,即电子从 B电极流向Y电极,从X
电极流回A电极,故B项正确;由图示可知,电极A发生了还原反应,即正极可发生反应:
2LiS +2Li++2e-===3LiS ,故C项正确;锂电极减重0.14 g,则电路中转移0.02 mol电子,
2 6 2 4
电解池中发生的总反应为Fe+2HO=====Fe(OH) +H↑,所以转移0.02 mol电子时,电解
2 2 2
池中溶液减少0.02 mol HO,即减轻0.36 g,故D项错误。
2
3.用石墨电极完成下列电解实验。
实验一 实验二
装置
a、d处试纸变蓝;b处变红, 两个石墨电极附近有气泡产
现象
局部褪色;c处无明显变化 生;n处有气泡产生……
下列对实验现象的解释或推测不合理的是( )
A.a、d处:2HO+2e-===H↑+2OH-
2 2
B.b处:2Cl--2e-===Cl↑
2
C.c处发生了反应:Fe-2e-===Fe2+
D.根据实验一的原理,实验二中m处能析出铜
答案 B
解析 A项,a、d处试纸变蓝,说明溶液显碱性,是溶液中的水放电生成氢气和氢氧根离
子造成的,正确;B项,b处变红,局部褪色,说明是溶液中的氯离子放电生成氯气同时与
HO反应生成HClO和H+,发生的反应为Cl--2e-+HO===HClO+H+,错误;C项,c处
2 2
为阳极,铁失去电子生成亚铁离子,正确;D项,实验一中ac形成电解池,bd形成电解池,
所以实验二中也形成电解池,n(钢珠右面)有气泡生成,为阴极产生氢气,n的另一面(钢球
左面)为阳极产生Cu2+,Cu2+在m的右面得电子析出铜,正确。
4.(2020·太原质检)采用电化学法还原CO ,是一种使CO 资源化的方法。如图是利用此法
2 2
制备ZnC O 的示意图(电解液不参与反应)。下列说法正确的是( )
2 4A.Zn与电源的负极相连
B.ZnC O 在交换膜右侧生成
2 4
C.电解的总反应式为2CO+Zn=====ZnC O
2 2 4
D.通入11.2 L CO 时,转移0.5 mol电子
2
答案 C
解析 电解过程中Zn被氧化,作阳极,所以Zn与电源的正极相连,A错误;Zn2+透过阳离
子交换膜到达左侧与生成的C O形成ZnC O,B错误;没有给出气体所处的温度和压强,D
2 2 4
错误。
5.(2020·湖北宜昌部分示范高中教学协作体期中)现有二氧化硫—空气质子交换膜燃料电池,
其原理如图所示。下列说法不正确的是( )
(注:质子指H+,质子交换膜仅允许H+通过)
A.Pt2电极附近发生的反应为O+4e-+2HO===4OH-
2 2
B.该电池工作时质子从Pt1电极经过内电路流到Pt2电极
C.Pt1电极附近发生的反应为SO +2HO-2e-===SO+4H+
2 2
D.该电池实现了制硫酸、发电、环保三位一体的结合
答案 A
解析 酸性条件下,氧气得电子生成水,则 Pt2电极附近发生的反应为O +4e-+4H+
2
===2HO,A项错误;放电时,质子向正极移动,Pt1电极为负极,Pt2电极为正极,则该电
2
池工作时质子从Pt1电极经过内电路流到Pt2电极,B项正确;Pt1电极通入SO ,SO 在负
2 2
极失电子生成SO,则Pt1电极附近发生的反应为SO +2HO-2e-===SO+4H+,C项正确;
2 2
二氧化硫—空气质子交换膜燃料电池吸收了空气中的二氧化硫,起到了环保的作用,产物
中有硫酸,而且发电,实现了制硫酸、发电、环保三位一体的结合,D项正确。
6.(2020·天津高三模拟)在混合导体透氧膜反应器中只需一步就可同时制备氨合成气(N 、
2
H)和液体燃料合成气(CO、H),其工作原理如图所示,下列说法错误的是( )
2 2
A.膜Ⅰ侧发生的反应为HO+2e-===H↑+O2-、O+4e-===2O2-
2 2 2
B.膜Ⅱ侧相当于原电池的负极C.膜Ⅱ侧发生的反应为CH+O2--2e-===2H+CO
4 2
D.膜Ⅱ侧每消耗1 mol CH ,膜Ⅰ侧一定生成1 mol H
4 2
答案 D
解析 膜Ⅰ侧,HO和O 在正极均发生还原反应,结合题图可写出其电极反应式为 HO+
2 2 2
2e-===H↑+O2-、O+4e-===2O2-,A项正确;原电池中阴离子由正极向负极移动,结合
2 2
题图中O2-的移动方向可知,膜Ⅰ侧相当于原电池的正极,膜Ⅱ侧相当于原电池的负极,B
项正确;膜Ⅱ侧CH 发生氧化反应,其电极反应式为CH +O2--2e-===2H +CO,C项正
4 4 2
确;膜Ⅰ侧发生的反应为HO+2e-===H↑+O2-、O+4e-===2O2-,膜Ⅱ侧发生的反应为
2 2 2
CH +O2--2e-===2H +CO,则膜Ⅱ侧每消耗1 mol CH ,膜Ⅰ侧生成的H 小于1 mol,D
4 2 4 2
项错误。
7.三室式电渗析法处理含NaSO 废水的原理如图所示,采用惰性电极,ab、cd均为离子交
2 4
换膜,在直流电场的作用下,两膜中间的Na+和SO可通过离子交换膜,而两端隔室中离子
被阻挡不能进入中间隔室。
下列叙述正确的是( )
A.通电后中间隔室的SO向正极迁移,正极区溶液pH增大
B.该法在处理含NaSO 废水时可以得到NaOH和HSO 产品
2 4 2 4
C.负极反应为2HO-4e-===O+4H+,负极区溶液pH降低
2 2
D.当电路中通过1 mol电子的电量时,会有0.5 mol的O 生成
2
答案 B
解析 电解池中阴离子向阳极移动,阳离子向阴极移动,即 SO向正极区移动,Na+ 向负极
区移动,正极区水电离的OH-发生氧化反应生成氧气,H+留在正极区,该极得到HSO 产
2 4
品,溶液pH减小,负极区水电离的H+发生还原反应生成氢气,OH-留在负极区,该极得
到NaOH产品,溶液pH增大,故A、C错误,B正确;该电解池相当于电解水,根据电解
水的方程式可计算出当电路中通过1 mol电子的电量时,会有0.25 mol的O 生成,D错误。
2
8.用NaSO 溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这
2 3
种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有
关说法不正确的是( )A.X为直流电源的负极,Y为直流电源的正极
B.阳极区pH增大
C.图中的b>a
D.该过程中的产品主要为HSO 和H
2 4 2
答案 B
解析 A项,由图示可知Pt(Ⅰ)极上H+→H ,发生还原反应,故Pt(Ⅰ)为阴极,X为直流电
2
源的负极,Y为直流电源的正极,正确;B项,Pt(Ⅱ)为阳极,在阳极,SO、HSO被氧化为
HSO ,SO+HO-2e-===2H++SO,HSO+HO-2e-===3H++SO,溶液的酸性增强,pH
2 4 2 2
减小,错误;C项,由B项分析可知,阳极有HSO 生成,故b>a,正确;D项,阳极产物
2 4
为HSO ,阴极产物为H,正确。
2 4 2
9.硼酸(H BO)可以通过电解NaB(OH) 溶液的方法制备,工作原理如图所示。下列有关表
3 3 4
述错误的是( )
A.M室的电极反应式为2HO-4e-===O↑+4H+
2 2
B.N室中,进口和出口的溶液浓度大小关系为a%